2,5K
As próteses metálicas de aposição luminal, lumen-apposing metal stents (LAMS),
representam um avanço significativo devido ao seu desenho com flanges perpendiculares e capacidade de segurar duas
estruturas luminais em aposição.
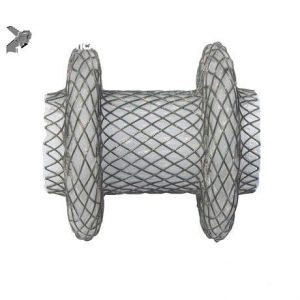
São compostas de uma malha de nitinol trançada e totalmente recobertas por uma membrana
de silicone, prevenindo assim vazamentos, ingrowth (crescimento interno de tecido) e possibilitando sua remoção com certa facilidade.
Sua forma de haltere e amplo diâmetro interno oferecem uma melhor drenagem interna,
redução da taxa de oclusão, prevenção da migração, bem como passagem interna do endoscópio para procedimentos
terapêuticos adicionais [1].

 Outros modelos de LAMS são: as sul-coreanas Spaxus (Taewoong Medical™), Nagi (Taewoong Medical™) e Hanarostent (M.I. Tech™), além da alemã Aixstent (Leufen
Medical™).
Outros modelos de LAMS são: as sul-coreanas Spaxus (Taewoong Medical™), Nagi (Taewoong Medical™) e Hanarostent (M.I. Tech™), além da alemã Aixstent (Leufen
Medical™).

 Dê uma conferida no site da empresa: https://www.bostonscientific.com/pt-BR/produtos/stents-gastrointestinais/axios-stent-e-sistema-de-entrega-aprimorado-de-eletrocautery.html
Dê uma conferida no site da empresa: https://www.bostonscientific.com/pt-BR/produtos/stents-gastrointestinais/axios-stent-e-sistema-de-entrega-aprimorado-de-eletrocautery.html

Figura 1: prótese de aposição luminal Axios (Boston Scientific™
1ª Geração: requerem uma abordagem em múltiplas etapas. As lesões são acessadas por punção com agulha 19-G, seguido da passagem de um fio guia de 0,025 ou 0,035 polegadas para manter a posição e subsequente dilatação (com cistótomo ou needle knife seguido de balão hidrostático) do trato para passagem do dispositivo de introdução do LAMS. O introdutor LAMS é passado pelo aparelho, e o flange distal é liberado sob controle ecoendoscópico. Uma vez que o flange distal está totalmente aberto, uma leve tensão é aplicada para opor as 2 estruturas antes da liberação do flange proximal sob visualização endoscópica direta [1]. 2ª Geração (hot): possibilitam a realização em etapa única usando eletrocauterização. A inserção hot é feita por meio da aplicação de corrente de corte de alta frequência pela ponta do dispositivo, permitindo o acesso transmural sem dilatação prévia do trato. A inserção em uma única etapa minimiza trocas de acessórios, reduzindo erros técnicos e tempo de procedimento [1].
Figura 2: sistema de liberação da LAMS
Axios (Boston Scientific™)
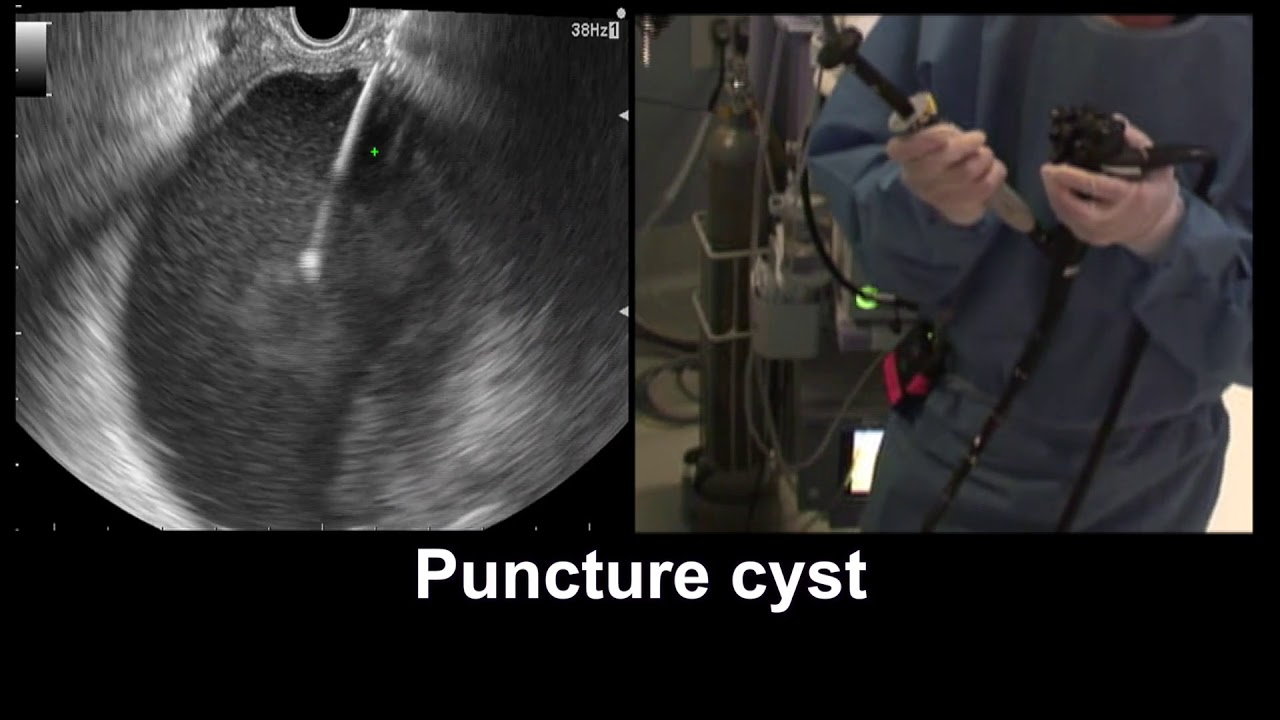
É a mais utilizada e bem estudada da literatura. Devido à facilidade de manejo, atualmente, é mais optada a versão Hot Axios (2ª geração). Apresenta tamanhos de diâmetro de lúmen de 6, 8, 10, 15 e 20 mm. O sistema de liberação é controlado por um único operador e é dividido em um controle de introdução do cateter (inferior) e um controle de liberação do stent (superior). O mecanismo de liberação do cateter também oferece uma parada rígida entre a implantação do flange distal e proximal, evitando liberação inadvertida no lúmen do cisto. Veja abaixo o vídeo do sistema de liberação:
Indicações [2]
- Drenagem de coleções pancreáticas (pseudocisto e walled-off necrosis);
- Drenagem da via biliar: coledocoduodenostomia;
- Drenagem da vesícula biliar (colecistite);
- Gastrojejunostomia (obstruções gastroduodenais);
- Confecção de fístula gastrogástrica (acesso à CPRE em paciente com by-pass);
- Realização de enteroenteroanastomose (tratamento da síndrome da alça aferente);
- Estenoses benignas do trato gastrointestinal (seu formato diminui a taxa de migração comparado com próteses tradicionais);
- Drenagem de coleções cavitárias.
Drenagem de coleções pancreáticas
Representam um grupo heterogêneo de doenças, e a decisão de usar um LAMS em vez de stents plásticos permanece uma escolha caso a caso. Os stents plásticos parecem ter eficácia equivalente para drenagem de pseudocisto simples e provavelmente são mais baratos quando usados nesse cenário. Coleções heterogêneas e walled off necrosis parecem mais adequados para o uso de LAMS, e resultados clínicos superiores mostram essa direção [1]. Recente revisão sistemática e metanálise que incluiu 1534 pacientes confirmou que o LAMS apresenta vantagens sobre os stents plásticos, com maior taxa de sucesso clínico e menor taxa de infecção e oclusão [3]. Outro benefício dos LAMS nas coleções complicadas é a possibilidade de acesso endoscópico direto para realização de sessões de necrosectomias (LAMS de 15 e 20 mm). Os LAMS não podem ficar locados definitivamente, se após 3 ou 4 semanas a coleção já tiver sido resolvida, eles devem ser retirados e, apenas nos casos de ruptura de ducto pancreático não resolvida, colocados stents plásticos duplos pigtail. Vídeo 1: uso de LAMS seguido de passagem de prótese duplo pigtail na drenagem de pseudocisto. Cortesia do Dr. Gustavo Luís Rodela Silva, GLR.Drenagem biliar
São utilizados os stents de 6 e 8 mm. As indicações mais comuns para esse procedimento são a falha na canulação papilar por neoplasia maligna avançada ou falta de acesso à papila devido à anatomia alterada cirurgicamente. Em revisão sistemática e metanálise publicada em 2020, demonstrou segurança e efetividade do uso de LAMS nos casos de falha na CPRE [4], entretanto, outra recente revisão, apesar da facilidade técnica do uso das LAMS, demonstrou resultados semelhantes comparado à drenagem ecoguiada com próteses metálicas biliares tradicionais [6].Colecistite
Em pacientes sem condições cirúrgicas, a drenagem ecoendoscópica demonstrou sucesso técnico e clínico comparável com a drenagem percutânea, além de menor tempo de internação, dor e necessidade de reintervenções [6].Gastrojejunostomia
Esse procedimento é uma alternativa nos casos de obstrução gastroduodenal, especialmente tumoral, perante a passagem de prótese metálica ou mesmo a gastrojejunostomia cirúrgica. A técnica consiste em uma punção através da parede gástrica de uma alça jejunal distendida por líquido infundido previamente, ou mesmo por um balão preenchido, permitindo a identificação da alça. O procedimento ecoendoscópico tem o potencial de oferecer permeabilidade luminal de longa duração, evitando o ingrowth que ocorre nas próteses duodenais e tem menor morbidade comparado a um procedimento cirúrgico. Foi demonstrando um sucesso técnico de até 90% [7] e taxa de reintervenção de 6,1%, comparado aos 30,3% nos stents duodenais [8].Confecção de fístula gastrogástrica
Nos pacientes com doenças pancreatobiliares com necessidade de CPRE, porém com anatomia cirúrgica alterada (gastroplastia redutora em Y de Roux), é possível a realização de fístula com estômago excluso, seguida de espera de 2 a 3 semanas para maturação local e posterior passagem do duodenoscópio para acesso à papila. Apesar de rebuscada, pode ser uma opção à enteroscopia ou mesmo à realização de gastrostomia cirúrgica para passagem do duodenoscópio.Confecção de enteroenteroanastomose
Na síndrome da alça aferente ocorre uma obstrução na alça biliopancreática, levando a dor, vômitos biliosos e distensão da alça. Apesar do tratamento ser tradicionalmente cirúrgico, uma opção de menor morbidade é a colocação de LAMS drenando o segmento obstruído, criando um pertuito para drenagem local.Estenoses benignas do trato gastrointestinal
Em algumas estenoses complexas, ou mesmo nos casos em que ocorreu migração prévia de prótese metálica tradicional, o uso do LAMS pode ser uma opção de resgate no tratamento dessas condições. Outra indicação é para casos de estenoses em reto distal, em que próteses longas causam tenesmo.Drenagem de coleções cavitárias
O uso de LAMS para drenagem de abscessos surgiu como uma alternativa à técnica percutânea, devido inclusive a algumas limitações, como interposição de órgãos e desconforto do paciente com a drenagem externa. A drenagem ecoguiada não tem essas limitações, e os abscessos costumam estar próximos ao trato gastrointestinal [9]. Outra possível aplicação futura pode ser no tratamento da obesidade. Após a sutura endoscópica do piloro, uma fístula gastrojejunal pode ser criada usando LAMS, semelhante a uma gastroplastia em Y de Roux [9].Eventos adversos [9]
Sangramento intraprocedimento
O sangramento da mucosa pode ser interrompido pela aplicação local de corrente pelo eletrocautério. Quando a hemorragia intralesional é observada, um fio guia pode ser avançado através do lúmen do sistema introdutor do LAMS e trocado por uma agulha FNA 19-G. A ponta da agulha FNA é então posicionada no local do sangramento, e a epinefrina pode ser administrada até que o sangramento cesse. Se o sangramento for persistente, a radiointervenção pode ser necessária.Sangramento tardio
São geralmente secundários à coagulopatia, entretanto podem ocorrer devido à trauma do LAMS em vasos adjacentes, especialmente após drenagens pancreáticas. Dessa forma, após a resolução da coleção, devem ser retirados para prevenir esse tipo de complicação.Adesão à parede (burried)
Após longos períodos, o LAMS pode ficar aderido à parede gástrica, com dificuldade de sua retirada. Nesses casos, deve ser realizada uma dilatação do lúmen para 15 mm, seguido de tração com pinça de corpo estranho.Obstrução biliar
Nas drenagens no duodeno proximal, uma vez que a coleção foi resolvida, o flange distal do LAMS pode comprimir a via biliar causando icterícia. A remoção do LAMS e a colocação de um stent plástico resolverão a complicação. As LAMS representam um grande avanço técnico na endoscopia terapêutica transluminal, possibilitando o acesso de estruturas adjacentes, levando a uma gama de intervenções e diminuindo a necessidade de acesso cirúrgico e/ou percutâneo. Sua pesquisa e desenvolvimento deverão aprimorar sua segurança, bem como expansão de sua aplicação para outras indicações. Veja também alguns casos com a utilização dos LAMS:- Drenagem ecoguiada de formação pseudocística pancreática;
- Tratamento endoscópico da síndrome da alça aferente com LAMS;
- Gastroenterostomia guiada por EUS.


Agradecimentos
Agradeço ao Dr. Gustavo Luís Rodela Silva pela cessão do vídeo sobre LAMS.Como citar este artigo
Oliveira JF. Prótese Metálica de Aposição Luminal (LAMS). Endoscopia Terapêutica; 2021. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/protese-metalica-de-aposicao-luminal-lams-2/Referências
- Stier MW, Waxman I. Lumen-Apposing Metal Stents: Which One and Why? Gastrointest Endosc Clin N Am. 2018 Apr;28(2):207-217. doi: 10.1016/j.giec.2017.11.008. Epub 2018 Feb 3. PMID: 29519333.
- Saumoy M, Yarber C, Kahaleh M. Novel Uses of Lumen-Apposing Metal Stents. Gastrointest Endosc Clin N Am. 2018 Apr;28(2):197-205. doi: 10.1016/j.giec.2017.11.007. PMID: 29519332.
- Tan S, Zhong C, Ren Y, et al. Are Lumen-Apposing Metal Stents More Effective Than Plastic Stents for the Management of Pancreatic Fluid Collections: An Updated Systematic Review and Meta-analysis. Gastroenterol Res Pract. 2020 Apr 20;2020:4952721. doi: 10.1155/2020/4952721. PMID: 32382266; PMCID: PMC7189322.
- Krishnamoorthi R, Dasari CS, Thoguluva Chandrasekar V, et al. Effectiveness and safety of EUS-guided choledochoduodenostomy using lumen-apposing metal stents (LAMS): a systematic review and meta-analysis. Surg Endosc. 2020 Jul;34(7):2866-2877. doi: 10.1007/s00464-020-07484-w. Epub 2020 Mar 5. PMID: 32140862.
- Amato A, Sinagra E, Celsa C, et al. Efficacy of lumen-apposing metal stents or self-expandable metal stents for endoscopic ultrasound-guided choledochoduodenostomy: a systematic review and meta-analysis. Endoscopy. 2020 Nov 27. doi: 10.1055/a-1324-7919. Epub ahead of print. PMID: 33246343.
- Irani S, Ngamruengphong S, Teoh A, et al. Similar Efficacies of Endoscopic Ultrasound Gallbladder Drainage With a Lumen-Apposing Metal Stent Versus Percutaneous Transhepatic Gallbladder Drainage for Acute Cholecystitis. Clin Gastroenterol Hepatol. 2017 May;15(5):738-745. doi: 10.1016/j.cgh.2016.12.021. Epub 2016 Dec 30. PMID: 28043931.
- Itoi T, Baron TH, Khashab MA, Tsuchiya T, Irani S, Dhir V, Bun Teoh AY. Technical review of endoscopic ultrasonography-guided gastroenterostomy in 2017. Dig Endosc. 2017 May;29(4):495-502. doi: 10.1111/den.12794. Epub 2017 Jan 27. PMID: 28032663.
- Ge PS, Young JY, Dong W, Thompson CC. EUS-guided gastroenterostomy versus enteral stent placement for palliation of malignant gastric outlet obstruction. Surg Endosc. 2019 Oct;33(10):3404-3411. doi: 10.1007/s00464-018-06636-3. Epub 2019 Feb 6. PMID: 30725254; PMCID: PMC6684873.
- Bang JY, Varadarajulu S. Lumen-apposing metal stents for endoscopic ultrasonography-guided interventions. Dig Endosc. 2019 Nov;31(6):619-626. doi: 10.1111/den.13428. Epub 2019 Jun 5. PMID: 31050068.
Endoscopista no Hospital Vila Nova Star, Hospital Nipo-Brasileiro, Hospital Alemão Oswaldo Cruz, Alta Excelência Diagnóstica e Clínica do Aparelho Digestivo.
Mestre em Gastroenterologia pela Faculdade de Medicina da Universidade de São Paulo.
Especialização em Endoscopia Oncológica no Instituto do Câncer do Estado de São Paulo – ICESP.
Residência médica em Endoscopia Gastrointestinal no Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira
- Joel Fernandez de Oliveira

