1. Introdução
As lesões císticas pancreáticas tem sido cada vez mais diagnosticadas, tanto pelo aumento da incidência dessas lesões quanto pela realização e acesso crescente a exames de imagem que eventualmente identificam tais lesões. A neoplasia mucinosa papilar intraductal (IPMN) é uma das principais lesões císticas do pâncreas, tanto pela sua incidência quanto pelo seu potencial de transformação maligna, porém sua apresentação e evolução apresentam um espectro amplo de possibilidades. Como o potencial maligno do IPMN de ducto secundário varia de 1 a 38%, é fundamental identificar quais lesões apresentam risco aumentado e quais podem ser apenas acompanhadas, evitando cirurgias desnecessárias que envolvem riscos e morbi-mortalidade consideráveis. Já o IPMN de ducto principal apresenta um potencial maligno maior, de 33 a 85%, sendo indicada a ressecção cirúrgica sempre que o ducto pancreático principal (DPP) esteja dilatado em 10 mm ou mais e o paciente apresente condições clínicas e expectativa de vida compatível com a abordagem cirúrgica (1).
Para padronizar o manejo dos IPMN com base nas melhores evidências disponíveis, a Associação Internacional de Pancreatologia (IAP) publicou o primeiro guideline contemplando as lesões císticas pancreáticas mucinosas – IPMN e cistoadenoma mucinoso – em 2006 (2). Este guideline foi revisado em 2012 (3) e, posteriormente em 2017, um novo guideline com foco apenas nos IPMN foi publicado, e ficou conhecido como o consenso de Fukuoka (4). Os critérios de Fukuoka foram amplamente divulgados e discutidos ao longo dos últimos anos, sendo ferramenta chave no manejo dos IPMN, que já foi tema de publicação no Endoscopia Terapêutica (clique aqui para Critérios de Fukuoka para IPMN). Mais recentemente, em 2022 no encontro da IAP realizado em Kyoto, o consenso de Fukuoka foi revisado, sendo o novo guideline publicado na Pancreatology em 2024 (5).
Neste artigo, iremos abordar o novo guideline de Kyoto, enfatizando o que mudou desde o último consenso em Fukuoka à luz do recente artigo publicado na The New England Journal of Medicine sobre o tema (1), sendo essas as duas referências para os próximos tópicos (1, 5).
2. Conceitos e definições
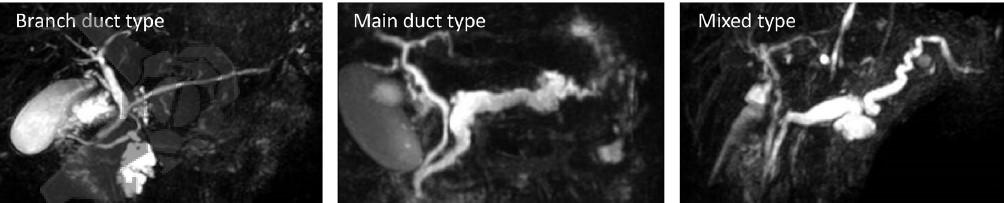
Não houve mudança em relação às definições dos três tipos de IPMN, que podem ser de ducto secundário (“Branch duct-IPMN” ou BD-IPMN), de ducto principal (“Main-duct IPMN” ou MD-IPMN) ou misto – quando contempla os critérios tanto para BD-IPMN quanto para MD-IPMN. Os cistos pancreáticos >5mm com comunicação com o DPP devem ser classificados como BD-IPMN, enquanto uma dilatação do DPP >5mm sem fator obstrutivo é classificado como MD-IPMN. A importância e manejo de cistos pancreáticos assintomáticos <5mm permanece controverso.
Os IPMN podem apresentar displasia de baixo grau ou displasia de alto grau – que também pode ser chamada de carcinoma in situ -, podendo chegar a carcinoma invasivo (CI). O objetivo no manejo dos IPMN é distinguir os IPMN de baixo grau (maioria) dos de alto grau, que evoluirão para carcinoma invasivo.
Em relação aos subtipos morfológicos, são reconhecidos três tipos: gástrico (mais frequente e melhor prognóstico), intestinal e pancreatobiliar (maior risco de malignização). O tipo oncocítico foi separado como entidade própria, sendo denominado neoplasia oncocítica papilar intraductal, devido principalmente estudos genéticos que identificaram diferenças significativas.
3. Investigação diagnóstica e exames complementares
Os exames de imagem primários na avaliação dos IPMN são a ressonância magnética (RM) e a tomografia computadorizada (TC), sendo a ecoendoscopia indicada para avaliação de achados sugestivos de displasia de alto grau e carcinoma invasivo.
Punção ecoguiada
A punção ecoguiada não está indicada de rotina. Ela deve ser indicada apenas quando há dúvida diagnóstica para diagnóstico diferencial com outras lesões císticas ou em casos nos quais a punção poderá mudar a conduta. Quando há evidência de alto risco para displasia de alto grau ou carcinoma invasivo na RM, a cirurgia está indicada e não há indicação de punção ecoguiada.
Para o diagnóstico diferencial com as demais lesões císticas pancreáticas, o CEA e a amilase são tradicionalmente os principais marcadores utilizados, porém estudos mais recentes destacam a glicose como importante marcador para distinguir lesões mucinosas de não mucinosas. Glicose <50ng/ml apresenta sensibilidade de 93%, especificidade de 89% e acurácia que pode chegar até 90 a 94%, tendo um rendimento melhor que o CEA – que apresenta uma sensibilidade de 58% e especificidade de 87%. É importante ressaltar que tais marcadores não apresentam relação com displasia de alto grau ou carcinoma in situ.
Em relação a punção ecoguiada com o objetivo de identificar displasia de alto grau ou carcinoma invasivo em casos limítrofes, a sensibilidade para identificação citológica no fluido cístico é de apenas 28,7%, porém o achado suspeito ou positivo apresenta especificidade de 91-100% e 100% respectivamente, e a ressecção cirúrgica estaria indicada. Para superar a baixa sensibilidade da punção aspirativa, foram desenvolvidos “microforceps” para biópsias através da agulha, que apresentam maior sensibilidade, apesar de um risco um pouco aumentado de pancreatite e sangramento. A punção ecoguiada também pode possibilitar a análise genética do conteúdo, que pode se relacionar tanto na confirmação do diagnóstico de IPMN (alterações nos genes KRAS e GNAS) quanto com risco de displasia de alto grau e carcinoma invasivo (alterações nos genes TP53, CTNNB1, CDKN2A, SMAD4, e genes envolvidos na via mTOR) – estes apresentando alta especificidade (92-98%) porém baixa sensibilidade (9-39%). Quando identificada áreas sólidas, as punções (se indicada) devem ser dirigidas a estas áreas, onde o rendimento diagnóstico é maior. No caso de avaliação de nódulos murais, a ecoendoscopia com contraste pode definir o caráter neoplásico ou não-neoplásico do nódulo, evitando a necessidade de punção ecoguiada, que apresenta um risco de “seeding” de cerca de 0,3%.
Pancreatoscopia
Pode ser útil nos casos de MD-IPMN e tipo misto com indicação de cirurgia para delimitar a extensão da ressecção e evitar a pancreatectomia total em alguns casos. Ela não deve ser realizada no intra-operatório pelo risco de disseminação neoplásica peritoneal e pela possível super-estimativa da extensão da lesão a ser ressecada, uma vez que a acurácia para diferenciar displasia de baixo grau (que não precisa ser ressecada) de alto grau (que deve ser ressecada) é baixa. Dessa forma, quando indicada, a pancreatoscopia deve ser realizada antes do procedimento cirúrgico, ficando a margem intra-operatória a critério da avaliação anatompatológica de congelação.
O que mudou: 1) a análise genética do material da punção ecoguiada pode auxiliar no diagnóstico e identificação de lesões de alto risco. 2) a pancreatoscopia pode auxiliar em alguns casos de MD-IPMN e tipo misto e, quando indicada, deve ser realizada antes da cirurgia (e não no intra-operatório).
4. Avaliação do risco – estigmas de alto risco e características preocupantes
Talvez a principal contribuição dos guidelines que abordam os IPMN seja identificar os achados e fatores que aumentam o risco de evolução para câncer e atribuir condutas a partir desses fatores. Desde a publicação de 2012 os termos “estigmas de alto risco” (high risk stigmata – HRS) e “características preocupantes” (worrisome features – WF) vem sendo utilizados para identificar os fatores que apresentam alto risco e risco intermediário, respectivamente.
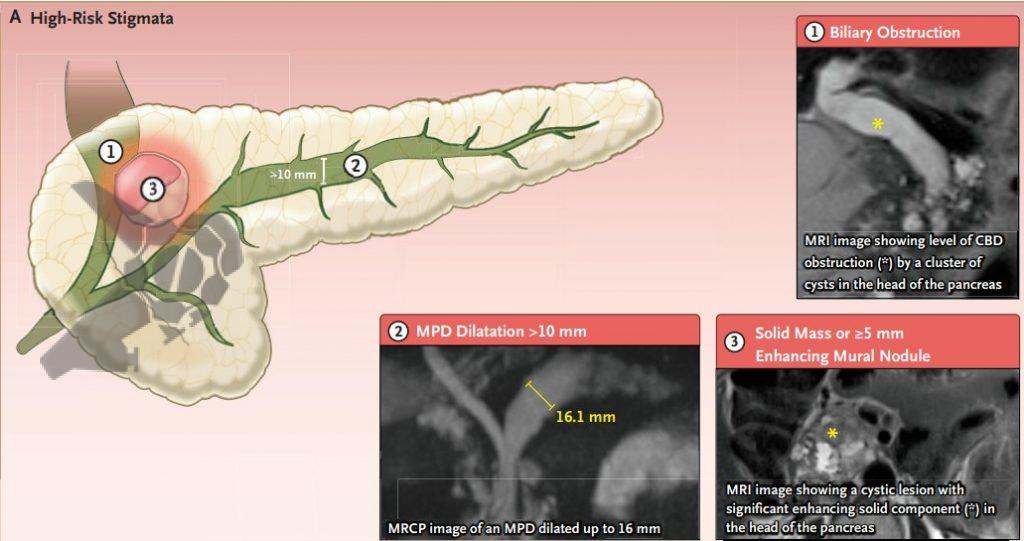
4. a) Estigmas de alto risco
- Icterícia obstrutiva em paciente com lesão cística na cabeça do pâncreas
- Nódulo mural com realce ≥ 5mm ou componente sólido
- Ducto pancreático principal ≥ 10mm
- Citologia suspeita ou positiva (caso tenha sido indicada punção ecoguiada)
O que mudou: citologia suspeita ou positiva foi definida como estigma de alto risco
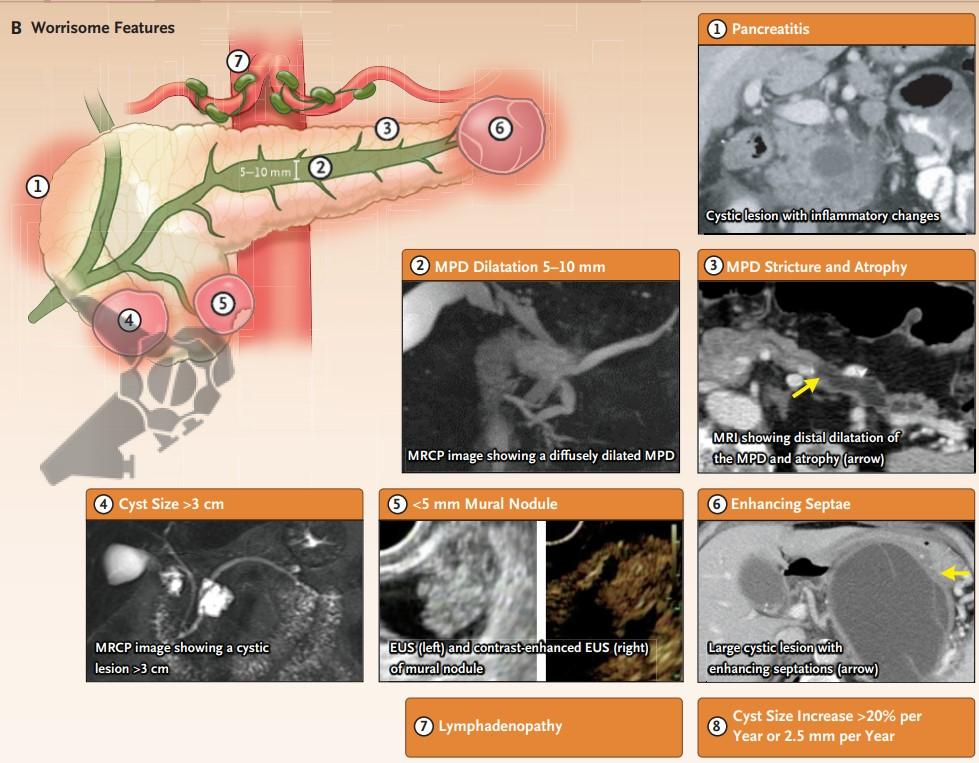
4. b) Características preocupantes (CP)
> Clínica
- Pancreatite aguda
- Aumento de CA 19-9
- Início ou exacerbação aguda de Diabetes no último 1 ano
> Imagem
- . Cisto ≥ 30mm
- Nódulo mural com realce < 5mm
- Paredes císticas espessadas ou com realce
- Ducto pancreático principal ≥ 5mm e <10mm
- Mudança abrupta de calibre do DPP com atrofia distal
- Linfadenopatia
- Crescimento cístico ≥ 2,5mm/ano
A presença de múltiplas CPs aumenta significativamente o risco de displasia de alto grau e carcinoma invasivo:
– 1 CP: 22% de risco
– 2 CP: 34% de risco
– 3 CP: 59% de risco
– ≥4 CP: até 100% de risco
O que mudou: 1) um critério clínico novo foi incorporado – início ou exacerbação de diabetes no último ano; 2) um critério foi alterado – crescimento cístico ≥ 2,5mm/ano (antes era ≥ 5mm/2 anos; 3) foi incorporado o conceito de que múltiplas características preocupantes aumentam o risco de displasia de baixo grau e carcinoma invasivo.
5) Fatores adicionais para avaliação nos pacientes com “características preocupantes”
Os pacientes que não têm estigmas de alto risco, porém apresentam alguma CP, devem ser avaliados para fatores adicionais que possam direcionar a conduta para o seguimento clínico ou uma tendência à indicação cirúrgica.
Foram alterados os três fatores considerados previamente em Fukuoka (que eram: presença de nódulo mural definitivo > 5mm, características suspeitas para envolvimento do DPP e citologia suspeita ou positiva). No atual guideline de Kyoto, esses fatores são: 1) pancreatite de repetição com piora da qualidade de vida; 2) múltiplas características preocupantes; 3) jovem com bom status clínico para cirurgia. A presença de um desses três fatores direciona para uma abordagem cirúrgica, enquanto a ausência dos três direciona para o seguimento clínico com exames de imagem periódicos.
O que mudou: os três fatores adicionais a serem avaliados em pacientes sem estigmas de alto risco porém com alguma CP – 1) pancreatite de repetição com piora da qualidade de vida; 2) múltiplas características preocupantes; 3) jovem com bom status clínico para cirurgia.
6) Seguimento de IPMN não ressecado
O risco de progressão dos BD-IPMN apresenta relação com o tamanho inicial do maior cisto ao diagnóstico, e, portanto, o seguimento preferencialmente com RM das lesões não candidatas à ressecção cirúrgica baseia-se no tamanho do maior cisto:
- < 20mm: reavaliação em 6 meses. Se estável, a cada 18 meses
- ≥ 20 mm <30mm: reavaliação em 6 e 12 meses. Se estável, a cada 12 meses
- ≥ 30mm: a cada 6 meses
Em relação ao seguimento de lesões <20mm sem CP que permanecem estáveis, há controvérsia na literatura, de forma que o novo guideline admite duas possibilidades: manter o seguimento OU parar o seguimento após 5 anos. Dessa forma, os candidatos a interrupção do seguimento com exames de imagem são:
- Cistos <20mm sem estigmas de alto risco ou CPs, estáveis por pelo menos 5 anos;
- Pacientes não candidatos à cirurgia ou com expectativa de vida < 10 anos.
O seguimento dos IPMN é importante não só devido ao risco de progressão da lesão, mas também pelo risco aumentado em desenvolver adenocarcinoma de pâncreas sem relação com o IPMN, que pode ser até 5x maior do que a população geral, segundo estudos japoneses. Esse mecanismo foi chamado de “dupla carcinogênese” dos IPMN, e é um dos argumentos defendidos por aqueles que advogam em manter o seguimento mesmo em lesões pequenas estáveis.
Em relação aos BD-IPMN multifocais – que correspondem a 20-40% dos casos – não há risco aumentado de progressão e o manejo e seguimento deve ser de acordo com a maior lesão.
O que mudou: o seguimento de acordo com o tamanho do maior cisto, que antes distinguia quatro grupos (<1cm, 1-2cm, 2-3cm e > 3cm) foi reduzido para apenas três grupos (< 2cm, ≥ 2cm <30cm e ≥ 3cm).
7) Seguimento de IPMN não invasivo ressecado
- Seguimento de IPMN não invasivo ressecado:
- – Pancreatectomia total: seguimento por 5 anos;
- – Pancreatectomia parcial: a cada 6-12 meses, até o paciente não ser mais candidato à cirurgia.
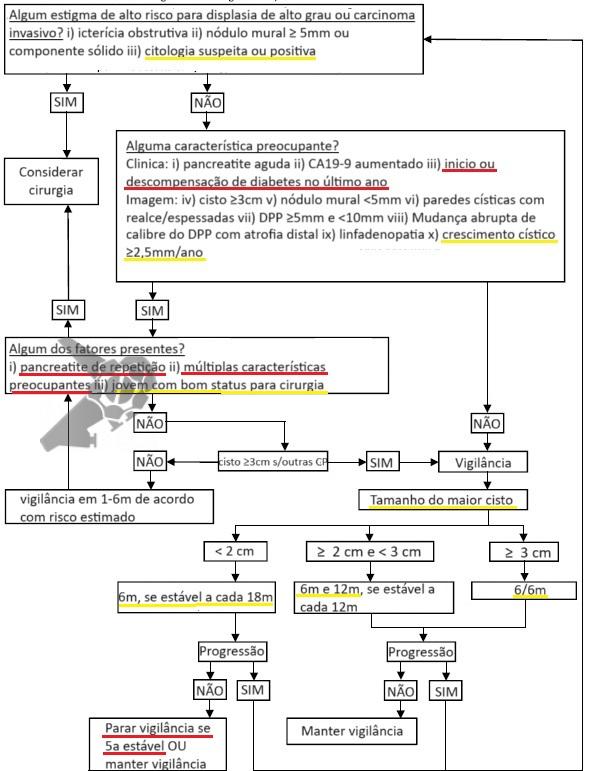
8) Algoritmo de manejo de BD-IPMN pelo guideline de Kyoto (adaptado)
- Sublinhado em vermelho: critério novos;
- Sublinhado em amarelo: critério que foram modificados em relação à Fukuoka.
Referências:
- Gonda TA, Cahen DL, Farrell JJ. Pancreatic Cysts. N Engl J Med. 2024;391(9):832-843. doi:10.1056/NEJMra2309041
- Tanaka M, Chari S, Adsay V, et al. International consensus guidelines for management of intraductal papillary mucinous neoplasms and mucinous cystic neoplasms of the pancreas. Pancreatology. 2006;6(1-2):17-32. doi:10.1159/000090023
- Tanaka M, Fernández-del Castillo C, Adsay V, et al. International consensus guidelines 2012 for the management of IPMN and MCN of the pancreas. Pancreatology. 2012;12(3):183-197. doi:10.1016/j.pan.2012.04.004
- Tanaka M, Fernández-Del Castillo C, Kamisawa T, et al. Revisions of international consensus Fukuoka guidelines for the management of IPMN of the pancreas. Pancreatology. 2017;17(5):738-753. doi:10.1016/j.pan.2017.07.007
- Ohtsuka T, Fernandez-Del Castillo C, Furukawa T, et al. International evidence-based Kyoto guidelines for the management of intraductal papillary mucinous neoplasm of the pancreas. Pancreatology. 2024;24(2):255-270. doi:10.1016/j.pan.2023.12.009
Como citar este artigo
Proença IM. Endoscopia Terapeutica. IPMN: o que mudou de Fukuoka à Kyoto, 2024 vol II. Disponivel em: https://endoscopiaterapeutica.net/pt/assuntosgerais/ipmn-o-que-mudou-de-fukuoka-a-kyoto/
Médico e Cirurgião Geral pela Escola Paulista de Medicina/UNIFESP.
Endoscopia Digestiva pelo HC-FMUSP.
Especialização em Endoscopia Biliopancreática no HC-FMUSP.
Médico Assistente do Serviço de Endoscopia do HC-FMUSP.
Mestre em Ciências em Gastroenterologia pela FMUSP.

