Quiz ! Colonoscopia de rastreio
Paciente feminina de 49 anos em colonoscopia de rastreio foi evidenciada a seguinte alteração.
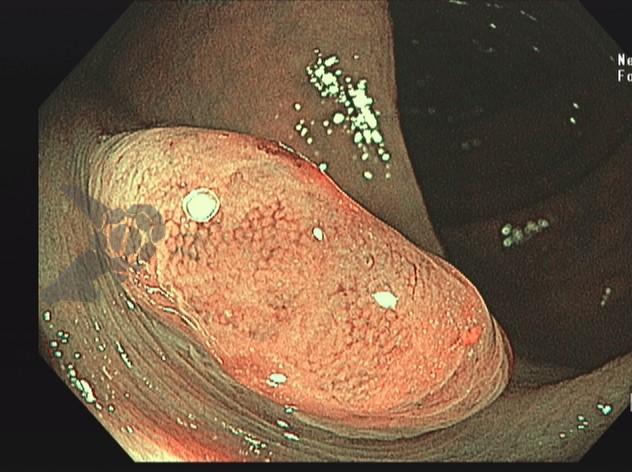
Paciente feminina de 49 anos em colonoscopia de rastreio foi evidenciada a seguinte alteração.

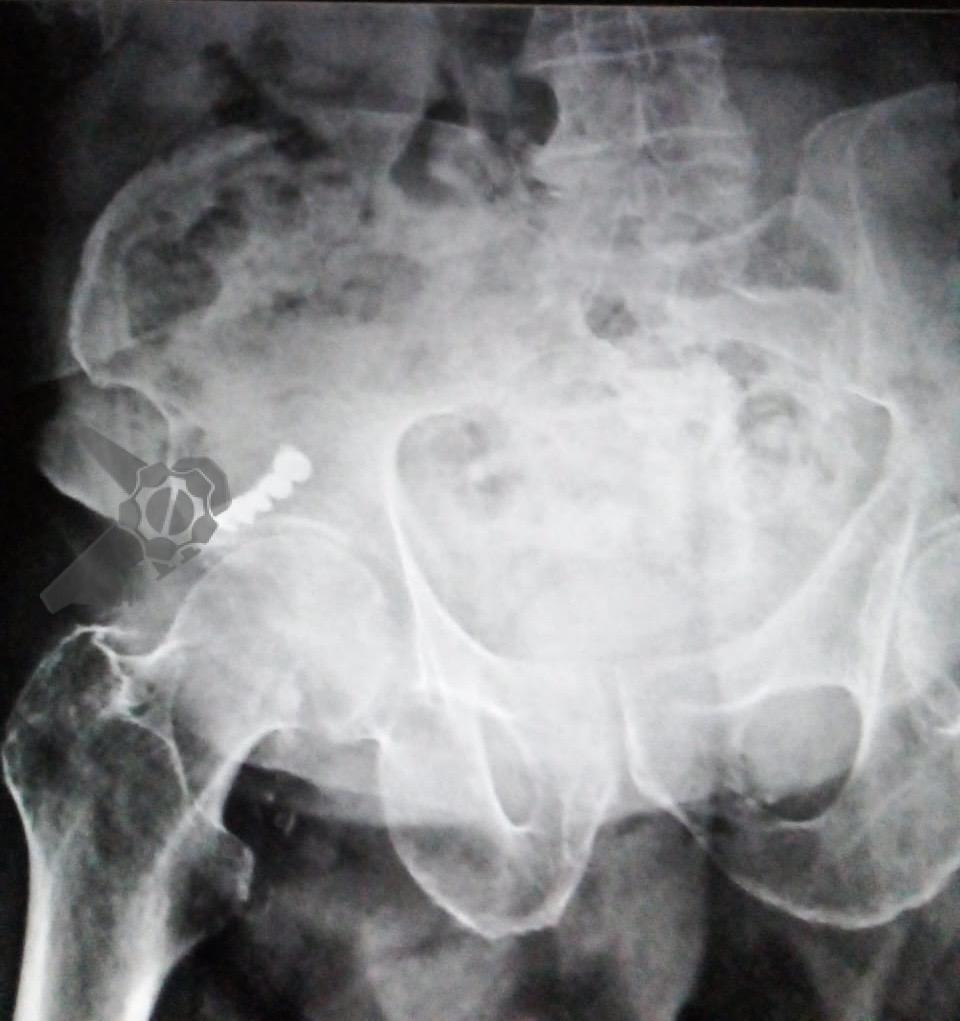
Masculino, 88 anos, aposentado, apresentando quadro demencial leve, assintomático, foi encaminhado ao serviço de endoscopia após a ingestão acidental de sua prótese dentária fixa. O incidente ocorreu há 15 dias, sem eliminação do objeto nas fezes desde então. Ele buscou atendimento na unidade de emergência de sua cidade, onde uma radiografia revelou a presença do objeto na topografia da fossa ilíaca direita (foto 1). Ao exame físico, não havia alterações relevantes com palpação do abdome inocente.
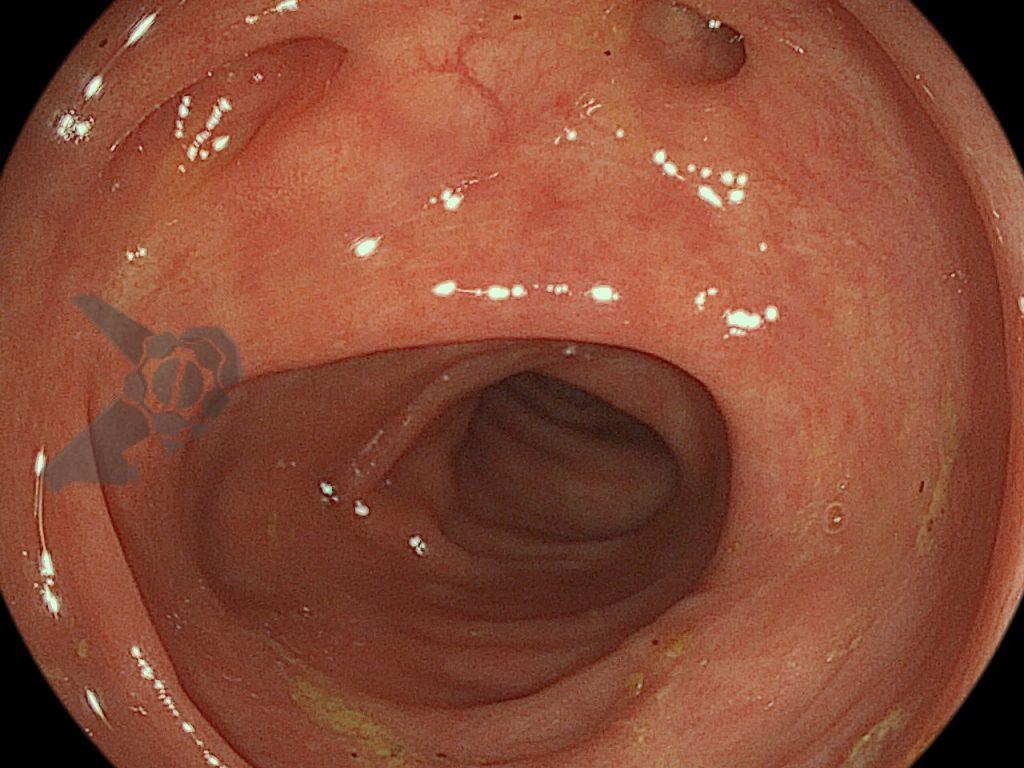
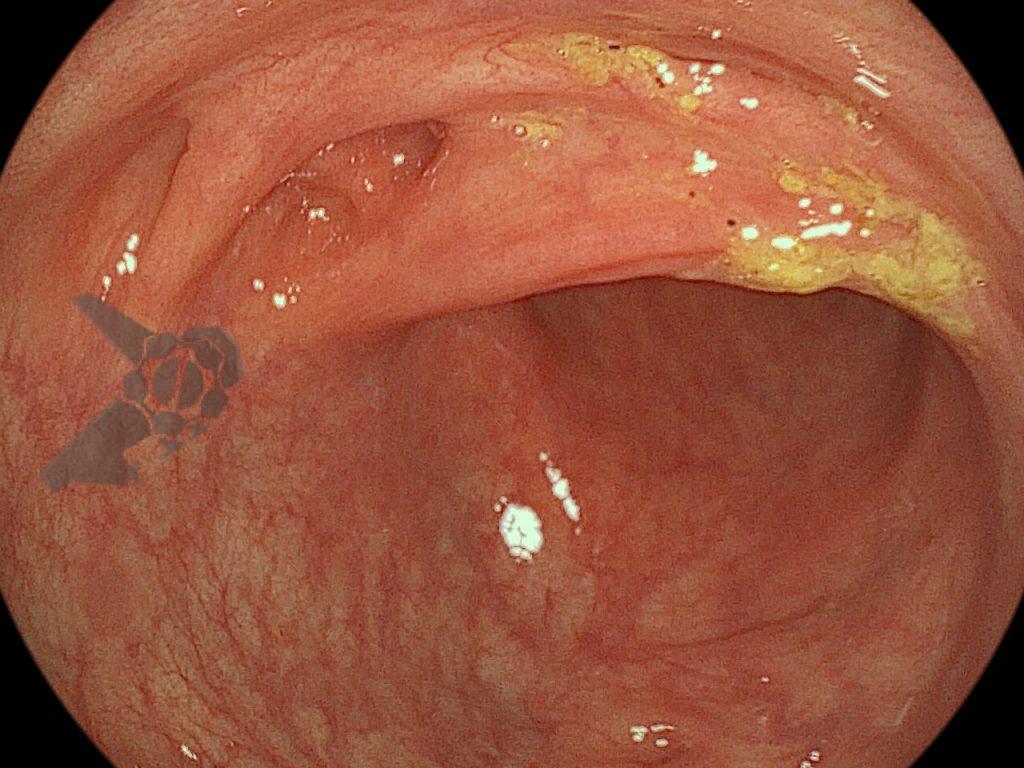
Após preparo colônico com manitol e a realização de uma nova radiografia, que não apontou qualquer mudança na posição inicial da prótese dentária desde a admissão, o paciente foi submetido a colonoscopia. Até a intubação cecal o corpo estranho não foi encontrado, com presença de doença diverticular no hemicólon esquerdo (foto 2 e 3).
Percorridos cerca de 15 cm do íleo distal, a prótese dentária foi localizada. Com o auxílio de uma alça multifilamentar, foi possível mobilizá-la e, em seguida, capturar o corpo estranho impactado, trazendo-o até o ceco (vídeo 1). A remoção cuidadosa através dos cólons foi realizada com insuflação máxima e manobras delicadas nas angulações até a extração por via retal. Durante todo o procedimento, utilizou-se CO2 como gás insuflador e foi administrado antiespasmódico (escopolamina). Na revisão pós-remoção, não havia laceração da mucosa ou sinais de perfuração nos segmentos avaliados.
A prótese mediu 3 cm sendo composta por 5 dentes com três espiculas de superfície pontiaguda (pinos de fibra de vidro), tornando o segmento envolvido na impactação vulnerável a perfuração. (vídeo 2).
Clique aqui para visualizar outro caso de corpo estranho tratado por colonoscopia.
A ingestão de corpos estranhos (CE) afeta diversos grupos etários e pode ser extremamente desafiador. Na maioria dos casos (quase 80%), não é necessária uma intervenção invasiva, já que os corpos estranhos passam pelo trato gastrointestinal (TGI) sem agravos. No entanto, cerca de 20% dos pacientes podem enfrentar complicações relativa a migração de objetos ao longo do trajeto pelo TGI, incluindo impactação (com ou sem obstrução), formação de fístulas, abscessos, sangramento e perfuração. Esta última, embora seja extremamente rara, ocorrendo em até 1% dos casos, é a complicação mais temida e potencialmente grave.
Desde o primeiro relato em 1972 da remoção bem-sucedida de um CE usando um endoscópio flexível por McKechnie et al, este método continua a evoluir. A técnica endoscópica representa uma abordagem segura e minimente invasiva, com baixa morbidade e taxa de sucesso na remoção próximo a 95%.
Entre os grupos com risco aumentado para ingestão acidental de corpos estranhos estão crianças, idosos, pessoas com transtornos psiquiátricos, aqueles sob intoxicação (alcoólica/entorpecentes), além dos indivíduos encarcerados (proposital para ganho secundário). Adultos e idosos, como no relato do caso, com problemas bucais e dentários (p. ex. usuários de próteses), estão particularmente expostos a ingestão acidental de CE devido a dificuldades mastigatórias e à redução da sensibilidade da cavidade oral.
Os segmentos do TGI mais expostos à perfuração por CE são aqueles estreitados e com angulações naturais. Por essa razão possuem risco aumentado os esfíncteres esofágicos superior e inferior, o piloro, o duodeno, a válvula ileocecal, o apêndice e o cólon sigmoide. Quando o objeto ultrapassa o canal pilórico o intestino delgado se torna particularmente vulnerável devido ao seu lúmen ser relativamente reduzido. Pacientes com histórico cirúrgico abdominal (com anastomoses/aderências), doença diverticular, bem como massas intra-abdominais, merecem atenção especial.
Existem diretrizes claras para as indicações de intervenções endoscópicas quando o objeto se encontra no trato gastrointestinal proximal ao ligamento de Treitz. No entanto, atualmente, há evidências limitadas sobre o papel da colonoscopia após a migração distal de corpos estranhos para o íleo e cólon, assim como escassos protocolos sobre o manejo para remoção desses objetos.
Quando optado pelo tratamento conservador, em assintomáticos, o monitoramento por até uma semana pode ser realizado, visto que a maioria dos corpos estranhos ingeridos é excretada sem intercorrências pelo trato digestivo. A radiografia seriada a cada 72 horas é uma estratégia para acompanhar a progressão do CE ao longo do TGI.
As indicações para a intervenção cirúrgica após ingestão de corpos estranhos incluem: (1) falha na remoção endoscópica, (2) inaptidão do paciente para endoscopia, (3) presença de complicações graves (perfuração, sangramento maciço, sinais de peritonite, abscessos cavitários, etc.).
Avaliar as características do corpo estranho ingerido como sua forma, quantidade, tamanho, superfície, consistência, mobilidade, entre outros, é crucial ao considerar a remoção colonoscópica, a fim de traçar uma estratégia terapêutica e prever possíveis complicações. Esse risco aumenta consideravelmente quando o objeto é alongado e possui uma superfície pontiaguda, como espinhas de peixe, ossos de galinha ou palitos de dente. Há uma variedade de dispositivos disponíveis para auxiliar a extração, e a escolha deve ser feita após análise minuciosa das peculiaridades do corpo estranho. Estes dispositivos incluem CAPs (rígidos, flexíveis, plásticos, de látex), alças e pinças de diferentes tamanhos e formatos, rede coletora (Roth Net), overtube, fio guia, entre outros. A radiografia e a tomografia de abdome são importantes para definir o posicionamento do CE ao longo do TGI, se possível, deve ser realizado antes e após o preparo do cólon, para se certificar que não houve mudança do posicionamento do objeto.
Com relação ao intestino delgado a válvula ileocecal constitui uma barreira anatômica natural a progressão. A enteroscopia, quando disponível, pode ser utilizada para recuperar corpos estranhos nessa topografia.
A abordagem endoscópica para remoção de corpos estranhos é uma alternativa segura e eficaz quando a intervenção se torna imperativa. Apesar de não estar isenta de riscos, sua natureza menos invasiva e traumática, em comparação com procedimentos cirúrgicos, a torna uma opção a ser considerada, especialmente para pacientes sem sinais de complicações, conforme exemplificado neste caso.
Vieira B B. Remoção endoscópica de corpo estranho impactado no íleo distal: relato de caso e revisão da literatura. Endoscopia Terapeutica 2024 vol 1. Disponível em: https://endoscopiaterapeutica.net/pt/?p=18662
Paciente masculino 73 anos, obeso, hipertenso e diabético, submetido a cirurgia de quadril devido a fratura no colo do fêmur. No segundo dia de pós-operatório, iniciou com quadro de dor e distensão abdominal associado a parada de eliminação de fezes. Rx de abdome demonstrava dilatação difusa do cólon, sem dilatação significativa de alças de delgado. Foram iniciadas, então, medidas de suporte clínico, como jejum, hidratação, passagem de sonda nasogástrica e suspensão de medicamentos opioides. Paciente evoluiu sem melhora clínica, com piora da distensão abdominal sendo submetido a TC de abdome no quinto dia de pós-operatório. Exame mostrou grande dilatação difusa de todo cólon, com diâmetro estimado do ceco de 14 cm. A equipe de endoscopia foi chamada para realização de colonoscopia descompressiva.
Paciente de 16 anos, feminina, portadora de síndrome de West, desnutrida com importante sequela motora e retardo mental em decorrência de doença de base caracterizada por crises convulsivas frequentes desde a infância. Genitora relata que a paciente foi admitida em unidade de emergência com quadro de vômitos, dor abdominal, diarreia há cerca de 4 dias, tendo recebido tratamento com hidratação, analgesia e lavagem retal, sendo liberada em sequência. A paciente permaneceu com os mesmos sintomas, tendo evoluído com piora importante da distensão abdominal levando a novo atendimento em unidade de emergência após 3 dias.
Na admissão a paciente encontrava-se caquética, com posição viciosa de membros, taquipneica, murmúrio vesicular abolido em bases, padrão respiratório de esforço, taquicárdica, hipotensa com distensão abdominal severa sendo possível identificar mosqueamento cutâneo em região do abdômen, dor abdominal difusa sem sinais de irritação peritoneal, ausência de ruídos hidroaéreos, toque retal sem fezes ou lesões.
Os principais exames laboratoriais evidenciam hemoglobina 7,7 g/dl, leucograma 26.850 com 8% de bastões, plaquetas 173.000 Uréia 20 Creatinina 0,5. Na gasometria arterial pH 7,48 com PCO2 19,8 bicarbonato de 19,1 e lactato de 3,5mmol/l.
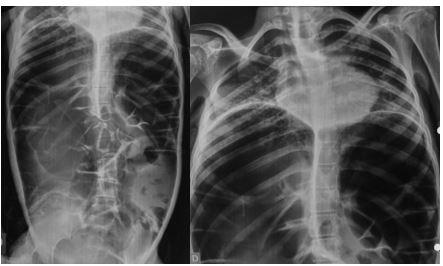
Radiografia simples de abdome demonstra congestão pulmonar, redução dos espaços intervertebrais em tórax, distensão abdominal severa, ausência de pneumoperitônio (Figura 1). A tomografia de abdome corrobora os achados do raio X simples de abdome, evidenciando ainda diâmetro do cólon de aproximadamente 13cm (Figura 2).
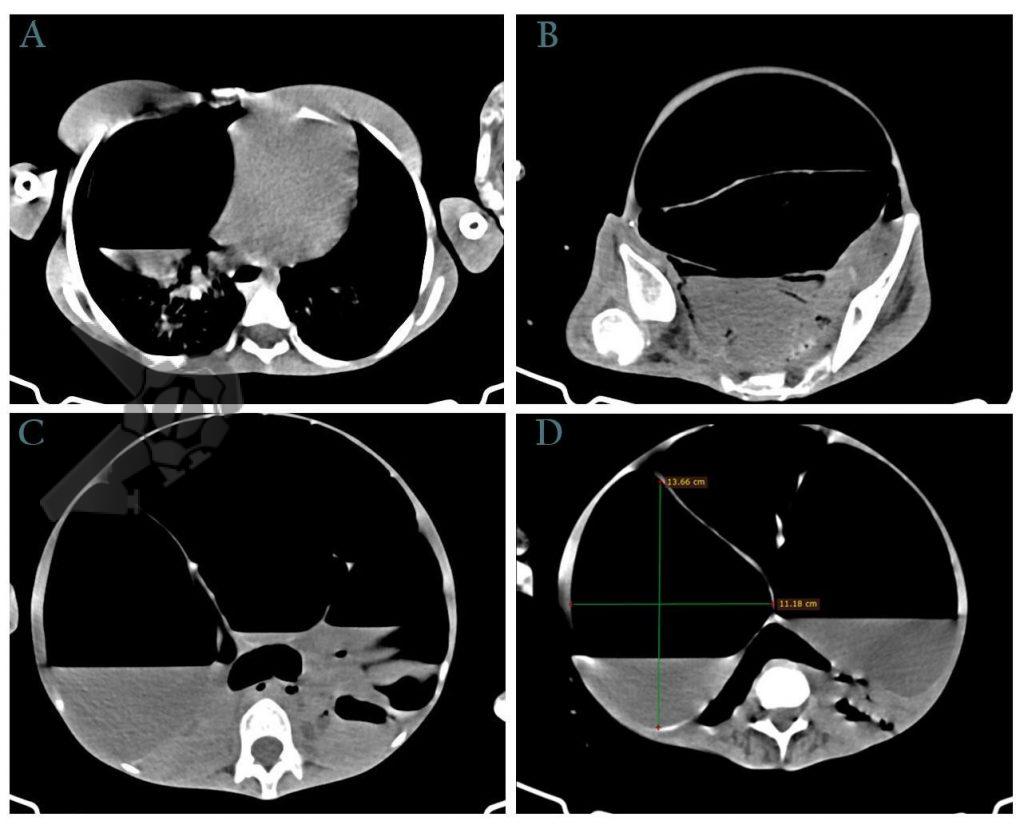
Após discussão multidisciplinar, optou-se pela tentativa de colonoscopia descompressiva, com equipe cirúrgica em sala para abordagem em caso de não resolução ou complicações.
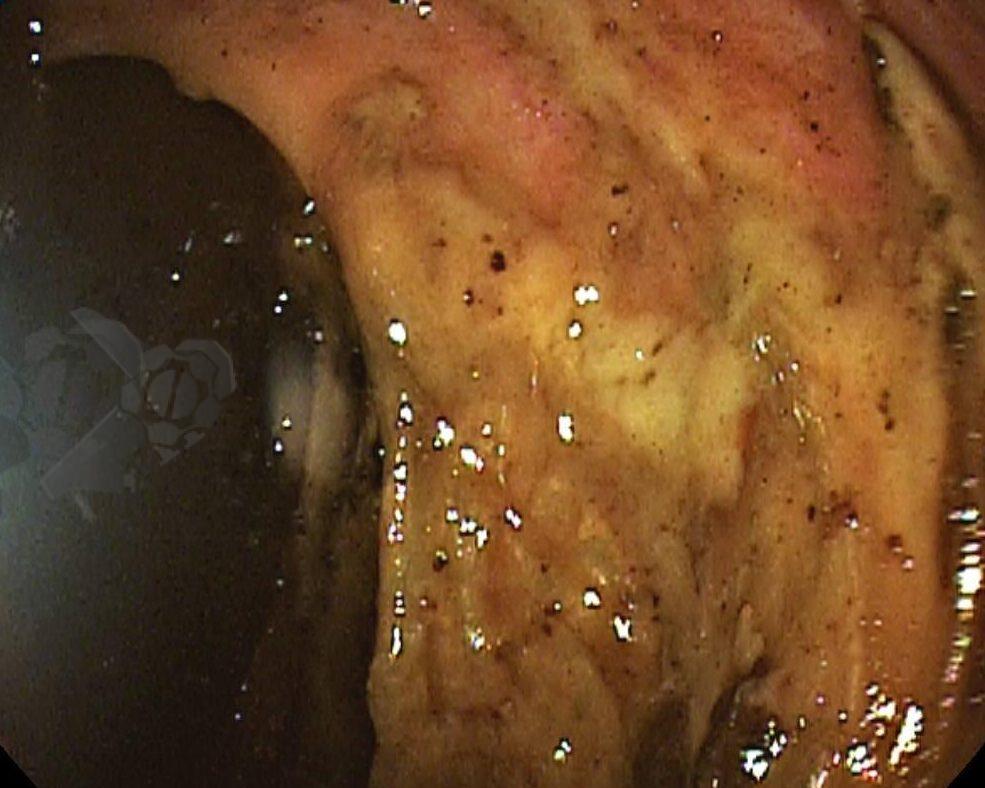
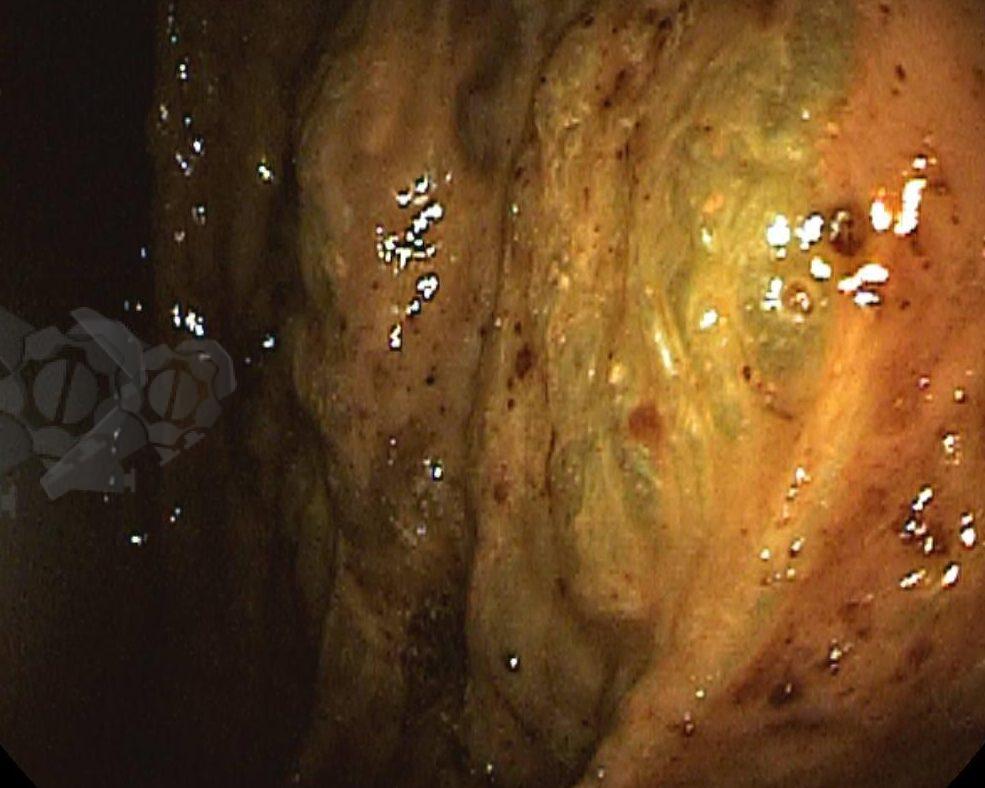
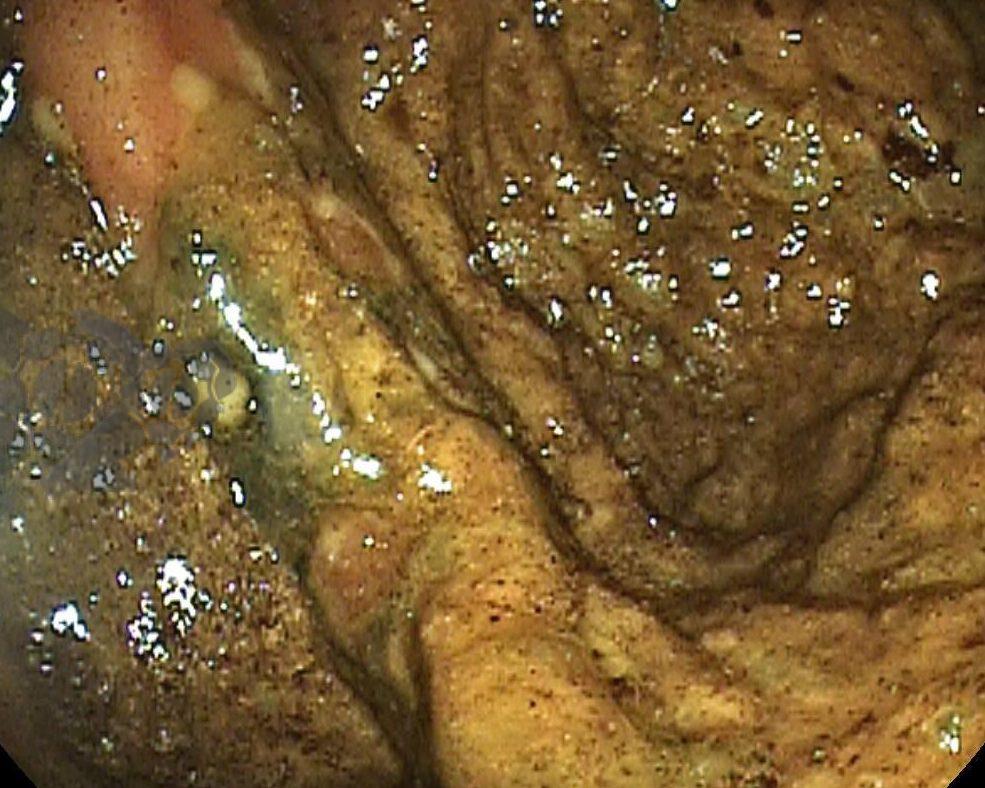
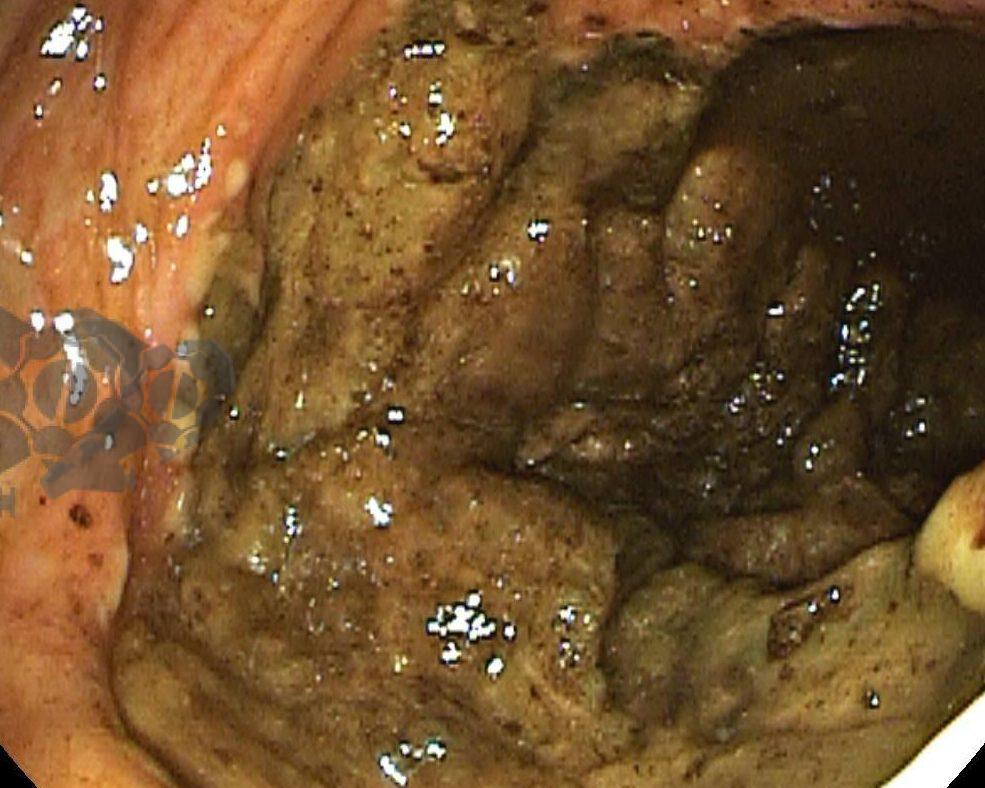
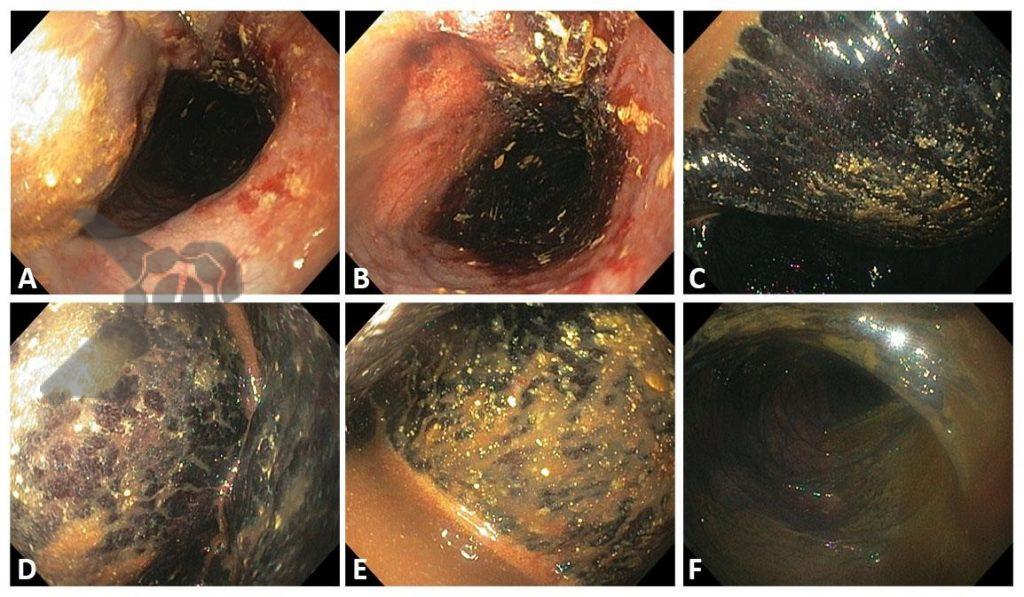
Durante a colonoscopia percebe-se presença de resíduos fecais em moderada quantidade, distensão não importante de reto e sigmoide. Progressão do aparelho por um segmento relevante sendo evidenciados resíduos fecais, mucosa com áreas de enantema e certa friabilidade. Em determinado ponto, não sendo possível identificar qual segmento colônico, o aparelho atingiu uma área de torção com mucosa difusamente violácea, congesta. Após a transposição desta área o aparelho atinge cólon extremamente distendido com mucosa enegrecida, friável, indicando isquemia e necrose (Figura 3). Aspirado mais de 2000ml de líquido de estase e gás com evidente redução do volume abdominal da paciente (Figura 4).
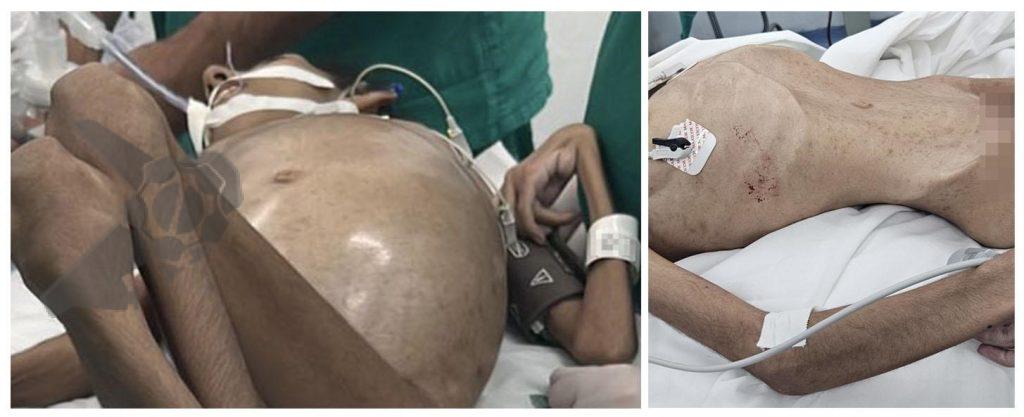
Equipe cirúrgica procedeu então laparotomia de emergência com achado de líquido citrino em cavidade abdominal, cólon sigmóide e descendente preservados; volvo em cólon transverso o qual apresentava isquemia irreversível e necrose; ceco e cólon ascendente distendidos porém sem evidências de isquemia (Figura 5). O procedimento cirúrgico realizado foi a ressecção do cólon transverso com colostomia e sepultamento do coto distal.
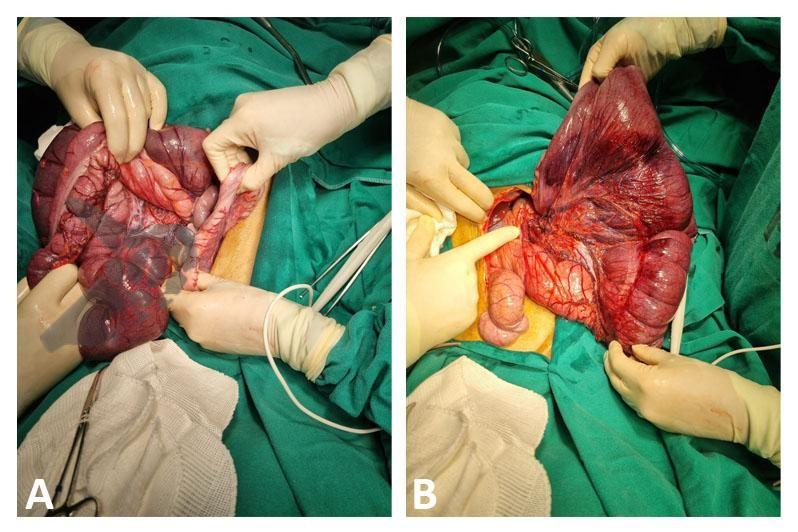
Paciente encaminhada para UTI no pós operatório, já em uso de drogas vasoativas, mantendo taquicardia, hipotensão e necessidade de ventilação mecânica. Durante sua evolução manteve-se com abdome flácido, colostomia de bom aspecto e funcionante. Seu quadro clínico no entanto sempre persistiu grave, com tentativas falhas de desmame de ventilação mecânica, agravamento das crises convulsivas já frequentes antes do internamento hospitalar. Neste cenário, considerando gravidade de doença de base em si com paciente apresentando convulsões frequentes, totalmente dependente para cuidados, com disfagia, dupla incontinência e a gravidade da paciente no momento, equipe médica e familiares optaram por manter medidas proporcionais de cuidado. Paciente faleceu no 11º dia de internamento hospitalar.
A síndrome de West corresponde a uma encefalopatia caracterizada em sua forma clássica por crises convulsivas na infância, hipsarrtimia (alterações de atividade elétrica na eletroencefalografia) e retardo do desenvolvimento psicomotor. No caso da paciente, a falta de acesso aos sistemas de saúde levaram a diagnóstico tardio e tratamento irregular determinando desenvolvimento de uma forma severa da doença com qualidade de vida limitada.
Volvos colônicos correspondem à rotação de um segmento de cólon determinando torção de seu mesentério com consequente isquemia e distensão à montante. Volvo de sigmóide é a forma mais frequente correspondendo a cerca 80% dos casos, seguido de ceco/cólon ascendente (menos de 20%) e raros casos de volvo de transverso. Os principais sintomas são dor e distensão abdominal, constipação, vômitos, interrupção de eliminação de fezes e flatos. Nos casos mais graves há perfuração de alça com sinais de peritonite e choque séptico. A evolução pode ser lenta com episódios recorrentes de dor alternados com remissão sintomática por distorção espontânea do volvo.
A radiografia simples de abdome pode evidenciar o sinal clássico em “grão de feijão” além de permitir a avaliação da extensão da obstrução, distensão concomitante de delgado e presença ou não de pneumoperitônio. A tomografia de abdome pode evidenciar os mesmos sinais e trazer maior detalhamento dos segmentos colônicos com medidas precisas do calibre do órgão, fato este relevante pois há risco aumentado de perfuração quando o diâmetro cecal é superior a 12 cm.
Pacientes sem sintomas ou sinais radiológicos sugestivos de perfuração devem ser submetidos a colonoscopia para desobstrução do volvo. O preparo anterógrado é contraindicado, no entanto a lavagem retal pode ser utilizada. O exame deve ser realizado com mínima insuflação sendo necessário ultrapassar a região da torção, descomprimir o cólon (aspirando o conteúdo líquido e removendo o gás). A avaliação da viabilidade da mucosa é essencial, buscando sinais de isquemia ou perfuração para determinar se será necessário realizar tratamento cirúrgico imediato ou não. A taxa de sucesso da colonoscopia descompressiva é alta (60-95%), no entanto a taxa de recorrência a longo prazo é elevada (43 a 75%) caso o paciente não seja submetido a tratamento cirúrgico posteriormente.
Pacientes com sinais de perfuração, com insucesso técnico na descompressão endoscópica ou que apresentem sinais de inviabilidade do cólon durante colonoscopia devem ser submetidos a cirurgia de urgência com ressecção do segmento com isquemia irreversível.
O tratamento cirúrgico de escolha, posterior a colonoscopia descompressiva bem sucedida, é a ressecção do segmento colônico envolvido. Tratamento cirúrgico sem ressecção (pexia) possui taxa de recorrência variável na literatura podendo chegar a 29-36%, devendo ser considerado apenas em casos selecionados.
Clique aqui para saber mais sobre o assunto com outras imagens como o sinal do “grão de café” e publicações sobre volvo colônico.
Ferreira F. Volvo de transverso em paciente com Síndrome de West. Endoscopia Terapeutica 2024 vl. 01. Disponível em: https://endoscopiaterapeutica.net/pt/?p=18604
O guideline da ESGE publicado em 2022 recomenda que ressecções R0 em monobloco, com invasão submucosa superficial (sm1), bem a moderadamente diferenciadas, sem invasão linfovascular e sem budding de graus 2 ou 3, devam ser consideradas curativas.1
Isto pois, tumores com pelo menos uma característica citada acima, podem estar associados a um risco acometimento linfonodal de até 20%.2 Dessa forma, tradicionalmente cerca de 65% desses pacientes são submetidos a ressecção cirúrgica.3
No entanto esse é um conceito que está sendo revisto. O mesmo guideline, apesar da baixa qualidade de evidência nesse quesito, sugere que pacientes ressecções R0 atendendo ao critério único de alto risco de invasão submucosa mais profunda que sm1 (bem a moderadamente diferenciada, sem invasão linfovascular e sem budding 2 ou 3), possam ser submetidos a quimioradioterapia ou mesmo apenas acompanhamento, após uma avaliação individual e multidisciplinar.
Essa conduta conservadora já é muito utilizada especialmente para reto. Apesar de lesões nessa topografia serem um fator de risco para acometimento linfonodal (OR 1,36, P = 0,003), as opções cirúrgicas são também mais agressivas do que no cólon (incluindo amputação abdominoperineal) com taxas de mortalidade de 3% e morbidade de até 40%.1,4,5
Com objetivo de avaliar pacientes submetidos a resseções R0 de alto risco, um recente estudo publicado comparou retrospectivamente entre 14 centros terciários, pacientes submetidos a complementação cirúrgica versus seguimento conservador (vigilância).6
Foram incluídos pacientes com pelo menos um dos fatores de risco citados e excluídos pacientes sem condições cirúrgicas com objetivo de homogeneizar os grupos. O grupo cirúrgico incluiu 107 pacientes e apresentou mais comumente riscos histopatológicos múltiplos e localização em cólon. No grupo vigilância foram incluídos 90 pacientes, sendo nestes mais prevalentes comorbidades clínicas e utilização da técnica ESD.6
Após um balanceamento das características dos grupos afim de se evitarem vieses, não foram encontradas diferença significativas nas taxas de morte e recorrência do câncer (taxa de risco ponderada 0,95; IC 95%, 0,52 -1,75). Não foram também encontradas diferenças significativas na sobrevida global entre os 2 grupos (1,19; IC 95%, 0,49-2,88) ou na taxa de morte e recorrência de câncer à distância (1,17; IC 95%, 0,66-2,1).6
Em uma análise de sensibilidade restrita a pacientes submetidos à ressecção em monobloco, comparando 87 pacientes submetidos à cirurgia com 75 pacientes controle, não foram encontradas diferenças significativas na taxa de morte e recorrência de câncer entre os grupos (1,42; IC 95%, 0,66-3,04).6
Apesar do contraste destes resultados com trabalhos anteriores, em um recente estudo multicêntrico retrospectivo, que incluiu mais de 200 pacientes submetidos a ESD com achados histopatológicos de alto risco, foram obtidos desfechos semelhantes.7 Numa meta-análise publicada, o risco de recorrência à distância da ressecção endoscópica comparado com ressecção endoscópica seguida de cirurgia adicional, foi também semelhante, 7,2% e 5,6%, respetivamente.8
Mesmo com maior presença de acometimento linfonodal nas ressecções de alto risco, estes pacientes não apresentam pior prognóstico clínico. A teoria que explica isso consiste em que os gânglios preservados são importantes para a educação imunológica, contribuindo para erradicação tumoral local. Entretanto esses achados não foram evidenciados em reto, demonstrando provavelmente um maior efeito imune no cólon.6
Novos estudos sugerem que pacientes com ressecções T1 de alto risco podem não se beneficiar de cirurgia adicional, especialmente na indicação de cirurgias retais ou em pacientes de alto risco cirúrgico. Pacientes devem estar sempre envolvidos na decisão, sendo informados sobre os riscos associados à cirurgia em relação à sua idade e comorbidades e os riscos de recorrência do câncer no longo prazo. Por outro lado, uma localização retal parece associado a um maior risco de recorrência, o que pode necessitar de tratamento adjuvante.
Ressecção R0 T1 de alto risco, em casos selecionados, pode ser optado pela vigilância ao invés do procedimento cirúrgico. Entretanto lesões de reto ainda devem receber tratamento adjuvante.
Oliveira JF. Ressecções de cólon com invasão acima de 1000 micras (sm1), acometimento linfovascular, pouco diferenciadas e budding de alto risco, tem sempre indicação cirúrgica? Endoscopia Terapeutica 2024, vol 1. Disponível em: https://endoscopiaterapeutica.net/pt/uncategorized/resseccoes-de-colon-com-invasao-acima-de-1000-micras-sm1-acometimento-linfovascular-pouco-diferenciadas-e-budding-de-alto-risco-tem-sempre-indicacao-cirurgica/
Paciente do sexo feminino, 4 anos de idade, apresentando episódios recorrentes de sangramento retal (hematoquezia) há 11 meses, sem instabilidade hemodinâmica ou necessidade de hemotransfusão. Histórico atual de intolerância à lactose, sem outras doenças crônicas ou cirurgias. Apesar da exclusão de lacticínios e derivados da dieta, os episódios de sangramento persistiram.
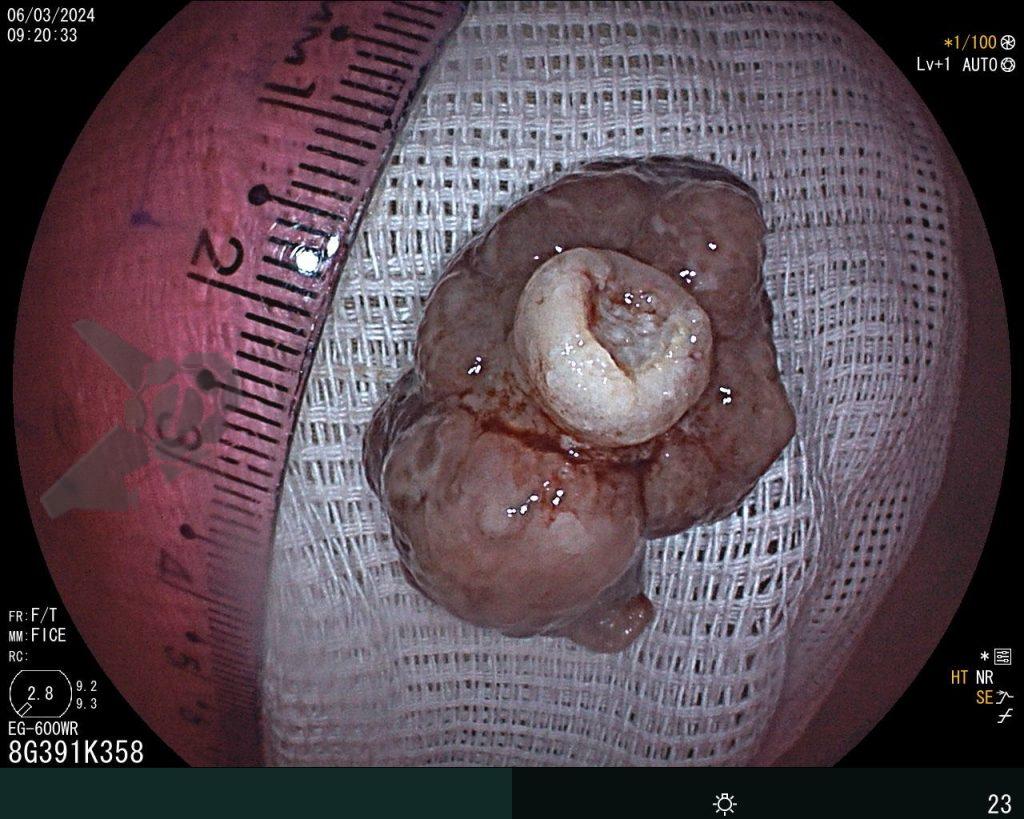
Realizou colonoscopia, ambulatorialmente, onde foi identificado um pólipo pediculado lobulado no cólon descendente distal, com mucosa congesta e edematosa, coberta por fibrina e áreas hiperêmicas, com padrão de criptas tipo II de Kudo (Fig.1-2). O pólo cefálico tinha aproximadamente 3 cm de diâmetro, com um pedículo longo e largo (Fig.3-4). Foi realizada a polipectomia utilizando alça diatérmica, com ressecção completa em monobloco (Fig.5-6). Optou-se pelo fechamento do sítio da excisão com um endoclipe, sem complicações (Fig.7-8). Não houve achados adicionais nos demais segmentos estudados. O procedimento teve duração de 30 minutos, com alta da paciente após sua conclusão.
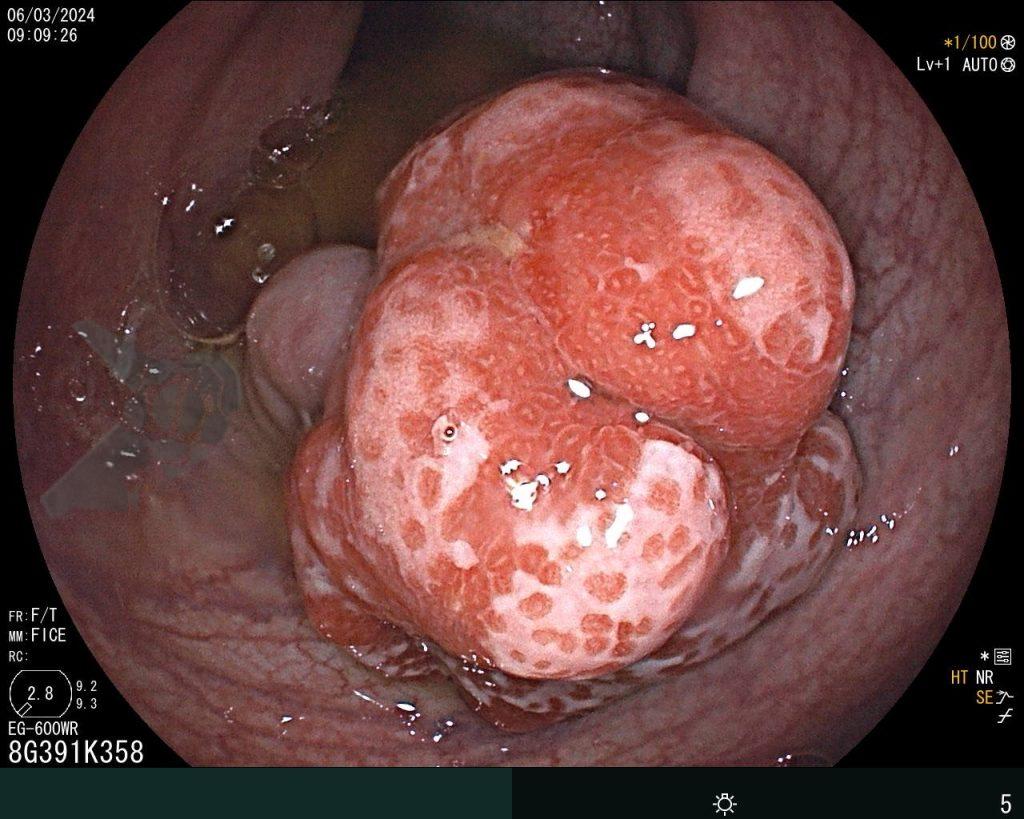
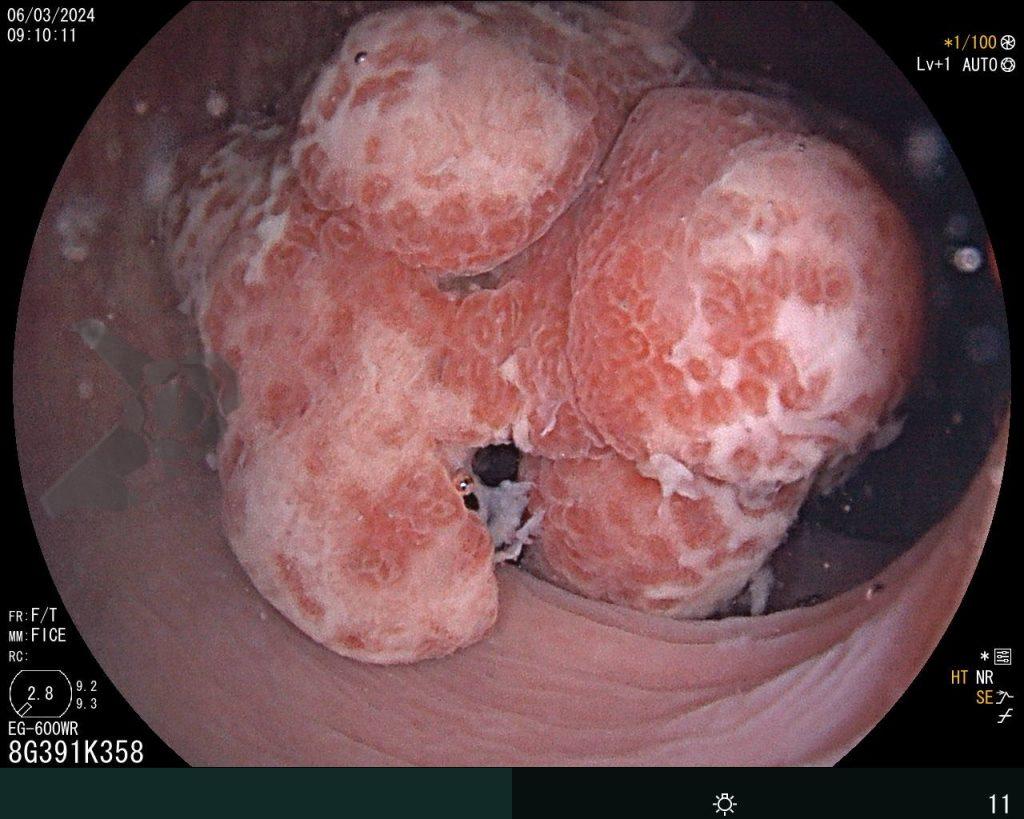
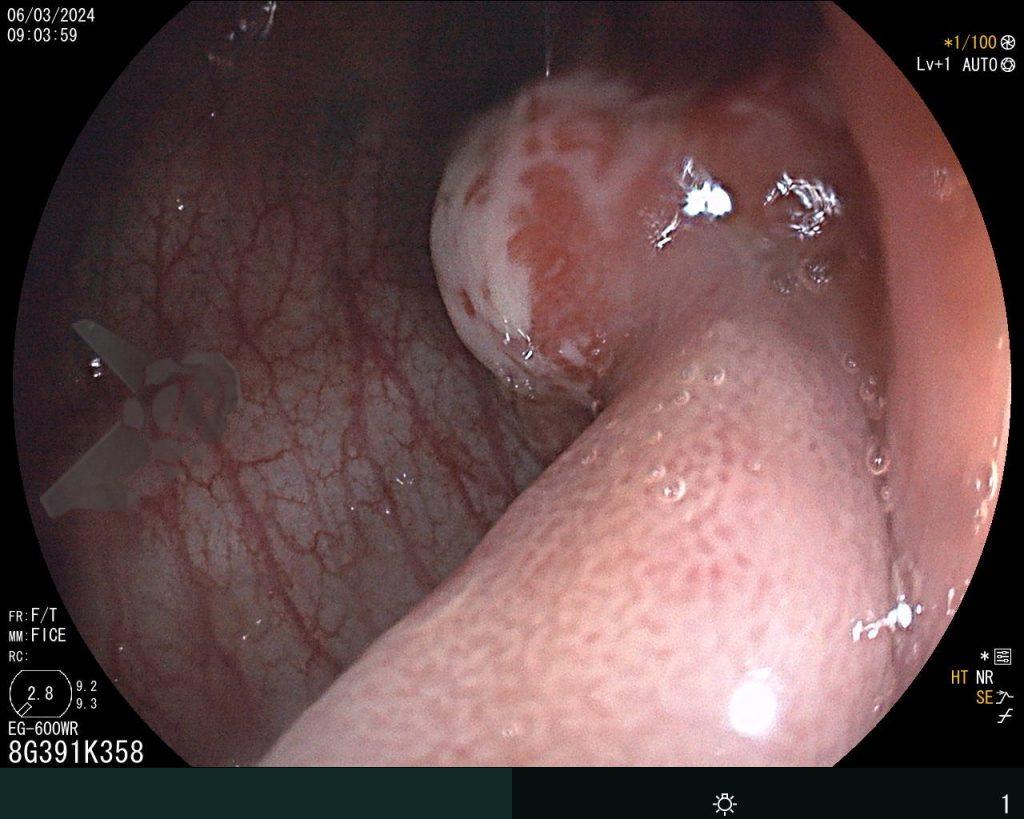
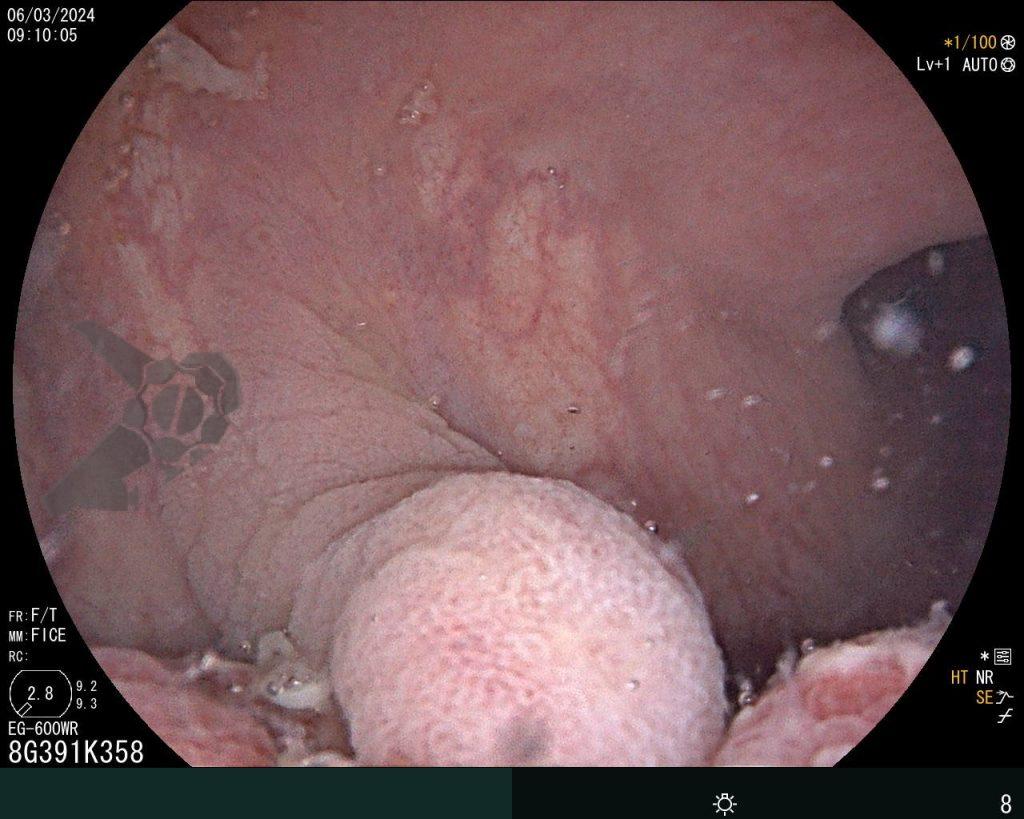
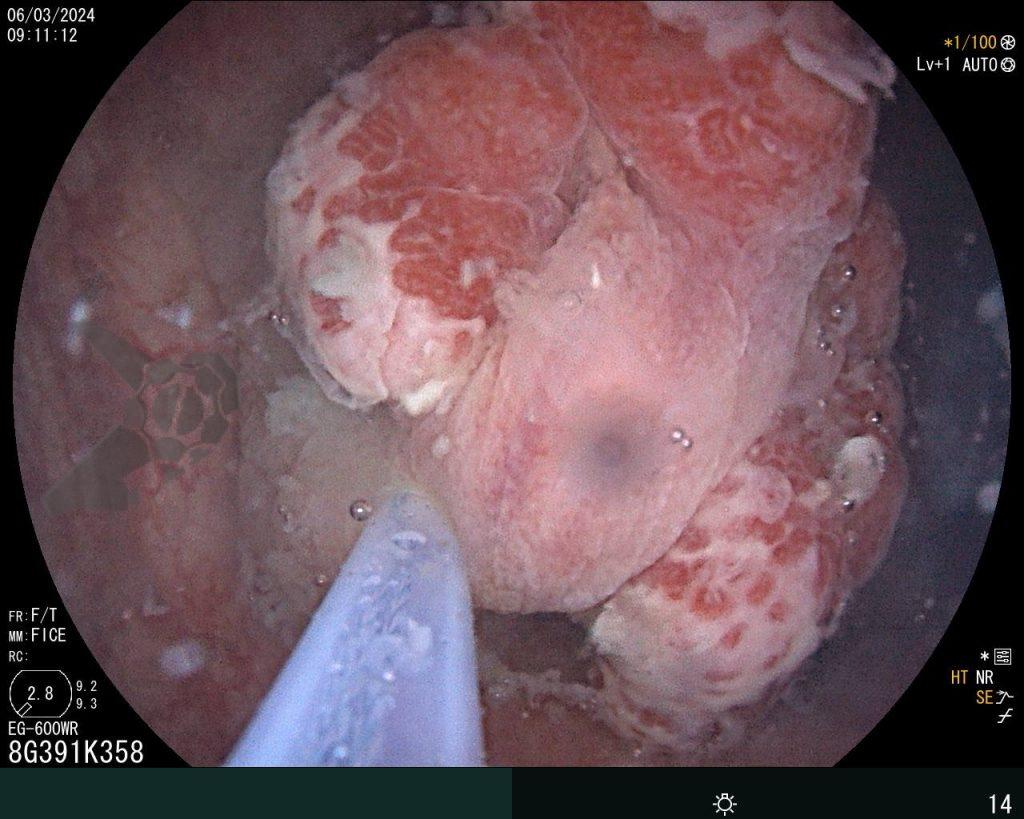
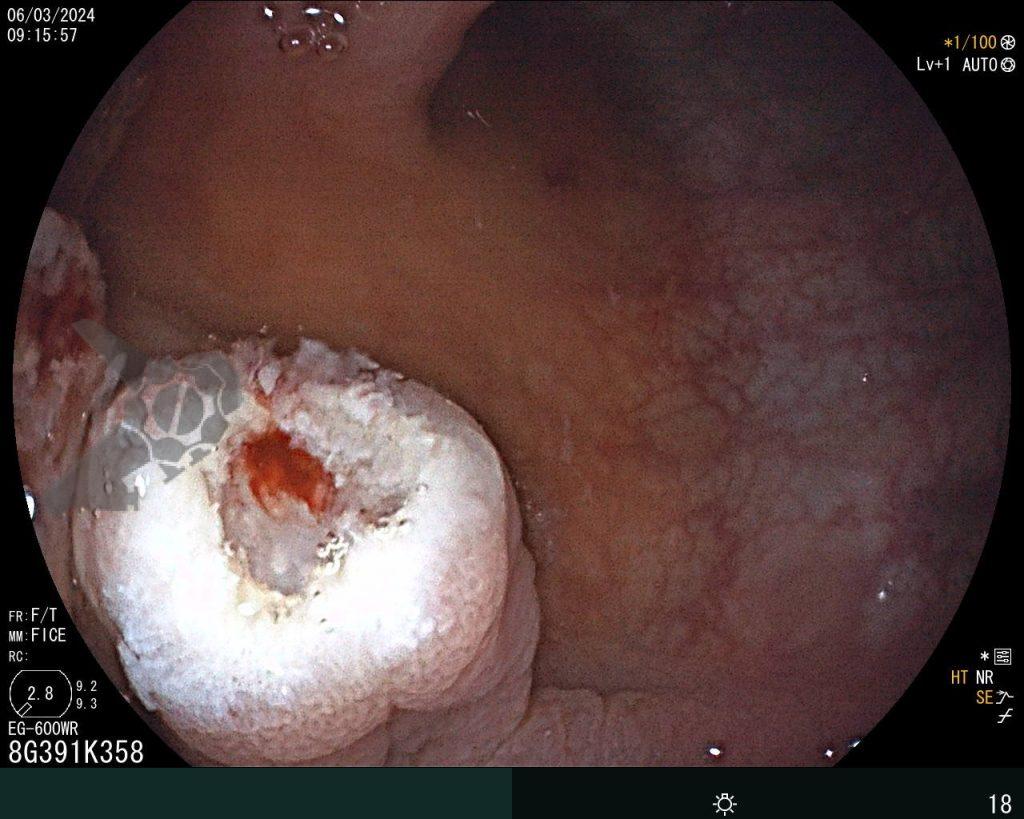
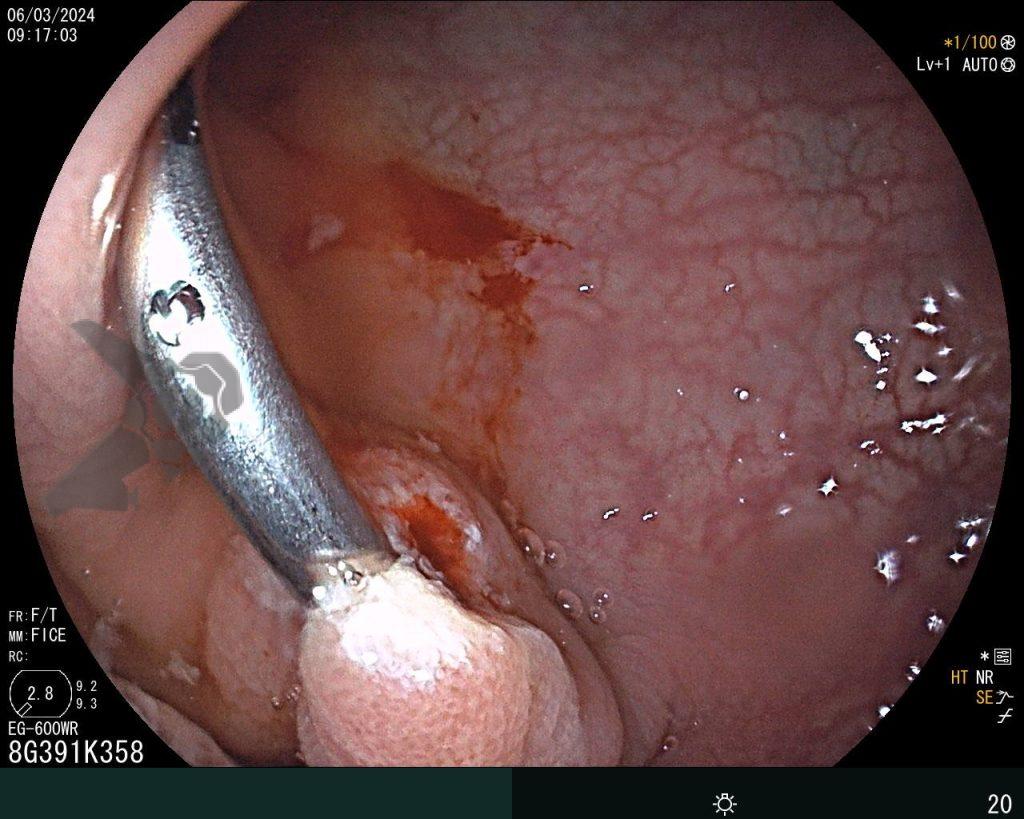
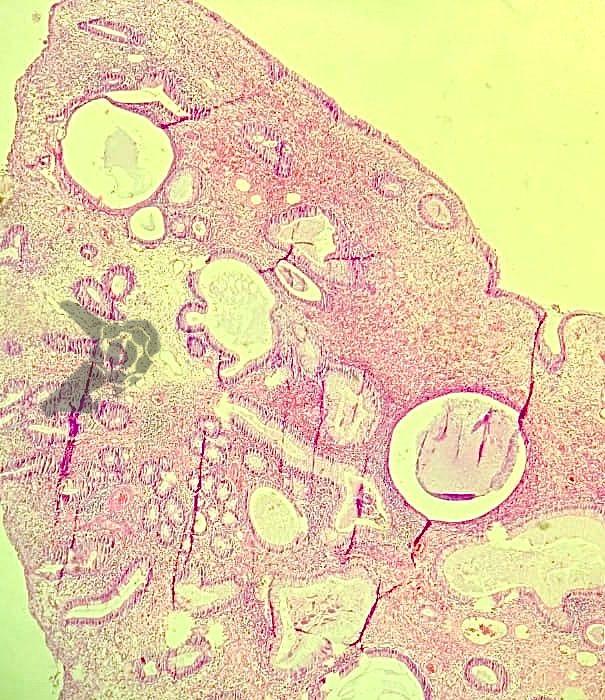
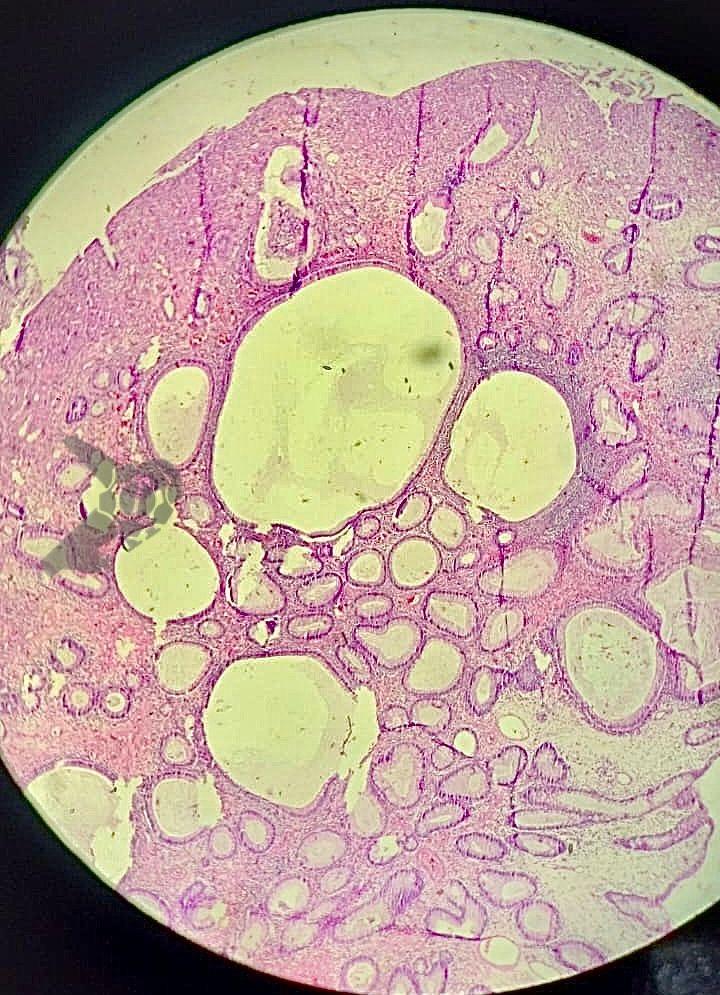
O exame anatomopatológico revelou tratar-se de uma lesão polipóide hiperplásica benigna, com estroma frouxo (Fig.9-10). As estruturas glandulares estavam hiperplásicas, variando de tamanho e ocasionalmente dilatadas cisticamente, sem apresentar atipias. O diagnóstico é compatível com pólipo hamartomatoso juvenil.
As principais causas de hemorragia digestiva baixa, em crianças de 2 a 12 anos, incluem fissura anal, pólipo juvenil, enterocolite infecciosa e DII (Doença Inflamatória Intestinal). Mais raramente, podem estar relacionadas à úlcera retal solitária, duplicação intestinal, púrpura de Henoch-Schönlein, síndrome hemolítico-urêmica e malformação vascular colônica.
A presença de pólipo hamartomatoso juvenil solitário (esporádico), em crianças com menos de 10 anos de idade, tem incidência de até 2%. O termo “juvenil” refere-se ao tipo anatomopatológico do pólipo e não à idade de aparecimento. Apesar de serem infrequentes, também são descritos casos em adultos. Esses pólipos não são neoplásicos, apresentando histologicamente espaços císticos dilatados, inflamação, aumento da vascularização e áreas de destruição epitelial.
Distribuem-se por qualquer segmento colônico, com predileção pelo hemicólon esquerdo, sendo a topografia retossigmoidea a mais comum. O tipo pediculado é o mais frequente. Apesar da denominação “pólipos juvenis solitários”, eles podem ser únicos ou ocorrer em até 5 pólipos, sendo que 50% das crianças com essa condição apresentam mais de um pólipo. A verdadeira incidência de pólipos juvenis solitários é subestimada devido à sua apresentação clínica discreta e, geralmente, indolor, além da dificuldade do acesso a exame confirmatório.
O tipo pediculado é o mais frequente. Eventualmente, pode ocorrer torção no próprio eixo e autoamputação do pólipo, com consequente hemorragia, que pode ser volumosa.
Ao exame, o tamanho varia de 1 a 3 cm de diâmetro, com friabilidade associada, o que leva ao sangramento retal. Pode haver prolapso do pólipo através do ânus e, raramente, dor abdominal. Um terço das crianças apresenta-se com anemia microcítica em consequência do sangramento crônico, fato que pode induzir erroneamente o diagnóstico de doença inflamatória intestinal e postergar a solicitação da colonoscopia.
É essencial frisar que o pólipo hamartomatoso juvenil solitário difere da síndrome da polipose juvenil familiar (SPJ). A SPJ também é caracterizada pela presença de pólipos hamartomatosos contudo trata-se de uma doença genética autossômica dominante, causada por mutações nos genes SMAD4 e BMPR1A, que confere um risco aumentado de desenvolver câncer no trato gastrointestinal ao longo da vida. A SPJ abrange a Síndrome da Polipose Juvenil, a Síndrome de Peutz-Jeghers e a Síndrome do Tumor Hamartomatoso PTEN. O diagnóstico da SPJ requer o preenchimento de um dos seguintes critérios:
A SPJ familiar é uma condição pré-neoplásica, distinguindo-se do pólipo hamartomatoso solitário, que é esporádico, benigno e apresenta baixo risco de malignização.
A colonoscopia é uma ferramenta amplamente utilizada em todo o mundo para diagnosticar sangramentos gastrointestinais baixos e, frequentemente, serve como método terapêutico em muitos desses casos. No entanto, os exames endoscópicos pediátricos apresentam particularidades que exigem cuidados mínimos essenciais, devendo ser realizados em hospitais que possuam serviços de pediatria e anestesia preparados, tendo assegurado o apoio multiespecialidades indispensáveis ao tratamento de possíveis complicações, sobretudo quando se pratica endoscopia terapêutica. Além disso, o preparo adequado dos cólons é outro aspecto crucial, que pode representar um desafio, podendo atrasar ou adiar o acesso ao exame, diagnóstico e tratamento.
Como tratamento padrão, preconiza-se a remoção desses pólipos por via endoscópica, utilizando a técnica e os recursos adequados.
A investigação do sangramento corretal persistente em crianças com menos de 10 anos deve incluir a realização de colonoscopia. Na presença de um pólipo hamartomatoso juvenil esporádico, após a completa remoção, dado o baixo risco de transformação maligna, não há indicação de repetir a colonoscopia rotineiramente ou encaminhamento para aconselhamento genético, eliminando a necessidade de qualquer acompanhamento posterior adicional.
Vieira BB. Pólipo hamartomatoso juvenil solitário pediátrico: relato de caso e revisão de literatura. Endoscopia Terapeutica 2024, Vol I. disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/polipo-hamartomatoso-juvenil-solitario-pediatrico-relato-de-caso-e-revisao-de-literatura/
Nesse artigo, darei continuidade às dicas e truques da dissecção submucosa endoscópica – ESD (clique aqui para saber mais sobre o artigo prévio de ESD gástrica) e abordarei informações necessárias sobre a técnica de ESD de cólon.
Esse é um dos passos principais. O aparelho retificado responde aos comandos, enquanto a formação de loop leva a movimentos paradoxais, dificultando muito a ESD. Se você estiver tendo dificuldade de ver a lesão porque o aparelho está instável, é muito provável que a ESD não seja bem-sucedida. Então, não tenha medo de perder tempo retificando o aparelho para encontrar a melhor posição!
OBS: Considere usar o gastroscópio para lesões no reto e cólon esquerdo e o colonoscópio pediátrico para as lesões no cólon direito. Avalie também se a lesão é acessível com o aparelho em retrovisão, pois pode ser que seja necessário usar essa estratégia.
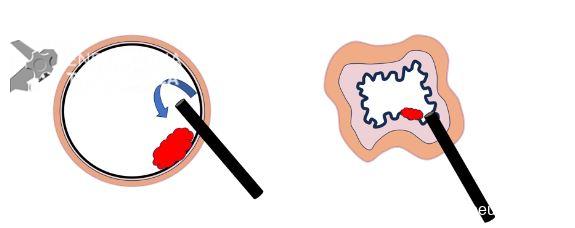
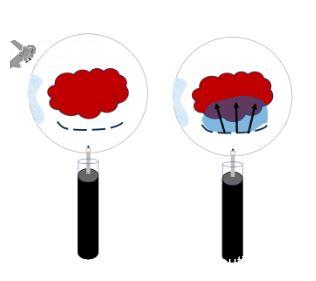
O canal de trabalho da maioria dos colonoscópios fica às 6-7hs. Posicionando a lesão nessa mesma posição, o knife fica paralelo à mucosa e a lente do aparelho permite visualizar todo o lúmen intestinal. Se a lesão está localizada às 12hs, por exemplo, o knife fica apontado para a camada muscular (aumentando o risco de perfuração) e o campo de visão é limitado (FIGURA 1).
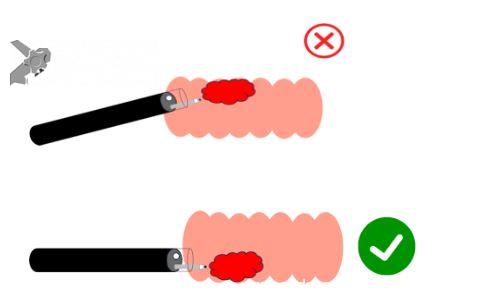
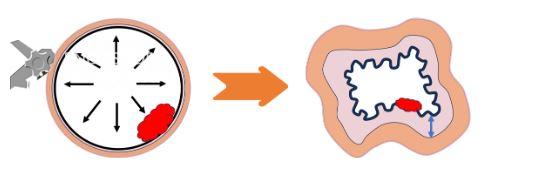
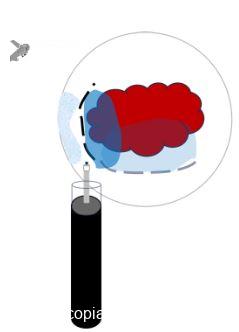
Quando trabalhamos sob baixa insuflação, o aparelho fica mais estável, pois pode se apoiar na parede do cólon (FIGURA 2). Além disso, a submucosa fica mais espessa, diminuindo o risco de perfuração (FIGURA 3).
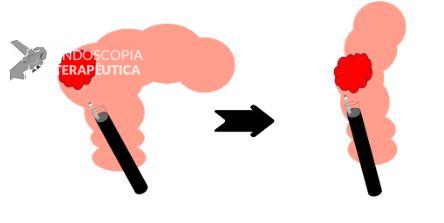
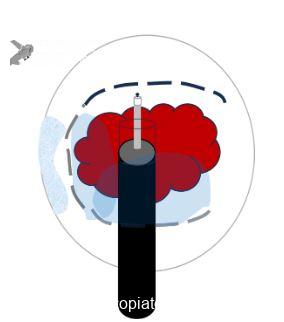
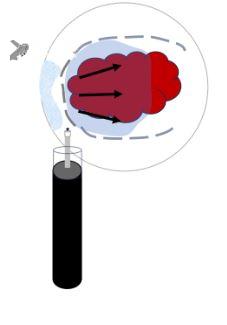
Lesões que estão em localizações difíceis, como em angulações, quando aspiramos o lúmen, estas tendem a se aproximar do aparelho, facilitando a dissecção (FIGURA 4).
Na ESD, vale a máxima: o que é difícil agora pode se tornar impossível depois. Portanto, comece a incisão nas partes mais complicadas, principalmente em localizações desafiadoras como próximas ao canal anal ou válvula ileocecal. Caso contrário, a abordagem fica muito mais difícil no final.
É de extrema importância também verificar a posição da lesão considerando o lado da gravidade. Geralmente, as partes que estão a favor da gravidade são as mais difíceis; então tentar manter a lesão no lado contralateral ajuda na dissecção. Esteja preparado (se o paciente estiver intubado, prepare o anestesista também!) para mudar o decúbito sempre que necessário!
Dois erros frequentes são injetar muito superficial ou muito profundo. As camadas superficiais (mucosa e muscular da mucosa) possuem pouco tecido elástico e muitos vasos. Dessa forma, a tensão gerada pela injeção superficial causa um hematoma que tende a persistir durante todo o procedimento. O problema desse hematoma é que ele também prejudica a identificação das margens da lesão e do plano submucoso. Caso você veja que começou a formar um hematoma, pare imediatamente a injeção e puncione outro lugar. Se já foi formado, tente atingir a submucosa profunda dissecando por debaixo dele, para que o sangue não atrapalhe a visão endoscópica.
Ao contrário, quando a injeção é muito profunda, através da muscular, o líquido pode ir para cavidade peritoneal ou para a subserosa, formando uma bolha não tão proeminente e difícil de reconhecer. Isso não é incomum de acontecer no cólon, principalmente nos locais onde as paredes são mais finas, como no cólon direito. Suspeitar que a injeção está muito profunda quando estiver injetando e não houver elevação ou escape do líquido para fora. Como a submucosa não é elevada, isso prejudica a dissecção e aumenta o risco de perfuração. Nesse caso também, assim que você perceber que a injeção foi inadequada, recue a agulha para achar o plano correto ou a remova e injete em outro ponto.
Se a injeção inicial não correr bem e você fizer isso repetidas vezes, as condições pioram. Outro erro é injetar diversas vezes em pontos diferentes, pois isso pode aumentar a chance de sangramento, além de permitir o extravasamento da solução.
Dicas para fazer uma boa injeção na submucosa:
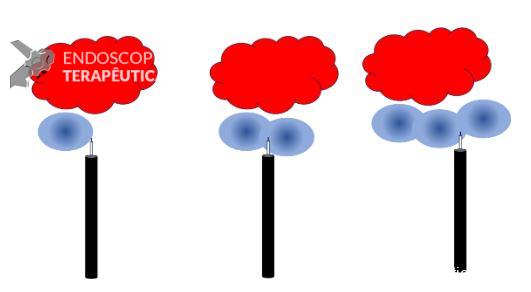
O local de injeção também é muito importante! Ao contrário da mucosectomia, quando o objetivo é elevar somente a lesão, na ESD o objetivo é obter um plano de dissecção para entrar embaixo da lesão, então a injeção não deve ser feita muito próxima à lesão (geralmente, a injeção deve ser feita a uma distância média de 1cm da lesão, para que a bolha máxima – onde será feita a incisão- fique a uma distância de 0,5cm da lesão). Lembrar que o local onde puncionamos com a agulha não é onde a bolha fica mais alta! (FIGURA 6).

OBS: Se a lesão estiver numa prega ou for grande e séssil, injete mais longe ainda (+1,5cm) para facilitar o posicionamento do endoscópio por debaixo da lesão e evitar que a muscular fique perpendicular ao plano de dissecção.
A incisão da mucosa é provavelmente o passo mais importante da ESD porque além de permitir que a ressecção seja feita com margens, permite também o acesso à submucosa.
A incisão deve ser iniciada em um ponto distante da lesão e com o instrumento perpendicular à mucosa, usando a corrente Endocut (FIGURA 7).
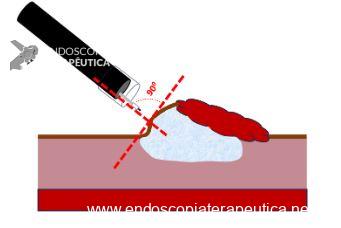
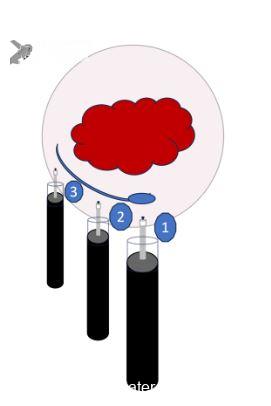
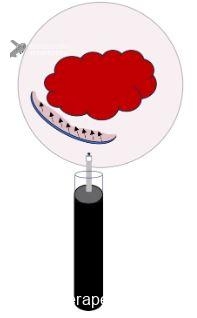
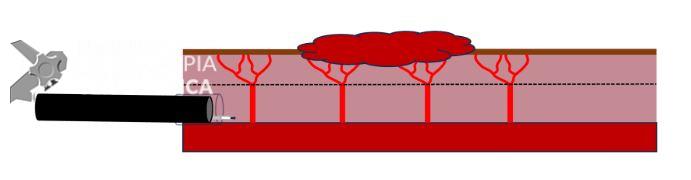
Geralmente, os vasos se ramificam perto da mucosa. Uma dissecção superficial pode danificar a lesão, enquanto a dissecção profunda pode causar perfuração. Portanto, mantenha um plano de dissecção constante na submucosa, com a camada muscular sempre à vista (FIGURA 10).
Existem várias técnicas de ESD de cólon (convencional, túnel, pocket, etc). Escolha a mais adequada de acordo com as características da lesão e sua experiência!
Clique aqui para saber mais sobre uma das principais técnicas de ESD.
Caso haja uma complicação durante a ESD, respire fundo e tente minimizar o dano. Lembre-se que a maioria das perfurações e sangramentos podem ser tratados de maneira eficaz com métodos endoscópicos!
Sangramentos são comuns, não sendo considerado uma complicação por si só. Se ocorrer durante a incisão ou a dissecção, continue cortando até expor melhor o vaso (geralmente mais umas duas pisadas no pedal), porque muitas vezes o sangramento ocorre nos vasos mais profundos ao plano de dissecção e não são facilmente visíveis. Uma dica útil é pressionar o local com o cap para obter uma hemostasia mecânica até que o local exato do sangramento seja visualizado. Tente primeiro hemostasiar com a ponta do knife (aplique a corrente nos dois lados do vaso, para só depois cortá-lo). Caso não haja sucesso, use Coagrasper ou Hot biopsy.
Nos casos de perfuração, o fechamento com clipe é o método ideal, principalmente para as perfurações pequenas (<10mm). Mantenha a calma e foque no primeiro clipe, que é o mais importante na hora de aproximar as extremidades. Algumas vezes, o clipe pode atrapalhar a continuidade da ESD, portanto, nos casos de microperfurações (<3mm), continue a dissecção e clipe somente no final. Para perfurações grandes (>10mm), tenha em mãos outros métodos de fechamento como endoloop, over-the-scope clips, suturas endoscópicas, clipes e fio.
OBS: O uso de CO2, considerado padrão para a ESD de cólon, diminui muito a morbidade e mortalidade relacionada às perfurações.
Nobre R. Endoscopia Terapeutica. ESD de Cólon – Dicas e Truques, 2024 Vol 1. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/esd-de-colon-dicas-e-truques/
A técnica da dissecção submucosa endoscópica (ESD) é um técnica avançada que permite a ressecção com margem (R0) de lesões avançadas de cólon. Existem várias técnicas de ESD de cólon (convencional, túnel, pocket, etc) e o mais importante consiste em ter uma estratégia em mente antes de começar o procedimento de ressecção. Por isso, escolha a mais adequada de acordo com as características da lesão e sua experiência!
Dando continuidade às dicas e truques do ESD gástrica (clique aqui para visualizar o artigo prévio), irei abordar a técnica tradicional de ESD de cólon.
Basicamente, esses são os passos:
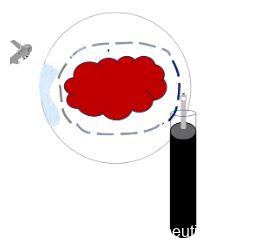
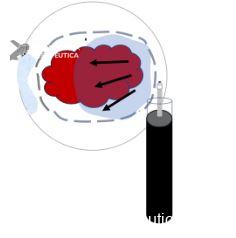
No proximo artigo falarei mais dicas e truques para realizar ESD de cólon. São 9 dicas fundamentais para uma boa execução do procedimento. Se quiser conferir agora clique aqui: https://endoscopiaterapeutica.net/pt/assuntosgerais/esd-de-colon-dicas-e-truques/
Nobre R. Técnica Convencional de ESD de cólon. Endoscopia Terapeutica, 2024 vol 1. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/tecnica-convencional-de-esd-de-colon/
O câncer colorretal (CCR) se trata de uma preocupação global com incidência ascendente com o decorrer dos anos, chegando a uma estimativa do número atual de 1.960.000 chegar a 3.600.000 casos em 2050 segundo a Organização Mundial da Saúde (OMS) [1]. A colonoscopia tem um papel importante no diagnóstico do CCR e também para diminuir sua incidência e mortalidade através do tratamento de afecções colorretais através de polipectomias e ressecções de lesões pré-malignas [2, 3].
Como em todo ato médico intervencionista, podem ocorrer eventos adversos inerentes a qualquer procedimento, e no caso das colonoscopias são: náuseas, vômitos ou distensão abdominal pelo preparo intestinal; hipotensão arterial, bradicardia, depressão respiratória e broncoaspiração pela sedação; dor abdominal, sangramento e perfuração pelo procedimento.
Cada paciente é um indivíduo particular, podendo ter anatomia variada congênita ou por cirurgias prévias, sendo que os dispositivos de endoscopia e colonoscopia seguem um design para um biotipo padrão. Como conseguinte, complicações como a perfuração podem ocorrer independente da técnica e expertise do endoscopista. As perfurações são efeitos adversos raros, inerentes a qualquer procedimento endoscópico, potencialmente graves e sua incidência estimada globalmente é de 0,016 a 0,8% para colonoscopias diagnósticas e 0,02 a 8% para colonoscopias terapêuticas [4].
Os mecanismos associados às perfurações de cólon após colonoscopia são:
Aproximadamente 45-60% das perfurações são diagnosticadas durante o procedimento e o restante é reconhecido após o exame com base em sinais e sintomas clínicos que se manifestam geralmente em até 48h como dor abdominal importante com distensão abdominal, sinais de peritonite, taquicardia, leucocitose e febre [4], ou identificados através de exames de imagem como radiografia simples ou tomografia computadorizada (TC) com sinais de pneumoperitônio. Um dos pontos mais críticos do manejo da perfuração tardia é o tempo do diagnóstico, já que a mortalidade nessas condições pode chegar a 5-25% [3,4].
Clique aqui para mais informações de perfurações de trato gastrointestinal alto.
A depender de diferentes fatores, visando minimizar a morbimortalidade da perfuração por colonoscopia e se baseando na diretriz da World Society of Emergency Surgery [4], a conduta varia conforme diferentes cenários apresentados a seguir.
Após colonoscopias diagnósticas ou terapêuticas recentes, devem ser orientados a procurar o pronto socorro e serem investigados para perfuração intestinal por exames laboratoriais e de imagem os pacientes que apresentem os seguintes sintomas:
Os marcadores bioquímicos solicitados no caso de suspeita de perfuração são essencialmente leucograma e proteína C reativa. A complicação pode ser confirmada com a demonstração de ar livre intra-peritoneal ou extra-peritoneal. A TC possui maior sensibilidade do que as radiografias abdominais para detectar pneumoperitônio.
Caso a perfuração seja detectada durante o procedimento pelo endoscopista, os seguintes detalhes das informações ajudam na tomada de decisão:
O tratamento endoscópico pode ser considerado como uma abordagem inicial se for viável dentro de 4 horas após o procedimento, com paciente estável e pouca contaminação peritoneal, a depender:
O manejo não operatório, conservador, das perfurações pode ser apropriado em pacientes selecionados, incluindo pacientes que estão hemodinamicamente estáveis, sem sepse, com dor localizada e sem líquido livre em exame de imagem. A TC abdominal é sugerida para ajudar a descartar peritonite ou formação precoce de abscesso. Um diagnóstico diferencial importante é a síndrome pós-coagulação.
Em casos de perfurações confirmadas não identificadas durante a colonoscopia, deve-se avisar imediatamente a equipe de cirurgia e endoscopia, seguida de internação hospitalar, em UTI a depender do estado e comorbidade do paciente, e avaliar necessidade de intervenção cirúrgica.
Pacientes com pequenas perfurações, ausência de sinais de sepse e peritonite, preparo de cólon adequado, assintomático ou com melhora dos sintomas:
A cirurgia de emergência é recomendada quando o paciente desenvolve sinais e sintomas de peritonite, em casos de deterioração clínica, suspeita de grande perfuração, falha no manejo conservador, preparo intestinal inadequado ou na presença de doença cólica subjacente que requeira cirurgia.
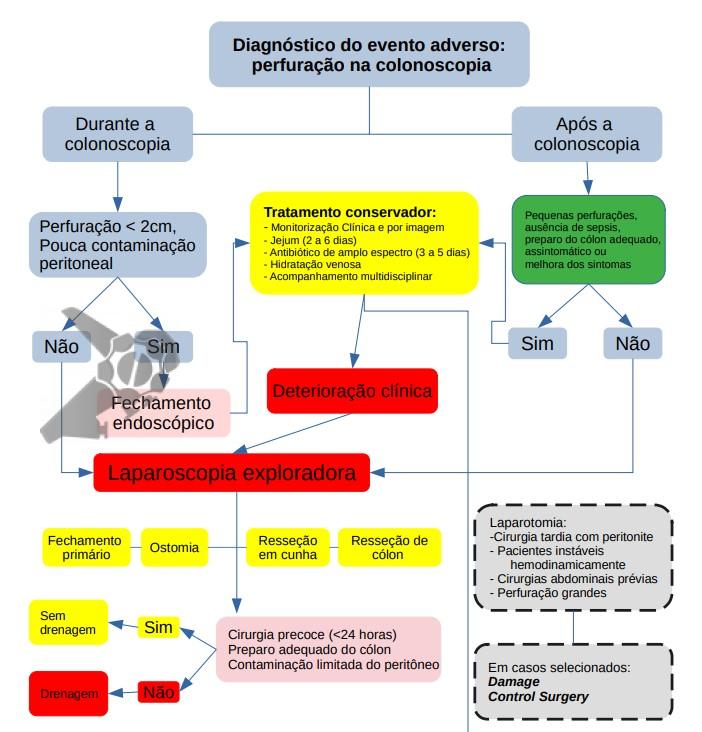
Santos JB, Vilela Filho TF, Furuya Júnior CK, Kuga R, Kum AST. Perfuração na Colonoscopia: Cuidados e Manejo. Endoscopia Terapeutica 2024, Vol I. Disponível em: https://endoscopiaterapeutica.com.br/assuntosgerais/perfuracao-na-colonoscopia-cuidados-e-manejo/
A lesão serrilhada séssil (LSS) é o novo termo para lesões anteriormente chamadas de adenoma serrilhado séssil (SSA) e LSS com displasia é o termo usado para as lesões anteriormente chamadas de SSA com displasia. Uma revisão detalhada das lesões serrilhadas você encontra nesse outro artigo.
Com base nisso, a Síndrome de Polipose Serrilhada (SPS) é uma condição rara caracterizada por várias lesões serrilhadas colorretais e risco aumentado de câncer colorretal.
Clique aqui para saber de outras síndromes de polipose colorretal.
Em comparação com a edição anterior, a OMS em 2019 atualizou os critérios diagnósticos, permanendo apenas 2 dos 3 critérios clínicos para a definição de SPS:
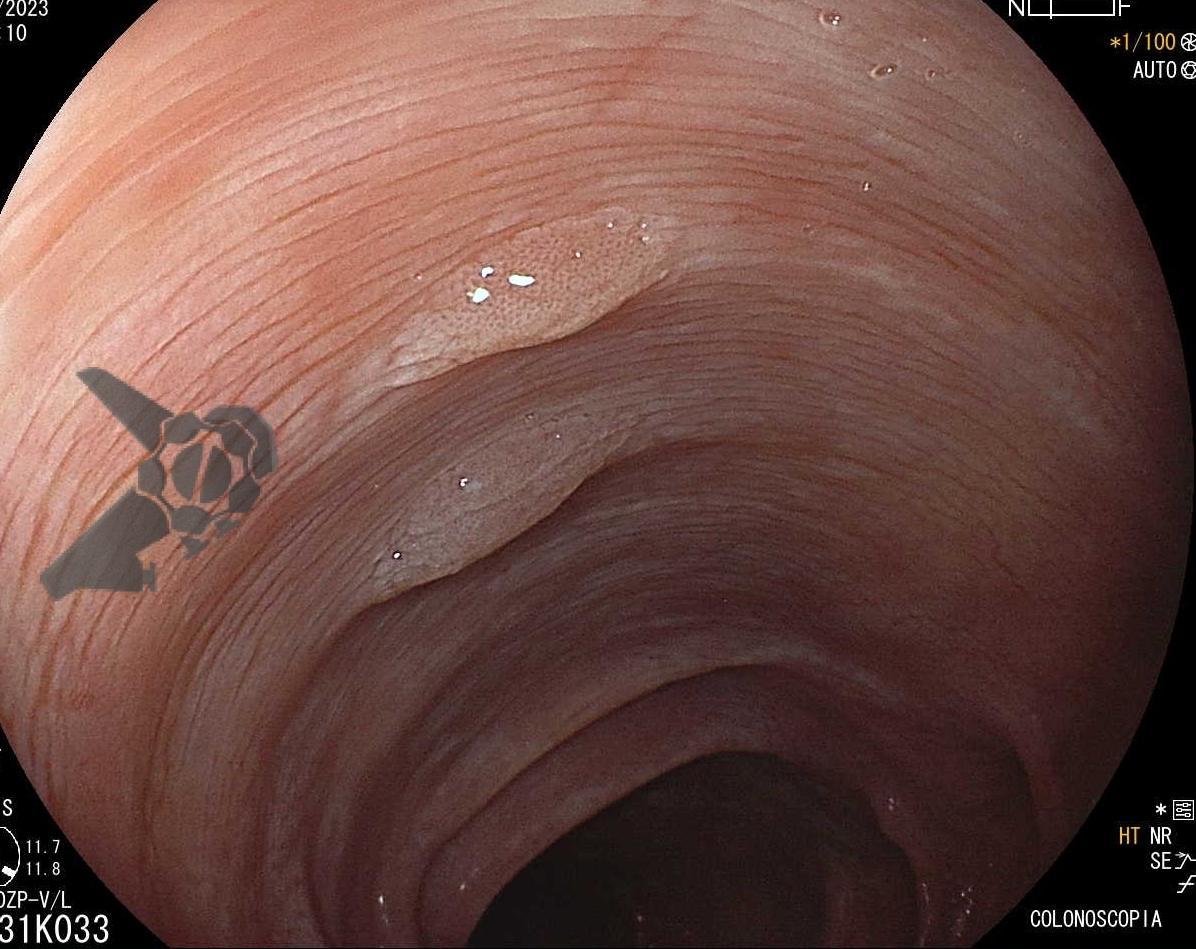
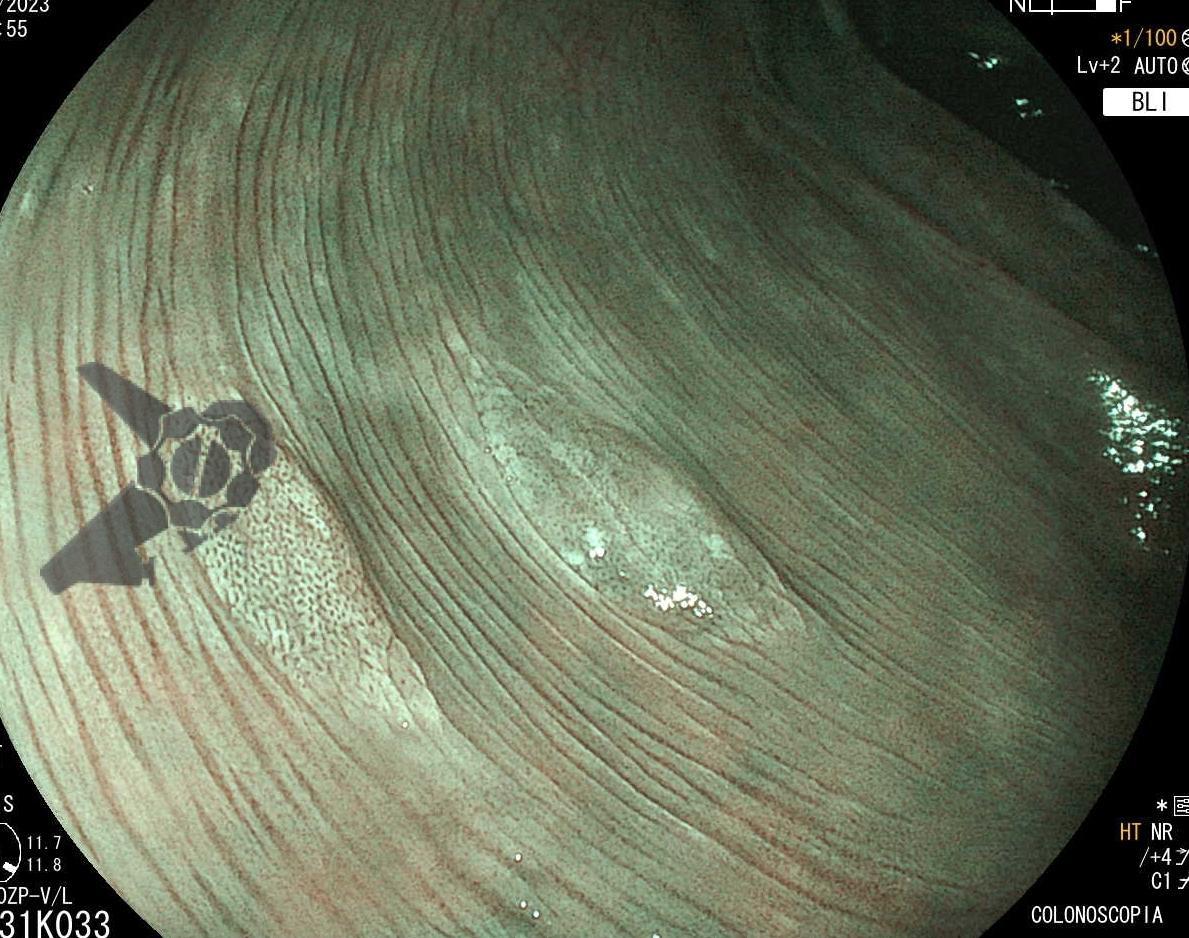
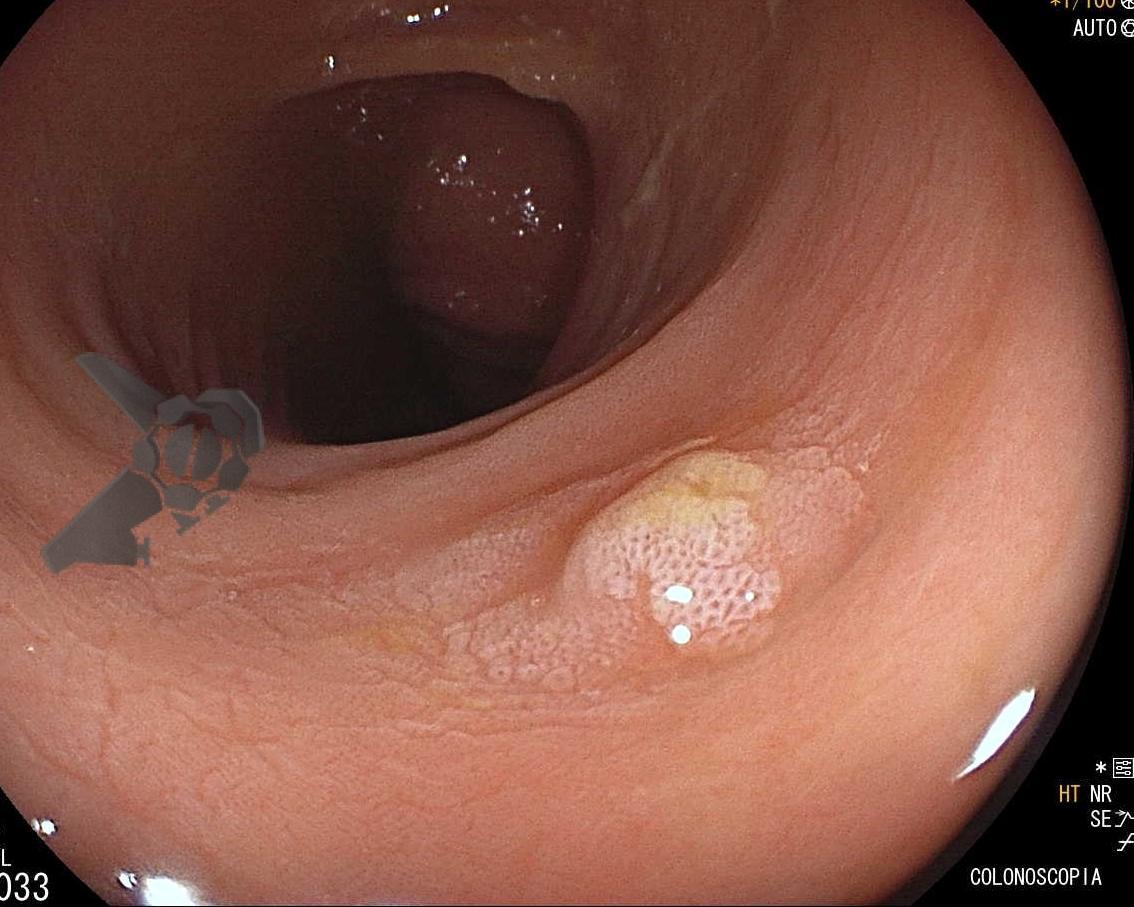
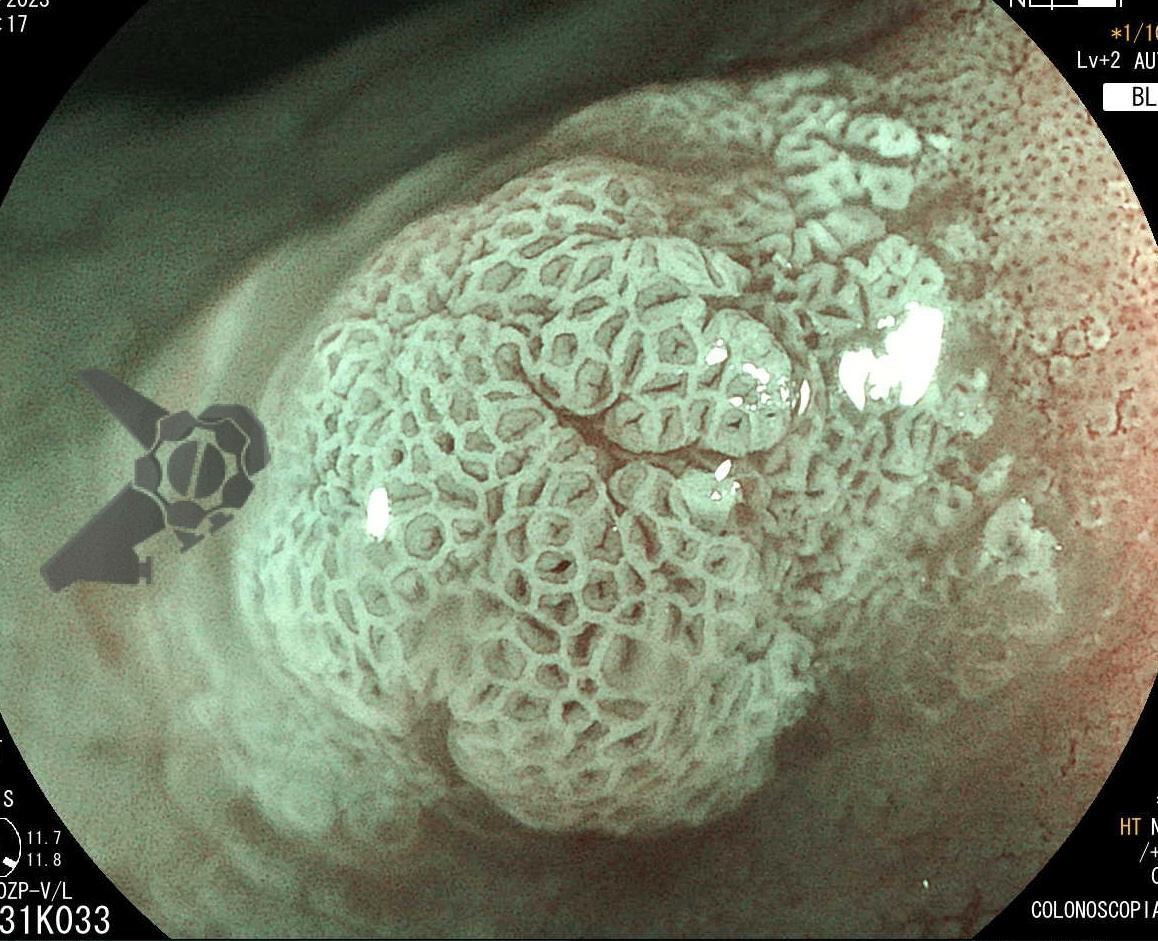

Martins BC e Tanigawa R. Síndrome de Polipose Serrilhada (SPS). Endoscopia Terapeutica, 2024 vol. 1. Disponível em: https://endoscopiaterapeutica.com.br/assuntosgerais/sindrome-de-polipose-serrilhada-sps/