Coledocoduodenostomia ecoguiada: um procedimento endoscópico-cirúrgico
INTRODUÇÃO:
A colangiopancreatografia retrógrada endoscópica (CPRE) é o procedimento de escolha para a drenagem da via biliar comum, no caso de obstruções distais. Contudo, em aproximadamente 5% de todos os casos, isso não é factível. Nos casos de pacientes operados com alteração da anatomia gastrointestinal e em casos oncológicos, como os tumores periampulares, por exemplo, a CPRE tem baixas taxas de sucesso e outro método se faz necessário. É aí onde surge a drenagem biliar ecoguiada (DBEG), como uma alternativa eficaz e segura.
As indicações atuais para DBEG são:
- falha da CPRE
- alteração anatômica
- tumor que impeça o acesso a árvore biliar
- contraindicações ao acesso percutâneo
Existem dois métodos para se realizar uma DBEG:
- Trans-hepática: onde através da pequena curvatura proximal realiza-se uma punção e drenagem ecoguiada do segmento III hepático, ou
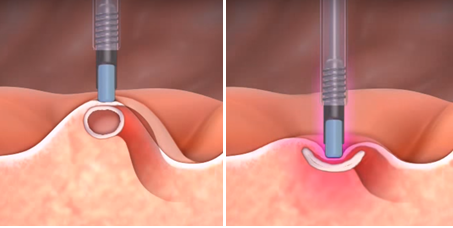
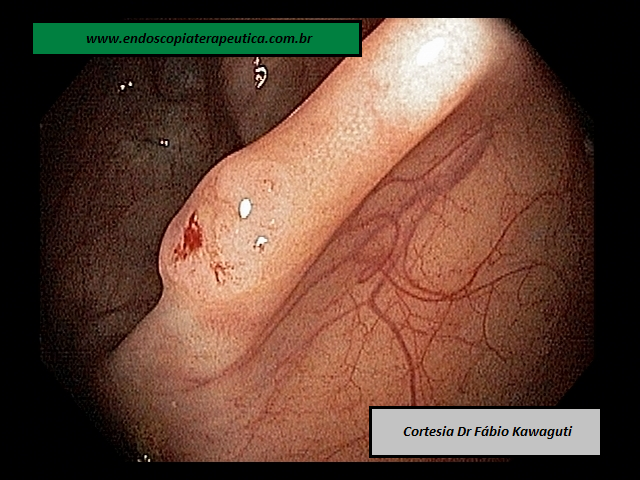
- Extra-hepático: também chamada de coledocoduodenostomia ecoguiada, onde, no bulbo duodenal realiza-se uma punção, dilatação e inserção de uma prótese entre o duodeno e o colédoco, sendo todos os passos sob visão direta da endoscopia agregada a visão radiológica e ecoendoscópica, simultaneamente.
CASO CLÍNICO:
Paciente de 80 anos, sexo feminino, com dor abdominal, icterícia progressiva e perda de peso não quantificada há 08 meses.
- Exames complementares indicavam colestase (AST: 55, ALT: 71, FA: 645, GGT 374, BT: 22,10, BD: 21,0)
- Ultrassom de fígado e vias biliares evidenciaram dilatação da via biliar intra e extra-hepática, com colédoco de 1,8cm.
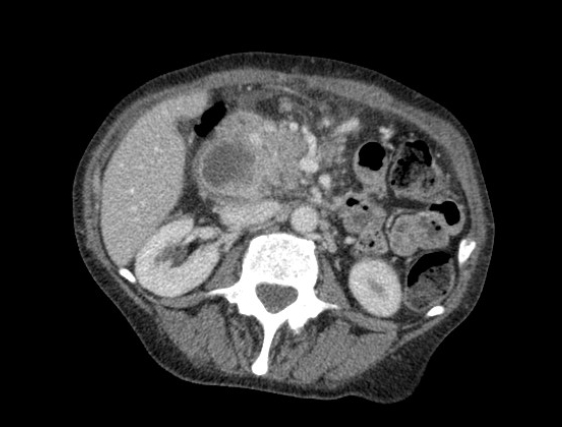
- A tomografia de abdome mantém o achado da dilatação, com evidência de interrupção do coléodoco a nível da cabeça do pâncreas, devido a lesão hipodensa, de 3,0 x 2,7cm, associado a dilatação do ducto de Wirsung, além de disseminação linfonodal da lesão.
Tentado inicialmente CPRE para drenagem biliar, sem sucesso por infiltração da papila duodenal e obstrução maligna da mesma. Foi então realizado uma biópsia da lesão que confirmou o diagnóstico da adenocarcinoma de pâncreas.
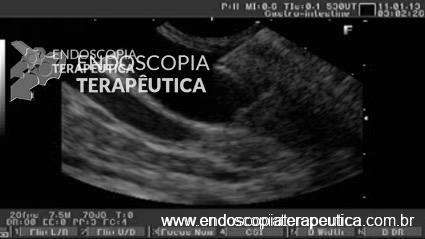
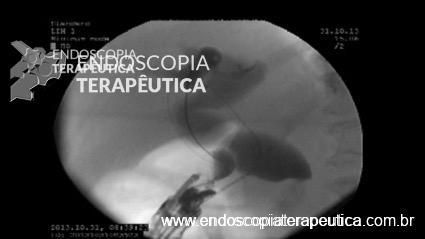
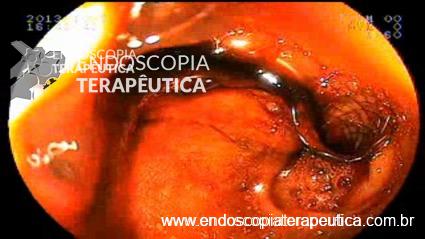
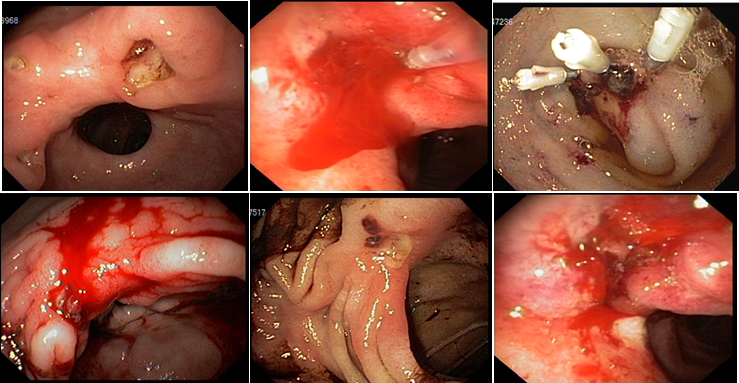
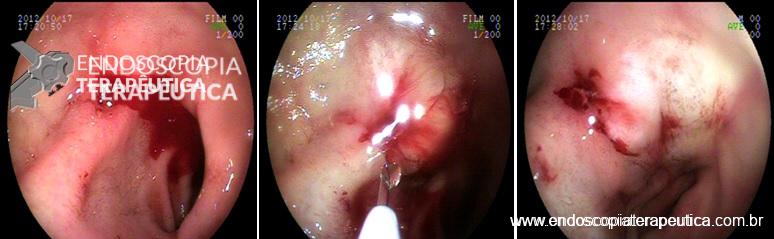
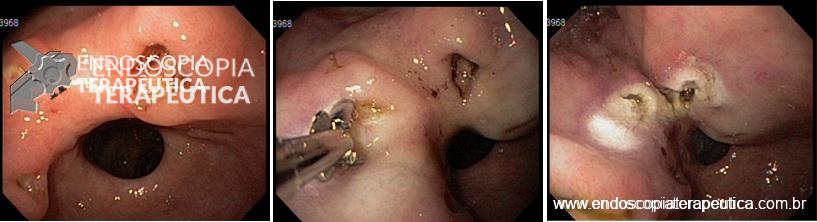
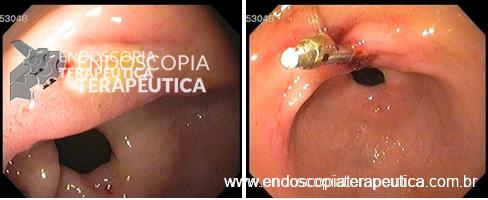
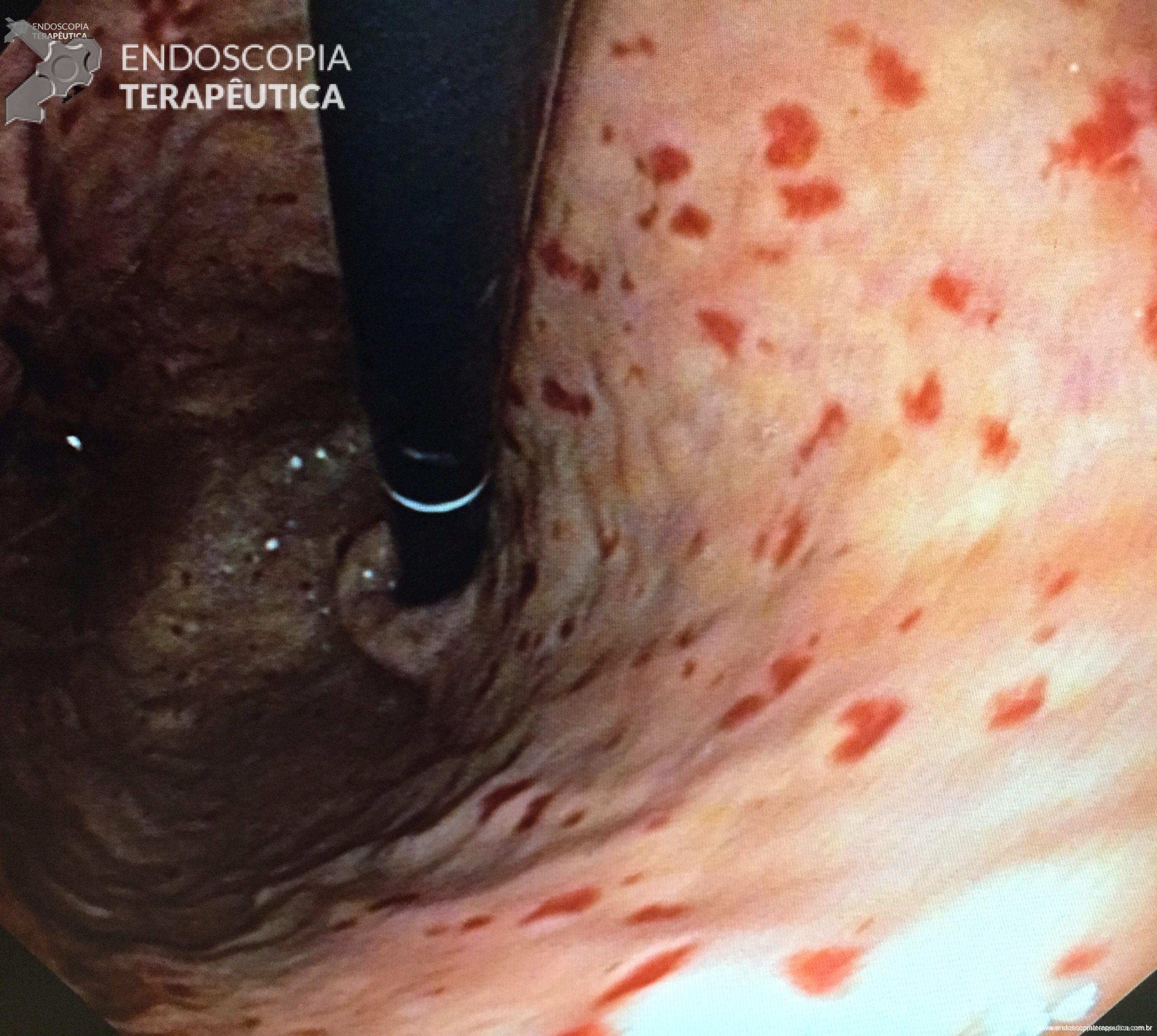
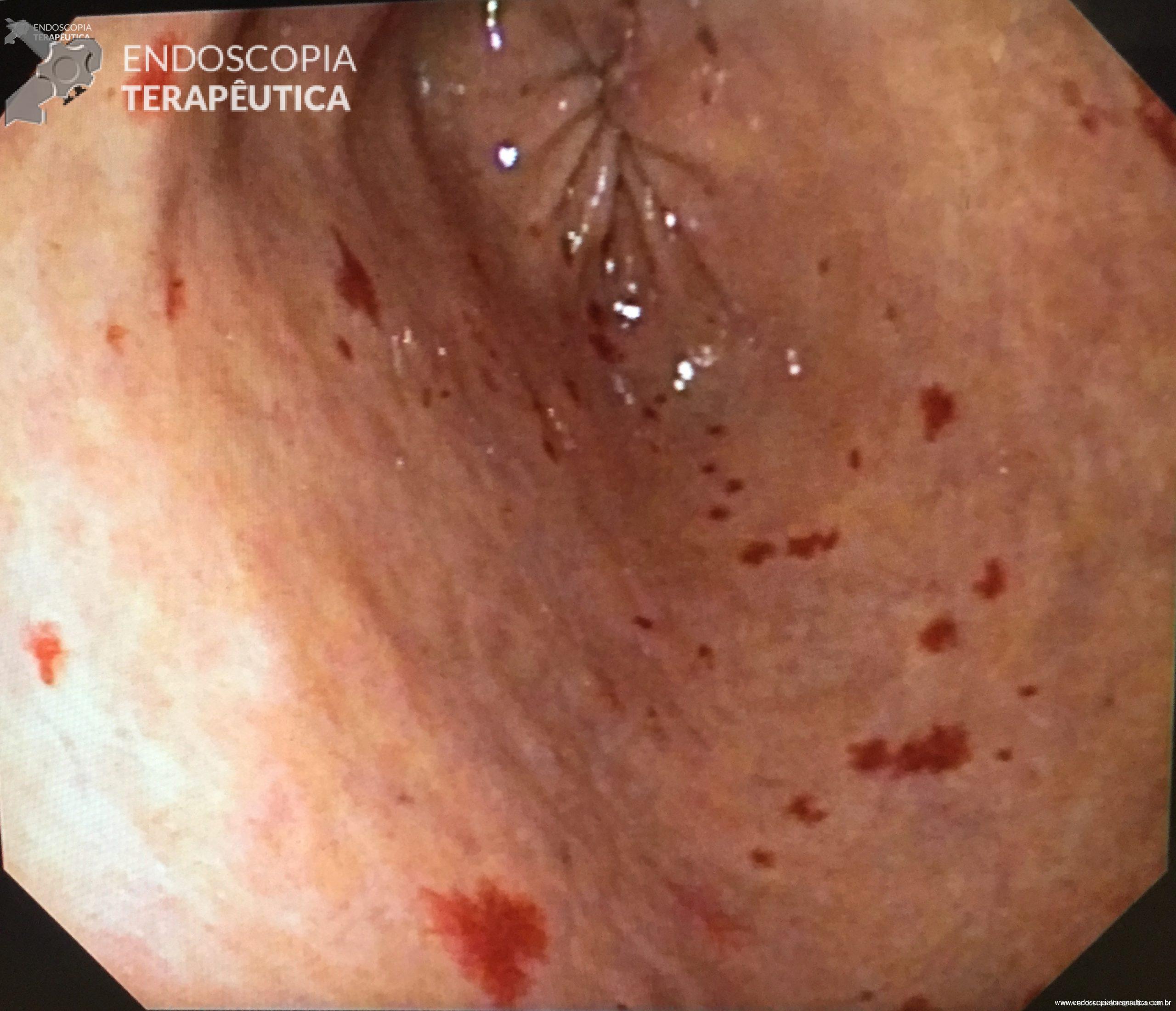
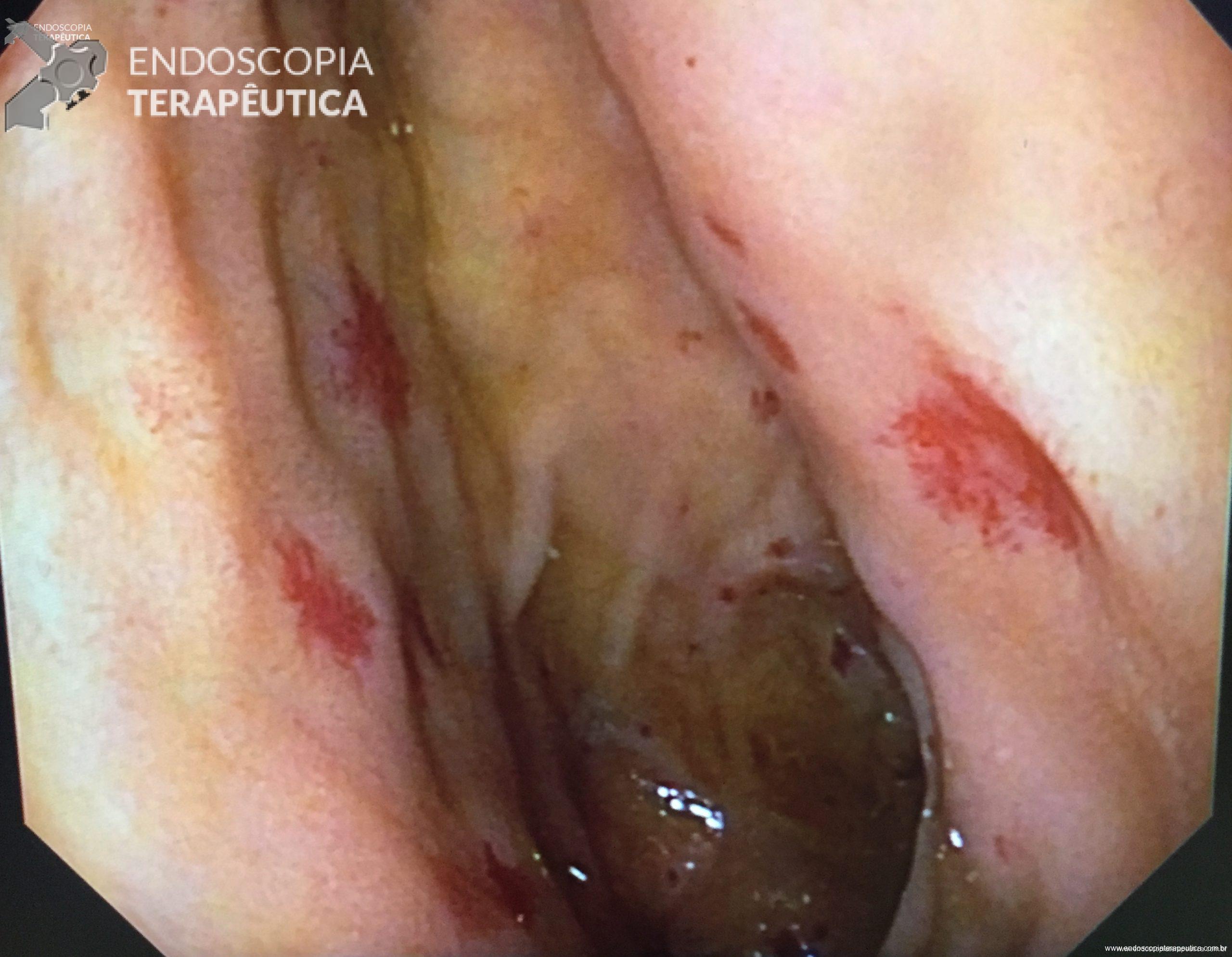
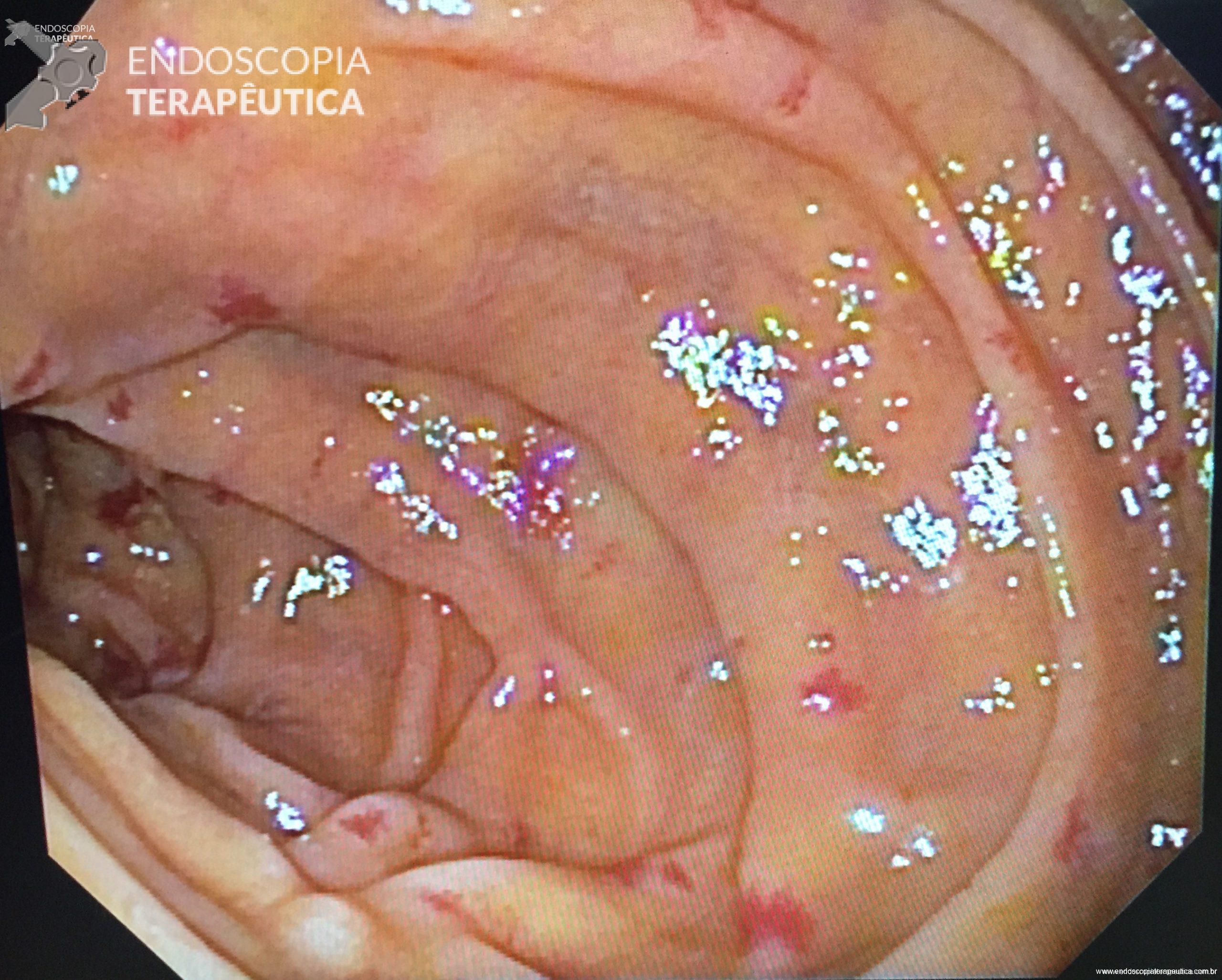
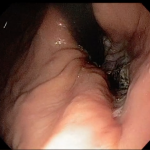
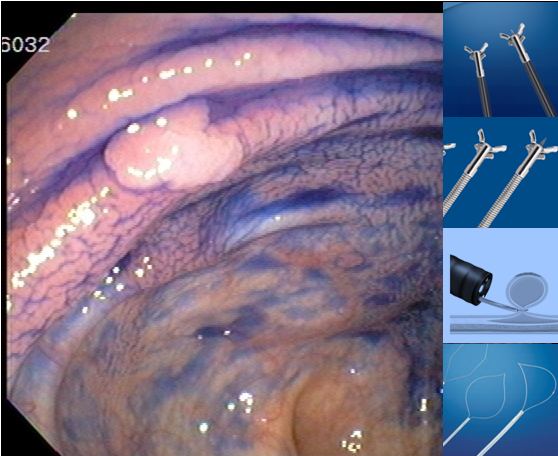
Diante desse contexto, após consentimento da paciente, foi realizado, sob anestesia geral e utilizando-se um ecoendoscópio setorial com canal de 2.8 mm, uma ecopunção no joelho bulbar junto a parede supero-anterior com intuito de se criar um trajeto fistuloso não anatômico para se proceder a uma drenagem biliar ecoguiada (coledocoduodenostomia), com passagem de prótese metálica parcialmente recoberta de 60 x 10 mm. O tempo total de procedimento foi de 35 minutos, sendo o tempo de passagem da prótese de 5 minutos. O método de dilatação utilizado foi por meio do estilete e apenas uma prótese foi utilizada, com escoamento imediato de bile esverdeada entremeada a alguns grumos biliares. O esvaziamento de contraste da via biliar após 20 minutos do procedimento foi considerado ótimo e não houve complicação técnica ou clínica durante ou após o procedimento (Figuras 1, 2, 3).
A paciente teve boa evolução, recebendo alta em 36h e, após uma semana, encontrava-se clinicamente bem, sem dor, com boa aceitação de dieta oral. Novos exames laboratoriais mostram queda significativa dos valores de bilirrubina (BT: 14,30, BD: 12,00). A paciente manteve seguimento clínico e clearance progressivo de bilirrubinas, mantendo-se assintomática por 06 meses e com sobrevida de 07 meses após o procedimento. Destaca-se a melhora da qualidade de vida comprovada objetivamente por meio de escores (SF-36) realizados antes e seriadamente após o acesso ecoguiado.
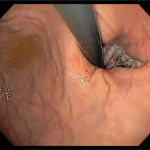
Figura 1: Imagem ecoendoscopica setorial demonstrando colédoco distal dilatado a montante da estenose neoplásica, a agulha e a veia porta.
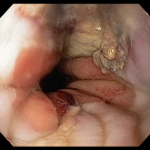
Figura 2: Imagem radiológica demonstrando a estenose distal na via biliar extrahepática e o aparelho de ecoendoscopia, alem do fio guia passando pelo ponto de punção que ocorreu na face supero-anterior do joelho duodenal.
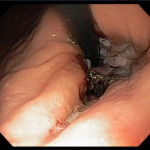
Figura 3: Prótese metálica disposta no bulbo duodenal e configurando a coledocoduodenostomia ecoguiada.
DISCUSSÃO:
Apresentamos um caso clínico onde uma neoplasia maligna periampular impedia a drenagem biliar por CPRE e sendo utilizado, com sucesso, método alternativo da drenagem biliar com a utilização da ecoendoscopia setorial: coledocoduodenostomia.
O acesso biliar ecoguiado compõe-se por técnicas intra e extra-hepáticas. A hepatogastrostomia é indicada nas lesões hílares com insucesso da CPRE e a coledocoduodenostomia destaca-se na obstrução do confluente bilioduodenopancreático.
Vale ressaltar que se trata de um procedimeno minimamente invasivo que, agregado a CPRE, permite-se a drenagem biliar em torno de 98% dos casos, portanto o acesso ecoguiado caracteriza uma técnica de resgate relevante. O sucesso terapêutico e técnico, na literatura, é de 85-100%. Ainda vale citar que a relação custo beneficio é favorável a este método quando comparado com o acesso transparietal e cirúrgico. Outrossim, a ciurgia é padrão ouro e deve ser o método de finalização na falha da supracitada técnica.
Em relação as opções de próteses, poder-se-á utilizar próteses metálicas (cobertas, parcialmente cobertas e não cobertas) e plásticas. Na coledocoduodenostomia pode-se utilizar tanto metálicas como plásticas, entretanto na hepatogastrostomia a preferência são as metálicas cobertas.
Concluindo, a coledocoduodenostomia ecoguiada compõe técnica elegante e efetiva de resgate ao acesso biliar na falha da CPRE convencional e deve ser realizada por profissionais com destacada proficiência em CPRE e Ecoendoscopia, além de ambiente com acessórios adequados e hospitalar bem estruturado.
REFERÊNCIAS BIBLIOGRÁFICAS:
Guedes HG, Lopes RI, de Oliveira JF, Artifon EL. Reality named endoscopic ultrasound biliary drainage. World J Gastrointest Endosc 2015; 7(15): 1181-1185 [PMID: 26504507 PMCID: PMC4613807 DOI: 10.4253/wjge.v7.i15.1181]