ASPIRE
Por Cynthia Teixeira e Sérgio Barrichello
A obesidade é uma doença crônica que afeta milhares de pessoas consituindo um problema de saúde pública impactando na saúde de um terço da população adulta.1-3
Doenças relacionadas à obesidade, incluindo o tipo 2 diabetes, hipertensão e apneia obstrutiva do sono, aumentam a morbimortalidade dos pacientes acarretando um impacto negativo na qualidade de vida dos mesmos.
Várias opções terapêuticas estão disponíveis, embora a eficácia esteja correlacionada com maior invasividade. Modificações dietéticas e no estilo de vida têm um sucesso limitado e a curto prazo na perda de peso na maioria dos pacientes.4
A cirurgia bariátrica é o tratamento mais bem sucedido para pacientes obesos porém é um procedimento cirúrgico invasivo e que altera a anatomia do trato digestivo. 5
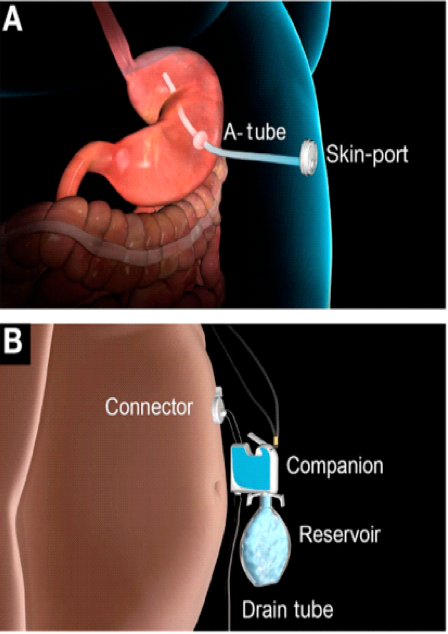
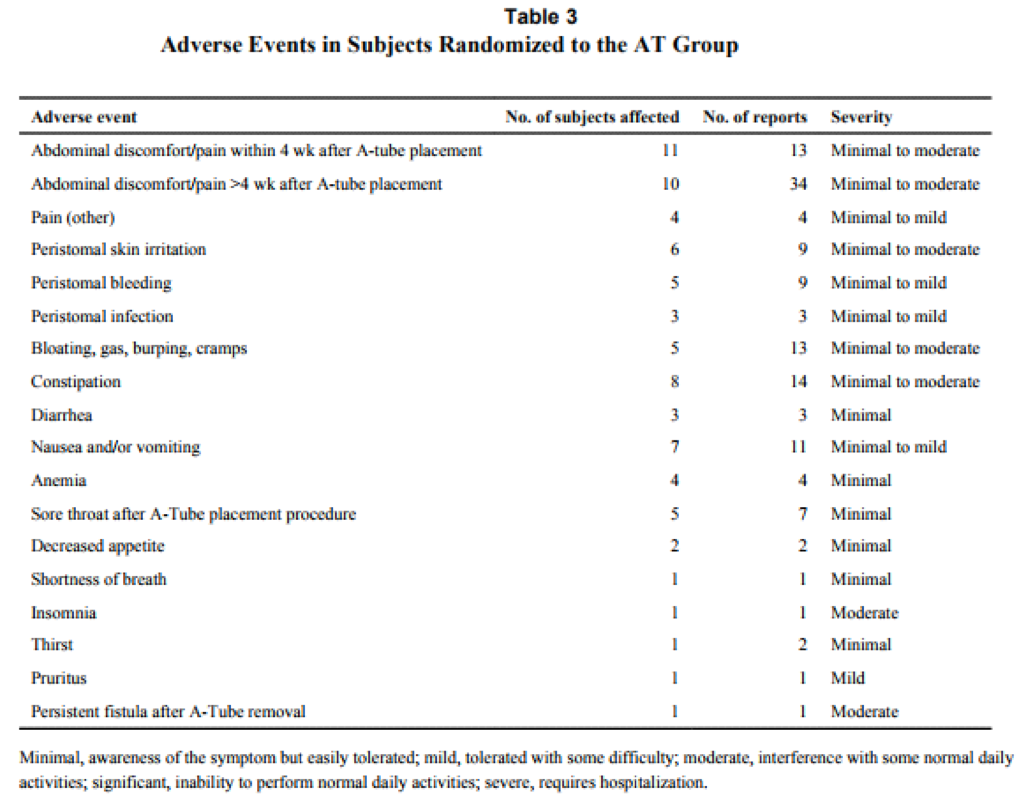
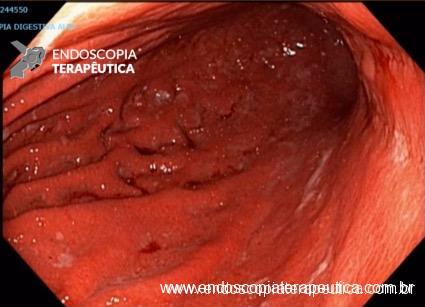
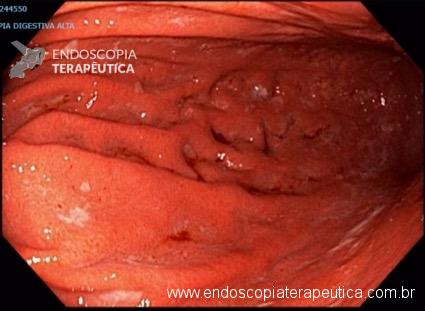
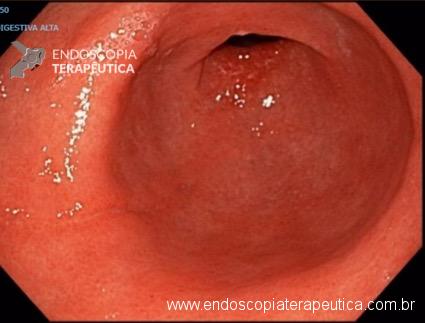
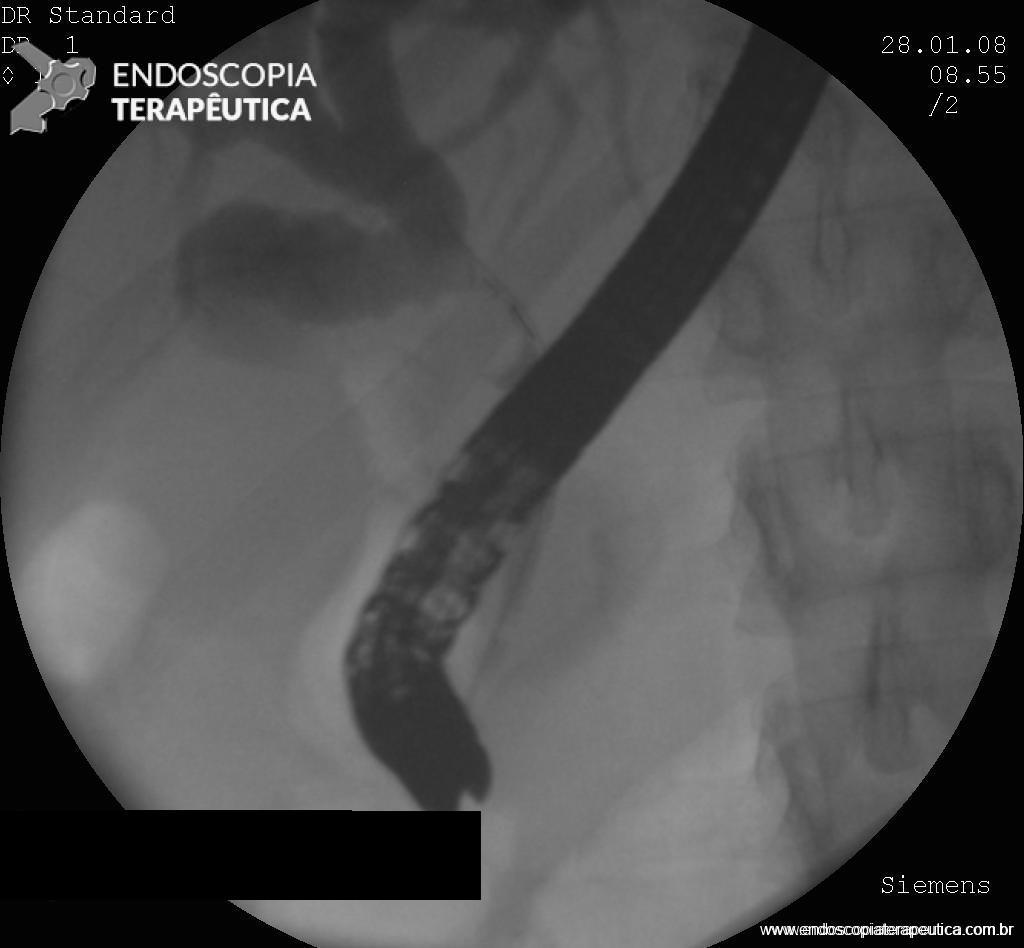
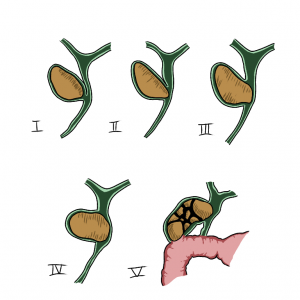
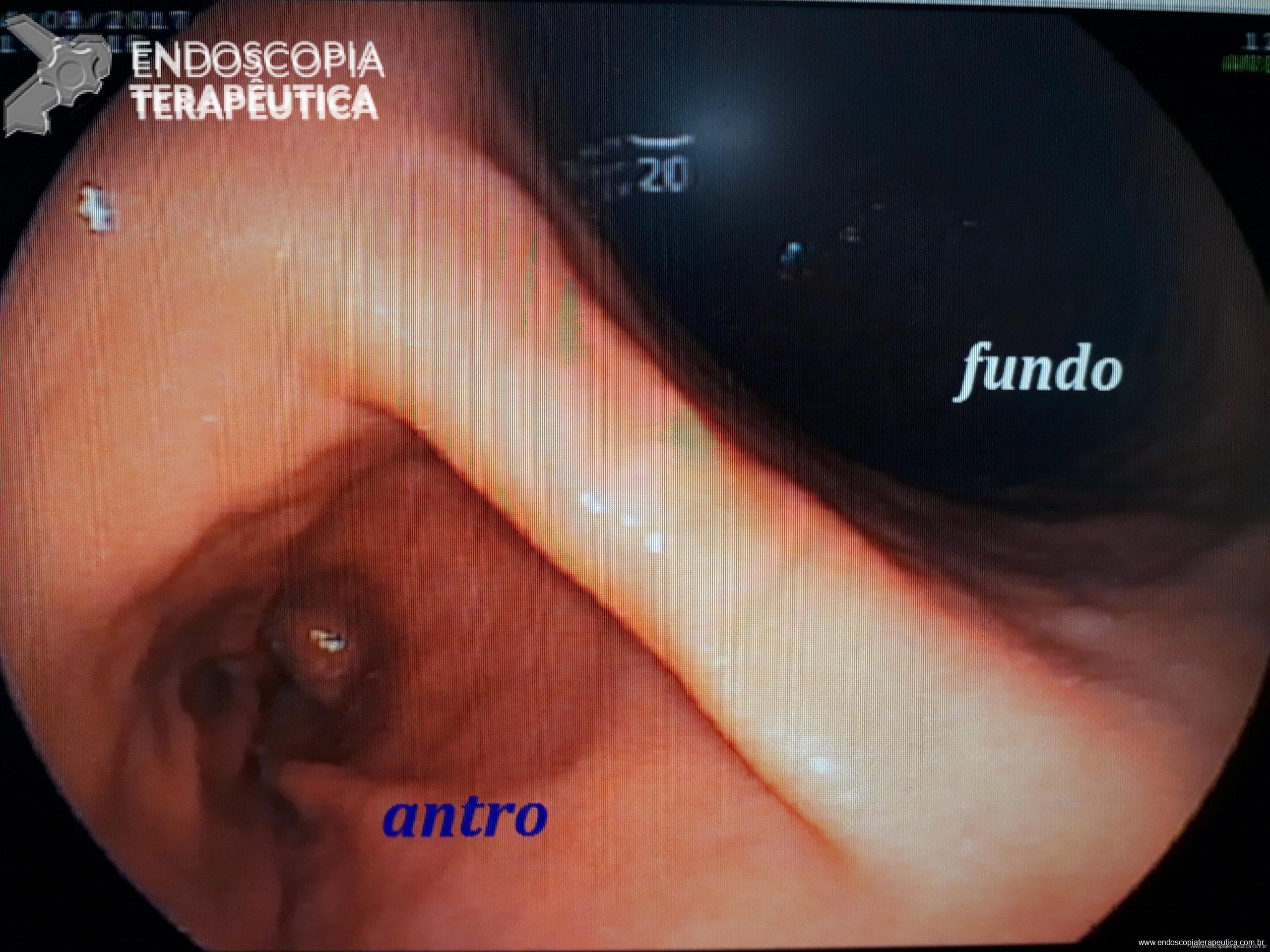
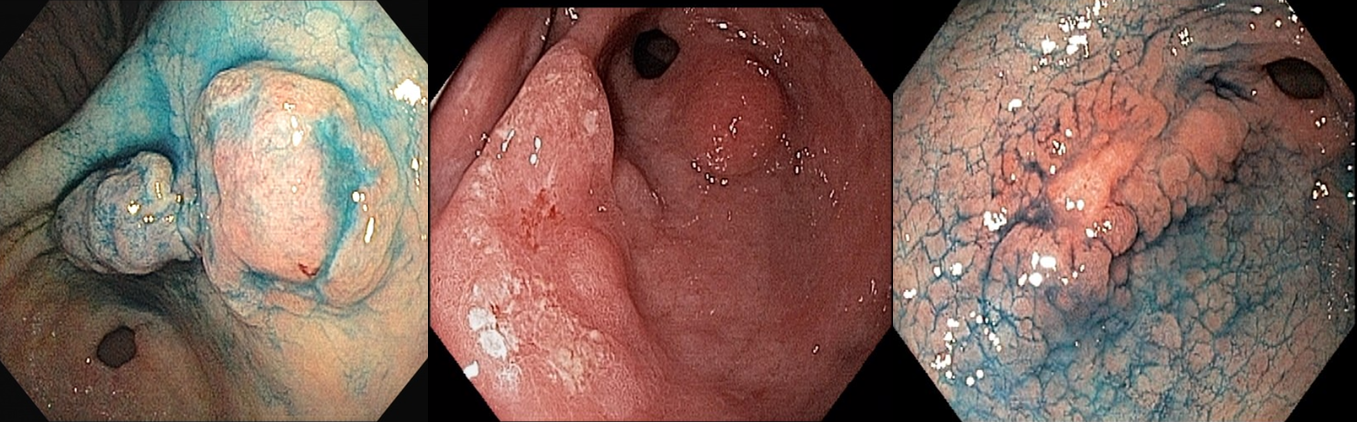
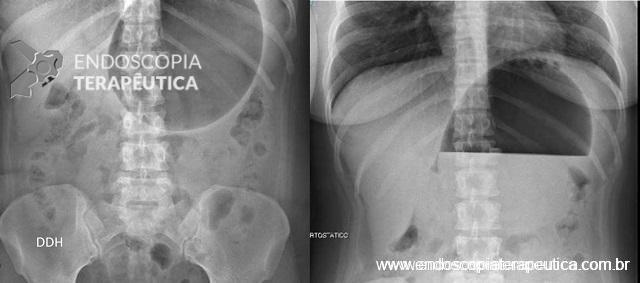
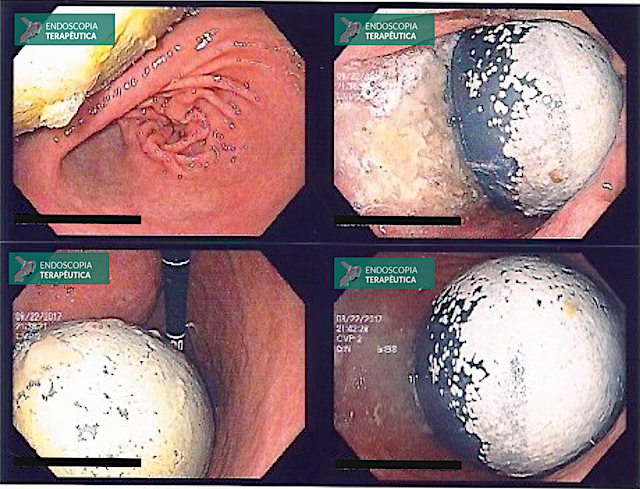
O AspireAssist permite a terapia de aspiração, em que o alimento é removido do estômago após a ingestão. Esse método foi aprovado pela FDA em 2016 para pacientes com IMC de 35-55 kg / m2 e consiste em uma gastrostomia endoscópica percutânea de 30Fr (chamado tubo de aspiração), uma porta externa na pele para aspiração e um dispositivo portátil que se conecta à porta para realizar a descarga e aspiração. O AspireAssist permite o consumo de uma refeição, infusão de água e, em seguida, aspiração de uma porção da refeição. O tubo de aspiração é inserido endoscopicamente pela técnica de tração.6
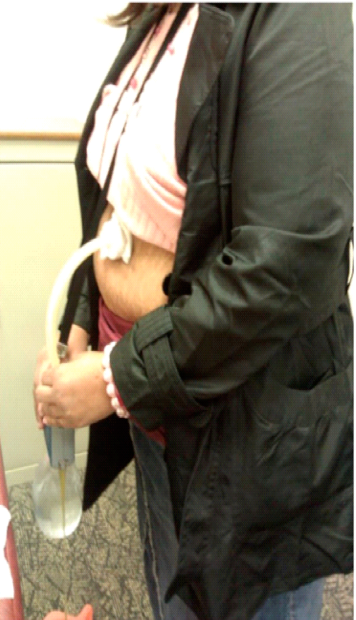
A aspiração do conteúdo gástrico é feita 20 minutos após o consumo de refeições e três vezes ao dia. A aspiração leva cerca de 10 minutos para executar e remove aproximadamente 30% das calorias ingeridas.
As imagens abaixo ilustram esse método:
Assim, visando entender melhor a segurança e a eficácia do método ASPIRE Sullivan e colaboradores desenvolveram o seguinte estudo piloto:
METODOLOGIA:
Dezoito adultos obesos (IMC entre 40,0 e 50,0 kg / m2 ou entre 35,0 e 39,9 kg / m2 com comorbidades) recrutados entre fevereiro e outubro de 2009 participaram deste estudo.
Os participantes foram randomizados em dois grupos sendo um grupo com a intervenção do ASPIRE mais a mudança do estilo de vida e o outro somente com a mudança do estilo de vida; acompanhados pelo período de 24meses.
RESULTADOS
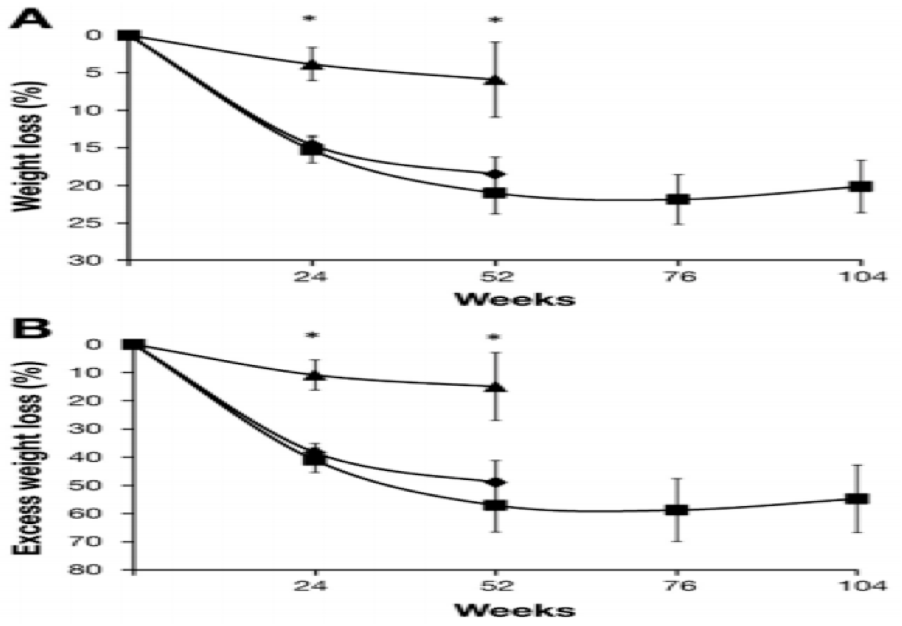
Os autores relataram uma perda significativamente maior de excesso de peso com a terapia de aspiração em combinação com a intervenção do estilo de vida do que a intervenção do estilo de vida isolado nas primeiras 52semanas e que nenhuma alteração significativa na perda de peso ocorreu da semana a partir de então, como ilustra a figura abaixo.
A perda média de excesso de peso por protocolo foi de 54,4% aos 12 meses e 61,5% aos 24 meses.
Os autores também concluíram que a terapia por aspiração não induz a comportamentos alimentares adversos ou altera os escores de depressão basais.
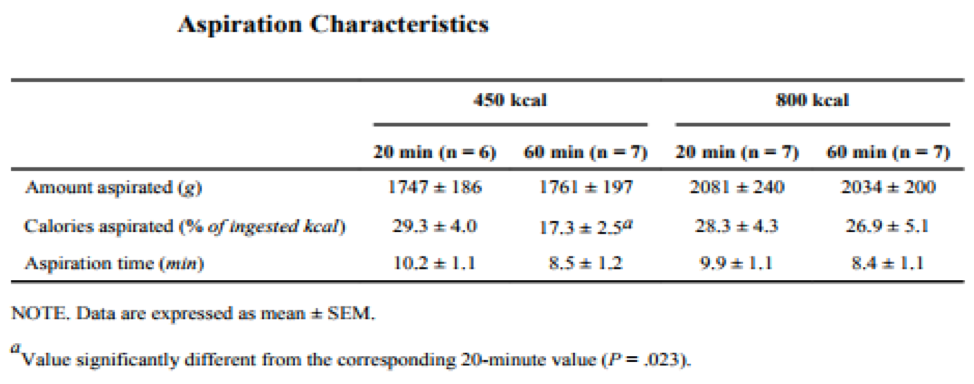
A quantidade de tempo necessário para a aspiração (~ 10 minutos) não foi diferente quando os sujeitos aspiravam aos 20 ou 60 minutos após uma refeição de 450 ou 800 kcal. Aproximadamente 30% das calorias ingeridas foram removidas por aspiração 20 minutos após o consumo de uma refeição de 450 ou 800 kcal. Aspirar 20 ou 60 minutos depois de consumir a refeição de 800 kcal não afeta significativamente a porcentagem de calorias removidas por aspiração. No entanto, a porcentagem de calorias aspiradas foi maior aos 20 minutos do que 60 minutos após o consumo a refeição de 450 kcal.
A perda de peso não resultou em alterações significativas no perfil lipídico e/ou dos eletrólitos tais como magnésio e cálcio. Houve uma tendência para uma diminuição da concentração plasmática de alanina transaminase (ALT) no grupo da intervenção em comparação com o grupo sem a intervenção.
No grupo da intervenção, 4 indivíduos necessitaram de suplementação de ferro, 3 indivíduos necessitaram de suplementação de vitamina D, e um sujeito exigiu suplementação de vitamina B12. Com suplementação, a terapia por aspiração não resultou em diferença nas concentrações plasmáticas de ferro, 25-hidroxivitamina D ou vitamina B12 em comparação com o grupo sem intervenção.
EFEITOS ADVERSOS
Nenhum evento adverso grave ocorreu nos grupos. Os eventos adversos mais comuns incluíram dor peristomal nas primeiras 4 semanas após a colocação do dispositivo, irritação peristomal e constipação (Tabela 3).
DISCUSSÃO
Esse estudo piloto concluiu que sujeitos do grupo que sofreu a intervenção do ASPIRE apresentaram uma perda de peso maior que os do grupo que só tiveram a mudança do estilo de vida e essa perda ponderal alcançada em 1 ano foi mantida por dois anos.
O reganho de peso, que normalmente é observada após 1 ano de terapia intensiva de emagrecimento e de 1 a 10 anos da cirurgia bariátrica não foi observada neste estudo.
Além disso, não foi observado nenhuma complicação grave. E não houve evidências de efeitos adversos sobre padrões alimentares, psicopatologia do transtorno alimentar ou fome no grupo da intervenção.
Estes dados mostram que a terapia de aspiração pode ser uma opção de tratamento de longo prazo segura e efetiva para pessoas com obesidade.7
Em outro estudo randomizado Thonson e colaboradores avaliaram em 52 semanas, 207 participantes com índice de massa corporal (IMC) de 35,0-55,0 kg / m 2 foram distribuídos aleatoriamente em uma proporção de 2:1 ao tratamento com AspireAssist e mudança do estilo de vida (n = 137; o IMC médio foi de 42,2 ± 5,1 kg / m 2) ou a mudança de estilo de vida isolada (n = 70; o IMC médio foi 40,9 ± 3,9 kg / m 2). E observaram que os participantes no grupo AspireAssist perderam uma média (± s.d.) de 31,5 ± 26,7% do seu excesso de peso corporal (12,1 ± 9,6% do peso corporal total), enquanto que aqueles no grupo mudança do estilo de vida isolada perderam uma média de 9,8 ± 15,5% do excesso de peso corporal.
Concluiram que o uso de AspireAssist causa considerável perda de peso e é mais eficaz do que a modificação intensiva do estilo de vida sozinha no tratamento da obesidade. O sistema foi projetado para o tratamento longo prazo da obesidade e necessita de monitoramento regular, ambos aspectos importantes para o tratamento de uma doença crônica. O procedimento de colocação é o mesmo que o utilizado para gastrostomia endoscópica percutânea e pode ser realizada a nivel ambulatorial. Também pode ser removido se posteriormente for decidido interromper a terapia e não causa alterações anatômicas que impediriam a futura cirurgia bariátrica. A eficácia da perda de peso e o perfil de segurança da AspireAssist sugerem esta abordagem de tratamento como ponte entre os tratamentos conservadores e os procedimentos cirúrgicos bariátricos estabelecidos para pessoas com obesidade Classe II e Classe III.8
REFERÊNCIAS BIBLIOGRÁFICAS:
- Allison DB, Downey M, Atkinson RL, et al. Obesity as a disease: a white paper on evidence and arguments commissioned by the council of the obesity society. Obesity (Silver Spring). 2008;16(6): 1161–1177.
- AMA. Report of the Council on Science and Public Health. Chicago, IL: AMA; 2013. Available from: http://www.ama-assn.org/assets/ meeting/2013a/a13-addendum-refcomm-d.pdf#page=19. Accessed December 14, 2016.
- Ward ZJ, Long MW, Resch SC, et al. Redrawing the US obesity landscape: bias-corrected estimates of state-specific adult obesity prevalence. PLoS One. 2016;11(3):e0150735.
- Turk MW, Yang K, Hravnak M, Sereika SM, Ewing LJ, Burke LE. Randomized clinical trials of weight-loss maintenance: a review. J Cardiovasc Nurs. 2009;24(1):58–80.
- Nguyen NT, Vu S, Kim E, Bodunova N, Phelan MJ. Trends in utilization of bariatric surgery, 2009–2012. Surg Endosc. 2016; 30(7): 2723–2727
- Kumar N, Sullivan S, Thompson CC. The role of endoscopic therapy in obesity management: intragastric balloons and aspiration therapy Diabetes Metab Syndr Obes. 2017; 10: 311–316. Published online 2017 Jul 6. doi: 10.2147/DMSO.S95118
- Sullivan S, Stein R, Jonnalagadda S, Mullady D, Edmundowicz S. Aspiration therapy leads to weight loss in obese subjects: a pilot study. Gastroenterology. 2013;145(6):1245–52.
- Thonson et al. Percutaneous Gastrostomy Device for the Treatment of Class II and Class III Obesity: Results of a Randomized Controlled Trial. Endoscopy Am J Gastroenterol 2017; 112:447–457; doi: 10.1038/ajg.2016.500; published online 6 December 2016
Autores
Cynthia Teixeira
Especialista em Gastroenterologia pela BP-SP
Especialista em Endoscopia pelo Hospital Estadual Mario Covas
Membro titular da FBG e SOBED
Medica Endoscopista do Hospital Albert Sabin SP