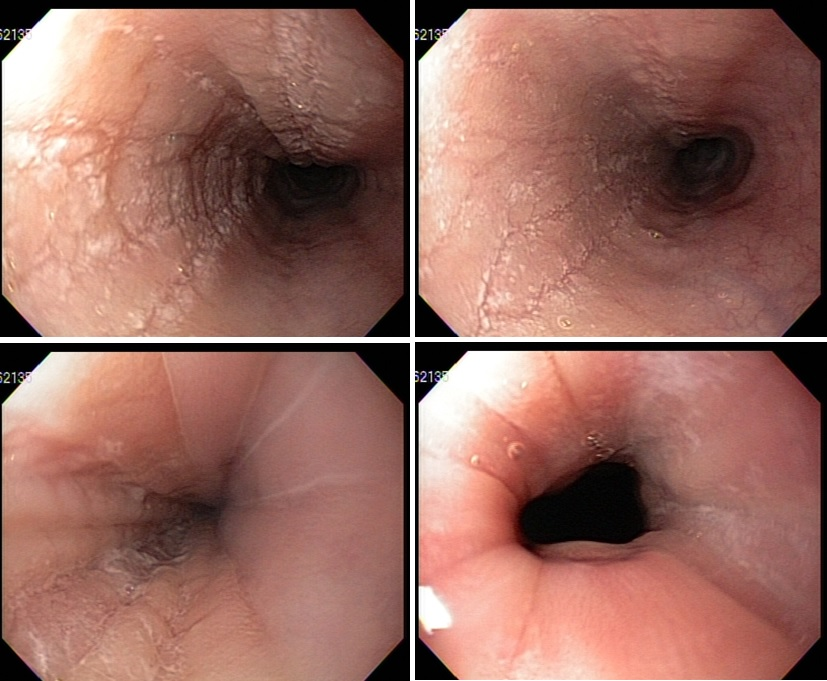
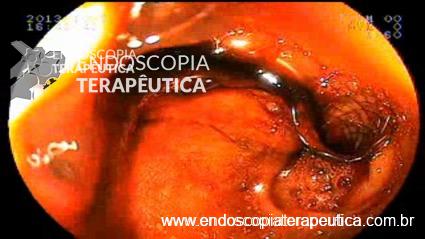
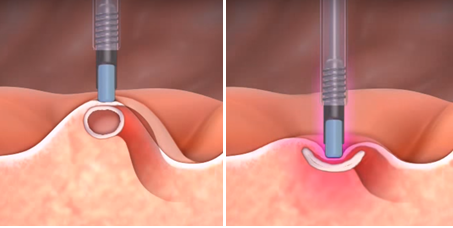
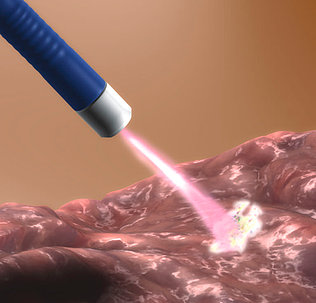
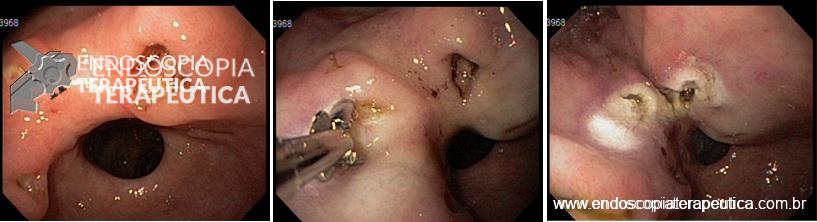
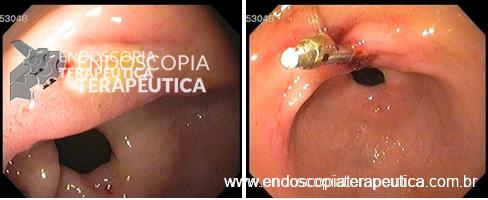
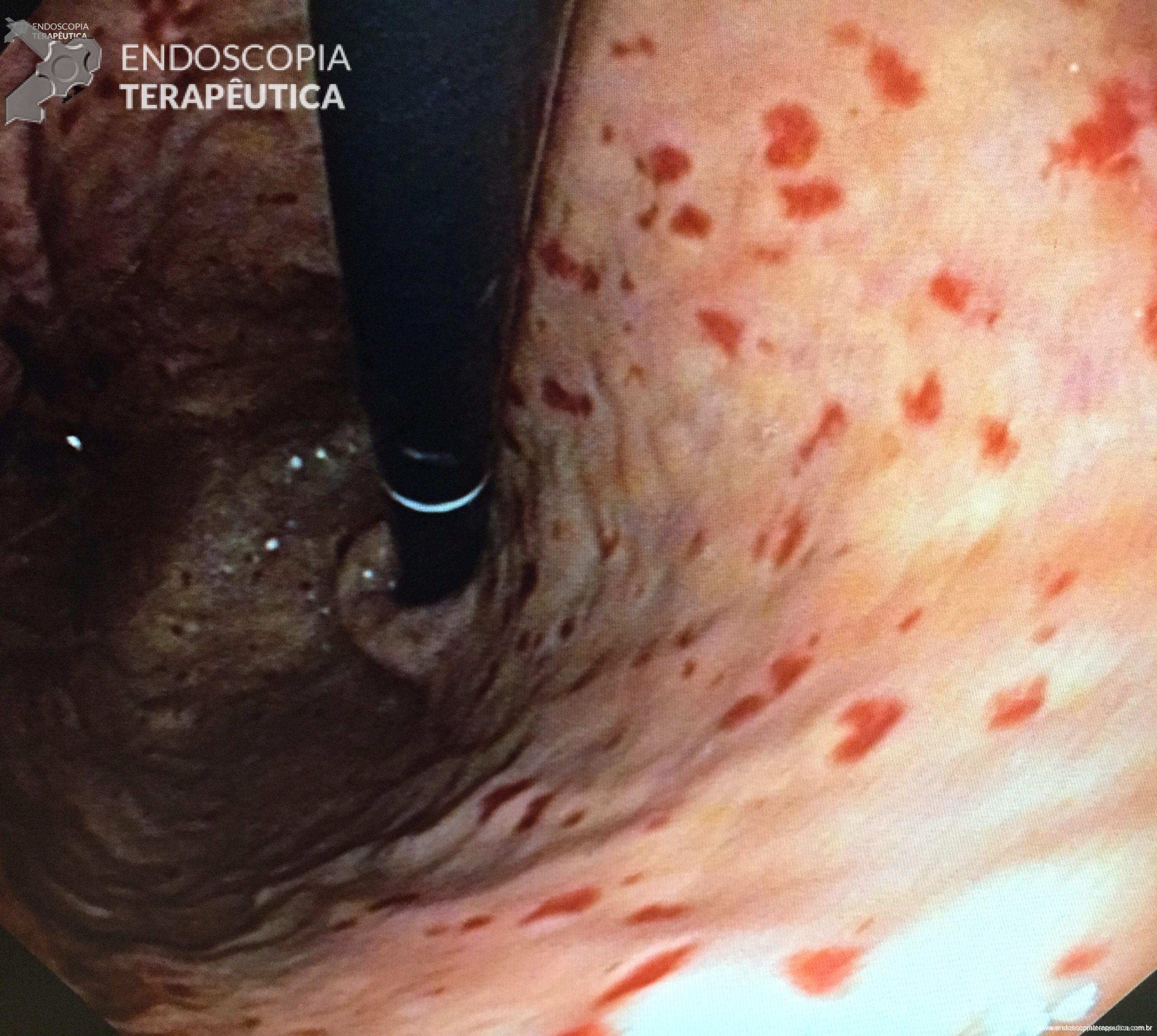
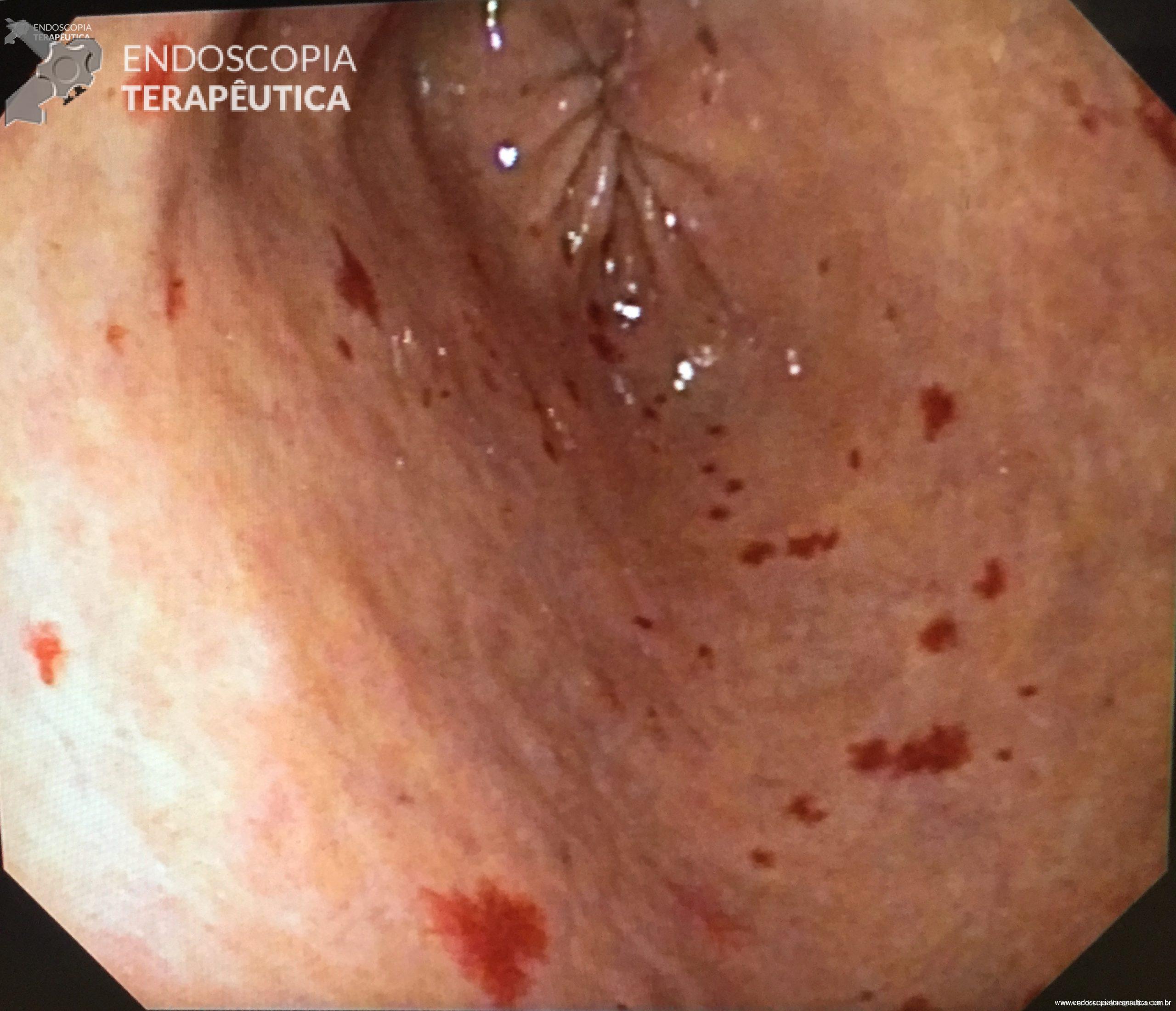
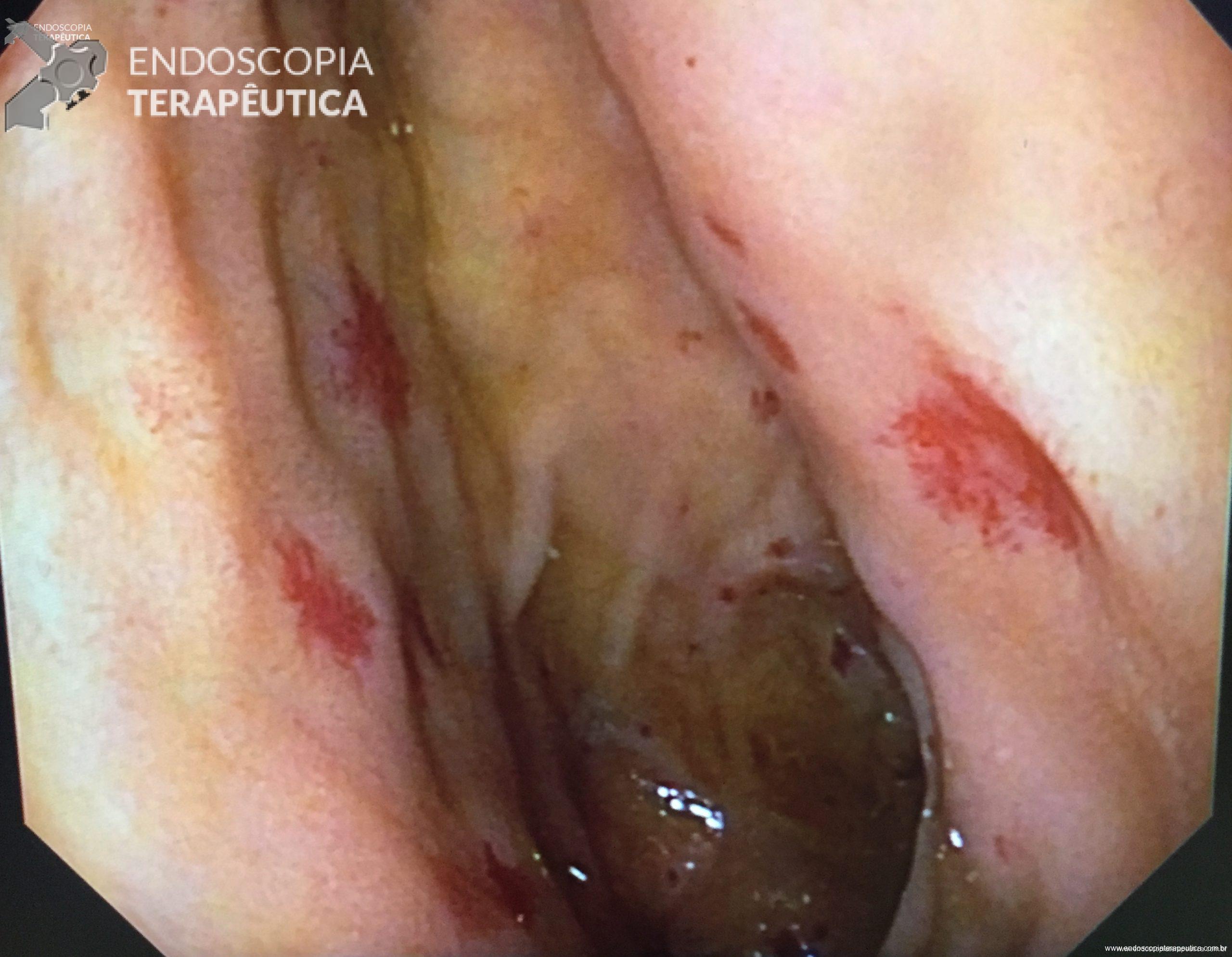
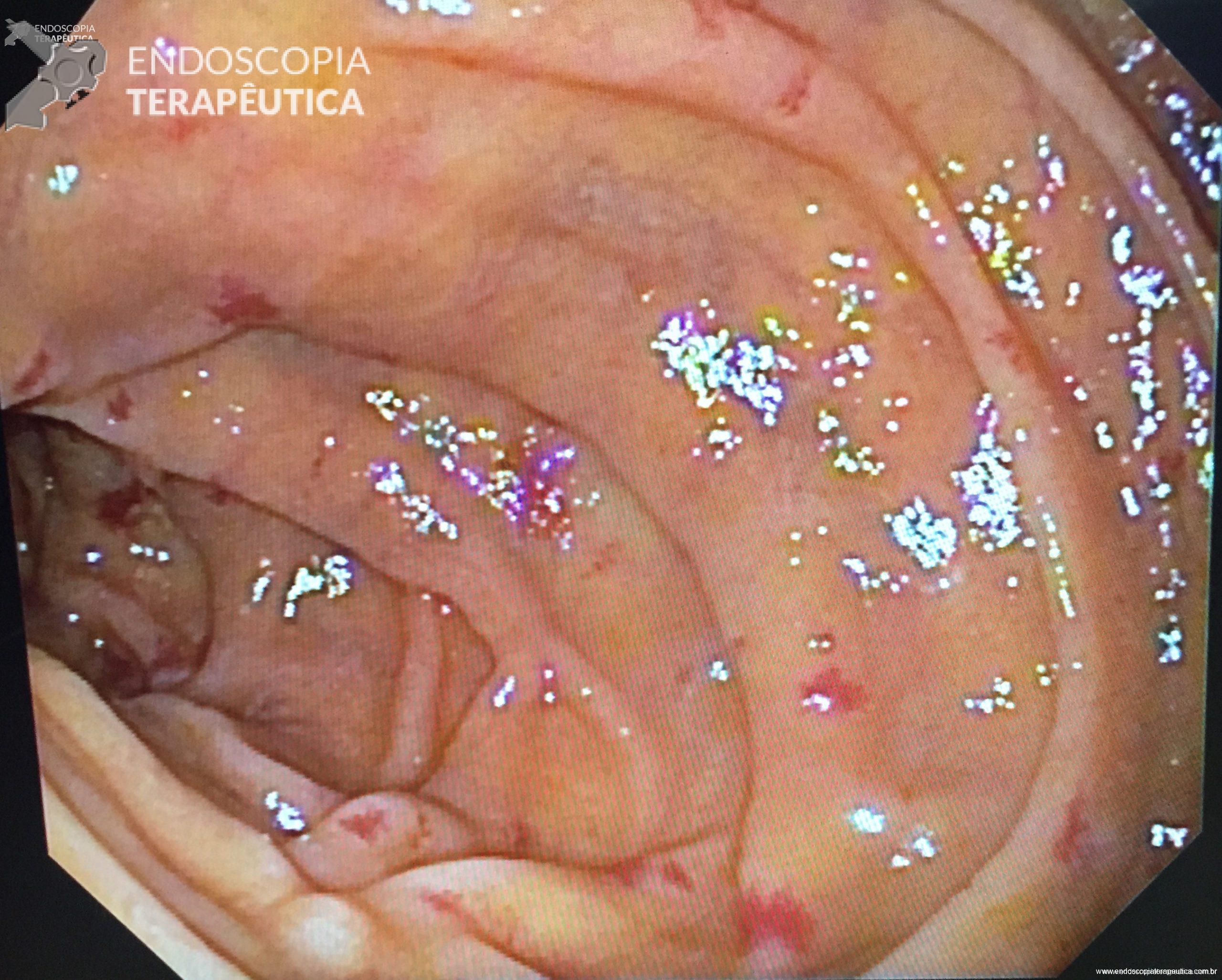
Video-based supervision for training of endoscopic submucosal dissection
Video-based supervision for training of endoscopic submucosal dissection.
Comments from the authors.
Amit Bhatt, MD, Cleveland Clinic.
Seiichiro Abe, MD, National Cancer Center.
1. Analysis of the results showed a similar performance between the experienced endoscopist and the resident. Regardless of technical challenge that ESD represents, do you believe this technique can be disseminated and performed by a growing number of endoscopists?
Amit Bhatt: While our study did not detect a performance difference between an experienced endoscopist and trainee in a porcine model, we believe endoscopic experience will likely have a larger impact in human ESD, where lesions are not always in optimal position and an endoscopist has to deal with respiratory movement, peristalsis, and bleeding.
ESD is technically challenging and should be performed by skilled endoscopists. We hope as the first generation of Western ESD endoscopists establish themselves they will teach and share the technique with others leading to the expansion of ESD outside of Asia. We are now beginning to train our own advanced endoscopy fellow hands on in ESD.
Seiichiro Abe: The results of our study indicated that the endoscopic maneuvers of ESD were totally different from those of other advanced endoscopy, but could be acquired by an expert supervision even in the video-based study. Actually, some Western endoscopists who had the supervision of Japanese experts successfully introduced human ESD in their countries. Thus, standardized training systems of ESD should be established in collaboration between Western countries and Japan.
2. Could video recording with further analysis by an expert replace or minimize the presence of a supervisor in the training room?
We still believe the best way to learn ESD is a mentor apprentice approach as used in Japan, but do realize this option is not available for most. For those without the options for hands on mentorship, video based supervision can be a great option for learning the technique.
3. How have you observed the expansion of ESD in the US? What are the main indications?
We started our ESD program at Cleveland Clinic in 2013, and since then have seen a rapid growth in our ESD cases. We primarily perform ESD on esophageal adenocarcinoma, gastroesophageal junction cancers, and lateral spreading tumors in the colon. While gastric cancer is less common in the West, there are specific at-risk patient populations (Asian descent, hereditary polyposis patients) that develop gastric cancer that we perform ESD on. A growing indication for ESD has been undifferentiated submucosal tumors not involving the muscularis propria. Many patients would prefer resection rather than continued EUS surveillance. We have also had good success with ESD for carcinoid tumors with negative free margin resection better than endoscopic mucosal resection.
4. In the US, magnifying devices are not approved for use by the FDA, what is the impact of this on doctors who are learning or performing ESD?
Amit Bhatt: In Japan, magnified endoscopic evaluation is used to differentiate non-neoplastic from neoplastic colorectal tumor and to estimate the depth of invasion with a high degree of accuracy. This allows appropriate triaging of patients to either colorectal ESD or surgery. Unfortunately magnifying endoscopies with optical zoom (from 80x to 100x) are not commonly available outside of Asia, leading many Western endoscopists to miss this important pre-procedure assessment. But there is growing belief that the Olympus near focus system (50x) is able to deliver similar magnified pit pattern and vessel analysis but this is yet to be validated.
Seiichiro Abe: Because magnified endoscopy allows appropriate treatment strategy based on the precise prediction of the histology and the depth of invasion, it can avoid oversurgery and unnecessary ESD. However, magnifying endoscopy has little impact on the technical performance and learning curve of ESD.
5. Is there any evidence of maintenance of after-training acquired skill with a minimum number of ESD procedures to be performed in a given period?
We believe just like ERCP, ESD needs to be performed on a regular basis to maintain and improve skill levels. As ESD is just beginning to develop and establish itself outside of Asia, it difficult to say what the “number of procedure per year” is to maintain proficiency. When we started performing ESD at least monthly allowed us to continue to develop our skill in the technique, and that could be used as a rough guide.
6. Congratulations on the excellent publication! Thank you very much for the opportunity to have your participation in our blog. Would you like to add any further comments?
Thank you for the opportunity to participate in your blog. We hope our study is beneficial for those learning ESD.