Antibioticoprofilaxia em pacientes com obstrução biliar submetidos à CPRE
Introdução
O uso de antibióticos profiláticos de rotina em pacientes submetidos à Colangiopancreatografia Retrógrada Endoscópica (CPRE) não é recomendado pelas principais sociedade de endoscopia do mundo, incluindo a American Society for Gastrointestinal Endoscopy (ASGE) e European Society of Gastrointestinal Endoscopy (ESGE) (1,2). Embora exista consenso de que a antibioticoprofilaxia peri-procedimento reduz a incidência de bacteremia pós-CPRE, seu impacto na prevenção de colangite e sepse ainda permanece controverso. Análises de subgrupos de diferentes trabalhos identificaram populações que poderiam se beneficiar do uso profilático de antibióticos antes da CPRE – pacientes com alto risco de drenagem biliar difícil/incompleta, imunocomprometidos e submetidos à colangioscopia – limitando a indicação do uso de antibioticoprofilaxia apenas para esses grupos (1,2).
Uma metanálise publicada em 2022, com 10 ensaios clínicos randomizados (ECR) comparando o uso de antibioticoprofilaxia em pacientes submetidos à CPRE eletiva, incluiu 1757 pacientes e demonstrou redução da bacteremia no grupo antibiótico, porém não houve diferença em relação à colangite ou sepse (3).
Uma importante crítica em relação aos estudos utilizados para embasar as recomendações é a falta de seleção adequada de pacientes. Trabalhos mais antigos sugeriram possível benefício da antibioticoprofilaxia em pacientes com obstrução biliar (4,5). Nesse contexto, um grupo sul-coreano conduziu um ECR comparando o uso de antibioticoprofilaxia em pacientes com obstrução biliar submetidos à CPRE (6).
Métodos
Desenho do estudo
Ensaio clínico randomizado 1:1, duplo-cego, realizado em centro terciário único.
Seleção de pacientes
Critérios de inclusão: adultos com obstrução biliar documentada por exame de imagem (tomografia ou ressonância magnética) submetidos à CPRE.
Critérios de exclusão: evidência de infecção (leucócitos > 11.000 e/ou febre T>= 38oC), uso de antibióticos nas últimas 72 horas, gravidez e alergia ao antibiótico.
Grupos do estudo
- Intervenção (antibiótico): Cefoxitina 1g IV em 10ml de SF0,9% 30min antes da CPRE.
- Controle (placebo): 10ml de SF0,9% 30 min antes da CPRE. A escolha do antibiótico foi baseada no perfil microbiológico local, em conjunto com a equipe de infectologia do hospital.
Desfechos
- Primário: incidência de complicação infecciosa pós-CPRE (bacteremia, colangite e colecistite).
- Secundário: incidência de cada complicação infecciosa específica, demais complicações pós-CPRE (pancreatite e sangramento).
Cálculo amostral
400 pacientes (considerando 10% de perda).
Resultados
População
- 378 pacientes randomizados entre 2017–2021
- 189 em cada grupo
- Análise final: 176 (antibiótico) vs. 173 (placebo)
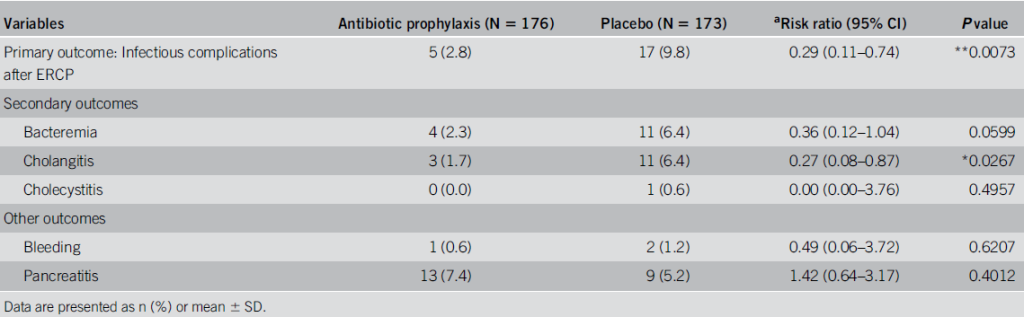
Desfecho primário
Houve redução significativa de complicações infecciosas no grupo antibiótico.
- Antibiótico: 2,8% (5/176)
- Placebo: 9,8% (17/173)
- Risco Relativo (RR): 0,29; IC 95%, 0,11–0,74; p=0.0073
Desfechos secundários
Bacteremia: sem diferença estatisticamente significativa.
- Antibiótico: 2,3% (4/176)
- Placebo: 6,4% (11/173)
- RR: 0,36; 95% CI, 0,12–1,04; p=0,0599
- Dos 15 pacientes com bacteremia, 10 evoluíram com sepse.
Colangite: houve redução significativa.
- Antibiótico: 1,7% (3/176)
- Placebo: 6,4% (11/173)
- RR: 0,27; 95% CI, 0.08–0.87; p=0,0267
Colecistite: ocorreu em apenas 1 paciente do grupo placebo.
Demais complicações (sangramento, pancreatite): sem diferença entre os grupos.
Análise de subgrupos
Etiologia maligna vs. benigna
Houve maior incidência de complicações no grupo placebo em ambas as etiologias.
Entretanto, a diferença foi significativa apenas para colangite na etiologia benigna, com incidência de 3,1% no grupo antibiótico vs. 10,2% no grupo placebo (p=0,0421)
Drenagem biliar completa
Mesmo nos casos em que houve drenagem biliar completa, observou-se benefício do antibiótico profilático:
Complicações infecciosas: antibiótico 3,1% vs. placebo 10,6% (p=0,0077)
Colangite: antibiótico 1,9% vs. placebo 6,9% (p=0,0279)
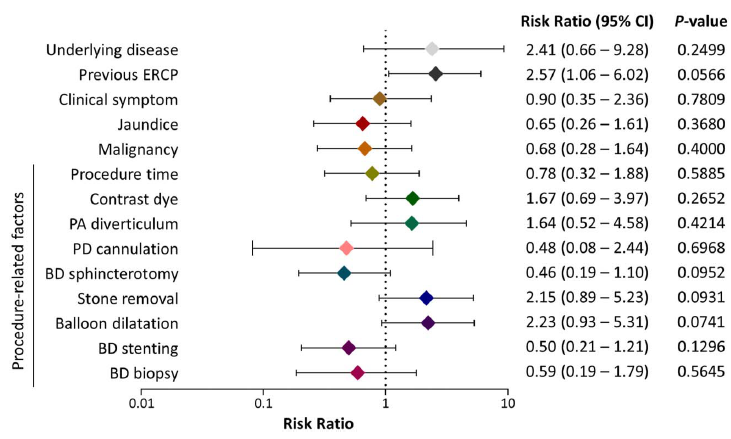
Fatores de risco relacionados ao procedimento, como CPRE prévia, retirada de cálculos e dilatação balonada, apresentaram tendência a maior risco de complicações infecciosas pós-CPRE no grupo placebo; contudo, não houve significância estatística (Figura 2).
Discussão
Este ECR duplo-cego robusto demonstrou que o uso de antibiótico profilático pré-CPRE, em pacientes com obstrução biliar sem infecção manifesta, reduz a incidência de complicações infecciosas pós-procedimento, incluindo colangite, mesmo em pacientes nos quais houve drenagem biliar completa.
Esses achados contrastam com as recomendações atuais dos guidelines das principais sociedades de endoscopia do mundo (ASGE e ESGE), e podem representar uma possível mudança de paradigma.
Embora a colangite tenha apresentado redução significativa, esse achado deve ser interpretado com cautela, pois se trata de desfecho secundário, o que significa que o estudo não foi dimensionado especificamente para avaliá-lo. Ainda assim, a magnitude do efeito observada sugere um possível benefício clínico real, que idealmente deve ser confirmado em estudos com cálculo amostral direcionado para esse desfecho.
Apesar dos benefícios demonstrados, os autores colocam que é importante estudar o impacto do aumento do uso de antibióticos profiláticos no perfil de resistência das bactérias, sendo importante uma avaliação conjunta com o serviço de infectologia de cada hospital para a escolha do antibiótico ideal.
É importante ressaltar que o estudo não recomenda antibioticoprofilaxia de rotina para toda CPRE, mas sim apenas em pacientes com obstrução biliar manifesta.
Por fim, os autores sugerem que o benefício da antibioticoprofilaxia pode ser maior em pacientes com CPRE prévia e quando há maior manipulação da via biliar – como quando há dilatação balonada e retirada de cálculos.
Conclusão
O estudo traz evidência robusta de que a antibioticoprofilaxia em pacientes com obstrução biliar submetidos à CPRE reduz complicações infecciosas, incluindo a colangite — mesmo em casos de drenagem completa.
Diante desses achados, é possível que as diretrizes passem por reavaliação nos próximos anos à luz de toda a literatura disponível. Enquanto isso, na prática clínica, vale considerar o uso de antibioticoprofilaxia em pacientes selecionados com obstrução biliar e indicação de CPRE, individualizando a decisão caso a caso.
Referências
- ASGE Standards of Practice Committee, Khashab MA, Chithadi KV, et al. Antibiotic prophylaxis for GI endoscopy. Gastrointest Endosc. 2015;81(1):81-89. doi:10.1016/j.gie.2014.08.008
- ASGE Standards of Practice Committee, Khashab MA, Chithadi KV, et al. Antibiotic prophylaxis for GI endoscopy. Gastrointest Endosc. 2015;81(1):81-89. doi:10.1016/j.gie.2014.08.008
- Merchan MFS, de Moura DTH, de Oliveira GHP, et al. Antibiotic prophylaxis to prevent complications in endoscopic retrograde cholangiopancreatography: A systematic review and meta-analysis of randomized controlled trials. World J Gastrointest Endosc. 2022;14(11):718-730. doi:10.4253/wjge.v14.i11.718
- Niederau C, Pohlmann U, L¨ubke H, et al. Prophylactic antibiotic treatment in therapeutic or complicated diagnostic ERCP: Results of a randomized controlled clinical study. Gastrointest Endosc 1994;40(5):533–7.
- van den Hazel SJ, Speelman P, Dankert J, et al. Piperacillin to prevent cholangitis after endoscopic retrograde cholangiopancreatography. A randomized, controlled trial. Ann Intern Med 1996;125(6):442–7.
- Leem G, Sung MJ, Park JH, et al. Randomized Trial of Prophylactic Antibiotics for Endoscopic Retrograde Cholangiopancreatography in Patients With Biliary Obstruction. Am J Gastroenterol. 2024;119(1):183-190. doi:10.14309/ajg.0000000000002495
Como citar este artigo
Proença IM. Antibioticoprofilaxia em pacientes com obstrução biliar submetidos à CPRE. Endoscopia Terapeutica, 2026 Vol I. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/antibioticoprofilaxia-em-pacientes-com-obstrucao-biliar-submetidos-a-cpre/
Para saber mais sobre as clássicas indicações de antibioticoprofilaxia na CPRE, confira este material: Profilaxia antibiótica em CPRE.