Perfurações de trato gastrointestinal alto e colônicas. Medidas práticas de prevenção e avaliação.
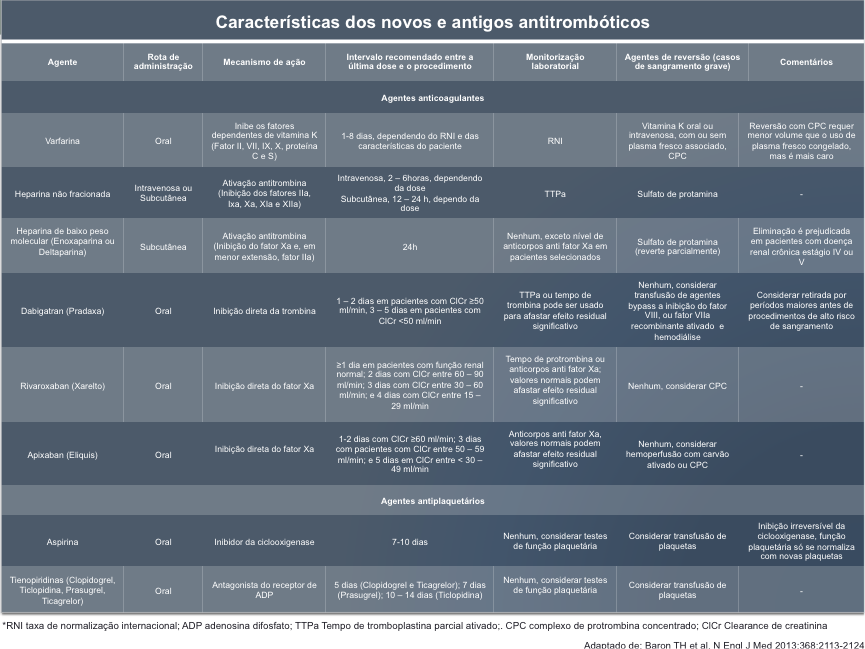
As perfurações do trato gastrointestinal são raras, porém, potencialmente graves. A gravidade não reside apenas nas possíveis complicações de morbimortalidade envolvidas (sepse, necessidade de internação prolongada, procedimentos cirúrgicos), mas principalmente porque podem afetar a relação médico paciente e até a confiança do endoscopista. Nesse artigo o autor destaca que para o endoscopista a perfuração iatrogênica em algum momento de sua carreira é tão certa quanto os impostos e a morte e a única maneira garantida de evitá-la é não realizar o procedimento endoscópico.
A incidência de perfuração aumenta quanto mais invasivo for o procedimento, mas em geral, é em torno de 0,1 % para endoscopia alta, 0,01 a 0,3% em colonoscopias, 0,4% em EUS e de 0,5 a 1,5% em CPRE.
A prevenção começa com a indicação do exame, se deve ser ou não realizado. Deve-se conhecer a história do paciente, presença de comorbidades, uso de medicações e cirurgias prévias. O procedimento deve ser agendado com tempo adequado (no nosso dia a dia é comum uma agenda com muitos exames nos levando a realizar procedimentos com curto espaço de tempo). Também é importante o conhecimento do material utilizado (clipes, bisturi elétrico, o endoscópio em uso), ter uma equipe de apoio com treinamento para manejo de emergências (material pronto e organizado) e principalmente, o endoscopista precisa conhecer seus limites pessoais. Este é o ponto mais importante. O profissional deve investir em treinamento (cursos e congressos) e saber o momento de referenciar a um centro ou endoscopista de maior prática.
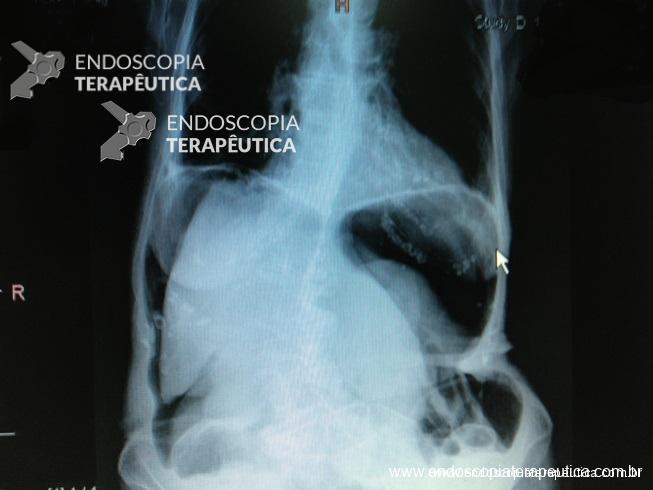
Outro ponto fundamental é reconhecer a perfuração. Isso nem sempre é simples. Não são todos os casos de perfuração que ocorre a clara visualização de gordura visceral. Um sinal bastante sugestivo que sempre nos deve fazer pensar em perfuração é a impossibilidade de se manter a insuflação do órgão por vezes associada à grande distensão abdominal. Nos casos em que a perfuração não foi identificada durante o ato endoscópico, deve-se lançar mão de exames radiológicos quando houver uma mínima suspeita (dor, taquicardia, distensão abdominal, sinais de pneumoperitôneo, enfisema subcutâneo). Muitas vezes a radiografia de abdome já confirma a presença de pneumoperitônio mas a tomografia computadorizada é o método mais sensível para perfurações menores.
Radiografia de abdome mostrando volumoso pneumoperitônio (clique para ampliar)
1- Perfurações do Esôfago :
São incomuns, mais frequentes com duodenoscópios ou aparelhos de EUS ou em pacientes com comorbidades como divertículos, estenoses ou durante procedimentos como colocação de próteses e dilatações. A perfuração pode ser identificada durante exame quando se visualiza uma laceração na mucosa. Na dúvida pode-se realizar exame com contraste iodado e fluoroscopia (se não houver, TC é o melhor exame).
Como prevenir ?
- Passagem cuidadosa de aparelhos de CPRE e EUS, por profissional com experiência na na área (considerar realizar endoscopia antes de EUS)
- Dilatações com controle endoscópico
- Não utilizar próteses por longo tempo em doenças benignas
O tratamento endoscópico deve ser individualizado, a depender do tamanho e localização. Podem ser aplicados clipes ou em casos selecionados, próteses recobertas. Sempre deve haver a avaliação conjunta da equipe de cirurgia.
2- Perfurações gástricas :
São muito raras e normalmente consequentes à procedimentos (dilatação de anastomoses, ESD, polipectomias). A avaliação para perfuração segue os princípios já descritos sendo a visualização de perfuração óbvia ou gordura as alterações mais fáceis de serem identificadas. Sempre lembrar que a dificuldade de insuflação é um dado sugestivo.
Como prevenir ?
- Evitar alça “excessiva” em duodenoscopias ou enteroscopias – pressão em quadrante superior esquerdo pode ajudar, assim como overtube em enteroscopias
- Injeção submucosa em ressecções (ter treinamento para ESD/EMR).
- Usar CO2 em procedimentos de risco.
- Antes de ressecar lesões subepiteliais, avaliá-las com EUS.
- Considerar uso de fluoroscopia em dilatações.
O tratamento depende do tamanho e natureza da lesão, mas em geral, envolve a colocação de clipes, com fechamento total da lesão.
3- Perfurações duodenais:
Podem ser não ampulares (polipectomias, ESD e dilatações) ou ampulares (CPRE). A identificação já foi discutida e segue os pricípios anteriores. Neste artigo o autor não aprofunda o tema em relação às perfurações durante CPRE por haver outros artigos específicos sobre o assunto.
Como prevenir ?
- Passagem cuidado do aparelho para segunda porção duodenal
- Conhecer os antecedentes cirúrgicos do paciente
- Injeção submucosa para tratamento de lesões mucosas
- Usar técnicas não térmicas associadas para terapia em úlceras profundas.
- CPRE – treinamento
4- Perfurações colônicas :
Ocorrem mais comumente em reto e sigmóide (53%) e ceco (23%). As perfurações são mais comuns em polipectomias de pólipos maiores que 10mm e em ESD de lesões extensas (risco pode chegar a 10%) ou em colocação de stents (7%). No contexto da colonoscopia diagnóstica normalmente se segue por trauma do aparelho, divertículo, presença de angulação, “alça excessiva” ou durante retrovisão.
São fatores de risco :
- Diverticulose intensa
- Colite em atividade
- Pacientes idosos
- Aderências (cirurgias previas)
- Radioterapia / uso de corticóides
- Pólipos volumosos
- Preparo de cólon irregular
Cerca de 30% dos casos são identificadas durante o exame com achado de lesão mucosa, visualização da serosa, gordura ou cavidade peritoneal. O uso de azul de metileno na solução injetada durante polipectomia/ESD pode revelar lesão esbranquiçada central (perfuração) com halo avermelhado (muscular) no local.
Quando não identificada a perfuração colônica costuma se manifestar em 24 horas , como qualquer outra perfuração do TGI, com taquicardia, dor e distensão abdominal, impondo-se o exame radiológico (em especial TC, onde pode avaliar coleções). As perfurações de reto extraperitoneais podem cursar com enfisema subcutâneo abdominal, nos membros e até na região cervical.
Como prevenir ?
- Exame sob visão. Evitar manobras “as cegas” (slide by);
- Evitar exame quando o preparo está irregular/ruim (remarcar). Lembrar que perfuração com cólon “sujo” pode piorar o prognóstico;
- Utilizar água durante o exame : Atua como lubrificante e seu peso “abre” áreas de angulação;
- Utilizar gastroscópios/ colonoscópios infantis em casos de estenose, tumores ou diverticulose intensa;
- Evitar “alça excessiva”, com manobras de compressão abdominal externa por auxiliar treinado;
- Saber o momento de para o exame e referenciar o paciente para endoscopista de referência ou realização de colonoscopia por TC;
- Evitar uso de pinça “hot biopsy” para pólipos pequenos;
- Durante polipectomia com alça, testar a movimentação do tecido alçado , notando a formação de “tenda”, a movimentação “em bloco” da parede colônica indica laçada total da parede;
- Injeção submucosa em pólipos largos (também evita a lesão térmica da camada muscular);
- Treinamento pessoal em ESD/EMR, referenciando procedimentos que não possua prática (evitar biópsias do centro da lesão ou tatuar muito perto da lesão, pois pode dificultar a abordagem da lesão pelo endoscopista referenciado);
- Uso de radioscopia durante dilatações e colocação de próteses.
Sempre na presença de perfurações a avaliação e acompanhamento do grupo de cirurgia é mandatório. O paciente nunca deve ser dispensado do hospital/clínica na suspeita de perfuração sem uma avaliação rigorosa do quadro. Sempre fornecer ao paciente meios para entrar em contato (contatos telefônicos/hospitalares) em casos de sintomas após os exames (dor, febre, distensão abdominal) e sempre informar o paciente e familiares sobre a realização de procedimentos endoscópicos durante seu exame, como polipectomias.
Você já teve um caso de perfuração ? Como conduziu ? Compartilhe suas experiências nos comentários abaixo!
Artigo original :
Para saber mais sobre este tema e outros relacionados, acesse o site Gastropedia clicando aqui!
Assuntos relacionado
Vídeo – Ressecção de adenoma de duodeno em paciente com PAF
Imagens – ESD de neoplasia precoce gástrica
Artigo comentado – Vigilância endoscópica em pacientes com múltiplos pólipos coloretais
O papel da endoscopia no manejo das lesões gástricas