Laringoespasmo
O laringoespasmo é até certo ponto uma ocorrência comum para os anestesiologistas, mas, muitas vezes, desconhecida do médico endoscopista.
Apesar de não ter uma frequência tão elevada, um episódio com tratamento tardio ou inadequado pode ser catastrófico.
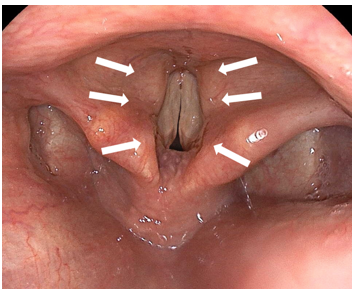
De forma resumida, seria o fechamento glótico causado por um reflexo exacerbado de constrição da musculatura intrínseca da laringe. É essencialmente um mecanismo de proteção para prevenir entrada de material estranho na árvore brônquica. Como resultado, haverá impedimento da ventilação, levando à hipoxia e à hipercapnia.
O problema é autolimitado na maior parte dos casos, pois por tempo prolongado, a hipoxia e a hipercapnia cessam o reflexo de espasmo. Contudo, em certos episódios, o espasmo pode se prolongar e trazer riscos ao paciente.
Etiologia
Apesar de ter etiologia multifatorial, a manipulação da via aérea é o principal fator implicado. A incidência é maior em crianças, pacientes com infecções do trato respiratório, ou asma, tabagistas, portadores de apneia obstrutiva do sono, refluxo gastresofágico importante e obesos. Além disso, o risco é maior em casos de manipulação de via aérea e em procedimentos na cavidade oral e faringe.
A endoscopia digestiva alta e a broncoscopia estão diretamente relacionadas ao laringoespasmo pelo estímulo direto da região. Outras associações seriam anestesia superficial no início e final desses procedimentos e regurgitação.
Muitas drogas têm sido estudadas na prevenção do laringoespasmo. Pré-medicaçao com benzodiazepínicos reduz os reflexos de via aérea. Lidocaína tópica (4mg/kg) ou venosa (1,5-2mg/kg) parece também trazer benefício. Cuidados não medicamentosos: manter o paciente em decúbito lateral esquerdo no periprocedimento.
O laringoespasmo pode ser parcial, havendo passagem de certa quantidade de ar, levando a estridor inspiratório; ou completo, não havendo passagem de ar e ausência de sons respiratórios. Em ambos os casos, sinais de obstrução podem ser notados, como: retração intercostal e movimentos paradoxais do tórax e do abdome. Sinais tardios: dessaturação, bradicardia e cianose.
Tratamento
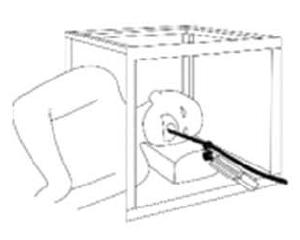
O tratamento consiste primeiramente em identificar e cessar o fator desencadeante.Após, aplicar pressão positiva com oxigênio a 100%, anteriorização da mandíbula e manobra de Larson (figura1). Essa técnica abre as vias aéreas e causa dor periosteal, ajudando a relaxar as cordas vocais pelo sistema nervoso autônomo.
- Cessar o fator desencadeante
- Pressão positiva com oxigênio a 100%,
- Anteriorização da mandíbula
- Manobra de Larson
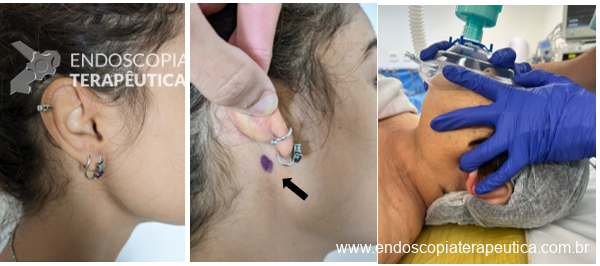
Após, aplicar pressão positiva com oxigênio a 100%, anteriorização da mandíbula e manobra de Larson (figura 1). Essa técnica abre as vias aéreas e causa dor periosteal, ajudando a relaxar as cordas vocais pelo sistema nervoso autônomo. Obtendo-se melhora do quadro, o diagnóstico seria de espasmo parcial. Persistindo o quadro, seria um caso de laringoespasmo completo, sendo importante a ajuda de outro profissional e aprofundamento da anestesia com Propofol (0,25-0,8mg/kg). Provavelmente será necessário ventilar o paciente em consequência de apneia transitória.
A chance de reversão do quadro com Propofol é bastante alta. Todavia, se não houver melhora, utiliza-se Succinilcolina (0,1mg/kg-1,2mgkg EV ou 3-4mg/kg IM). Ter em mente que o Propofol é preferível frente à Succinilcolina, já que nessa dose não acarreta muita repercussão hemodinâmica e não traz risco de paralisia muscular.
Algoritmo de tratamento escalonado enquanto não há melhora do quadro:
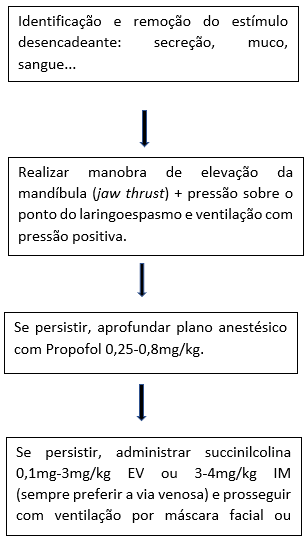
Conclusão
É de suma importância identificar os fatores de risco para o desenvolvimento do laringoespasmo e reconhecê-lo rapidamente, antes que a condição do paciente se deteriore. Uma sedação profunda para realização da endoscopia é essencial.
Além disso, o conhecimento das doses das principais medicações utilizadas para reverter o espasmo: propofol e succinilcolina.
Finalmente, importante avaliar se o paciente não cursou com broncoaspiração ou edema agudo de pulmão por pressão negativa pelo esforço respiratório contra obstrução.
Referências:
- Landsman IS. Mechanisms and treatment of Laryngospasm. Int Anesthesiol Clin. 1997 Summer;35(3):67-73. PMID: 9361977
- Alalami AA, Ayoub CM, Baraka AS. Laryngospasm: review of different prevention and treatment modalities. Paediatr Anaesth. 2008 Apr;18(4):281-8. doi: 10.1111/j.1460-9592.2008.02448.x. PMID: 18315632
- Soares RR, Heyden EG. Tratamento do Laringoespasmo em anestesia pediátrica por digitopressão retroauricular: relato de casos. Rev. Bras. Anestesiol. Dez 2008; 58:6:631-636
- Chen Y, Zhang X. Acute postobsctrutive pulmonry edema following laryngospasm in elderly patients: a case report. J Perianesth Nurs. 2019 Apr;34(2):250-258. PMID: 30100095
- Moura TSM, Silva FCP, Taves LOAF. Laringoespasmo em anestesia pediátrica. Rev Med Minas Gerais 2018;28 (Supl 8): S20-S27
Como citar este arquivo
Elder P. Laringoespasmo. Endoscopia Terapeutica 2023, Vol 1. Disponível em: https://endoscopiaterapeutica.net/pt/laringoespasmo/








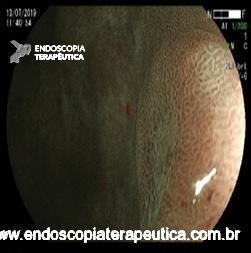
 procedimento – British Society of Gastroenterology.
procedimento – British Society of Gastroenterology.