Elaboração do laudo no exame de cápsula endoscópica do intestino delgado
O laudo da cápsula endoscópica do intestino delgado é um componente crucial no diagnóstico de diversas patologias gastrointestinais. Sua elaboração deve ser feita de forma detalhada, sistemática e precisa, uma vez que é baseado na análise de uma enorme quantidade de imagens geradas durante o exame. A qualidade desse laudo tem impacto direto tanto no diagnóstico quanto na condução clínica do paciente.
O processo de elaboração do laudo deve seguir uma estrutura lógica, que contempla aspectos anatômicos, localização dos achados, a natureza das alterações e uma estimativa de sua posição dentro do intestino delgado. Inicialmente, o laudo deve apresentar uma visão geral do exame. Devem ser incluídas informações sobre o tempo de percurso da cápsula pelo intestino delgado, a qualidade do preparo gastrointestinal e a presença de eventuais artefatos que possam interferir na interpretação, como reflexos luminosos, bolhas de ar ou resíduos. Também é importante relatar qualquer dificuldade técnica, como sobreposição de imagens ou imagens obscurecidas, e indicar se houve necessidade de intervenção endoscópica adicional. Outro ponto fundamental é informar se o exame foi completo, ou seja, se a cápsula alcançou o ceco.
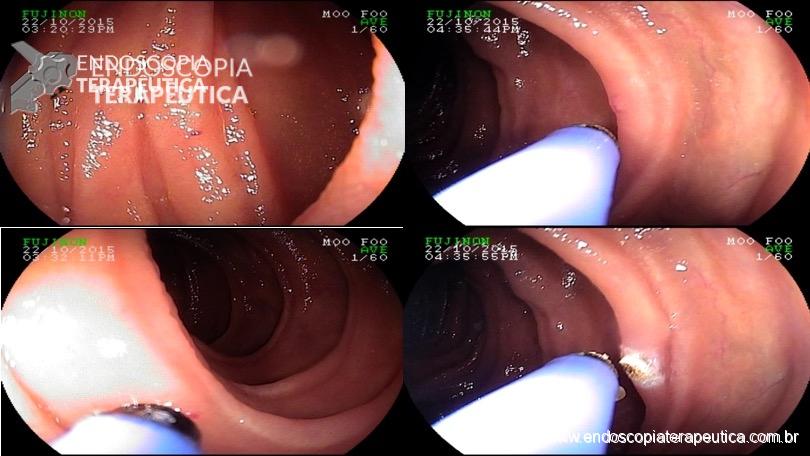
Em seguida, o laudo deve detalhar as condições anatômicas e patológicas observadas ao longo do exame. Pontos de referência anatômicos reconhecíveis, como a passagem pelo piloro e pela válvula ileocecal, além de características das pregas intestinais e da vascularização, devem ser utilizados para orientar a descrição. Apesar das limitações impostas pelo movimento peristáltico, que faz com que a cápsula avance e retroceda de forma irregular, o exame busca estimar a localização dos achados em segmentos como duodeno, jejuno proximal, médio, distal e íleo terminal.
Para facilitar essa estimativa, adota-se uma divisão pragmática baseada no tempo de percurso da cápsula entre o piloro e o ceco. O tempo total é dividido em três partes iguais, correspondendo aproximadamente aos terços proximal, médio e distal do intestino delgado. Assim, mesmo que a cápsula percorra segmentos de maneira não uniforme — por exemplo, permanecendo mais tempo em um segmento específico — os achados são descritos com base nessa divisão temporal, o que, embora não totalmente preciso, auxilia no planejamento de intervenções subsequentes, como a enteroscopia. Entender como se estabelece essa possível localização ajuda a quem recebe o laudo a formular a melhor intervenção a ser realizada.
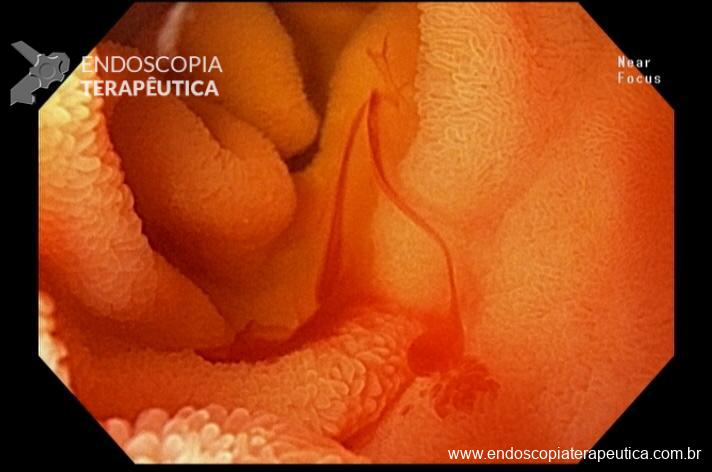
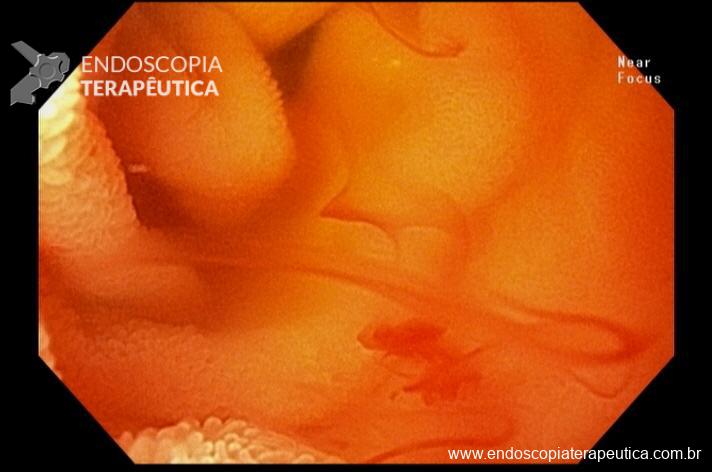
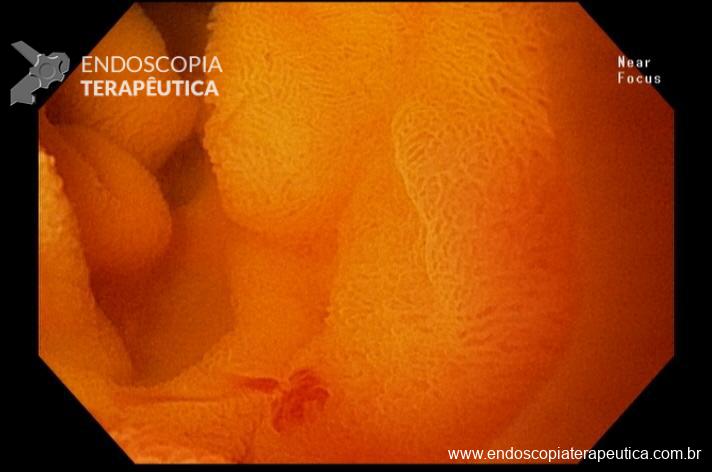
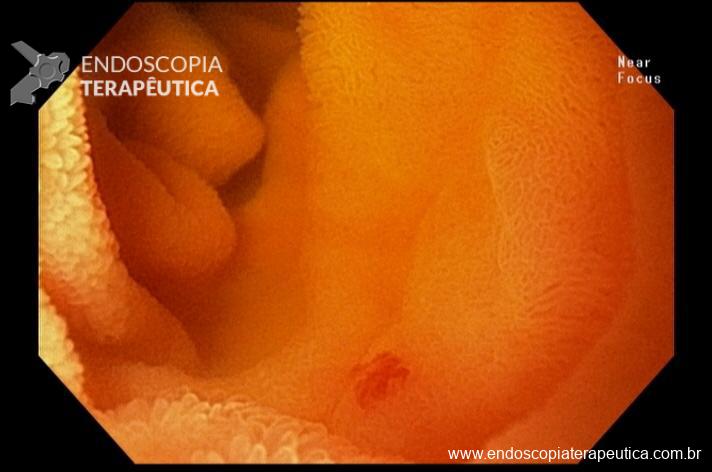
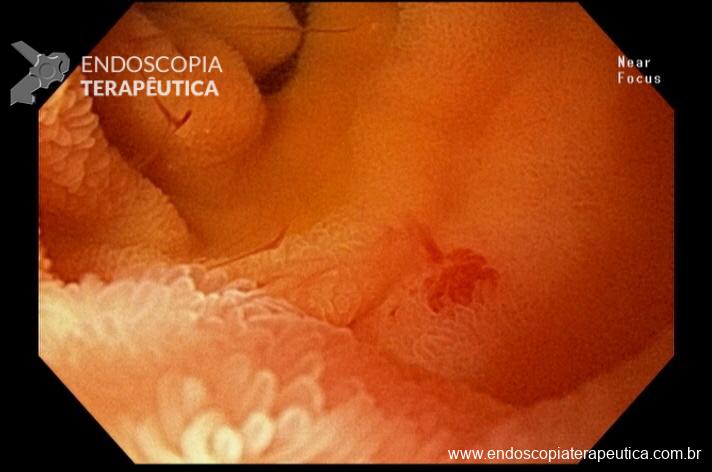
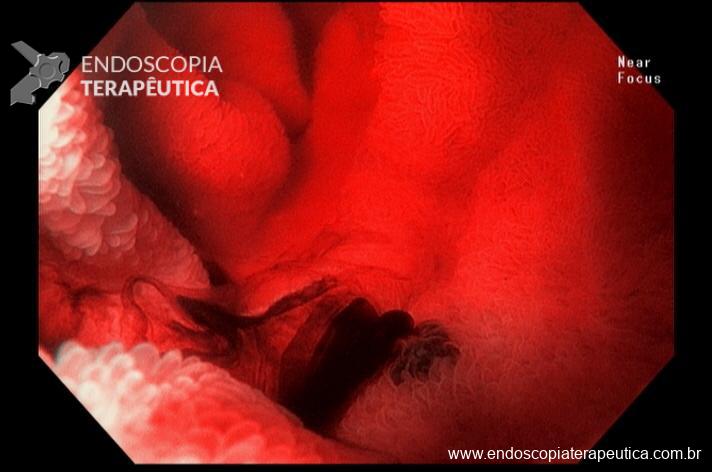
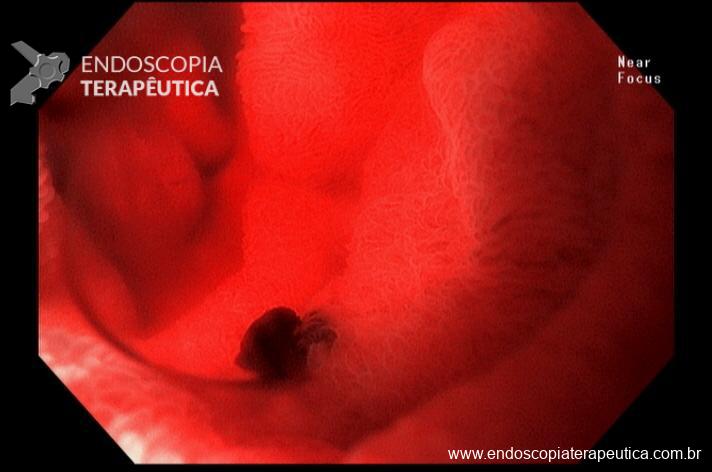
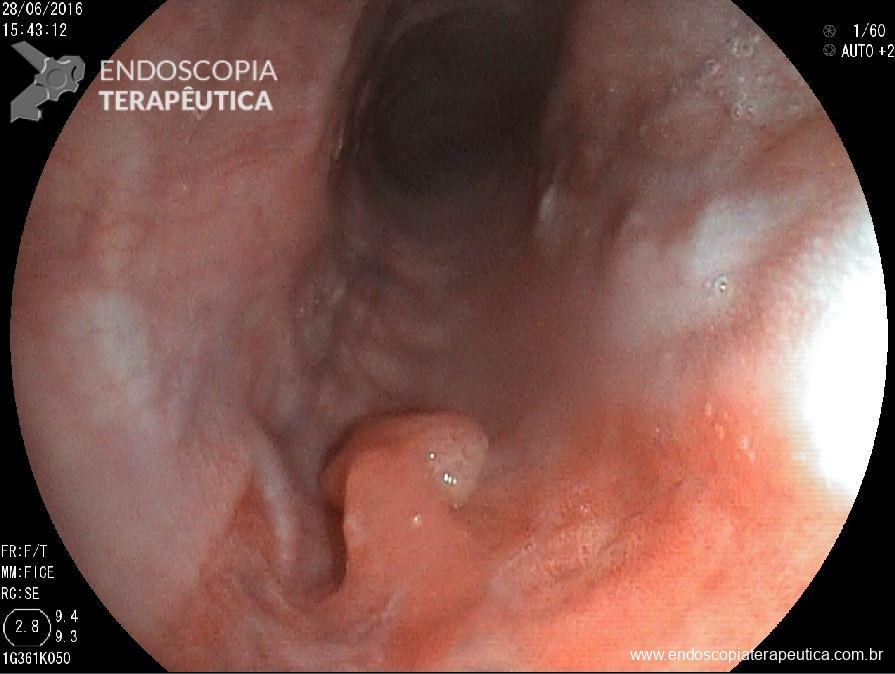
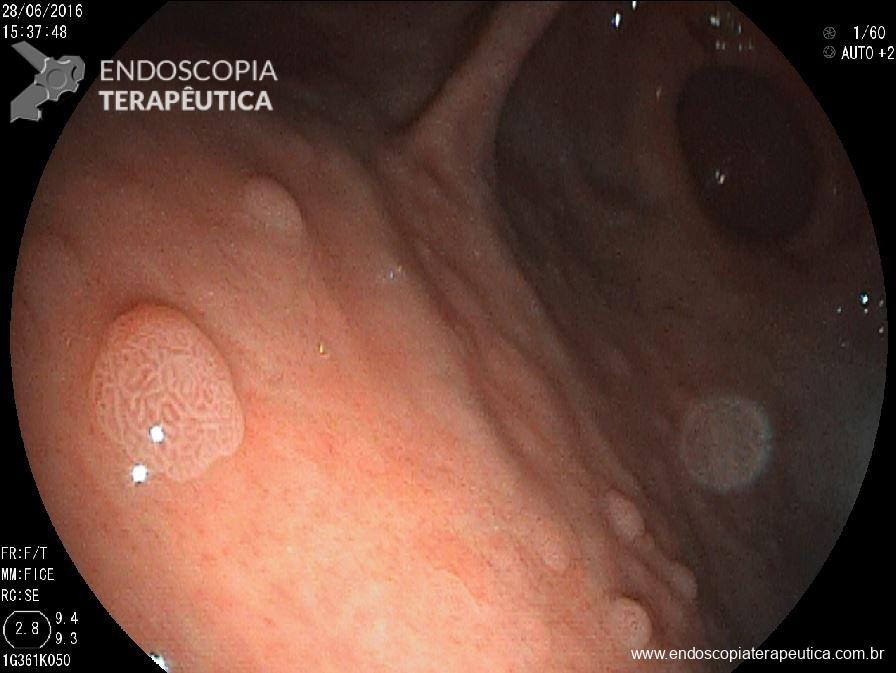
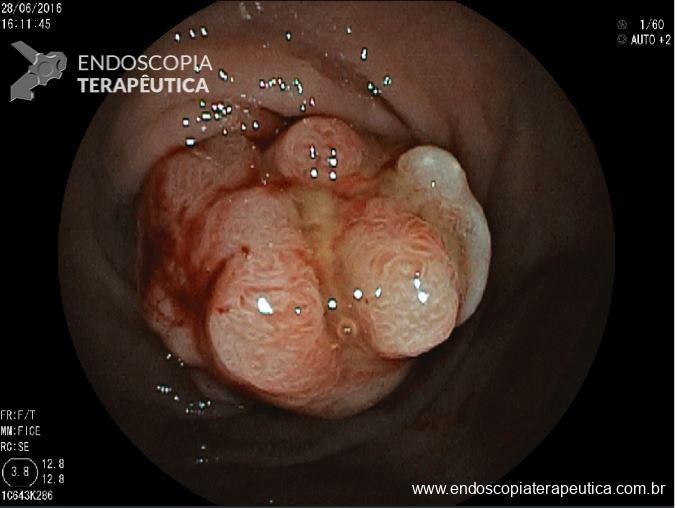
Além da localização, o laudo deve tentar caracterizar detalhadamente os achados. Devem ser descritos o tipo de alteração observada, sua aparência, a distinção entre anormalidades patológicas e variações anatômicas normais e, se possível, estimar seu tamanho. Entre os achados patológicos mais comuns estão úlceras, pólipos, angiectasias, áreas de edema e tumores. É essencial ainda avaliar se as características das lesões sugerem benignidade ou malignidade, informações que são fundamentais para guiar a conduta clínica.
Um dos grandes desafios na elaboração do laudo reside na identificação de lesões sutis. Algumas anormalidades podem ser pequenas ou apresentar características discretas, exigindo um olhar treinado para que não sejam negligenciadas. Outro fator complicador é a ausência de controle direto sobre o posicionamento da câmera, o que diferencia a cápsula endoscópica da endoscopia convencional. Isso limita a obtenção de imagens direcionadas e dificulta a captura de detalhes específicos.
Para aumentar a precisão e padronização do laudo, é recomendável utilizar terminologias e escores validados para descrever os achados. Isso facilita a interpretação por outros profissionais de saúde e contribui para a uniformidade dos relatos. É importante também reconhecer as limitações do exame. Caso alguma área não tenha sido adequadamente visualizada ou haja incerteza quanto à natureza de um achado, isso deve ser claramente explicitado no laudo, com recomendação, se necessário, de exames complementares.
O laudo deve ser concluído com um resumo dos principais achados, a provável localização das lesões, e uma avaliação do grau de certeza em relação às observações feitas. Além disso, recomendações para investigação adicional ou acompanhamento devem ser incluídas quando pertinentes.
Em resumo, a interpretação e elaboração do laudo de cápsula endoscópica do intestino delgado requerem um equilíbrio entre rigor técnico e pragmatismo clínico. A abordagem estruturada e a atenção aos detalhes tornam essa ferramenta diagnóstica extremamente valiosa na investigação de doenças do intestino delgado. Apesar das dificuldades para a leitura do exame, com um laudo bem elaborado é possível promover uma abordagem diagnóstica e terapêutica mais precisa, contribuindo significativamente para o manejo eficaz das condições gastrointestinais.
Tenham excelentes laudos!
Referências:
- Rondonotti E, Spada C, Adler S, May A, Despott EJ, Koulaouzidis A, Panter S, Domagk D, Fernandez-Urien I, Rahmi G, Riccioni ME, van Hooft JE, Hassan C, Pennazio M. Small-bowel capsule endoscopy and device-assisted enteroscopy for diagnosis and treatment of small-bowel disorders: European Society of Gastrointestinal Endoscopy (ESGE) Technical Review. Endoscopy. 2018 Apr;50(4):423-446. doi: 10.1055/a-0576-0566. Epub 2018 Mar 14. PMID: 29539652.
- Pennazio M, Rondonotti E, Koulaouzidis A. Small Bowel Capsule Endoscopy: Normal Findings and Normal Variants of the Small Bowel. Gastrointest Endosc Clin N Am. 2017 Jan;27(1):29-50. doi: 10.1016/j.giec.2016.08.003. PMID: 27908517.
Como citar este artigo
Brito HP. Elaboração do laudo no exame de cápsula endoscópica do intestino delgado Endoscopia Terapeutica 2025 Vol II. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/elaboracao-do-laudo-no-exame-de-capsula-endoscopica-do-intestino-delgado/