Diagnosticando corretamente a esofagite eosinofílica
A esofagite eosinofílica vem sendo cada vez mais diagnosticada em nosso meio devido ao conhecimento melhor desta patologia e maior acesso ao exame de endoscopia digestiva.
Classicamente a doença atinge mais homens jovens, com história de outra patologia alérgica e leva a sintomas desde disfagia até impactação de alimentos.
Para o diagnóstico necessitam-se dos seguintes critérios:
– Infiltrado eosinofílico no epitélio esofágico : mais 15 eosinófilos / campo grande aumento (400X)
– Histologia gástrica e duodenal normal (para afastar gastroenterite eosinofílica)
CASO 1
ID: LD, 30 anos, masculino, taxista, natural e procedente de São Paulo
QP: “Dificuldade para engolir”
HPMA: Paciente há 2 anos com disfagia e impactação alimentar. Refere quadro de pirose diariamente. Nega perda de peso.
HPMP: Asma (faz uso de corticóide inalatório)
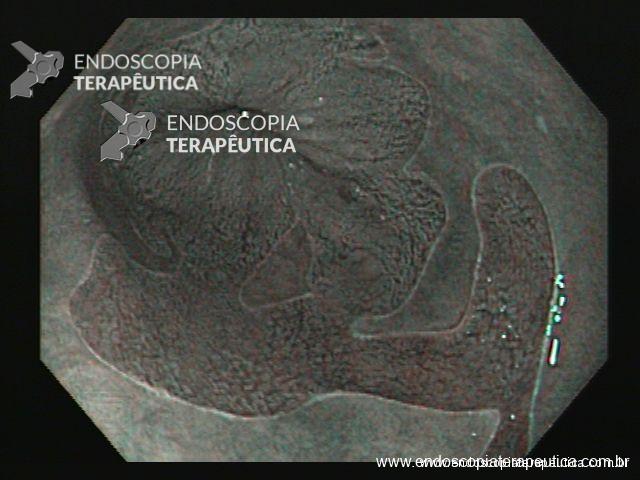
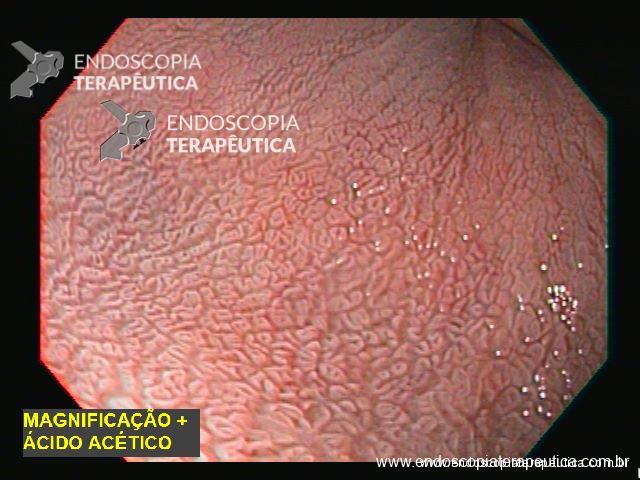
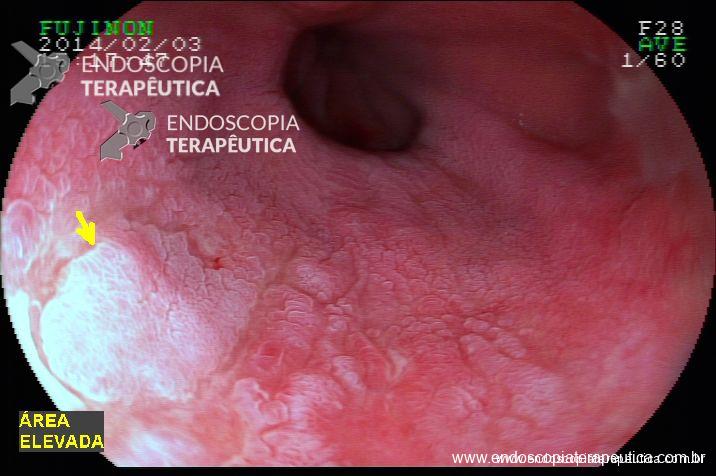
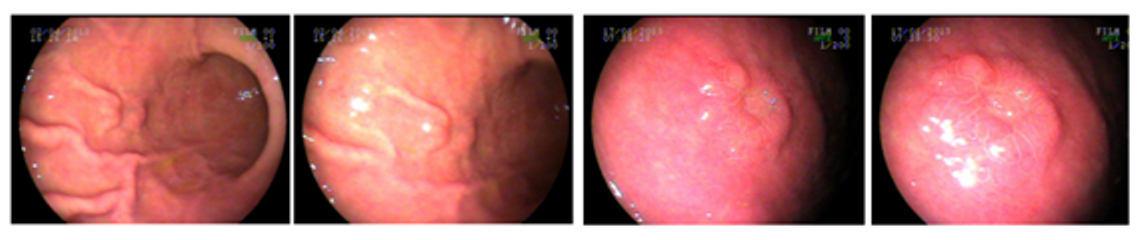
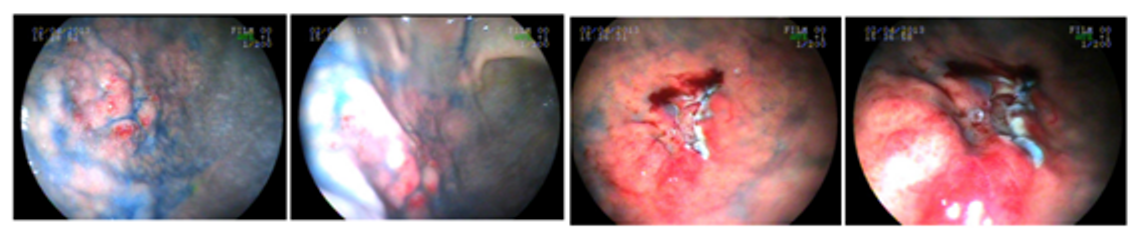
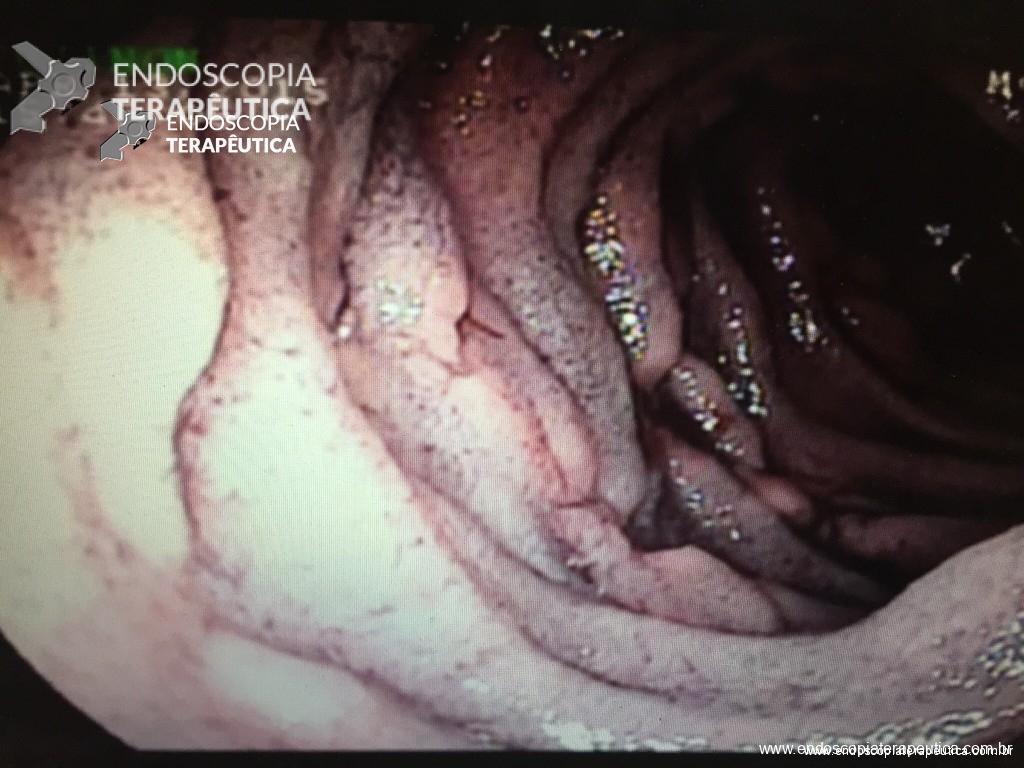
Endoscopia inicial demostrou os achados abaixo:
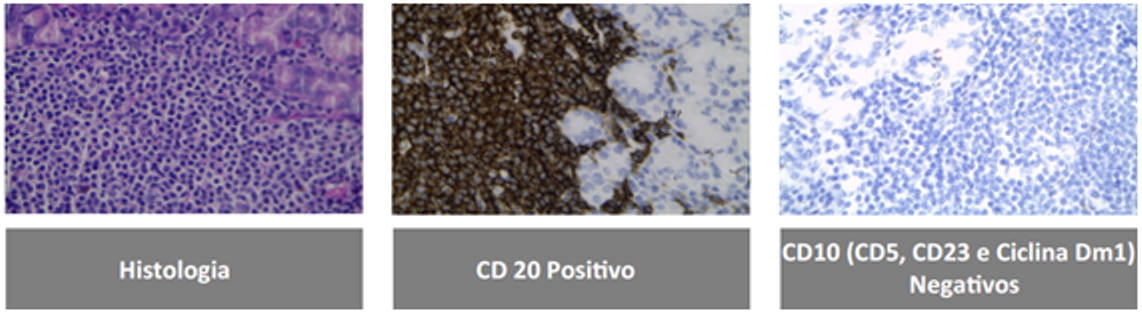
Anatomopatológico das biópsias: esofagite crônica ulcerada com eosinofilia em lâmina própria e intra-epitelial (até 35 eosinófilos / campo de grande aumento)
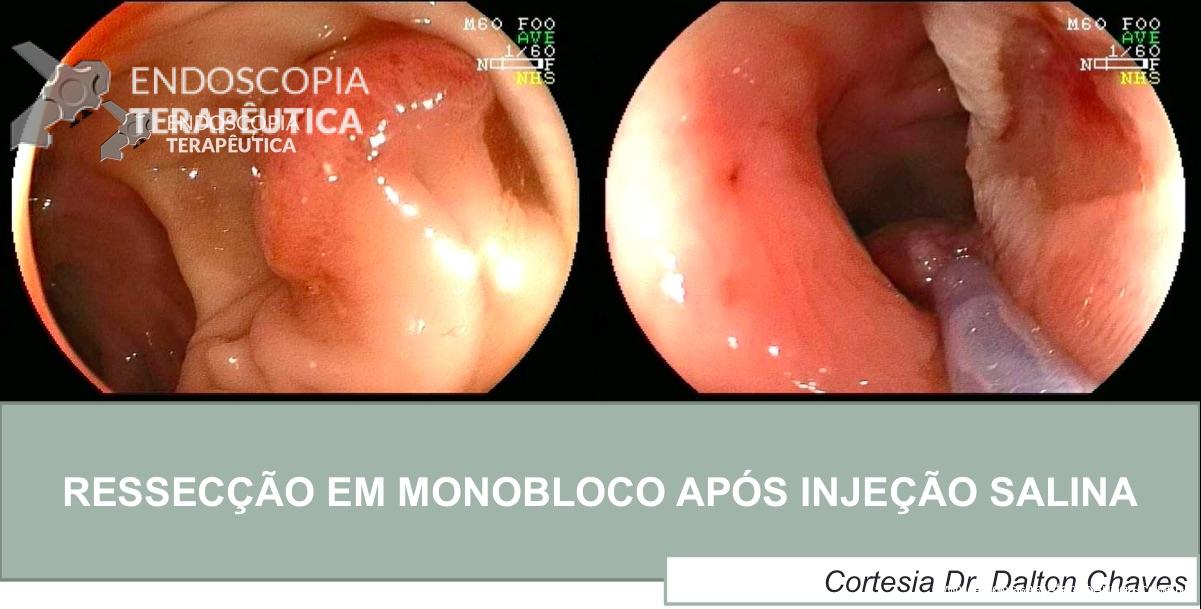
Nova endoscopia após 8 semanas de uso de IBP:
Biópsia esofágica proximal e distal: esofagite crônica moderada com 20 eosinófilos intraepiteliais / CGA
Biópsia de estômago e duodeno: ausência de eosinófilos
CONCLUSÃO: confirmado o diagnóstico de esofagite eosinofílica
CASO 2
ID: DVO, 20 anos, masculino, solteiro, sem filhos, natural e procedente de São Paulo
QP: “Queimação e dor no estômago”
HPMA: Paciente há 3 anos com quadro de pirose diariamente. Refere piora a noite e com a ingestão de determinados alimentos. Nega perda de peso.
HPMP: Nega asma, rinite ou alergias
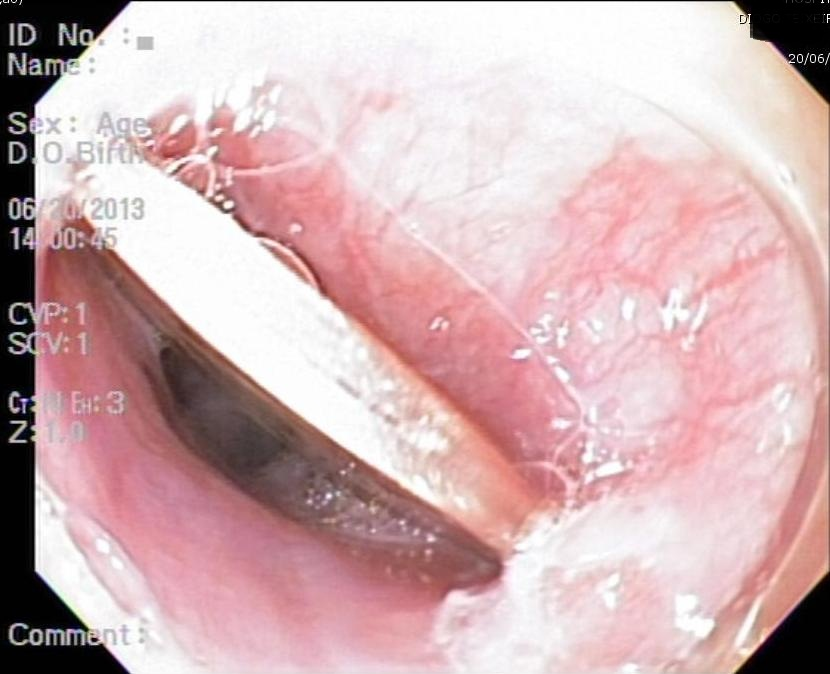
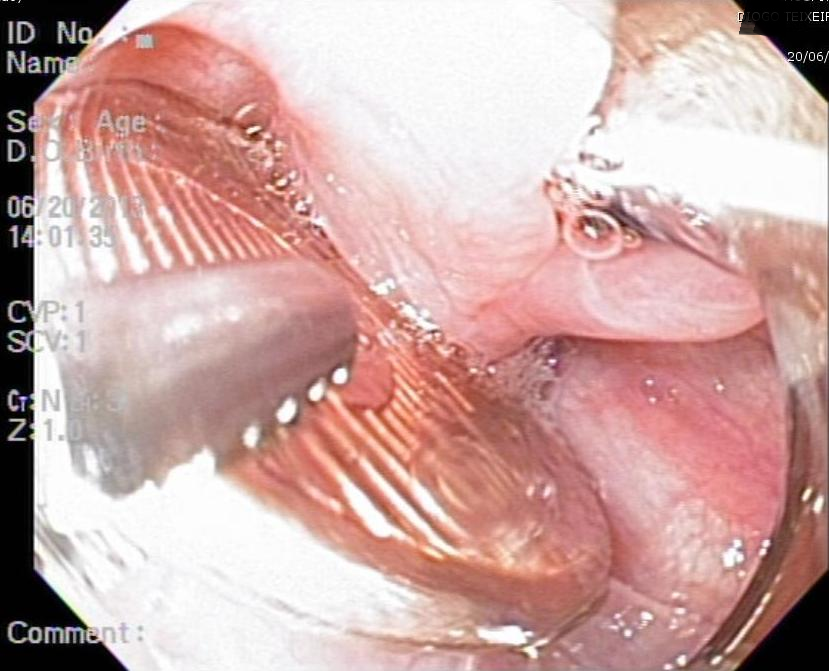
Descrição do esôfago na endoscopia inicial:
Mucosa esofágica de aspecto edemaciado e espessado em toda a extensão do órgão, apresentando estrias longitudinais e pontos de secreção mucóide aderidos difusamente, sugestivos de processo inflamatório eosinofílico. Biópsias.
Histologia: esofagite crônica moderada com 20 eosinófilos intraepiteliais / CGA
Exames laboratoriais: Leucograma: 7.650 / Eosinófilos: 24%
Dosagem de IgE: 114 UI/mL (<100 UI/mL)
Endoscopia após 8 semanas de uso de IBP:
Histologia:
Biópsia esofágica médio e proximal: esofagite crônica inespecífica. Ausência de eosinófilos neste material.
Biópsia de estômago e duodeno: ausência de eosinófilos
CONCLUSÃO: eosinofilia esofágica responsiva da IBP
Caso 3
ID: HHS, 17 anos, masculino, estudante, solteiro, natural de Urussuca-BA e procedente de São Paulo
QP: “Engasgo durante a alimentação”
HPMA: Paciente refere disfagia intermitente há 7 anos. Refere impactação alimentar tendo que subir e descer escadas para aliviar os sintomas. Nega perda de peso.
HPMP: Rinite alérgica. Asma na infância.
Descrição da endoscopia inicial:
Esôfago: mucosa com estrias enantemáticas lineares, associado a aspecto de “traqueização” em terço médio, sugestivos de esofagite eosinofílica. Biópsias.
Histologia: esofagite crônica com exocitose de eosinófilos (20 eosinófilos intraepiteliais / CGA)
Exames laboratoriais:
Leucograma: 5.480 / Eosinófilos: 12%
IgE: 993 UI/mL (<100 UI/mL)
Endoscopia após 8 semanas de uso de IBP:
Histologia:
Biópsia esofágica médio e proximal: esofagite crônica inespecífica. Ausência de eosinófilos neste material.
Biópsia de estômago e duodeno: ausência de eosinófilos
CONCLUSÃO: eosinofilia esofágica responsiva da IBP
DISCUSSÃO:
- Atualmente foi relatada uma condição chamada Eosinofilia esofágica responsiva a IBP. Esta é caracterizada por pacientes sem DRGE (endoscopia e pHmetria) que apresentam sintomas de esofagite eosinofilica e que melhoram com uso de IBP
- Relata-se também que cerca de 30-50% dos pacientes com EEo respondem ao tratamento com IBP
- Estes dois grupos de pacientes são iguais clinicamente e histologicamente, e não possuem características próprias para serem distinguidos
- Levanta-se a possibilidade de tratar-se da mesma patologia ou que os pacientes com eosinofilia responsiva ao IBP seriam na verdade pacientes que não foram diagnosticados corretamente para DRGE
- Relata-se também a possível ação anti-inflamatória dos IBPs que poderiam melhorar a eosinofilia dos pacientes com esofagite eosinofilica
Através destes conceitos podemos extrair que:
– Na suspeita de esofagite eosinofílica deve-se realizar as biópsias de rotina antes e depois do uso de IBP, para o diagnóstico e avaliação de resposta ao IBP.
– O achado de melhora da eosinofilia após 8 semanas de IBP, pode-se tratar de esofagite eosinofílica a qual teve melhora por uma outra ação do IBP que não da supressão ácida, como uma ação anti-inflamatória por exemplo.
– A DRGE ainda deve ser considerada mesmo com EDA e pHmetria normais. Nestes casos a realização de impedâncio-pHmetria aumenta a sensibilidade do diagnóstico de DRGE ácida e avalia também o refluxo não ácido. Deve-se ter em mente que os exames de phmetria e principalmente de impedâcio-pHmetria são examinador dependente, sendo importante a realização dos mesmos por profissionais capacitados e com experiência.
– Independente da nomenclatura usada para a definição da patologia (Eosinofilia responsiva a IBP x Esofagite eosinofílica) o tratamento inicial com IBP pode ser tentado como escolha terapêutica inicial.