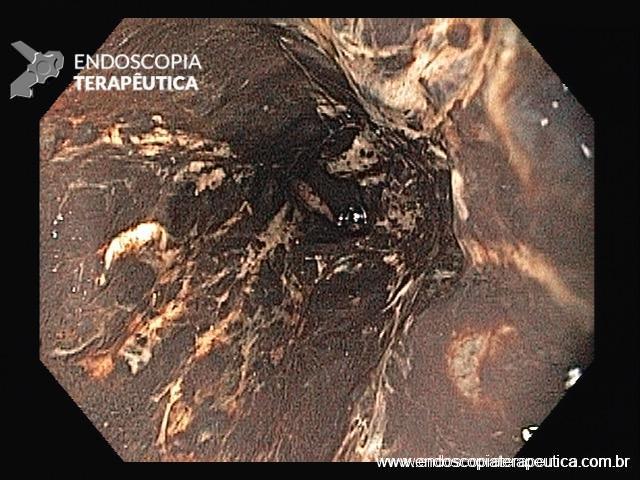
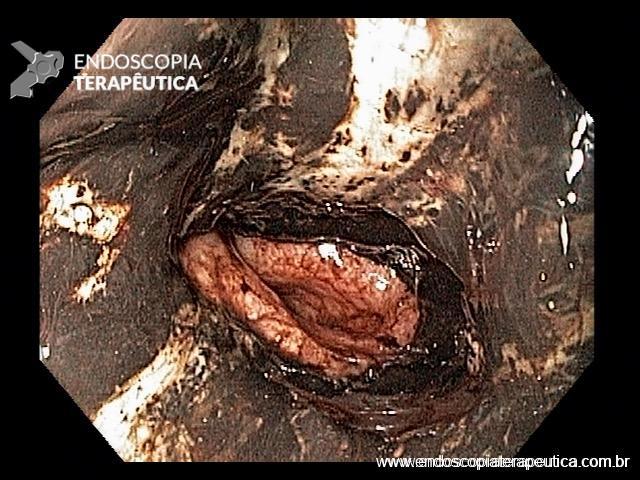
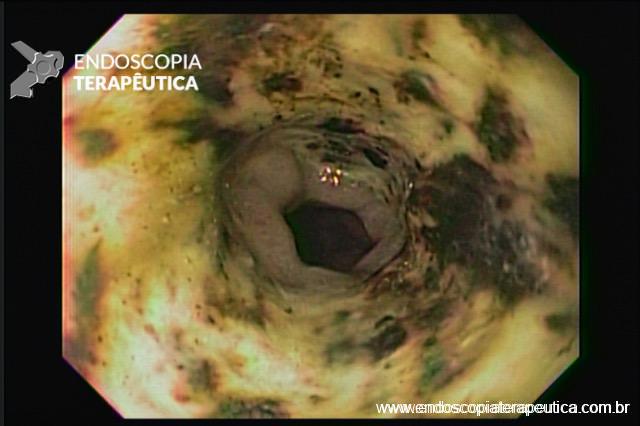
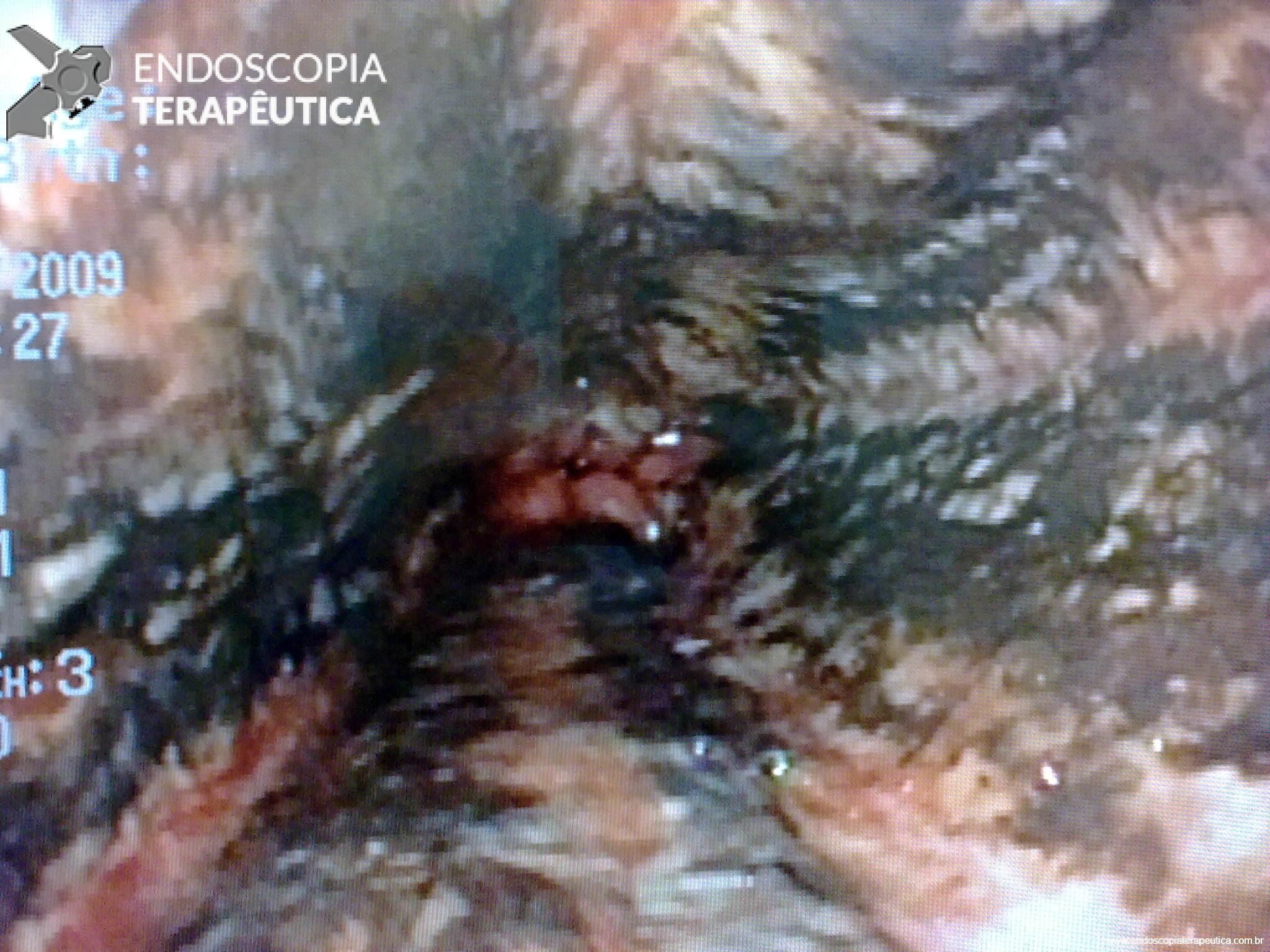
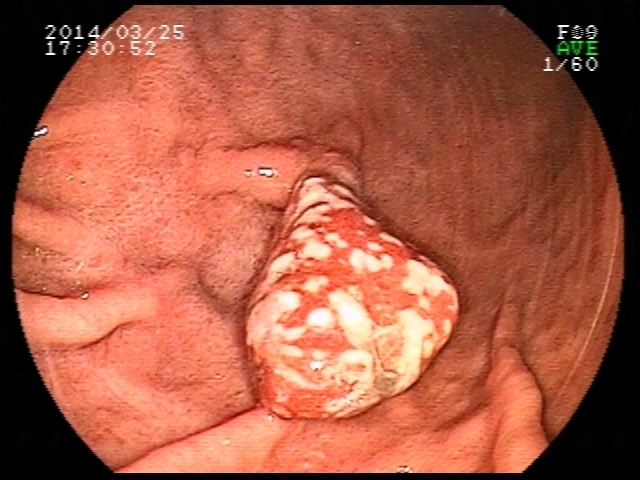
Esôfago negro
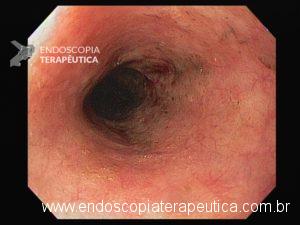
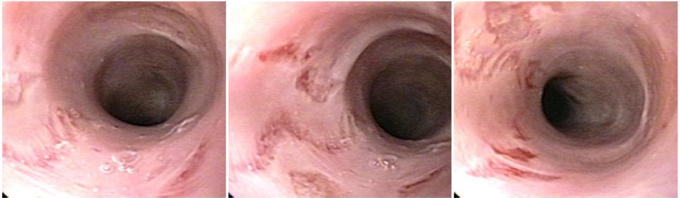
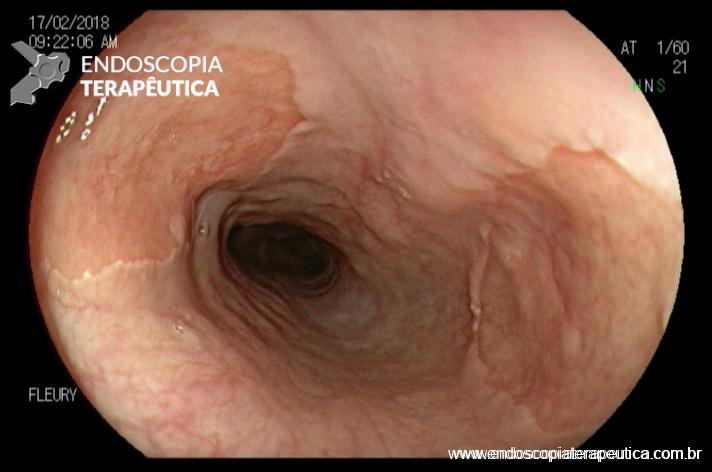
Esôfago proximal
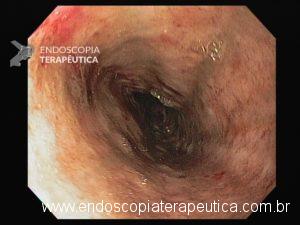
Esôfago proximal/médio
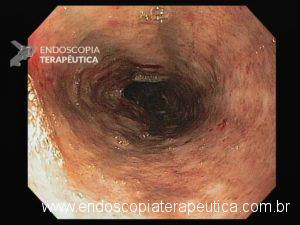
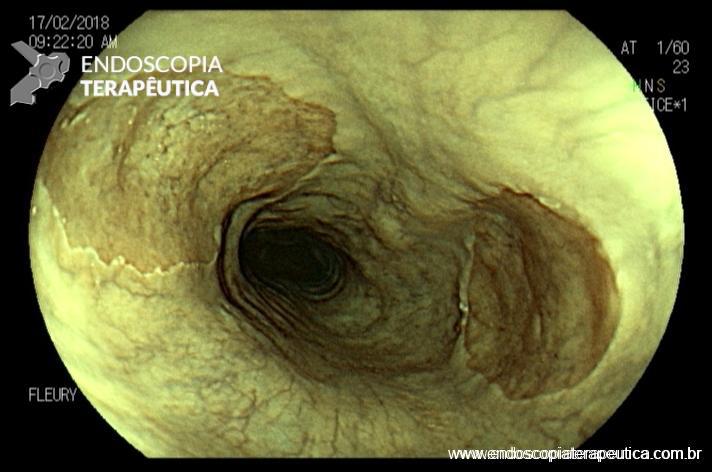
Esôfago médio
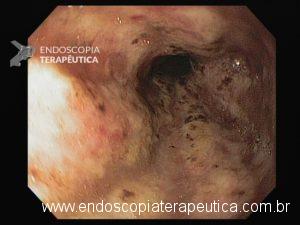
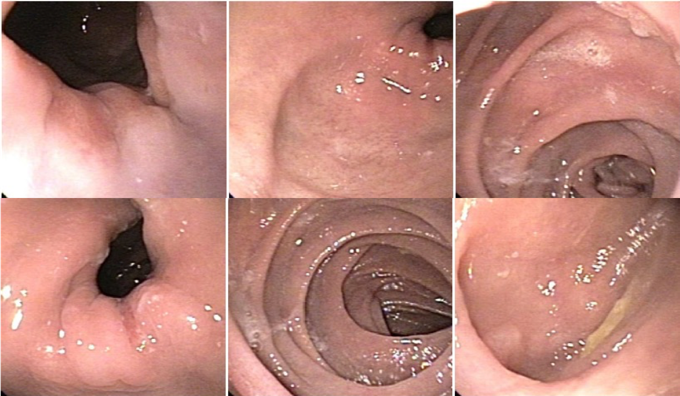
Esôfago distal
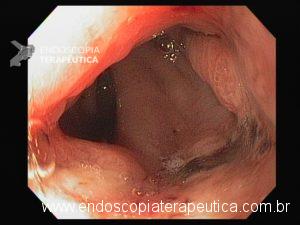
Esôfago distal
INTRODUÇÃO
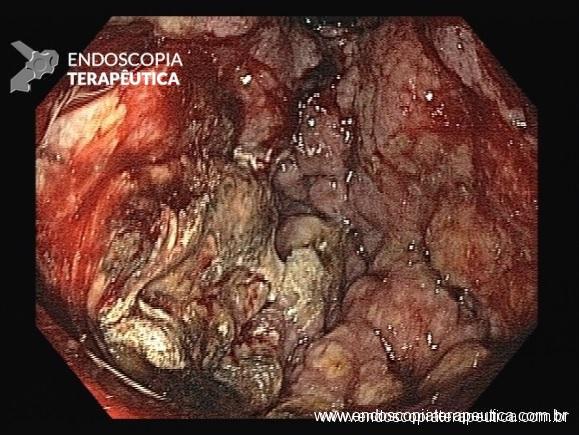
A necrose esofágica aguda (NEA), também conhecida como esôfago negro ou esofagite necrotizante, é uma síndrome rara caracterizada por uma aparência escurecida da mucosa, com comprometimento circunferencial difuso, que afeta principalmente os dois terços distais interrompendo-se abruptamente na junção gastroesofágica (a mucosa gástrica mantém-se normal).
EPIDEMIOLOGIA
A necrose esofágica aguda é uma condição rara com uma prevalência estimada de até 0,2 % em séries de autópsia. Em algumas séries de endoscopia, a prevalência da NEA variou de 0,001 a 0,2% dos casos. A incidência parece ser mais do que quatro vezes maior nos homens em comparação com as mulheres e os pacientes têm uma idade média de 68 anos no diagnóstico.
ETIOLOGIA E PATOGÊNESE
A etiologia da necrose esofágica aguda não é clara, mas a isquemia e a obstrução da saída gástrica podem ser eventos desencadeantes. Em alguns relatos tem sido associada ao uso de antibióticos de amplo espectro, infecções (por exemplo, candida albicans, citomegalovírus, vírus do herpes e klebsiella pneumoniae), volvo gástrico, hérnia paraesofágica, hiperglicemia, cetoacidose diabética, síndrome de Stevens-Johnson, vômitos intensos e prolongados, hepatite alcoólica, acidose lática e até dissecção aórtica. Ou seja, em geral são pacientes com quadro clínico bastante debilitado e com risco de comprometimento circulatório.
Outra hipótese para sua etiologia seria a presença de dois eventos associados, onde o inicial, um estado vascular de baixo fluxo, predisporia a mucosa à uma lesão intensa e o segundo causaria uma obstrução da saída gástrica levando à um acúmulo de líquido no estômago, o que promoveria um refluxo gastresofágico, resultando em lesão direta, e por fim, necrose. O que fortalece tal hipótese é que a redução temporária do fluxo sanguíneo esofágico pode resultar em necrose esofágica extensa que se resolve rapidamente quando o fluxo é reestabelecido. Além disso, a necrose esofágica aguda tende a ocorrer no terço distal do esôfago, que é relativamente hipovascularizado em comparação com outros segmentos esofágicos. A necrose da mucosa esofágica e submucosa, com trombose microscópica e recuperação rápida após o reestabelecimento do fluxo são eventos semelhantes aos ocorridos na colite isquêmica.
MANIFESTAÇÕES CLÍNICAS
Aproximadamente 70% dos pacientes com necrose esofágica aguda apresentam hemorragia digestiva alta com hematêmese e melena. Os sintomas podem aparecer rapidamente após um evento desencadeante. Outros sintomas gastrointestinais incluem: disfagia, dor epigástrica e dor torácica. Os pacientes também podem ter sintomas relacionados à patologia subjacente a qual predispôs ao evento desencadeante inicial e apresentarem-se com sinais de sepse, incluindo taquicardia e hipotensão.
ACHADOS LABORATORIAIS
Os achados laboratoriais não são específicos e frequentemente são devidos à doença subjacente. Eles incluem: acidose lática, hipoalbuminemia, anemia, insuficiência renal e hiperglicemia.
DIAGNÓTICO
A necrose esofágica aguda é habitualmente diagnosticada incidentalmente em pacientes submetidos à endoscopia digestiva alta para avaliação de sangramento gastrointestinal. Embora a aparência endoscópica seja sugestiva, são necessárias biópsias esofágicas para excluir outras etiologias e estabelecer o diagnóstico.
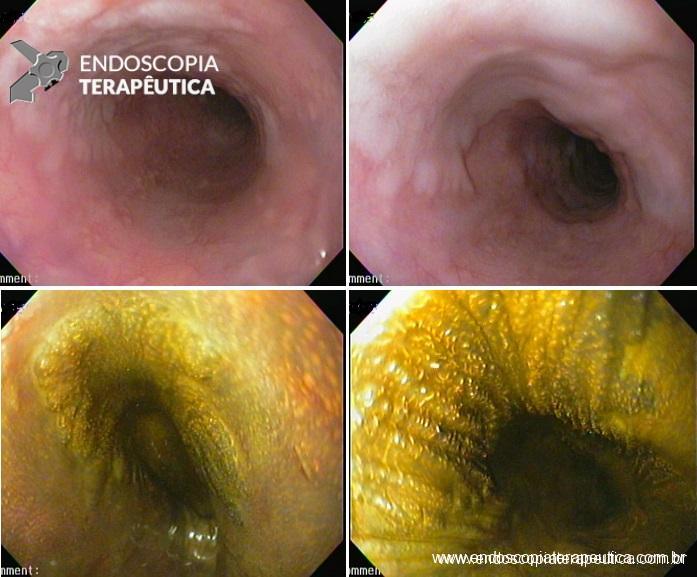
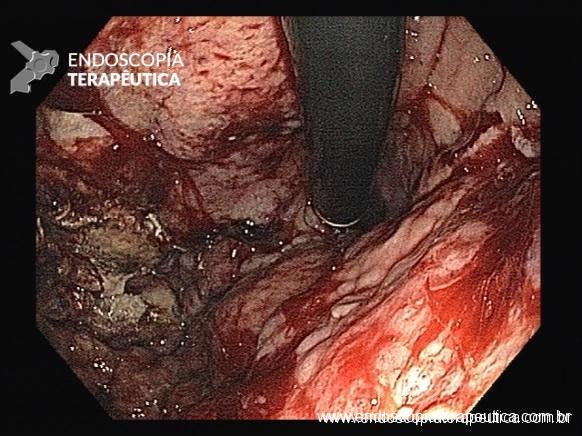
Endoscopia e biópsia – Na endoscopia, é caracterizada por descoloração periférica circunferencial com tecido hemorrágico friável subjacente associado a diminutos pontos enegrecidos, e também por uma delimitação precisa entre a mucosa esofágica e a gástrica, a qual tem aparência normal distalmente à junção gastroesofágica.
Geralmente envolve o terço distal do esôfago, embora o envolvimento proximal tenha sido descrito. À medida que a doença progride, o esôfago pode ficar parcialmente coberto com exsudatos brancos espessos que são descolados facilmente revelando um tecido de granulação rosa. Esses exsudatos provavelmente representam células mucosas espalhadas.
As biópsias servem para diferenciar a necrose de outras condições nas quais a mucosa também pode estar escurecida e também para descartar causas infecciosas, como por exemplo, candida albicans, citomegalovírus, vírus herpes simples e klebsiella pneumoniae.
Na histologia, há necrose extensa comprometendo a mucosa e a submucosa. Inflamação e destruição parcial de fibras musculares adjacentes podem ocasionalmente ser observadas, e os vasos sanguíneos às vezes são trombosados e/ou ocluídos.
DIAGNÓSTICO DIFERENCIAL
O diagnóstico diferencial inclui outras condições em que a mucosa esofágica também pode estar escurecida. A necrose esofágica aguda pode ser diferenciada destas condições pela história clínica e pela biópsia.
- Melanose – melanose esofágica tem sido descrita em pacientes com esofagite crônica subjacente. É mais comumente observada no esôfago distal. Em contraste com a necrose esofágica aguda, a descoloração é frequentemente focal. As biópsias revelam melanócitos com características de coloração de pigmento semelhantes à melanina.
- Pseudomelanose – A pseudomelanose é devida à deposição de tecido de pseudomelanina, um pigmento derivado da degradação lisossômica. Na histologia, um pigmento marrom composto por lipofuscina e melanina pode ser visualizado dentro dos macrófagos.
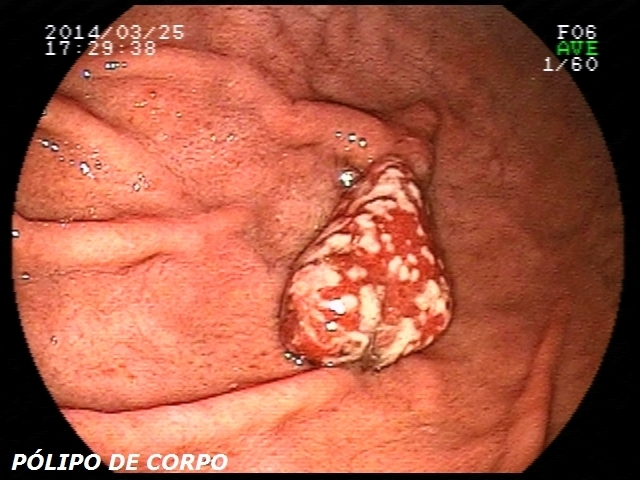
- Melanoma – O melanoma primário do esôfago é raro. Geralmente se origina no esôfago médio e distal e tem uma aparência polipoide. O diagnóstico é feito pela presença de atividade melanocítica juncional na avaliação histológica da mucosa esofágica.
- Acantose nigricans – é caracterizada por placas de aspecto aveludado, verrucoso e hiperpigmentado. Embora possa ser benigno, também pode ser um fenômeno paraneoplásico comumente associado a neoplasias malignas intra-abdominais.
- Resíduo de carvão – O pó de carvão ou o carbono é o pigmento exógeno mais comum a ser depositado nos tecidos do corpo humano. O mecanismo pelo qual o pó de carvão é depositado no esôfago não está claro.
- Ingestão cáustica – O dano esofágico grave causado pela ingestão de agentes corrosivos pode provocar desprendimento da mucosa e uma pigmentação preta da parede esofágica. Tais pacientes podem apresentar um histórico de ingestão cáustica e podem ter queimaduras orofaríngeas associadas.
- Esofagite Pseudomembranosa – geralmente é relatada em associação com graves doenças sistêmicas. Uma membrana concêntrica, fina, amarela ou preta, recobre os terços distais e, menos comumente, o esôfago inteiro. Pode ser desalojada da parede, revelando uma mucosa subjacente friável. Na histologia, a pseudomembrana não tem membrana basal e é composta por exsudato fibrinoso e células inflamatórias misturadas.
TRATAMENTO
Existem dados limitados para orientar o manejo da necrose esofágica aguda, e o gerenciamento de tal condição é amplamente baseado na experiência clínica.
A terapêutica inicial consiste em expansão de volume com fluidos intravenosos e tratamento da doença de base. A supressão do acidez gástrica com inibidores de bomba de prótons deve ser adotada para reduzir a lesão péptica adicional. A ingestão oral deve ser evitada por pelo menos 24 horas. O uso da suspensão de sucralfato deve ser considerado pelo seu papel na prevenção de lesão esofágica péptica associada.
As sondas nasogástricas ou nasoenterais devem ser evitadas, a menos que sejam usadas afim de descomprimir uma obstrução da saída gástrica ou se houver vômito persistente. Uma decisão sobre o uso de antimicrobiano e/ou antifúngico deve ser feita individualmente, especialmente na configuração de pacientes que estão criticamente doentes ou parecem estar sépticos.
HISTÓRIA NATURAL
Com cuidados de suporte, a resolução dos achados endoscópicos ocorre na maioria dos pacientes. No entanto, as taxas de mortalidade em pacientes com necrose esofágica aguda variam de 13 a 35%. A mortalidade é em grande parte devido à doença de base, sendo que apenas 6% das mortes são diretamente atribuíveis à complicações da NEA.
COMPLICAÇÕES
- Perfuração esofágica – A perfuração esofágica é uma complicação aguda da necrose esofágica que ocorre em menos de 7% dos pacientes, mas requer intervenção urgente dada a alta mortalidade associada. A presença de dor retroesternal ou lombar severa persistente pode indicar seu aparecimento. Pacientes com perfuração esofágica podem ter crepitação à palpação da parede torácica devido à presença de enfisema subcutâneo.
- Estenose esofágica – As estenoses esofágicas são complicações à longo prazo da necrose esofágica aguda e ocorrem em 25 a 40 % dos pacientes. Os pacientes com estenoses geralmente apresentam disfagia gradualmente progressiva e habitualmente requerem dilatação endoscópica.
VEJA MAIS IMAGENS ABAIXO
(clique para ampliá-las)

Confira também: Esofagite por cândida – Kodsi