Prótese Metálica Autoexpansível no manejo da Fístula Esofagorespiratória Maligna – Quando é apropriado utilizar?!
O câncer de esôfago (CE) é a oitava neoplasia maligna mais frequente em todo o mundo, ocupando também a sexta posição em causa de mortes entre todos os tipos de câncer. No Brasil, de acordo com dados do Instituto Nacional de Câncer (INCA), o CE está entre as dez neoplasias mais incidentes, sendo a sexta neoplasia mais frequente entre pessoas do sexo masculino e a décima terceira entre as do sexo feminino.
Os dois tipos histológicos principais do CE são o carcinoma epidermóide e o adenocarcinoma. Em nosso meio, o primeiro representa cerca de 96% das neoplasias esofágicas diagnosticadas. No entanto, a incidência do último vem aumentando progressivamente.
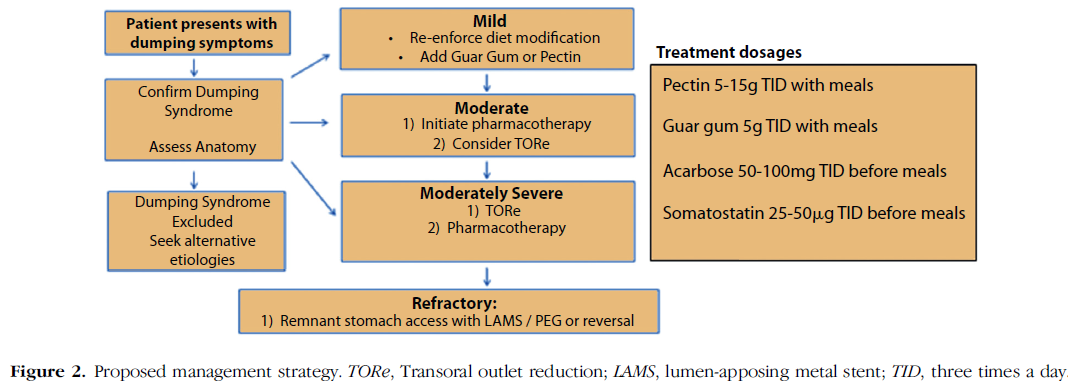
O diagnóstico definitivo do CE se dá através do exame de endoscopia digestiva alta com obtenção de biópsias da lesão e, muito frequentemente, é realizado já em fase avançada da doença, após o aparecimento dos primeiros sintomas disfágicos. Cerca de 50% dos pacientes apresentam doença locorregional avançada ou metastática ao momento do diagnóstico, com grave comprometimento nutricional e queda do estado geral, reduzindo a possibilidade de um tratamento curativo. Nestes, a paliação dos sintomas e o manejo das complicações ainda é a melhor opção, sendo a colocação de prótese metálica autoexpansível (PMAE) o método mais rápido com este propósito.
A fístula esofagorrespiratória (FER) é a temida complicação do câncer de esôfago. É definida como uma comunicação patológica entre o esôfago e a árvore respiratória, estando presente entre 5 a 15% dos indivíduos com neoplasia esofágica e em menos de 1% dos indivíduos com carcinoma broncogênico. Os sintomas típicos do paciente portador de FER são quadros de tosse associados à ingesta alimentar e pneumonias aspirativas de repetição, presentes em até 95% dos casos. Em média, a fístula se desenvolve cerca de oito meses após o diagnóstico do CE e, uma vez estabelecida sua presença, o tratamento deve ser prontamente instituído para evitar a contaminação contínua da via aérea e o óbito por sepse de foco pulmonar. Desta forma, o fechamento da FER e o restabelecimento da capacidade de ingesta alimentar por via oral são considerados tão importantes quanto o tratamento da doença subjacente.
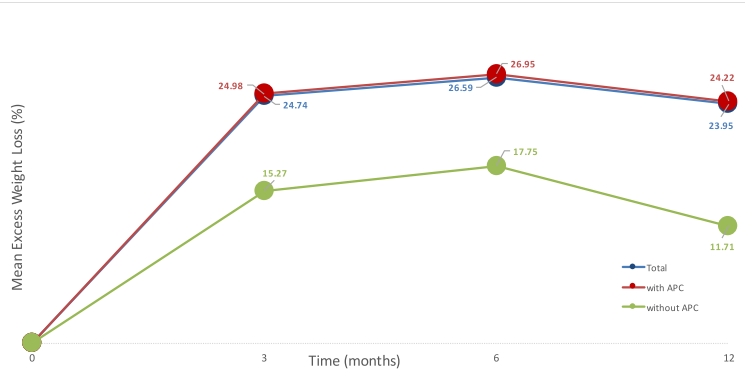
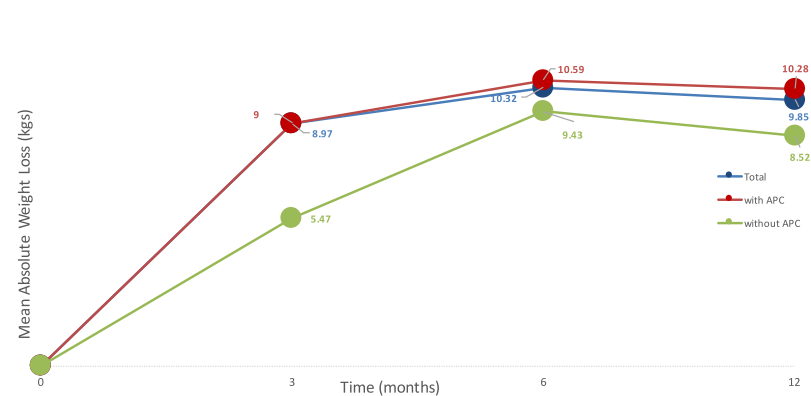
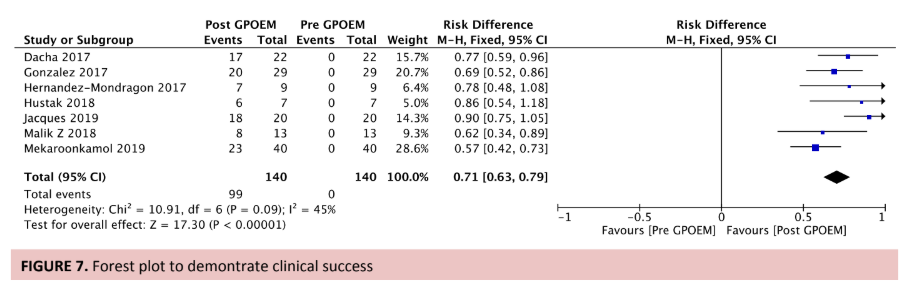
A taxa de sucesso no fechamento da fístula com PMAE varia entre 70% a 100% e pode promover melhora instantânea da disfagia através da restauração da patência esofágica, evitando alimentação pelo uso de sonda nasoenteral ou por gastrostomia percutânea, além de melhorar a qualidade de vida e reduzir o número de intervenções adicionais.
O CE complicado por FER leva à rápida deterioração do estado geral do paciente, seguida de morte num curto período de tempo, secundária às infecções respiratórias e à má nutrição. Não existem muitas opções terapêuticas disponíveis para o manejo da fístula maligna, haja vista a inoperabilidade da quase totalidade dos pacientes, sendo a PMAE método amplamente empregado nesses casos. No entanto, reconhece-se que existem eventos adversos relacionados ao método e, mais importante que isso, observa-se que parcela significativa dos pacientes que são submetidos à passagem da PMAE evoluem de forma desfavorável, com piora súbita do quadro clínico e pulmonar.
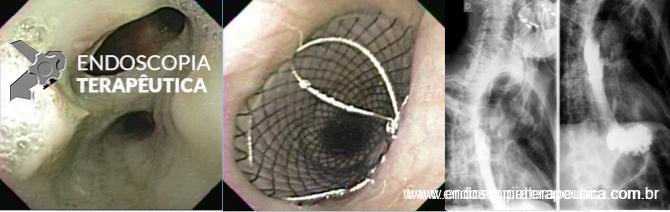
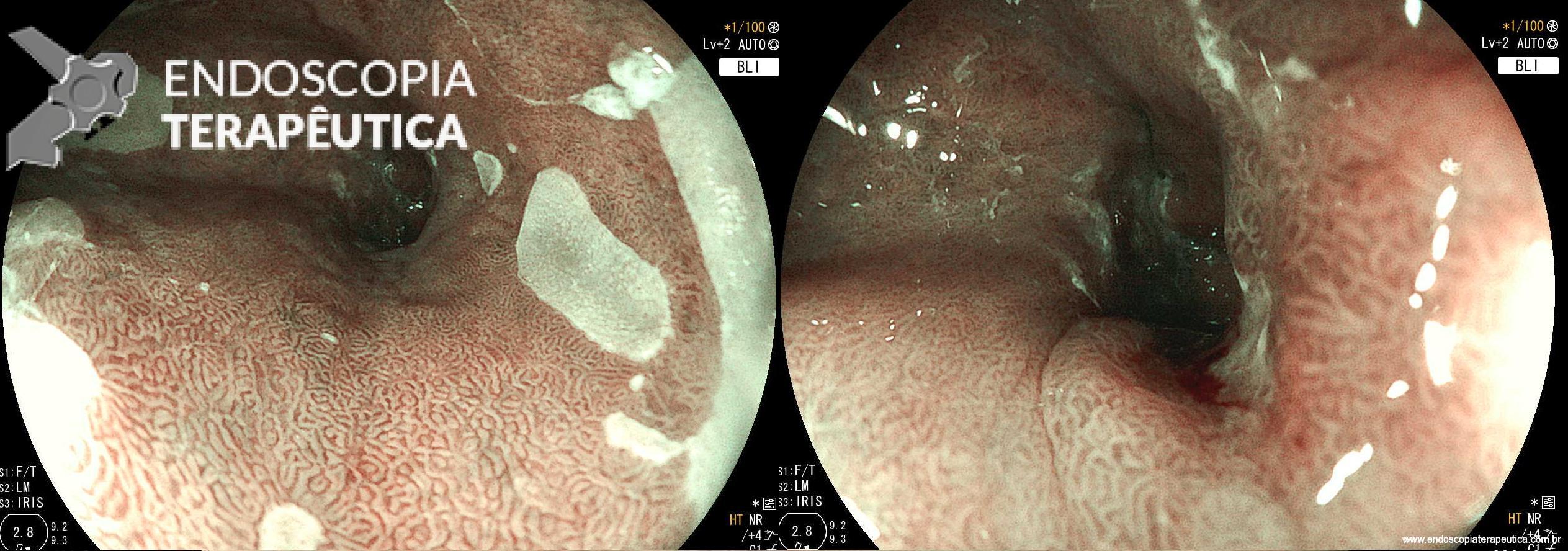
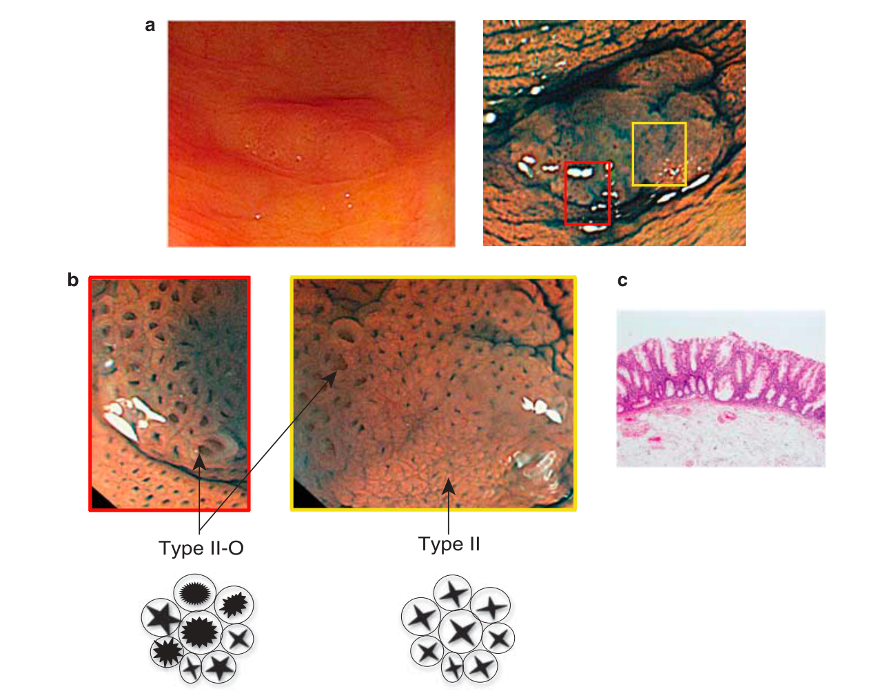
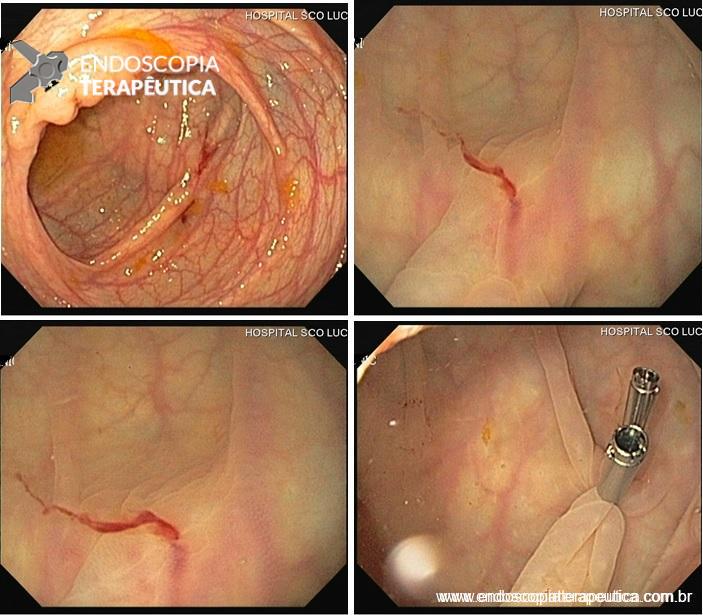
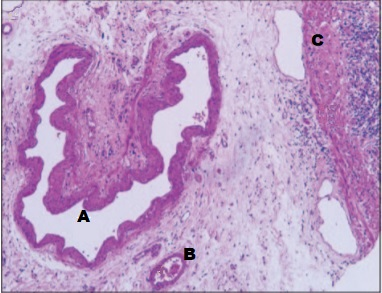
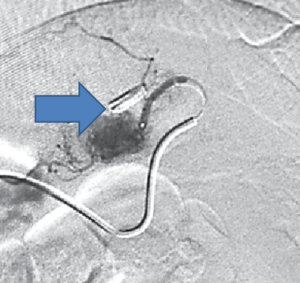
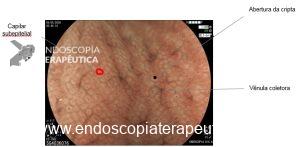
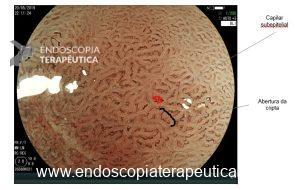
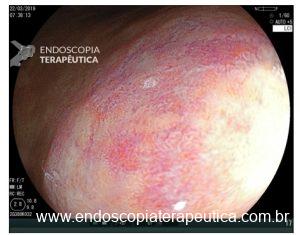
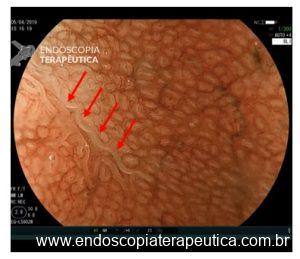
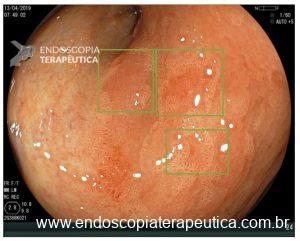
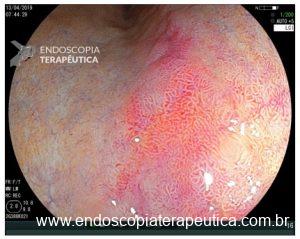
A: VISÃO ENDOSCÓPICA DA FÍSTULA ESOFÁGICA (SETA); B: VISÃO ENDOSCÓPICA DA PRÓTESE METÁLICA EXPANDIDA EM ESÔFAGO; C: INJEÇÃO DE MEIO DE CONTRASTE CONFIRMANDO A OCLUSÃO DA FÍSTULA PELA PRÓTESE (IMAGEM RADIOLÓGICA)
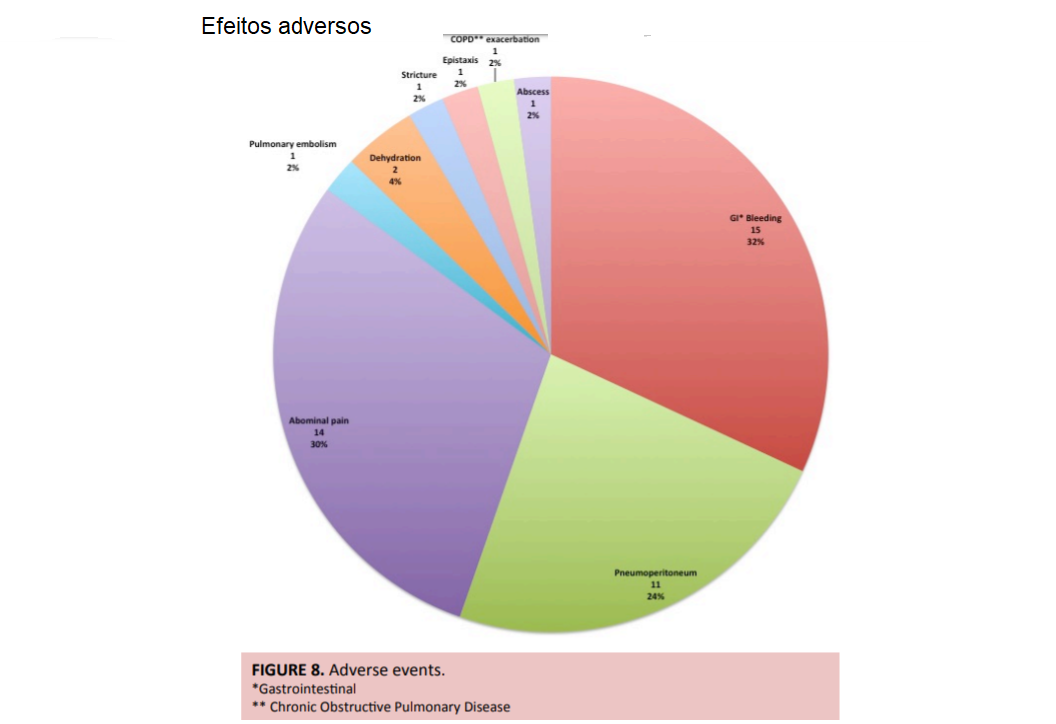
Quanto aos eventos adversos, a taxa total varia de 30% a 43%, sendo que a maior parte destes ocorrem tardiamente, ou seja, após 7 dias do procedimento. Os eventos adversos mais frequentes são, em ordem decrescente de prevalência: a migração, a obstrução da prótese por crescimento tumoral nas suas extremidades, a hematêmese e impactação alimentar.
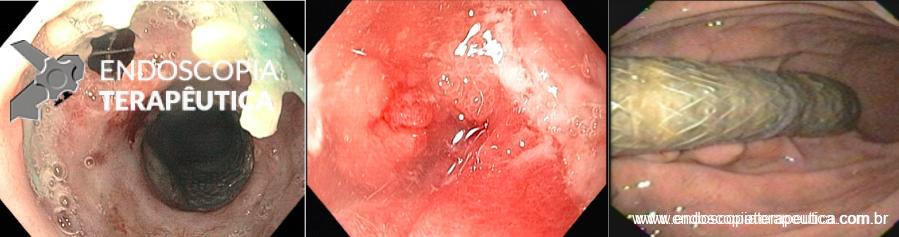
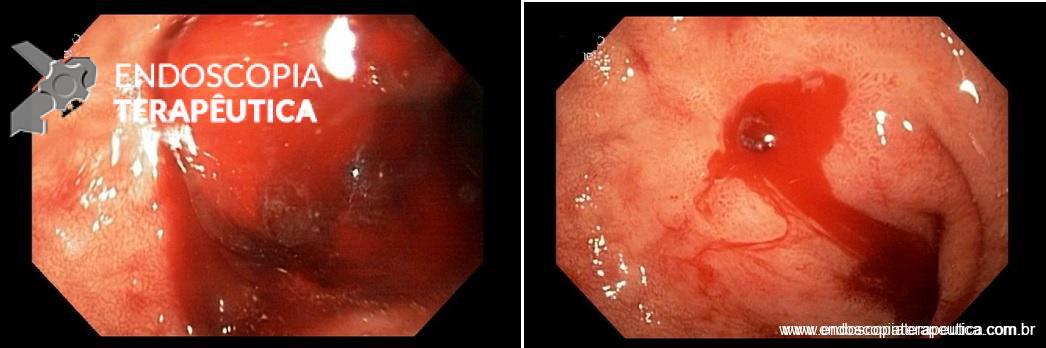
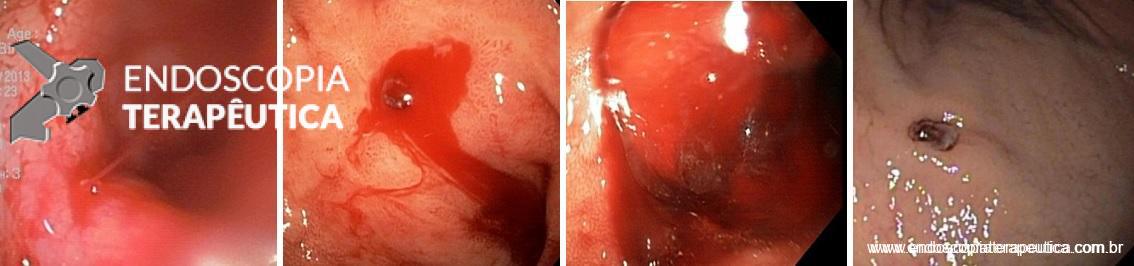
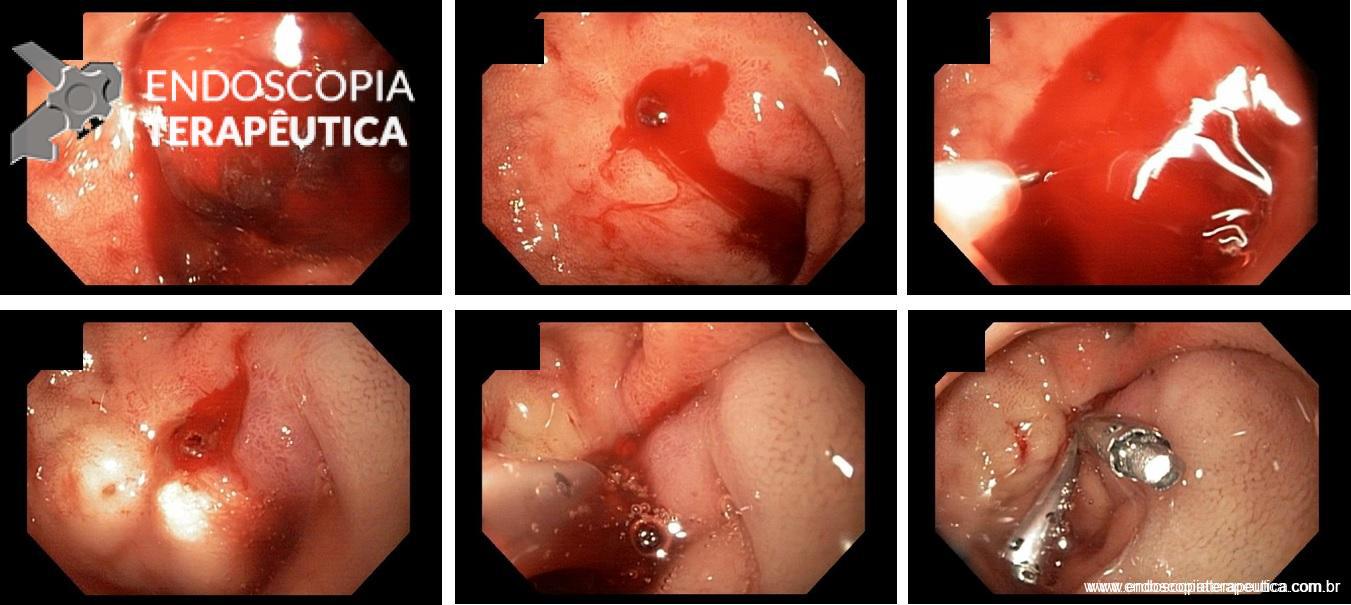
VISÃO ENDOSCÓPICA DE EVENTOS ADVERSOS DAS PRÓTESES METÁLICAS: A: FÍSTULA ESOFÁGICA (SETA); B: OBSTRUÇÃO DA PRÓTESE POR CRESCIMENTO TUMORAL NA EXTREMIDADE PROXIMAL DA PRÓTESE; C: MIGRAÇÃO DISTAL DA PRÓTESE PARA O ESTÔMAGO
O ideal seria haver uma base mais racional na qual se possa identificar quais pacientes se beneficiariam da utilização da prótese e quais não teriam benefício ou até mesmo teriam piora clínica com o tratamento. Se isso for possível, outros métodos paliativos podem ser indicados, evitando procedimento algo invasivo e oneroso ao sistema de saúde.
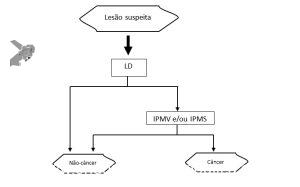
É evidente a escassez de estudos que se dedicaram à essa questão e não se sabe qual a vantagem da prótese na sobrevida do paciente. A maioria das publicações são pequenos estudos de coorte, com curto tempo de seguimento e índices variáveis de sucesso e complicações. Recentemente houve uma importante publicação que avaliou os fatores preditivos associados à falha clínica do uso de PMAE para o tratamento da FER, com as seguintes conclusões:
– Pacientes com ECOG (Eastern Cooperative Oncology Group) 3 e 4, desenvolvimento da fístula durante o tratamento do câncer esofágico e diâmetro da fístula igual ou superior a 1 cm foram fatores preditivos de insucesso clínico do tratamento das fístulas esofagorrespiratórias com prótese metálica autoexpansível em pacientes com câncer esofágico.
– Pacientes com ECOG (Eastern Cooperative Oncology Group) 3 e 4, tratamento oncológico prévio com radioterapia, isolada ou associada à quimioterapia e doença pulmonar infecciosa em atividade no momento da passagem da prótese foram fatores que impactaram negativamente a sobrevida dos pacientes.
Referência Bibliográfica:
Ribeiro MSI et al. Self-expandable metal stent for malignant esophagorespiratory fistula: predictive factors associated with clinical failure. GIE. 2018 Feb;87(2):390-396. PMID: 2896474. DOI: 10.1016/j.gie.2017.09.020.