Sangramento pós-drenagem endoscópica de necrose pancreática
Introdução
A pancreatite aguda necrotizante é responsável por até 10% dos casos de pancreatite aguda. A necrose do tecido pancreático, peripancreático ou ambos, permanece estéril na maioria dos pacientes, entretanto cerca de 30% dos pacientes apresentam infecção da coleção necrótica (WON), condição clínica que impõe alta mortalidade. Evolução com falência de órgãos, colangite ou necessidade de debridamento cirúrgico de WON infectado são fortes preditores de mortalidade, o que torna prudente a adoção de estratégias terapêuticas minimamente invasivas para o tratamento dessa complicação (1).
Na última década o conceito de estratégia minimamente invasiva do tipo “step-up approach” tornou-se amplamente utilizado e corroborado pela Associação Americana de Gastroenterologia (2). A drenagem endoscópica transluminal associada ou não à necrosectomia consolidou-se como a terapêutica de primeira escolha na abordagem de pancreatite aguda necrotizante complicada. Essa via de intervenção apresenta menor incidência de descompensação clínica por falência de órgãos, fístulas e perfuração quando comparada às técnicas cirúrgicas e por radiologia intervencionista minimamente invasivas (3).
Técnica Endoscópica
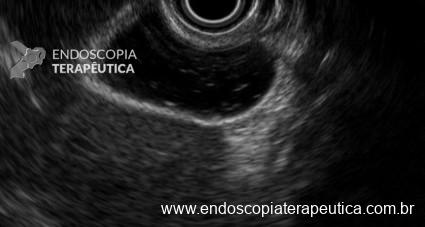
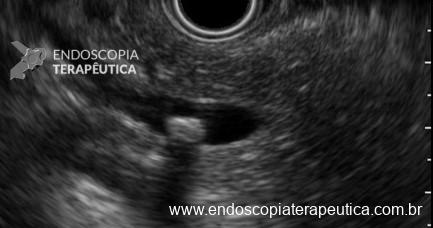
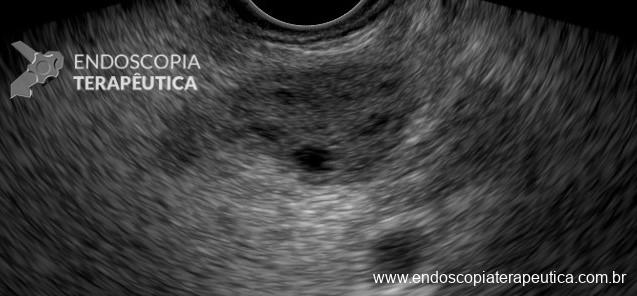
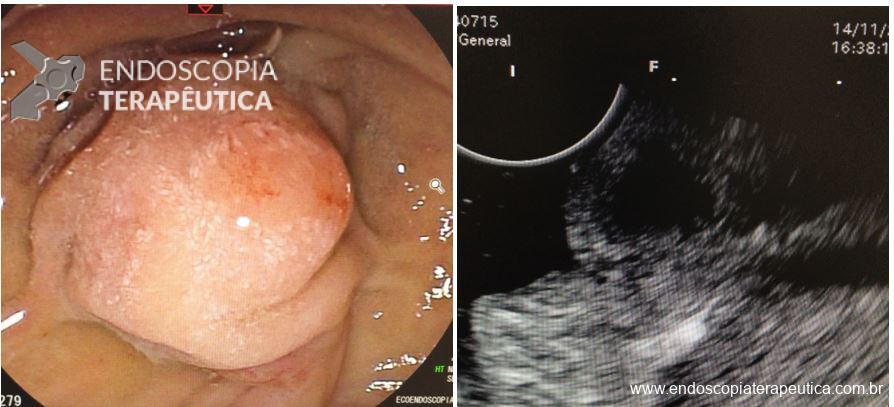
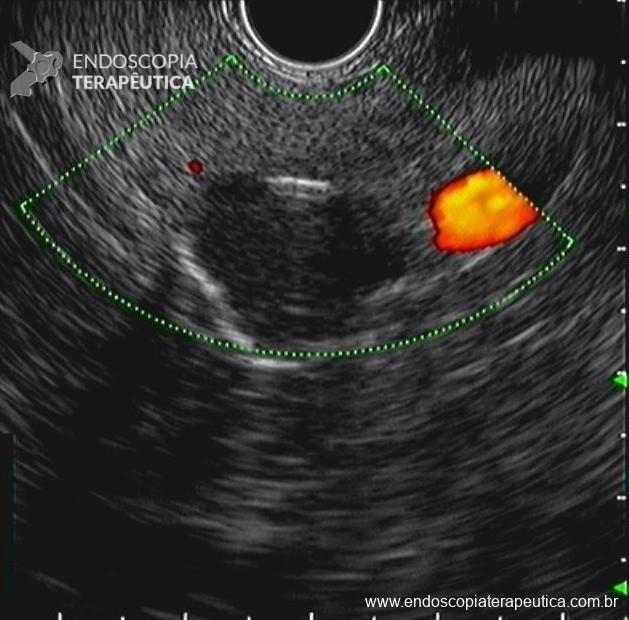
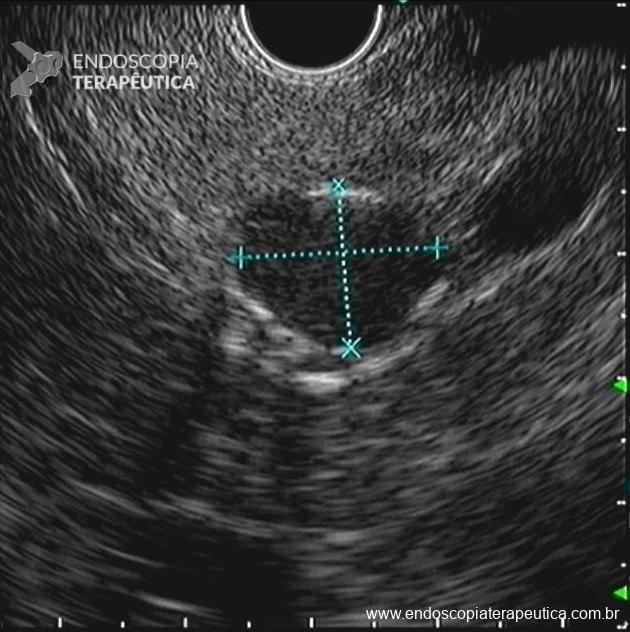
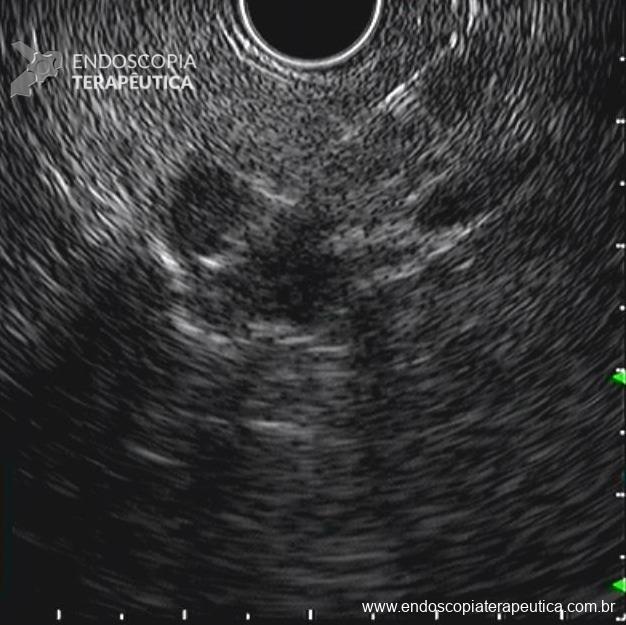
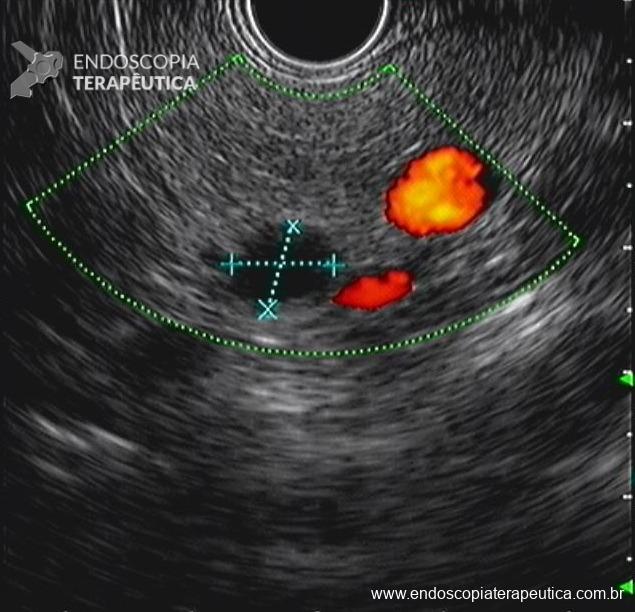
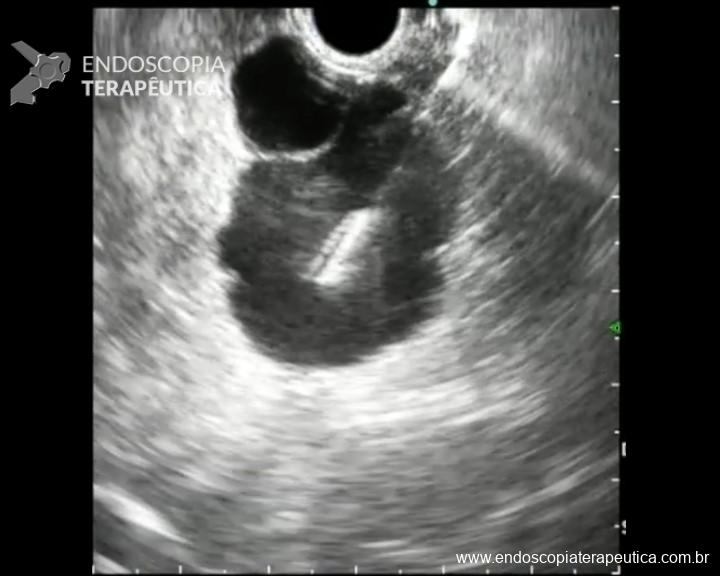
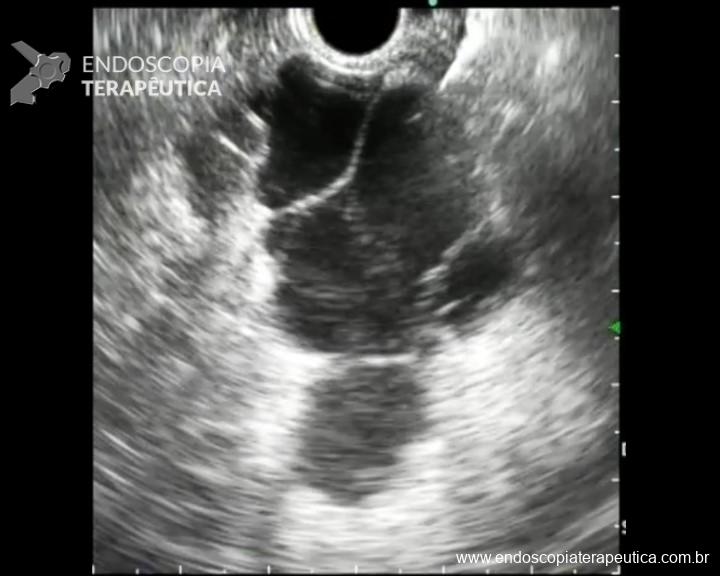
A primeira experiência de drenagem endoscópica de necrose pancreática remete ao final da década de 1980 e descrevia a utilização de endoscópico convencional, adotando como referência para punção a impressão criada pela coleção sobre a parede gástrica. Com o passar dos anos a técnica de drenagem guiada por ecoendoscopia tornou-se a modalidade de escolha para o procedimento, o que permitiu alta taxa de sucesso na criação do trajeto até a coleção, identificação de vasos sanguíneos, distribuição da coleção e janela adequada para a punção (4,5)
Recomenda-se aguardar período de pelo menos 4 semanas até a primeira intervenção, o que permite encapsulação e delineamento das margens da coleção necrótica. Entretanto na vigência de infecção, falência orgânica persistente ou ausência de melhora clínica a despeito das intervenções clínicas instituídas, é assertivo realizar a primeira intervenção em intervalo menor (2).
A via de drenagem endoscópica, transgástrica ou transduodenal, é definida de acordo com a localização do maior componente da coleção necrótica (cabeça, corpo ou cauda) e a relação com o estômago e duodeno. Não existe diferença em termos de sucesso terapêutico ou segurança entre as vias, embora a drenagem transgástrica permita acesso direto à coleção na necessidade de necrosectomia. O trajeto de drenagem pode ser assegurado por meio de Lumen-apposing metal stents (LAMS) ou double pigtail stents (DPS), de acordo com disponibilidade do stent, experiência do endoscopista e fatores econômicos, sem diferença no sucesso terapêutico (6).
Eventos adversos e sangramento
Apesar da efetividade clínica da drenagem endoscópica, a incidência de eventos adversos não é desprezível. Infecção, perfuração, migração de stent e hemorragia ocorrem em até 20% dos casos.
A ocorrência de sangramento é frequentemente descrita nas séries históricas e nos clássicos trabalhos que ratificam o tratamento endoscópico em termos de eficácia e segurança, tipo de prótese e tempo para abordagem da coleção necrótica. Entretanto são escassos os dados sobre etiologia do sangramento, abordagem adotada para hemostasia definitiva e os desfechos fatais (7).
Fatores de risco associados a sangramento
O desafio do manejo de sangramento nessa população motivou a publicação de dois recentes estudos retrospectivos, que avaliaram fatores preditores de sangramento nos pacientes submetidos à necrosectomia endoscópica. Zheng et al. estudaram 145 pacientes, dos quais 39 (26.9%) apresentaram sangramento pós-procedimento. A maioria dos episódios de sangramento (94.1%) foi efetivamente controlado com terapia hemostática endoscópica. Na análise multivariada, insuficiência renal, necrose infectada confirmada por cultura e três ou mais sessões de debridamento foram associados a maior risco de sangramento (9). Holmes et al. estudaram 151 pacientes, dos quais 18 (11.9%) apresentaram sangramento. Tratamento por radiologia intervencionista foi necessário para 8 pacientes. Na análise multivariada somente a presença de vaso identificado durante a necrosectomia endoscópica se mostrou fator de risco para sangramento (10).
Apesar de inúmeras publicações que não revelaram diferença significativa na ocorrência de sangramento entre os tipos de stents utilizado (LAMS x DPS x Fully covered metal stent), questionamentos sobre os dispositivos são frequentemente levantados. Especula-se que a rápida descompressão da coleção através do LAMS predispõe à erosão de vasos adjacentes e hemorragia. Além disso o maior diâmetro do LAMS permitiria maior influxo de secreção gástrica ácida para o interior da coleção, o que aumentaria a exposição de vasos e o risco de sangramento (para saber mais sobre LAMS clique aqui). Não obstante, os stents plásticos possuem menor diâmetro, exigem maior número de sessões de debridamento e são mantidos em posição por mais tempo, também aumentando o risco de hemorragia (7).
O sangramento pode se originar do sítio de punção, da própria parede gástrica ou duodenal, ramos colaterais gástricos ou duodenais, ou ainda vasos no interior da cavidade da coleção necrótica (WON). Menos comumente, os pseudoaneurismas de artérias viscerais impõem devido risco eminente de sangramento fatal. A utilização de TC de abdome com contraste na fase arterial permite a identificação de pseudoaneurisma e o tratamento preemptivo dessa condição, de modo a diminuir os riscos de sangramento periprocedimento (11).
Além das particularidades anatômicas, a irrigação do tecido necrótico com peróxido de hidrogênio tem maior risco de sangramento pós-procedimento quando comparado a solução de estreptoquinase nas sessões de debridamento (12).
Abordagem terapêutica de sangramento
Do ponto de vista terapêutico, o sangramento associado à drenagem endoscópica de WON pode ser dividido em sangramento intra-procedimento ou sangramento pós-procedimento. É fundamental que antes de iniciar o tratamento endoscópico de WON, a equipe envolvida certifique-se da disponibilidade de leito de terapia intensiva, reserva de hemocomponentes e retaguardas de radiologia intervencionista e cirurgia, e encontre-se preparada para a abordagem imediata da complicação (4).
Quando identificado sangramento durante o procedimento, a severidade da perda sanguínea orientará a abordagem. Em caso de sangramento autolimitado e de pequeno volume, é aceitável a admissão em terapia intensiva no pós-operatório imediato, com avaliação clínica e monitorização seriada dos níveis de hematimetria. Diferentemente, em caso de perda de volume sanguíneo significativo, terapias endoscópicas de hemostasia (clipe metálico, cauterização, agente tópico, tamponamento com balão dilatador ou prótese metálica) devem ser avaliadas e aplicadas no intraoperatório. Na falha terapêutica, o paciente deve ser encaminhado à radiologia intervencionista ou cirurgia imediatamente.
Na ocorrência de sangramento pós-procedimento, deve-se além de pesquisar alterações endoscópicas e anatômicas que o justifiquem, distúrbios da coagulação que possam precipitar o evento adverso. Na presença de lesão tratável por endoscopia, devem ser aplicados os princípios de hemostasia endoscópica. Na presença de aneurismas, pseudoaneurismas ou falha endoscópica, a abordagem por radiologia intervencionista deve ser programada.
Diante da experiência acumulada por diferentes grupos, Jiang et al. propuseram um algoritmo para manejo multidisciplinar de hemorragia na drenagem por ecoendoscopia de coleções fluidas peripancreáticas (Figura 1). O tratamento de coleção necrótica infectada é moroso e exige habilidades técnicas nos campos da clínica, cirurgia, endoscopia e radiologia. A difusão da prática de drenagem endoscópica gerou atenção para complicações inerentes ao procedimento, incluindo o sangramento. O emprego da terapia endoscópica ciente dos fatores de risco para sangramento e estratégias para tratá-lo permitem efetividade com menor incidência de eventos adversos.

Referências
- Podda M, Pellino G, Di Saverio S, Coccolini F et al. Infected pancreatic necrosis: outcomes and clinical predictors of mortality. A post hoc analysis of the MANCTRA‑1 international study. Updates in Surgery 2023; 75:493–522
- Baron TH, DiMaio CJ, Wang AY et al. American Gastroenterological Association Clinical Practice Update: Management of pancreatic necrosis. Gastroenterology 2020; 158: 67–75
- Bang JY, Wilcox CM, Arnoletti JP et al. Superiority of endoscopic interventions over minimally invasive surgery for infected necrotizing pancreatitis: meta-analysis of randomized trials. Dig Endosc 2020; 32: 298–308
- Baron TH, Thaggard WG, Morgan DE, Stanley RJ. Endoscopic Therapy for Organized Pancreatic Necrosis. Gastroenterology 1996;111:755 –764.
- Varadarajulu, S.; Christein, J.D.; Tamhane, A.; Drelichman, E.R.; Wilcox, C.M.Prospective Randomized Trial Comparing EUS and EGD for Transmural Drainage of Pancreatic Pseudocysts (with Videos). Gastrointest. Endosc. 2008; 68, 1102–1111.
- Bang JY, Wilcox CM, Navaneethan U, Hawes RH, Varadarajulu S. Treatment of walled-off necrosis using lumen-apposing metal stents versus plastic stents: a systematic review and meta- analysis of data from randomized trials. Endoscopy 2023; 56: 184-195
- Jiang TA & Xie LT. Algorithm for the multidisciplinary management of hemorrhage in EUS-guided drainage for pancreatic fluid collections. World J Clin Cases 2018; 6(10): 308-321
- Rana SS, Shah J, Kang M, et al. Complications of endoscopic ultrasound-guided transmural drainage of pancreatic fluid collections and their management. Ann Gastroenterol 2019;32:441-50.
- Zheng X, Li L, Li J, et al. Risk factors for bleeding in patients with acute necrotizing pancreatitis undergoing endoscopic necrosectomy. HPB (Oxford) 2021;23(12):1856–186
- Holmes I, Shinn B, Mitsuhashi S, et al. Prediction and management of bleeding during endoscopic necrosectomy for pancreatic walled-off necrosis: results of a large retrospective cohort at a tertiary referral center. Gastrointest Endosc 2022;95(03): 482–488
- Sekikawa Z, Yamamoto T, Aoki R, et al. Prophylactic Coil Embolization of the Vessels for Endoscopic Necrosectomy in Patients with Necrotizing Pancreatitis. J Vasc Interv Radiol. 2019 Jan;30(1):124-126. doi: 10.1016/j.jvir.2018.05.025. PMID: 30580813.
- Bhargava MV, Rana SS, Gorsi U, Kang M, Gupta R. Assessing the Efficacy and Outcomes Following Irrigation with Streptokinase Versus Hydrogen Peroxide in Necrotizing Pancreatitis: A Randomized Pilot Study. Dig Dis and Sciences 2022; 67(8): 4146-53
Como citar este artigo
Ide E. e Nascimento Filho Hm. Sangramento pós-drenagem endoscópica de necrose pancreática. Terapêutica Endoscópica 2024 vol 1. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/sangramento-pos-drenagem-endoscopica-de-necrose-pancreatica/