Caso Clínico – Fístula biliar pós trauma abdominal fechado
Relato do caso:
Paciente do sexo masculino, com 43 anos de idade, deu entrada no pronto socorro, após ter evadido de outro hospital .
Tinha antecedente de trauma abdominal fechado, após queda de andaime (7 metros), estando internado com conduta não cirúrgica por cerca de 18 dias. Após este período, “fugiu” do hospital de origem e procurou atendimento no PS-HC Marília.
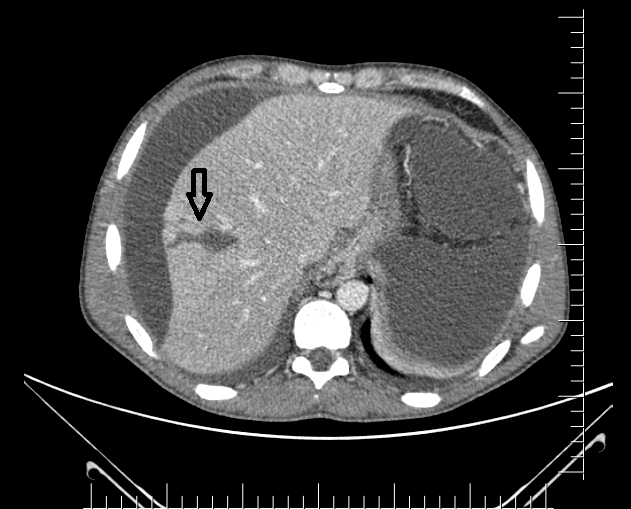
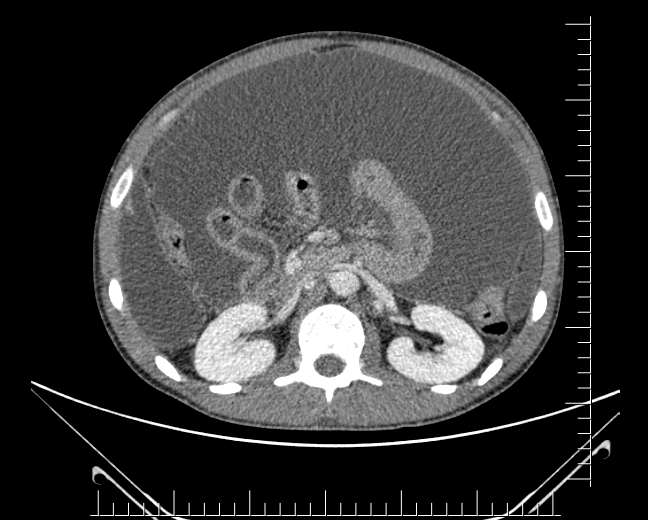
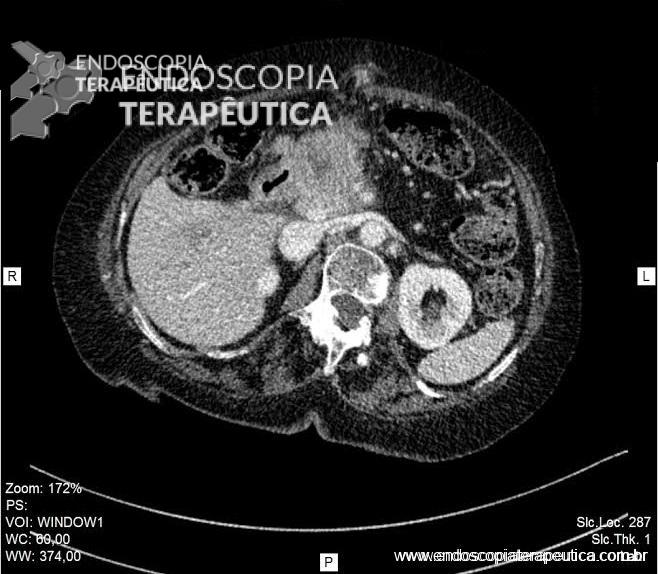
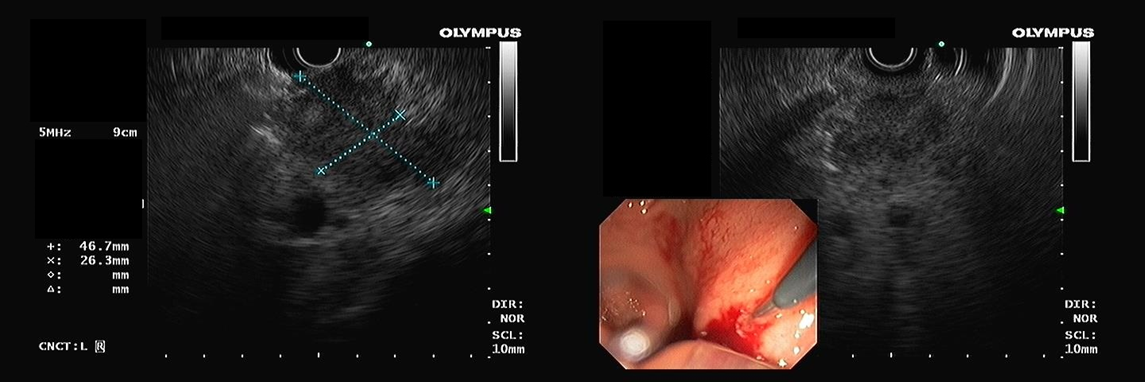
Na entrada, apresentava-se estável hemodinamicamente, porém emagrecido (estava em jejum desde o trauma), com dor em andar superior de abdômen, sinais de ascite volumosa, além de anasarca e leve icterícia. Foi submetido a tomografia de abdômen com contraste, que evidenciou laceração hepática Grau III, coleções subcapsulares e volumosa ascite. Optou-se por realizar paracentese, com saída de cerca de 11 litros de secreção biliar.
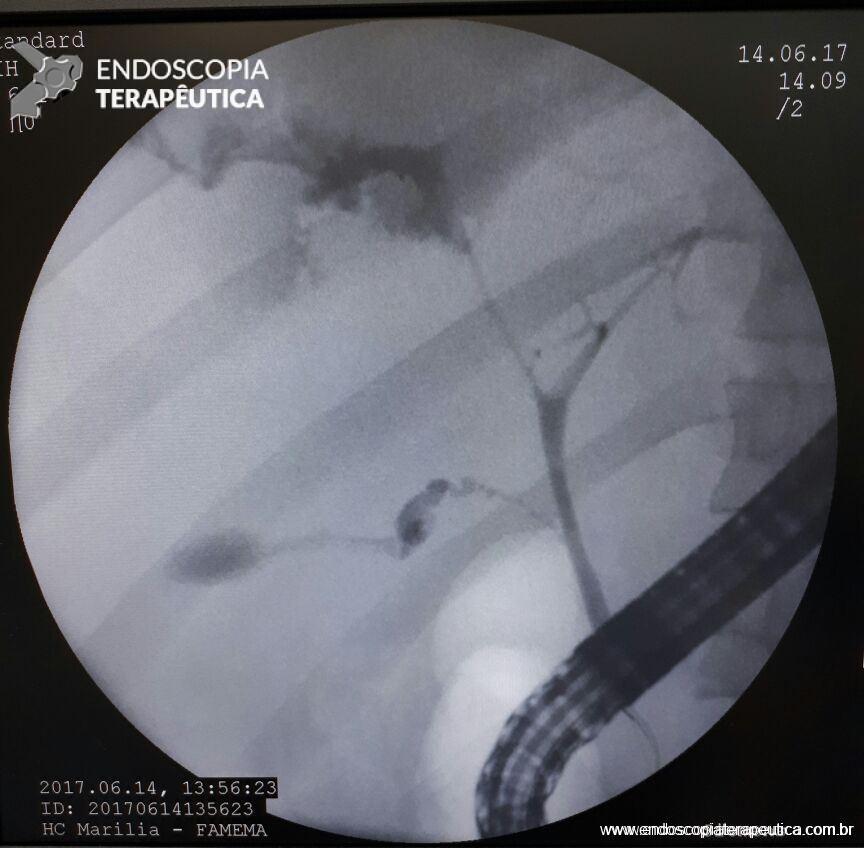
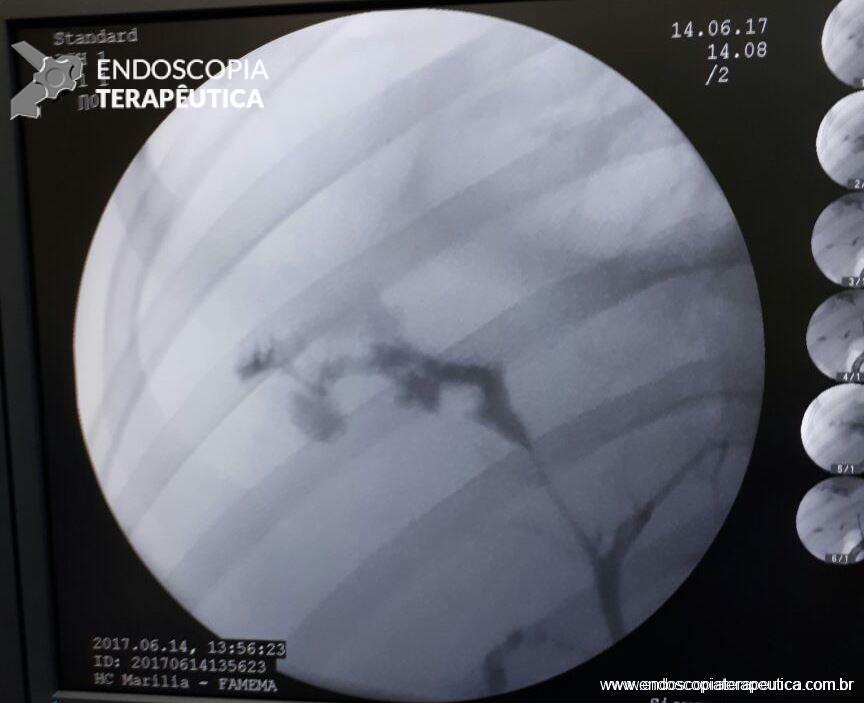
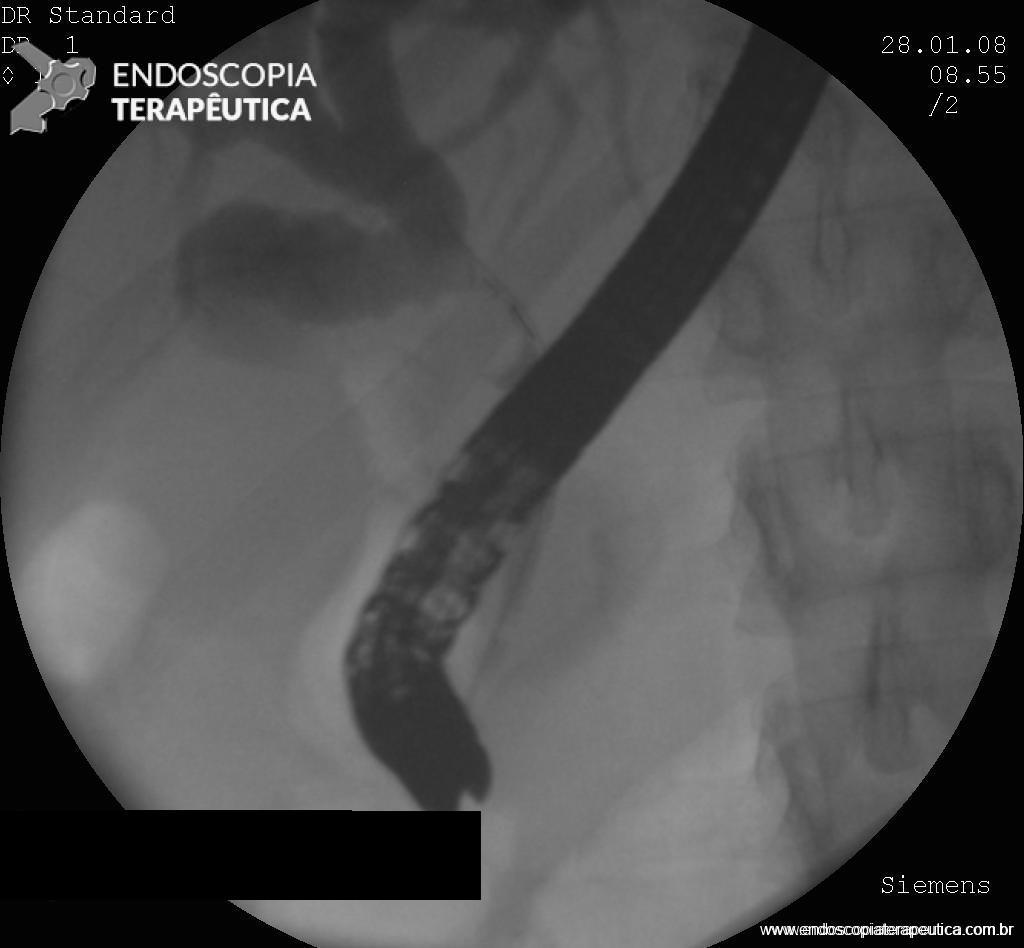
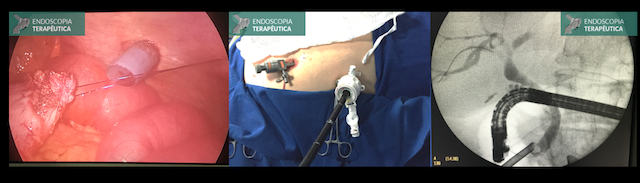
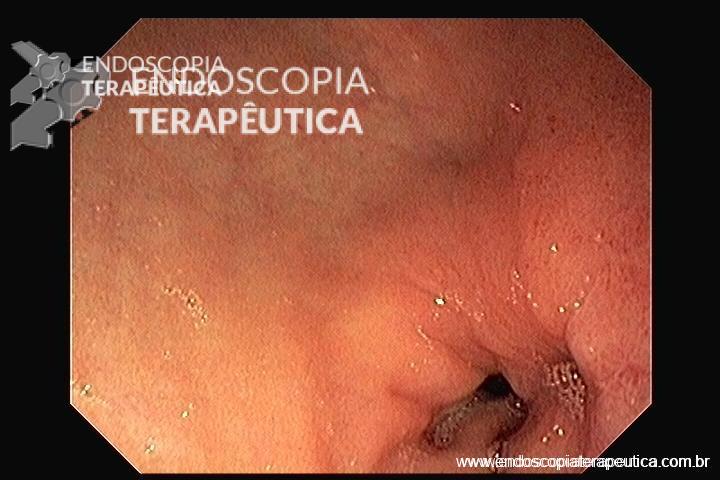
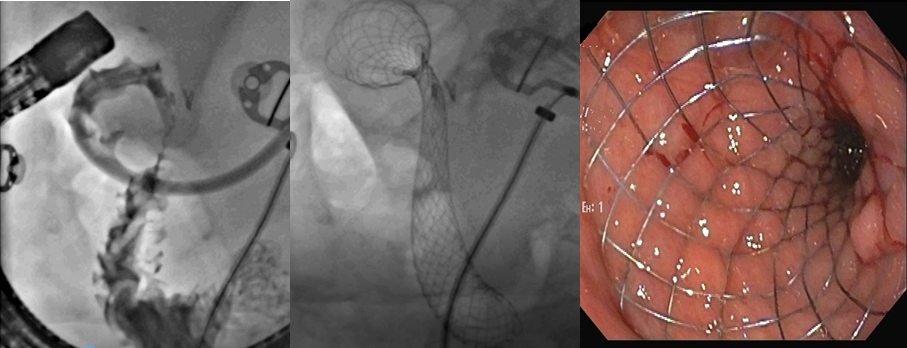
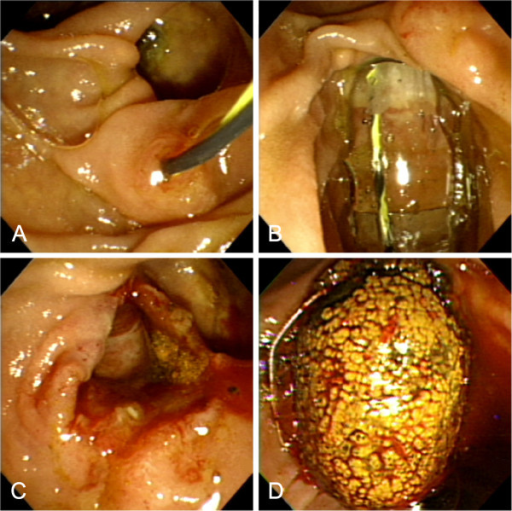
Diagnosticada a fístula biliar, paciente foi submetido a Colangiopancreatografia Retrógrada Endoscópica (CPRE), com papilotomia, sendo evidenciada fístula biliar em ramos secundários a direita. Não foi possível a colocação de prótese (em falta no serviço).
Após a CPRE, paciente ainda realizou outra paracentese com saída de cerca de 2 litros de bile. Neste momento, foi submetido a laparoscopia, com colocação de dreno perihepático com dificuldade (muitas aderências), para auxiliar na drenagem.
Mesmo com a drenagem externa paciente evoluiu com febre, e dor abdominal, sendo submetido a laparotomia exploradora, com drenagem de múltiplas coleções cavitárias. Foi necessário realizar peritoniostomia, para lavagens frequentes da cavidade. Em nenhuma das abordagens foi possível avaliar a lesão hepática ou tentar alguma terapêutica adicional sobre as vias biliares.
Após boa evolução, com parada de drenagem de bile e secreção purulenta, paciente foi submetido a fechamento da cavidade, pode ser realimentado oralmente, teve boa evolução e posterior alta, encontrando-se atualmente bem, trabalhando e sem alterações biliares.
Discussão:
Recentemente vem ganhando terreno as terapias não invasivas para traumas abdominais fechados, em especial de vísceras maciças, como rins, baço e fígado. As melhores condições de cuidados em UTI, associadas a evolução dos procedimentos diagnósticos e intervenções minimalistas, fazem com que terapias não operativas sejam a escolha em pacientes com lesões graves, antes sempre cirúrgicas, como lesões hepáticas acima de grau III.
A escolha da terapia não operativa em paciente com trauma abdominal fechado não reside apenas no grau de lesão das vísceras envolvidas (no caso vísceras maciças), mas na estabilidade hemodinâmica do paciente. Pacientes instáveis, são encaminhados imediatamente a cirurgia. Pacientes estáveis, são submetidos a exame de imagem, diagnóstico do tipo de lesão, e acompanhamento em UTI.
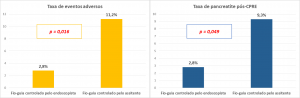
Especificamente no trauma hepático fechado, a principal preocupação e complicação é o sangramento. As fístulas biliares são incomuns, ocorrendo nos casos mais graves (graus de lesão maiores), com incidência estimada em cerca de 2,8 a 7,4% dos casos. Podem ocorrer de imediato, junto ao trauma, ou serem tardias, após cirurgias de controle de dano, ou após necrose de parênquima ou ruptura de biliomas.
O diagnóstico de complicações biliares nos casos de trauma hepático fechado pode ser difícil. Em geral podem aparecer sinais indiretos, como piora do quadro, febre e dor em hipocôndrio direito, e também, um sinal mais específico, a icterícia. Sugere-se que exames seriados de tomografia computadorizada podem evidenciar aumento de coleções com baixa atenuação, ou coleções perihepáticas tardias. Deve-se lembrar de que mesmo a tomografia computadorizada com contraste não é especifica para alterações biliares, com alguns autores sugerindo o estudo das vias biliares com técnicas de radioisótopos.
O tratamento inclui o suporte, antibioticoterapia e diagnóstico precoce. Como em geral as complicações biliares são tardias, os pacientes podem ser submetidos a técnicas minimamente invasivas. Inicialmente, pode-se colocar um dreno cavitário, no local da coleção, ou bilioma, transformando uma lesão biliar em uma fístula controlada, evitando-se a contaminação da cavidade e acumulo de fluídos.
Outra técnica já estabelecida é a realização de CPRE. A idéia do uso de tal terapêutica é que, devido a papilotomia, há diminuição da pressão biliar, deixando a bile de seguir pela fístula, causando o fechamento desta. Inicialmente após a papilotomia, pode haver ainda alguma dificuldade em drenagem da bile pela papila, secundária ao edema pela manipulação. Assim, hoje se indica o tratamento de fístulas biliares traumáticas com CPRE e próteses, principalmente em fístulas distais. A presença da prótese anula totalmente a pressão na via biliar, aumentando a taxa de fechamento de fístulas.
A evolução após a CPRE em geral é positiva, com o fechamento da fístula. Casos mais graves podem vir a necessitar de posterior cirurgia. Deve-se sempre acompanhar o paciente, principalmente quando da colocação de próteses, para evitar uma futura colangite por não retirada desta.
Você já tratou algum paciente assim? Como realizou o diagnóstico? Qual foi o tratamento e evolução?
Agradeço aos colegas Dr. Roberto Tucci Junior, pelo auxílio na condução do caso, e Dra. Flavia Ferreira Magalini na construção do relato.
Bibliografia:
Ragavan M, et al.Posttraumatic Intrahepatic Bilioma. Indian J Surg. 2015;77:1399-400.
Como citar esse artigo:
Sauniti, G. Caso Clínico – Fístula biliar pós trauma abdominal fechado. Endoscopia Terapêutica; 2018. Disponível em: https://endoscopiaterapeutica.net/pt/casosclinicos/caso-clinico-fistula-biliar-pos-trauma-abdominal-fechado/