Dicas em colonoscopia: intubação cecal.
A intubação cecal ou mesmo do íleo-terminal é um importante critério de qualidade em colonoscopia. Ela pode ser extremante frustrante no início da curva de aprendizado do residente, sendo que mesmo profissionais experientes podem encontrar casos desafiadores. O objetivo deste artigo é solidificar conhecimentos da prática diária para que possamos atingir esse objetivo inicial.
Anatomia da dor
O cólon é fixado pelo mesentério à parede abdominal posterior. É o alongamento do mesentério, e não a distensão, o principal responsável pelo desconforto abdominal durante a colonoscopia. Sempre que o instrumento é avançado, o mesentério retossigmoide é esticado o que leva ao quadro álgico sendo que nas pessoas mais jovens, especialmente nas mulheres onde o cólon tende a envolver o útero, a dor pode ser bastante intensa.
A única maneira de aliviar o desconforto é puxar o instrumento e relaxar a tensão. Em pacientes idosos ou obesos, o mesentério é mais complacente e se estende mais facilmente, geralmente sem dor.
Posição do paciente
Tradicionalmente o exame é iniciado com o paciente em decúbito lateral esquerdo. Uma mudança na posição do paciente pode, em alguns casos, ajudar o colonoscópio a avançar, particularmente eu uso esse recurso apenas após falha nas manobras de compressão abdominal. Entretanto muitos endoscopistas usam a mudança de posição de maneira sistemática para melhorar a configuração do cólon, especialmente o cólon sigmoide e descendente, onde a posição em decúbito dorsal ou lateral direita, frequentemente abre angulações agudas e ajuda no avanço do colonoscópio.
Gás X água
Sempre que possível, o dióxido de carbono deve ser usado para insuflar o intestino, e não o ar, o qual é eliminado mais lentamente podendo contribuir para o desconforto pós-procedimento. O cólon é como um balão cujo comprimento e diâmetro diminuem com a remoção do gás. Ao avançar o instrumento, assim que uma visão luminal for obtida, o gás deve ser aspirado para diminuir a tensão e tornar o eixo do instrumento mais estável. Por sua vez, isso minimiza o comprimento do cólon, reduzindo o potencial de formação de angulações a montante.
Outra opção é o preenchimento do cólon com água e não com gás. Não há regra sobre o volume de água, devendo ser pelo menos o suficiente para ver a direção luminal. Se o preparo estiver abaixo do ideal, faça a trocas de água conforme necessário. Quando forem encontradas bolsas de gás aspire-as. O enchimento de água mantém o cólon curto o que pode ajudar muito em alguns casos.
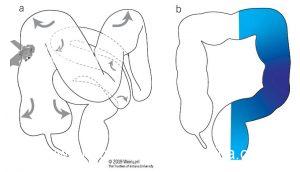
Figura 1. Esquema do impacto do enchimento de água e gás durante a inserção no cólon (a) Insuflação de gás na posição em decúbito lateral esquerdo. O gás (setas) distende e alonga o cólon, movendo o sigmoide medialmente abdome e o cólon transverso em direção à pelve. (b) O enchimento de água na posição em decúbito lateral esquerdo faz com que o sigmoide se deite no abdômen esquerdo, e o cólon permaneca mais curto e mais estreito em comparação com a insuflação de gás.
Compressão abdominal
Seu objetivo é diminuir a formação de alças direcionando o aparelho, sendo que raramente precisa ser aplicada por mais de 30 a 60 segundos. O conceito baseia-se que quando uma alça é sentida deve-se retificar o aparelho, pressionar nessa localização e após isso progredir o instrumento.
Tendo em vista que a maioria das alças são feitas no cólon sigmoide podemos iniciar realizando uma compressão sobre a área suprapúbica quando a ponta do colonoscópio retificada está entre 20 e 30 cm da borda anal ou uma compressão do quadrante inferior esquerdo, à medida que o instrumento está progredindo em direção à flexão esplênica ou cólon transverso.
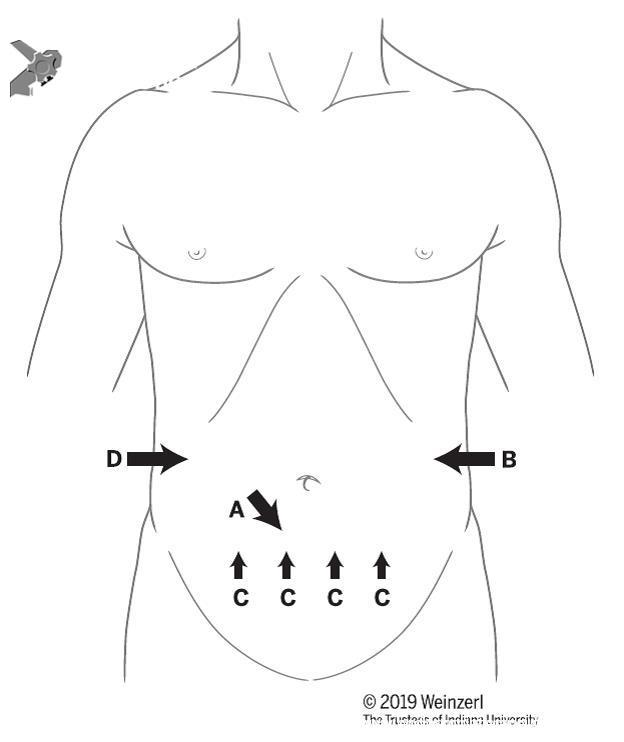
Um erro comum é o técnico simplesmente empurrar o abdômen diretamente em uma direção posterior, mas pode-se obter um maior sucesso empurrando do flanco em direção à linha média ou empurrando o abdome inferior em uma direção superior. Outro ponto é que em pacientes obesos, quatro mãos podem ser úteis na compressão. Na figura 2 temos um esquema dos locais de compressão de acordo com a formação de alças.
Figura 2. Locais e direções padrões da compressão abdominal: A. para alça em sigmoide. B. para passar a flexão esplênica. C. para alça em transverso. D. para passar do ascendente ao ceco.
Casos específicos
Cólon redundante
– Devido ao fato desse paciente tradicionalmente apresentar o cólon dilatado, pode muitas vezes ter histórico de preparo inadequado ou mesmo constipação crônica. Devemos nos certificar se esse paciente não necessita de um preparo diferenciado;
– Evite usar colonoscópios pediátricos pois esses têm uma maior tendências a formação de alças;
– Utilização de água ou invés de ar;
– Manobras de compressão abdominal;
– Mudança de decúbito;
– Overtube pode ser utilizado em casos extremos.
Angulação em sigmoide
– Principal causa é a doença diverticular;
– Utilização de aparelhos de menor diâmetro (colonoscópios pediátricos, enteroscópios ou mesmo gastroscópios);
– Utilização de água para evitar aumento de angulações e barotrauma.
Hérnias
– A hérnia inguinal esquerda é resolvida reduzindo a hérnia manualmente antes do procedimento e mantendo-se a mão sobre a abertura. Depois que a ponta do instrumento passa pelo cólon sigmoide, o problema está resolvido;
– Nos casos de hérnias em topografia de cólon transverso o paciente deve ser colocado em decúbito dorsal sendo que a hérnia deve ser reduzida com pressão manual e preferencialmente realizar a distensão do cólon com água ao invés de gás. Se encontrada uma resistência fixa não progredir o aparelho devido ao risco de iatrogenia.
Conclusão
Devemos ter em mente que o paciente merece o melhor tratamento possível, assim dedicando nossa total atenção tendo consciência dos nossos limites. Não podemos deixar de ter humildade para encaminhar o paciente a um colega mais experiente quando necessário.
Outro ponto importante é descrever as manobras utilizadas nos laudos, a fim de se contribuir com futuros exames nos casos desafiadores.
Referências
Waye JD, Thomas-Gibson S. How I do colonoscopy. Gastrointest Endosc. 2018;87(3):621‐624. doi:10.1016/j.gie.2017.09.002
Rex DK. How I Approach Colonoscopy in Anatomically Difficult Colons. Am J Gastroenterol. 2020;115(2):151‐154. doi:10.14309/ajg.0000000000000481