Uso de prótese metálica no câncer colorretal
INTRODUÇÃO:
Cerca de 10 a 30% dos pacientes com câncer colorretal (CCR) vão apresentar obstrução colônica como apresentação inicial.
A obstrução colônica aguda é uma condição grave que traz risco de vida, e que requer tratamento cirúrgico imediato.
Dentre os diversos tratamentos cirúrgicos, a cirurgia de Hartmann é o procedimento mais comumente realizado.
Entretanto a cirurgia realizada em caráter de emergência está associada a taxa de mortalidade de 10 a 30%, e de morbidade de 10 a 36%.
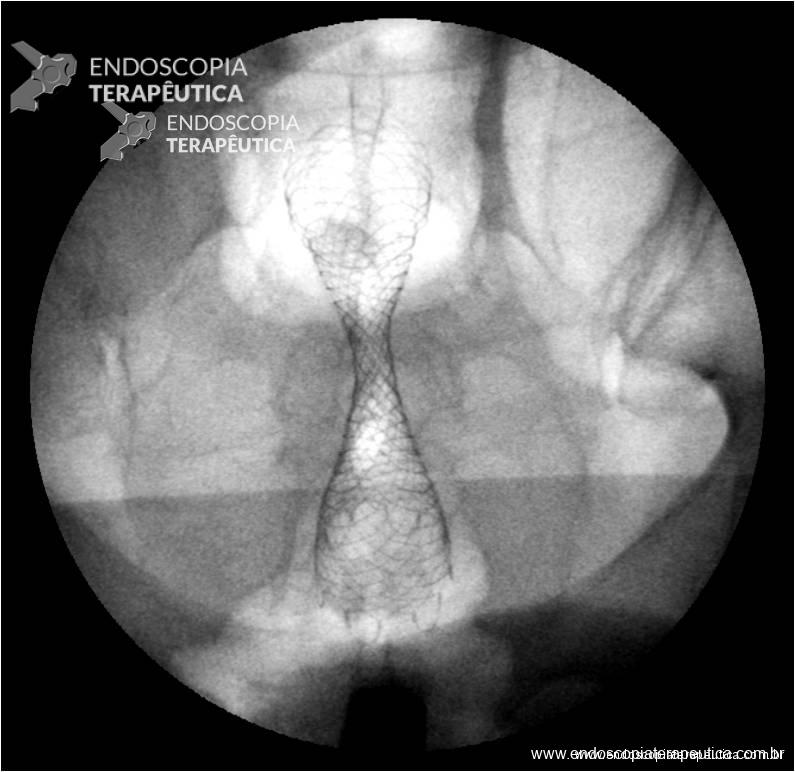
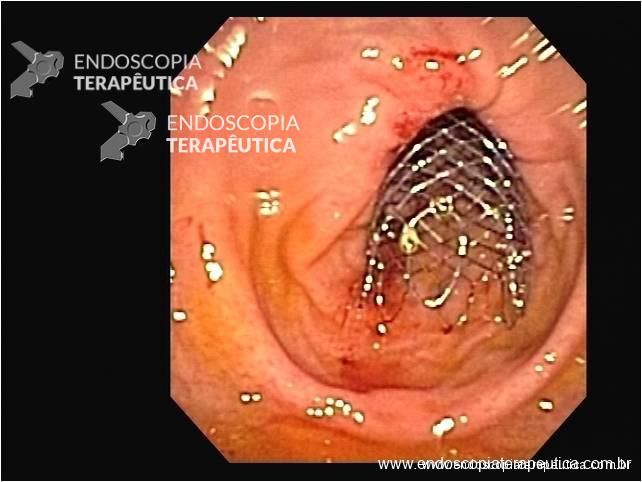
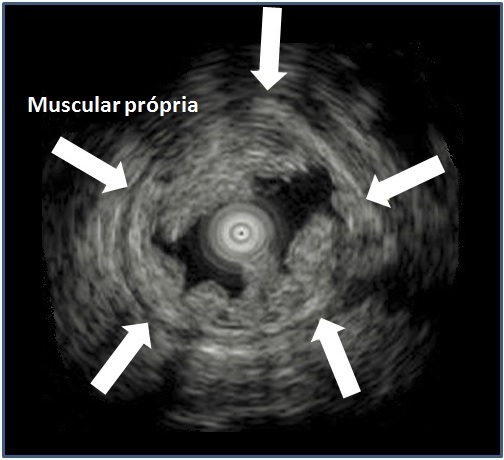
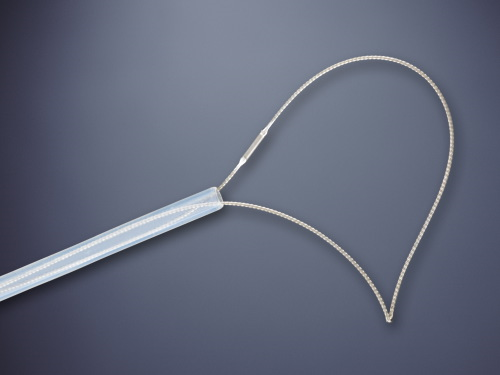
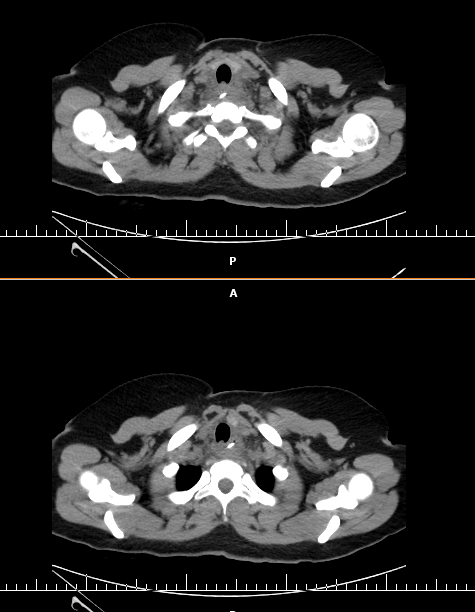
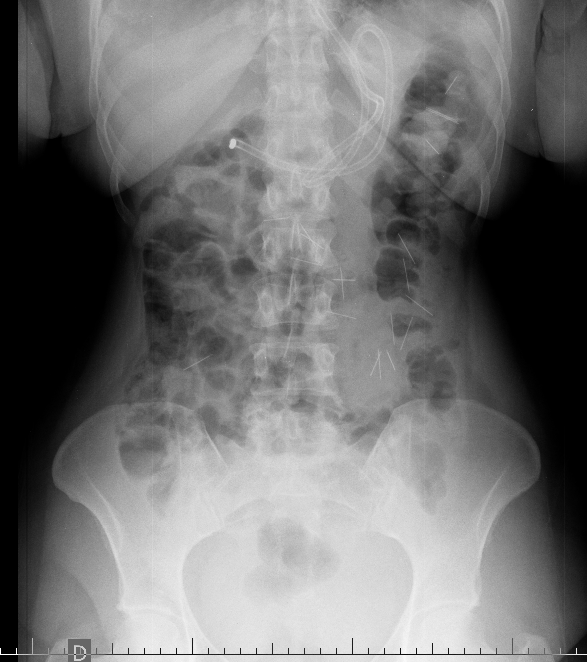
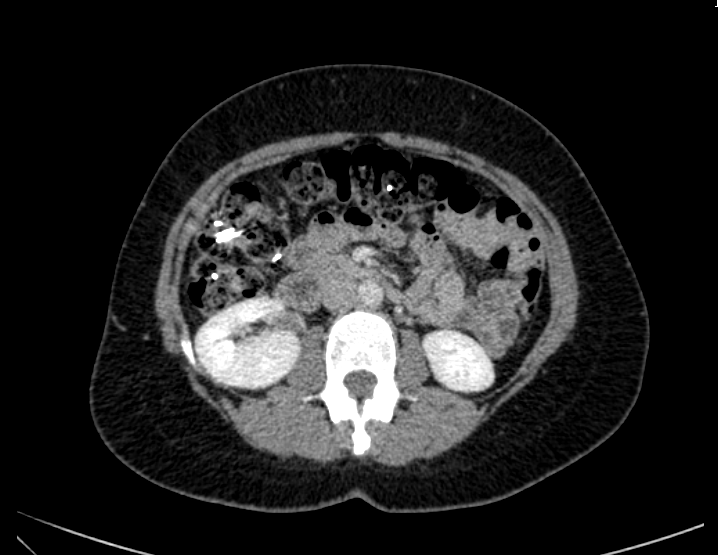
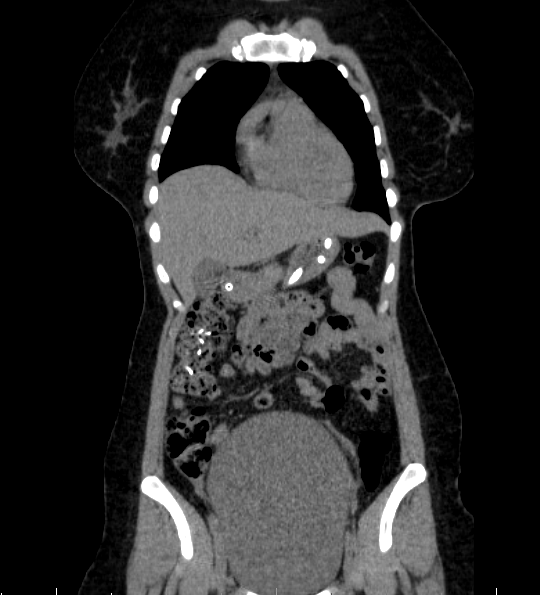
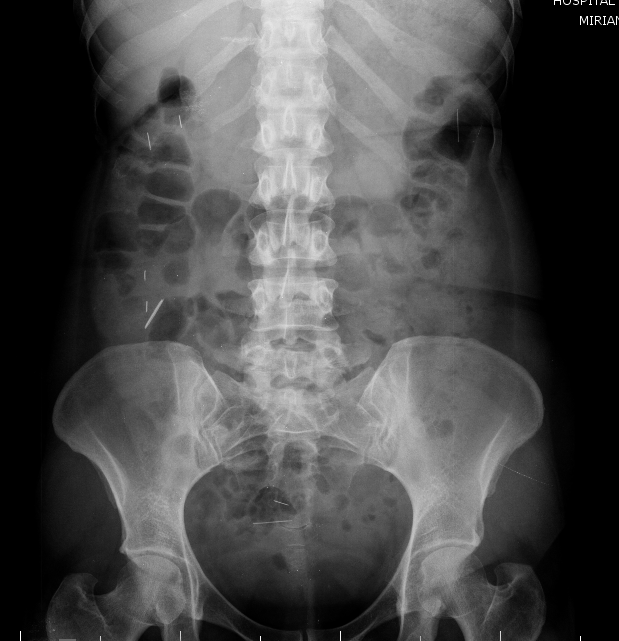
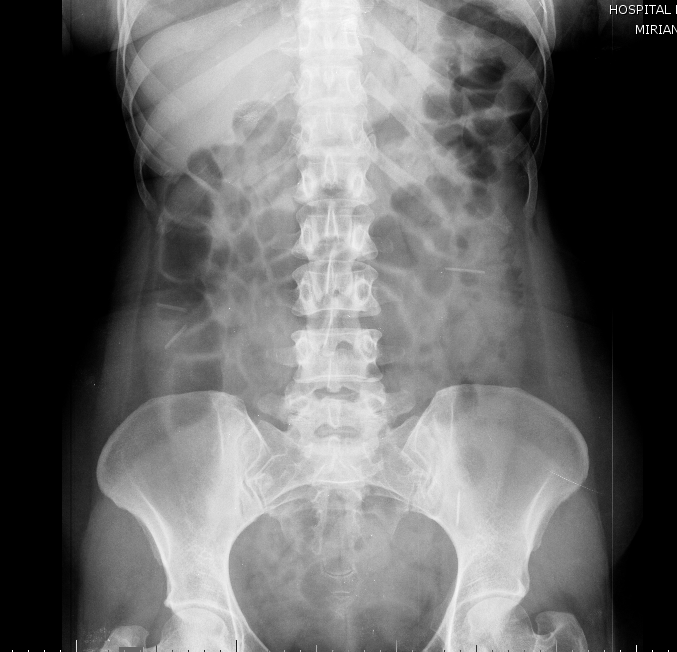
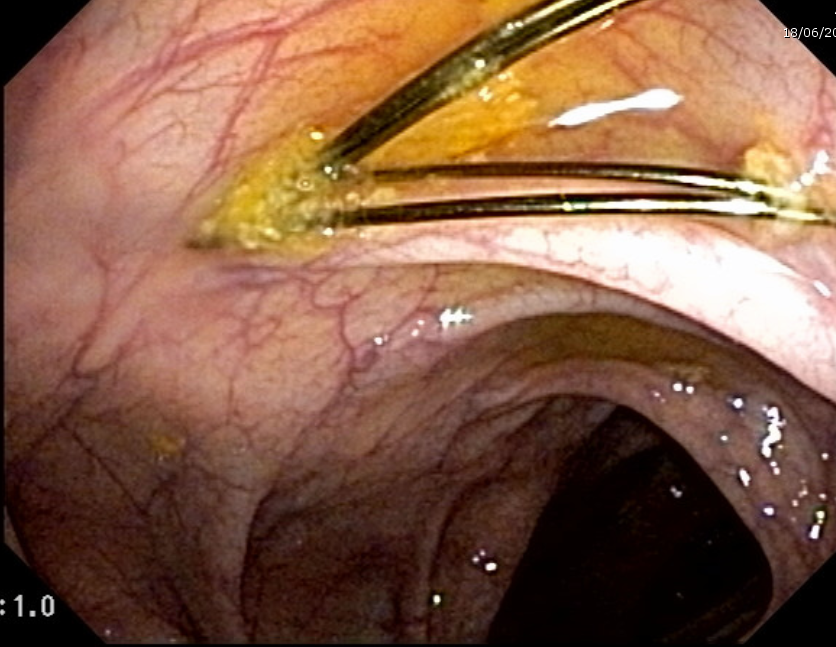
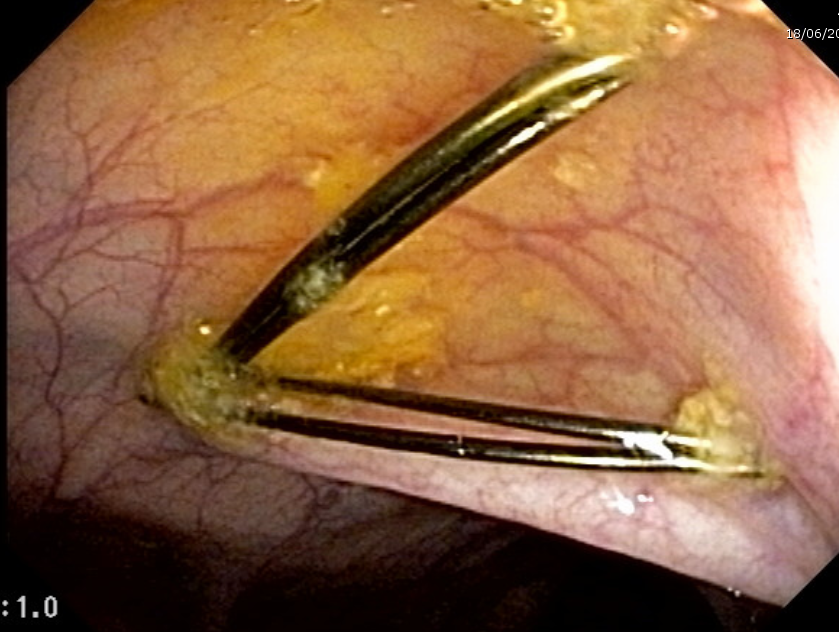
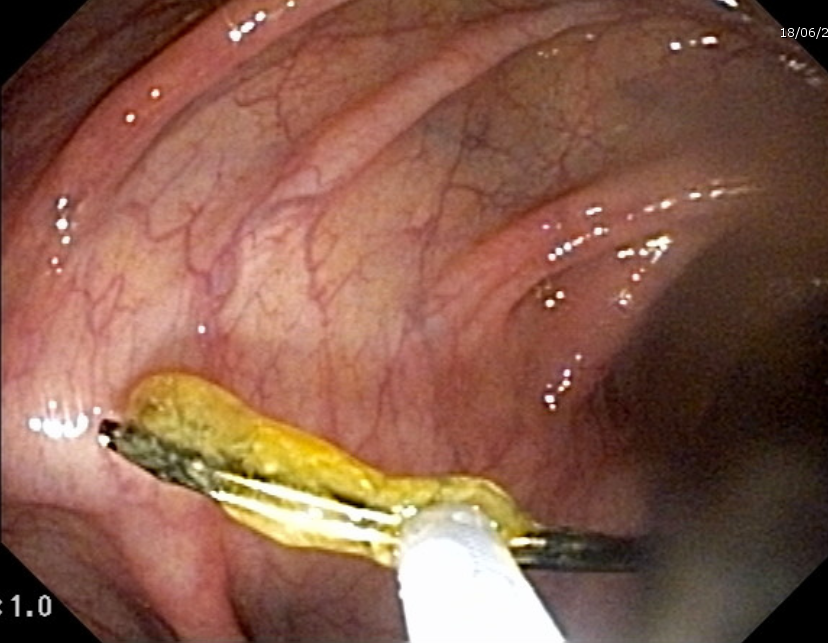
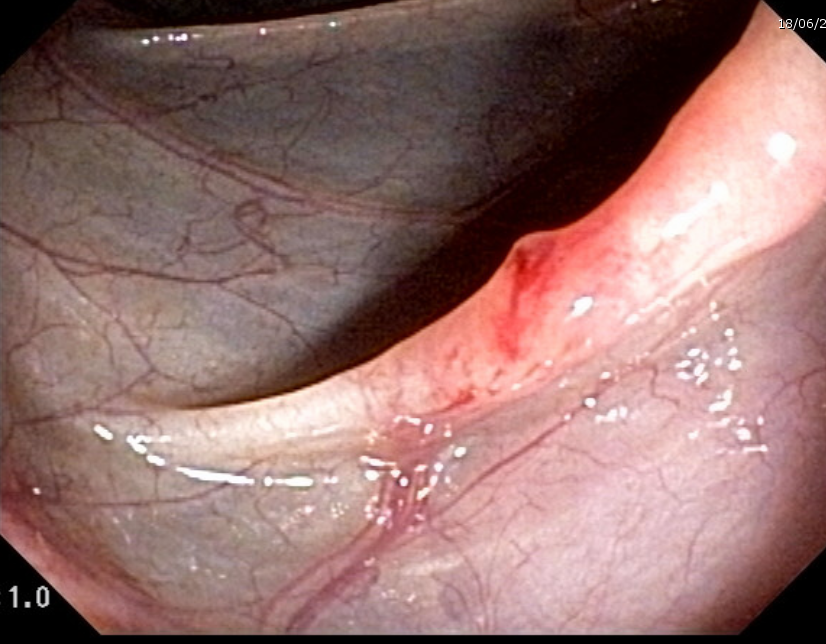
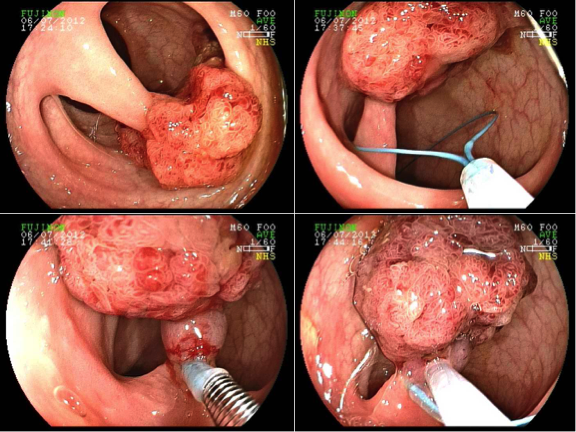
Esses dados encorajaram o desenvolvimento de procedimentos alternativos, com maior destaque para o uso endoscópico de prótese metálica auto-expansível (PMAE), que permite o alívio temporário da obstrução colônica aguda (ver figuras abaixo).
A PMAE pode ser utilizada em 2 indicações:
- Como ponte para cirugia;
- Para paliação dos sintomas obstrutivos.
Como ponte para cirurgia, a PMAE permite que o paciente possa receber um preparo pré-operatório adequado do cólon, e também possibilita converter uma situação de emergência em um cenário eletivo. Com esta conduta, diminui-se a necessidade de realização de uma ostomia, bem como aumenta a chance de realização de anastomose primária em um único tempo cirúrgico.
No tratamento paliativo da CCR irressecável, a PMAE permite a realização de radio e quimioterapia, e em comparação com a cirurgia está associada a menor tempo internação hospitalar, além de evitar a realização de ostomias.
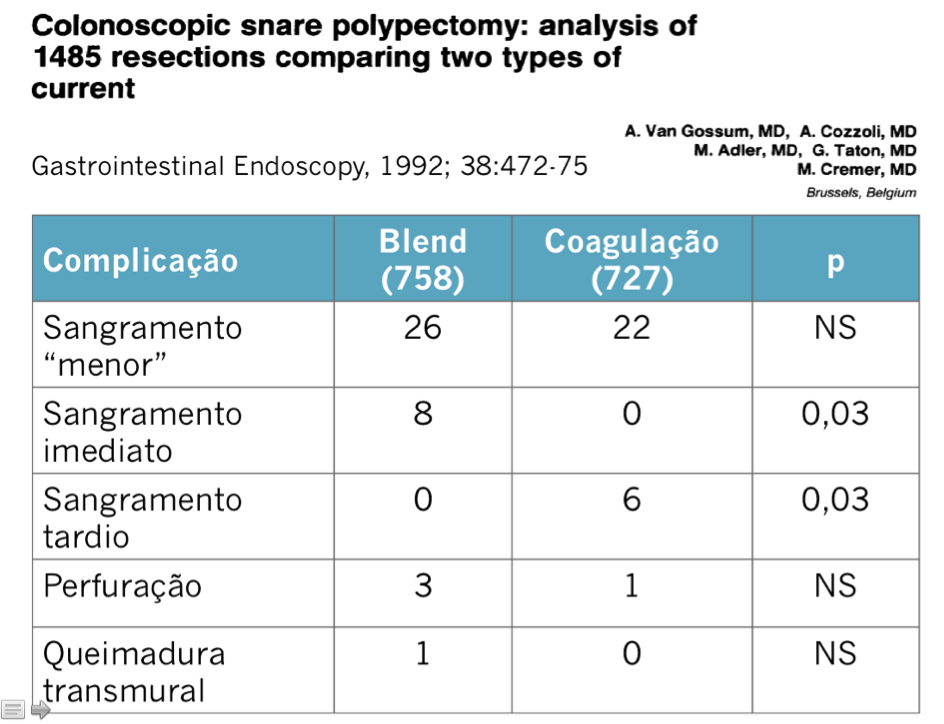
As complicações a curto prazo que podem ocorrer após a passagem da PMAE incluem perfuração, sangramento, tenesmo, dor e incontinência fecal. E a longo prazo as principais são reestenose e migração. Perfuração intestinal é a complicação mais grave pois pode levar a peritonite fecal, podendo ser fatal.
ESTUDO DO INSTITUTO DO CÂNCER DO ESTADO DE SÃO PAULO (ICESP):
Objetivo
Reportar a experiência do ICESP com o uso de PMAE no manejo da obstrução colônica de origem maligna, tanto para a paliação dos sintomas, como para ponte antes da cirurgia.
Metodologia
Análise retrospectiva de dados coletados prospectivamente, cm pacientes com obstrução colônica devido CCR submetidos a passagem de PMAE, entre julho de 2010 e Julho de 2014, no ICESP.
Sucesso técnico foi definido como a liberação correta da PMAE através da estenose maligna. E o sucesso clínico foi definido como a resolução dos sintomas de obstrução dentro das primeiras 72 horas após passagem da PMAE.
Resultados
Foram realizados 42 procedimentos de passagem de PMAE não coberta em 40 pacientes, com mediana de idade de 60.2 anos, e predomínio do sexo feminino (52.5%).
A intenção do tratamento foi paliação dos sintomas em 21 pacientes (52.5%), e ponte para cirurgia em 19 pacientes (47.5%).
A localização da obstrução foi mais predominantemente no: reto (30%), junção retossigmóide (22.5%), descendente/sigmóide (22.5%).
O aparelho de colonoscopia de 12.8 mm não pode traspor a estenose em 92.5% dos casos.
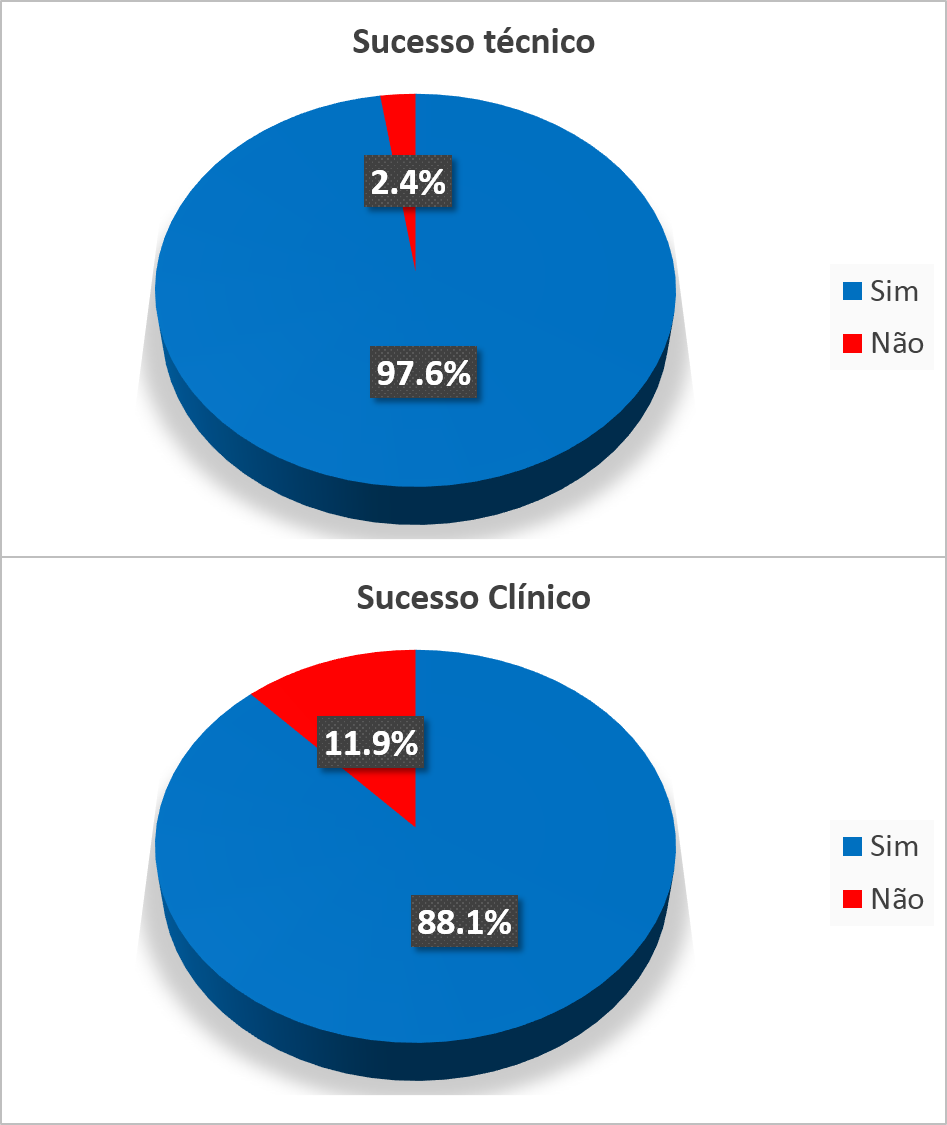
A taxa de sucesso técnico foi de 97.6%, e de sucesso clínico de 88% (ver gráfico 1 abaixo):
Dos 5 pacientes que foram submetidos a cirurgia de urgência após tentativa de PMAE sem sucesso, a taxa de criação de ostomia foi de 88% e de anastomose primária de 40%. Em comparação, dos 16 pacientes que receberam PMAE como ponte para cirurgia com sucesso, a taxa de criação de ostomia foi 50% e de anastomose primária de 75%. Ver gráfico 2 abaixo:
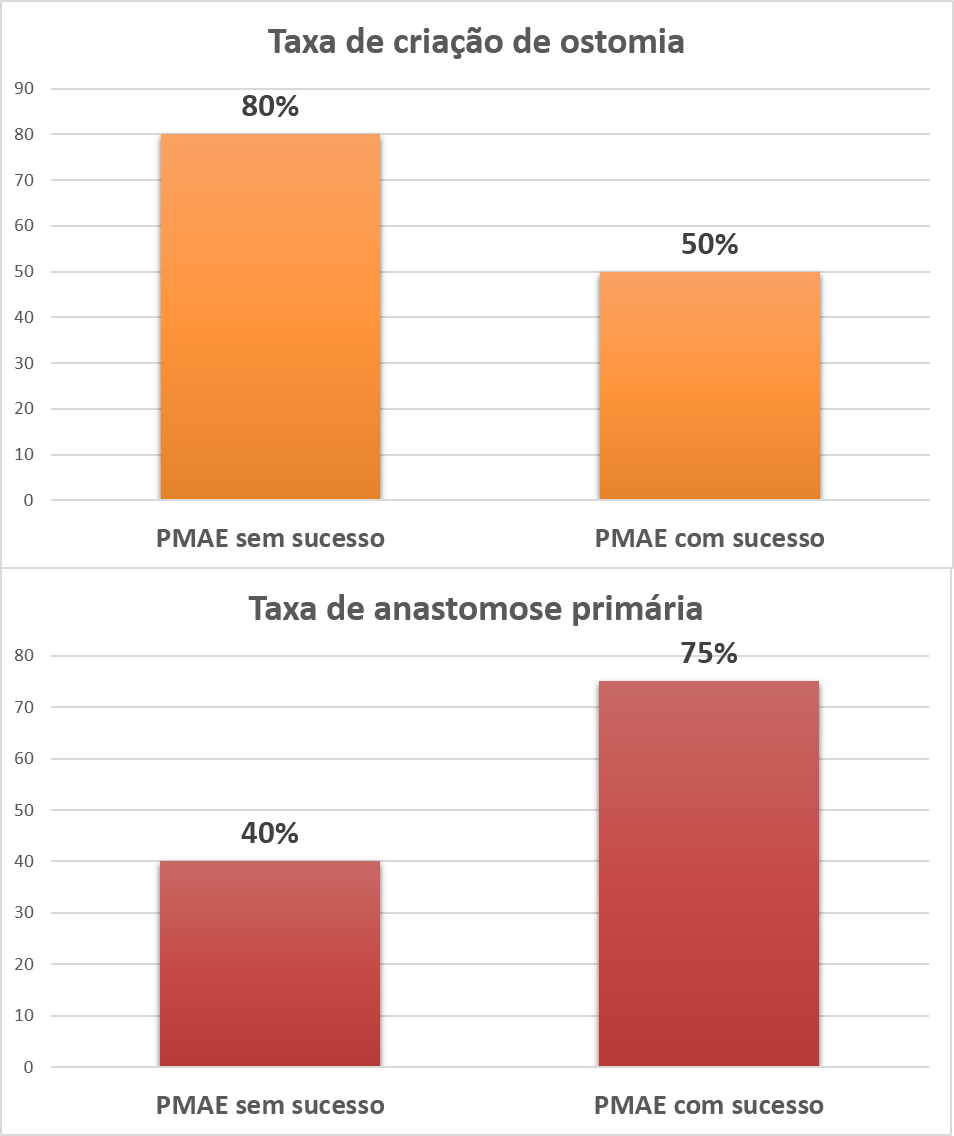
Gráfico 2: Taxas de criação de ostomia e anastomose primária, após passagem de prótese, com e sem sucesso, em pacientes com CCR.
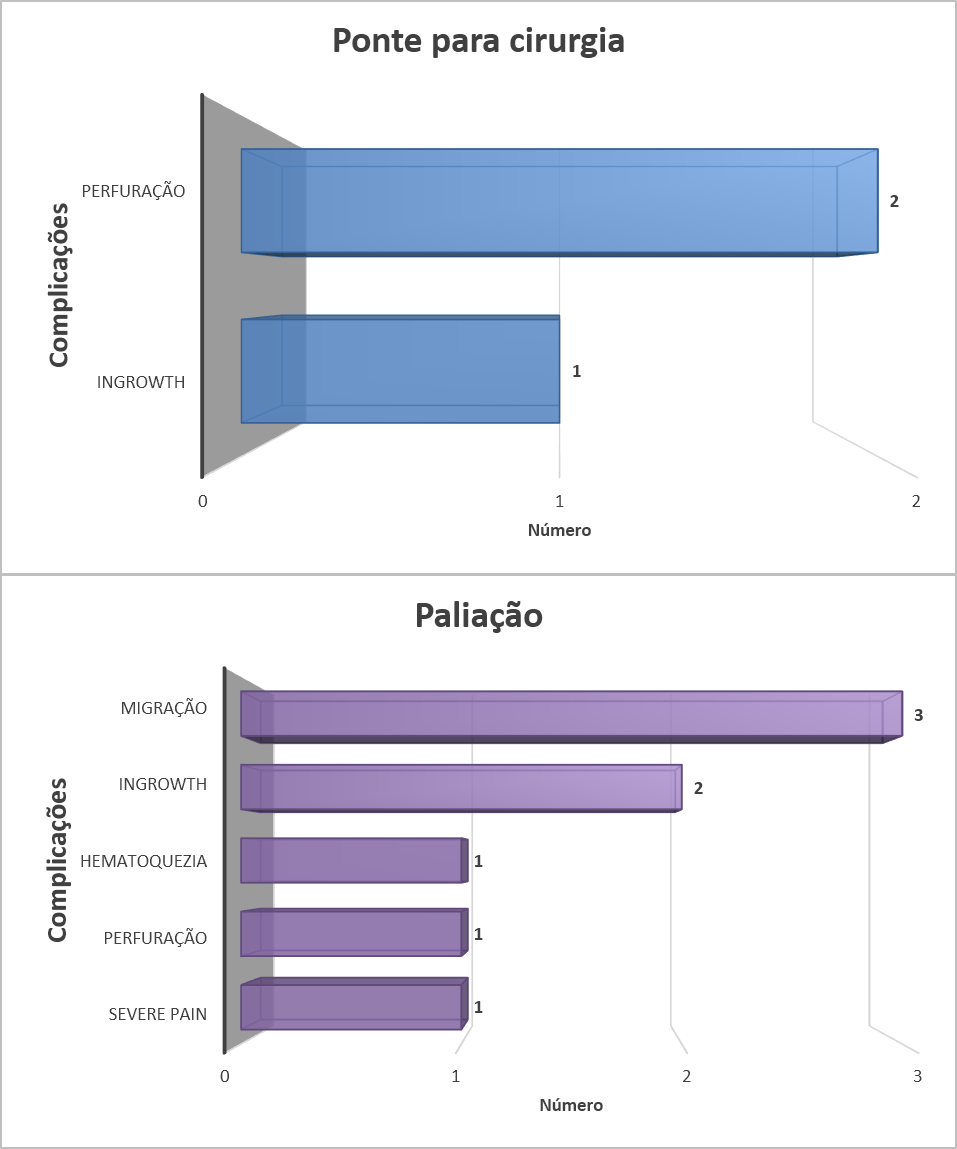
A média de tempo para realização de cirugia foi de 40 dias, e houveram 3 casos (18.7%) de complicações pela prótese: 2 perfurações e 1 ingrowth (ver gráfico 3).
Dos 21 pacientes que recebram PMAE para paliação dos sintomas obstrutivos, a taxa de sucesso foi de 91.3%. Quimio e/ou radioterapia foi realizada em 18 casos (85.7%). Durante uma mediana de acompanhamento de 3.12 meses, observaram-se complicações em 42.1%: 3 migrações, 2 ingrowth, 1 dor abdominal severa, 1 hematoquezia e 1 perfuração. A maioria desses casos foram manejados conservadoramente ou com uma segunda prótese, e apenas 1 paciente necessitou de cirurgia devido a perfuração relacionada à prótese. Ver gráfico 3 abaixo:
Conclusão
O tratamento da obstrução colônica aguda devido ao CCR com PMAE é seguro e efetivo. A PMAE evita a cirurgia de emergência, pode reduzir a taxa de criação de ostomia e permite a realização de tratamento oncológico de forma segura em pacientes com doença disseminada.
Referências:
Lujan HJ, Barbosa G, Zeichen MS, Mata WN, Maciel V, Plasencia G, Hartmann RF, Viamonte III M, Fogel R. Self-expanding metallic stents for palliation and as a bridge to minimally invasive surgery in colorectal obstruction. JSLS. 2013 Apr-Jun;17(2):204-11.
Repici A, de Paula Pessoa Ferreira D. Expandable metal stents for malignant colorectal strictures. Gastrointest Endosc Clin N Am. 2011 Jul;21(3):511-33.
Tan CJ, Dasari BV, Gardiner K. Systematic review and meta-analysis of randomized clinical trials of self-expanding metallic stents as a bridge to surgery versus emergency surgery for malignant left-sided large bowel obstruction. Br J Surg. 2012 Apr;99(4):469-76.