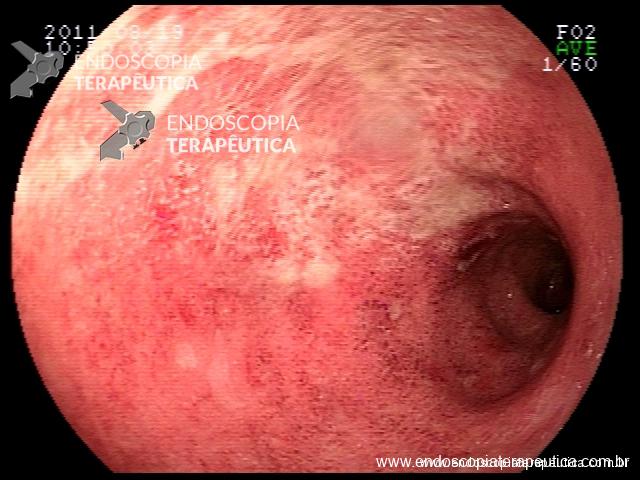
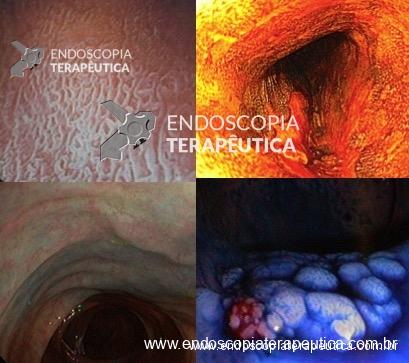
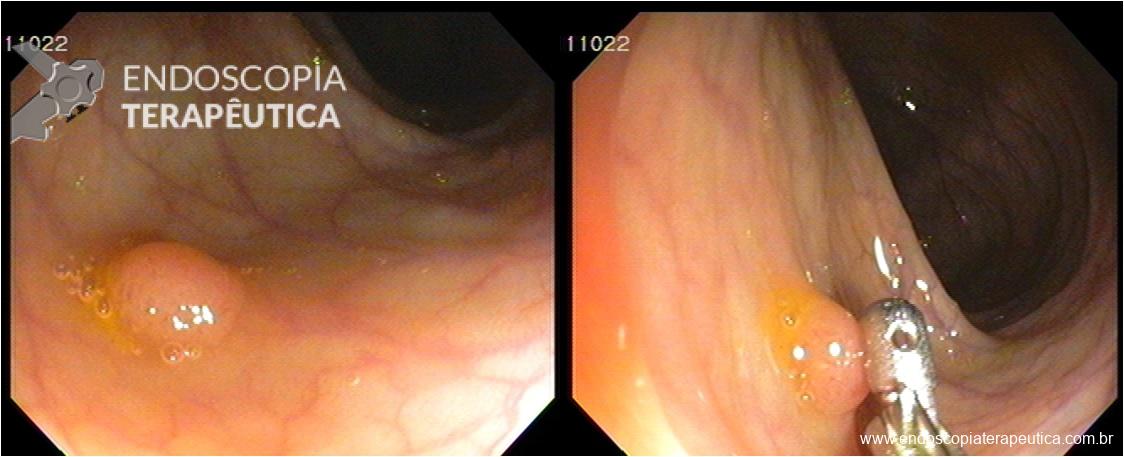
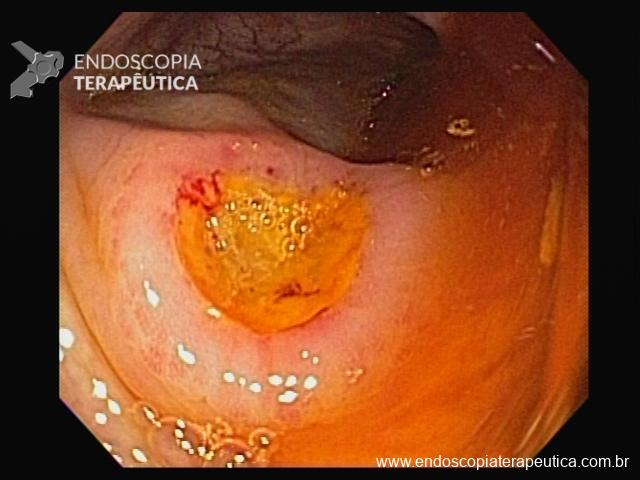
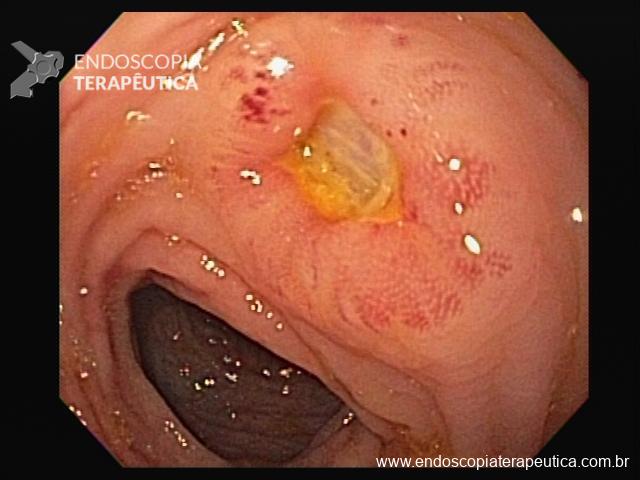
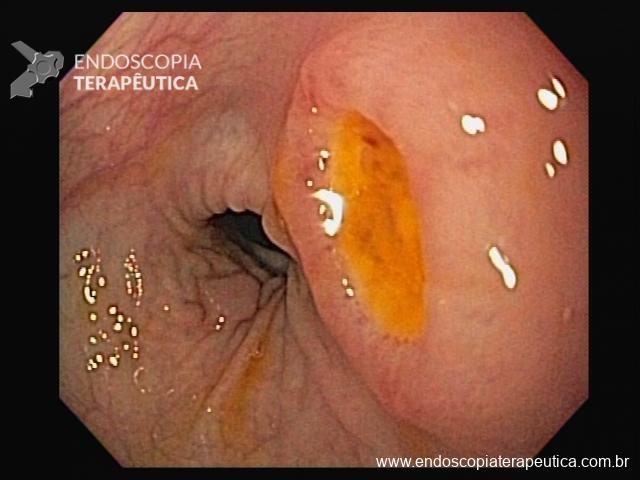
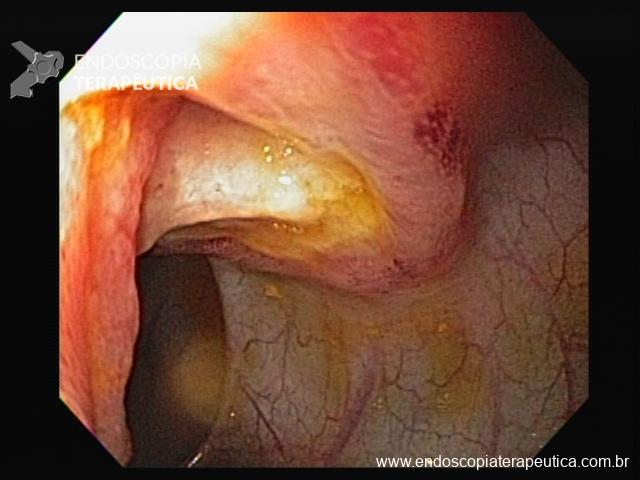
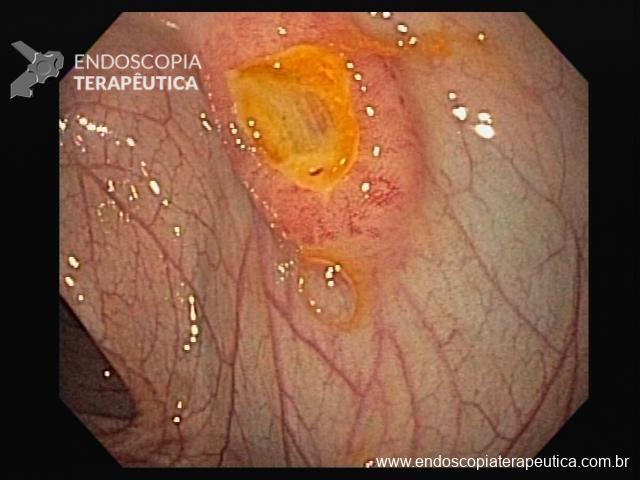
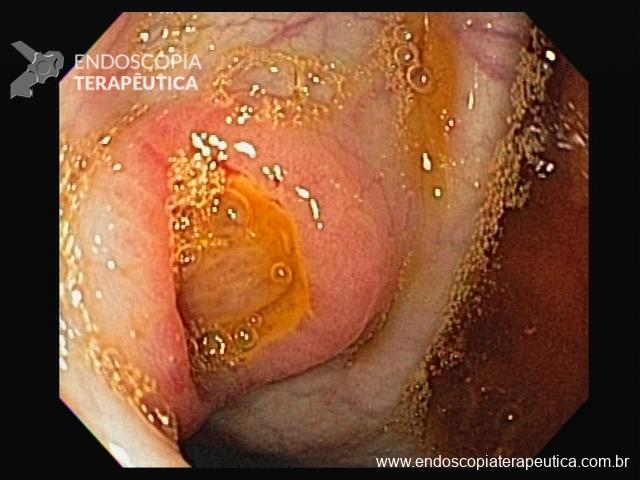
Cromoscopia com corantes
Classificação:
1- Corantes de absorção ou vitais (azul de metileno, violeta de genciana, lugol)
2- Corantes de contraste (índigo carmin)
3- Corantes químicos ou reativos (vermelho-congo, ácido acético)
4- Corantes permanentes (tatuagem). Clique aqui para ver mais
O uso de corantes na prática clinica é de fácil acesso, baixo custo e aumenta significativamente a qualidade do exame do ponto de vista diagnóstico e terapêutico.
FUNÇÕES:
– realça o relevo e depressões de lesões
– melhora o estudo da citoarquitetura das lesões
– direciona locais para biópsia em suspeita de câncer
Corantes mais usados:
- Lugol 2-3%
- Azul de metileno 0,5 -1%
- Ácido acético 1,5%
- Índigo Carmin 0,2 – 0,5%
1. Lugol
- Composto de iodo + iodeto de potássio
- A reação do iodo com o glicogênio do epitélio escamoso leva a uma coloração castanho escura, sendo que as áreas alteradas não se coram, ou ficam fracamente coradas
- Usado na concentração de 2-3%
Indicado em pacientes com:
- Tumor de cabeça e pescoço (11% *)
- Megaesôfago (2-7%* , doença há mais de 10 anos)
- Estenose cáustica (16%*, doença há mais de 20 anos)
- Alcoólatras e tabagistas
* prevalência de carcinoma de esôfago
Técnica:
- Material: Lugol 2% 20ml, Agua destilada 20ml , Hipossulfito de Sodio / Tiossulfato de sódio 5% 20ml
- Sedação e analgesia adequada pois o procedimento é doloroso pelos espasmos
- Começar da parte distal, junto a transição esofagogástrica, para a proximal
- Posiciona-se o cateter vaporizador a 2cm da extremidade do aparelho, mantendo a insuflação para que haja contato do corante em toda a circunferência do órgão
- Na ausência de cateter pode-se jogar o corante através do canal de biópsias. Geralmente 20ml, sendo 5ml a cada 5cm, na parede lateral direita. Quando chegar na parte proximal, aspirar e insuflar algumas vezes (para o esôfago abrir e fechar)
- Aspirar o excesso de corante e esperar um minuto
- Tirar o excesso de corante com 20ml de água destilada
- Voltar para a transição esofagogástrica e analisar as áreas que não foram coradas
- Após jogar 20ml de hipossulfito de sódio para neutralizar o efeito do lugol
Áreas não coradas:
- Carcinoma ou displasia severa de esôfago
- Epitélio colunar do esôfago (Barrett)
- Erosões pépticas
- Ectopias gástricas
- Acentuado processo inflamatório ou atrófico
Complicações:
- Dor retroesternal
- Tosse
- Espasmo de laringe
- Reação alérgica
*Contra-indicado para pacientes com alergia a iodo
Veja exemplo na galeria de imagem: https://endoscopiaterapeutica.net/pt/carcinoma-de-celulas-escamosas/
2. Azul de metileno
- Absorvido pelas células epiteliais do intestino delgado e cólon
- Usado na concentração de 0,5-1%
- Necessita do uso prévio de mucolítico (acetilcistína 10% ou ácido acético)
Aplicação clínica:
- Metaplasia de Barrett
- Metaplasia intestinal gástrica
- Metaplasia gástrica no duodeno (não cora)
Técnica:
- Material: Azul de metileno 20ml, Acetilcistína 10% ou ácido acético ,
- Instilar o mucolítico
- Após jogar o corante e esperar um minuto para a absorção
- Lavar com água destilada até que o padrão da coloração não mude mais
- Considerado positivo se permanecer corada após lavagem
Efeito colateral:
- Coloração azulada da urina e fezes
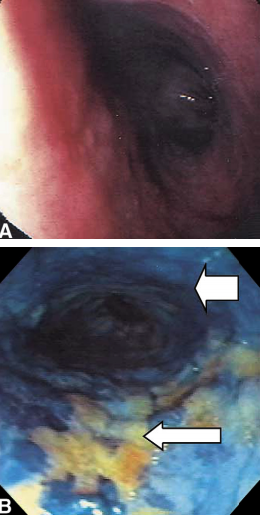
3. Ácido acético
- Produz degeneração reversível das proteínas intracelulares
- Interage com a camada externa de glicoproteínas que recobre a superfície mucosa do epitélio colunar, eliminando-a e conferindo uma coloração esbranquiçada
- Esta reação não ocorre no epitélio escamoso pois o AA é neutralizado pela rede vascular e pelo estroma subjacente
- Usado na concentração de 1,5%, 10-15ml
Técnica:
- Material: ácido acético 1,5% 40ml, água destilada
- Aplicação de 20ml sobre a área
- Lavagem com água destilada
- Nova aplicação de 20ml
- Deixa-se agir por 2 minutos (durante este tempo aspira-se o excesso depositado no lago gástrico)
Aplicação clínica:
- Esôfago de Barrett
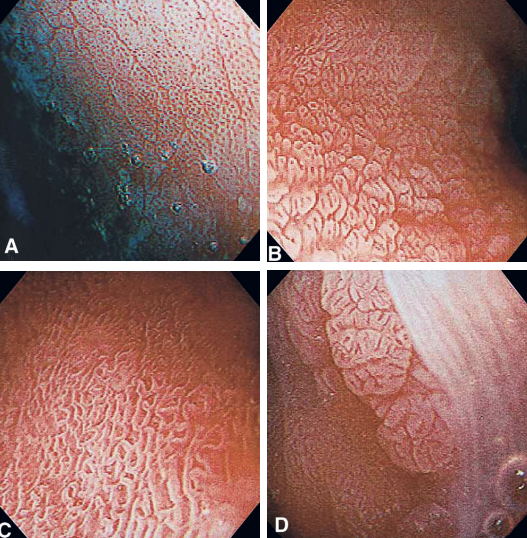
4. Índigo Carmim
- Composto por um corante vegetal azul (índigo) e de um agente vermelho (carmim)
- Corante de realce, não absorvível
- Usado na concentração de 0,1- 0,5%
- Contraste mais usado em estômago, duodeno e cólon
Efeitos colaterais:
- Muito raros
- Hipotensão leve
- Reações anafiláticas
Aplicação Clínica
- Diagnóstico do câncer precoce
- Avaliação na doença celíaca
Leia mais:
https://endoscopiaterapeutica.net/pt/neoplasia-gastrica-precoce/
Veja o uso do índigo carmin para terapêutica endoscópica no post abaixo:
Dissecção Endoscópica Submucosa (ESD): dicas para iniciar e aprimorar a técnica
Referência bibliográfica: Chromoendoscopy GIE Volume 66, No. 4 2007
Obstrução intestinal por fecaloma no cólon direito – uma doença potencialmente fatal
Paciente do sexo feminino, 76 anos, com história de diabetes, constipação crônica e ressecção segmentar de transverso há 10 anos por adenoma não ressecável por colonoscopia. Foi internada com quadro de distensão e dor abdominal difusa ha 2 dias e sem evacuar ha 5 dias. Nos dias anteriores ao início dos sintomas relatava evacuações a cada 2 dias, sempre em pequena quantidade.
A paciente estava em bom estado geral, abdome distendido com ruídos presentes e desconforto à palpação difusamente, sem sinais de peritonite e sem massas palpáveis. No toque retal não se notavam lesões e não havia fecaloma tocável.
Os exames laboratoriais mostravam eletrólitos, amilase e função renal normais. Hemograma com hemoglobina normal mas com 17000 leucócitos, sem desvio à esquerda.
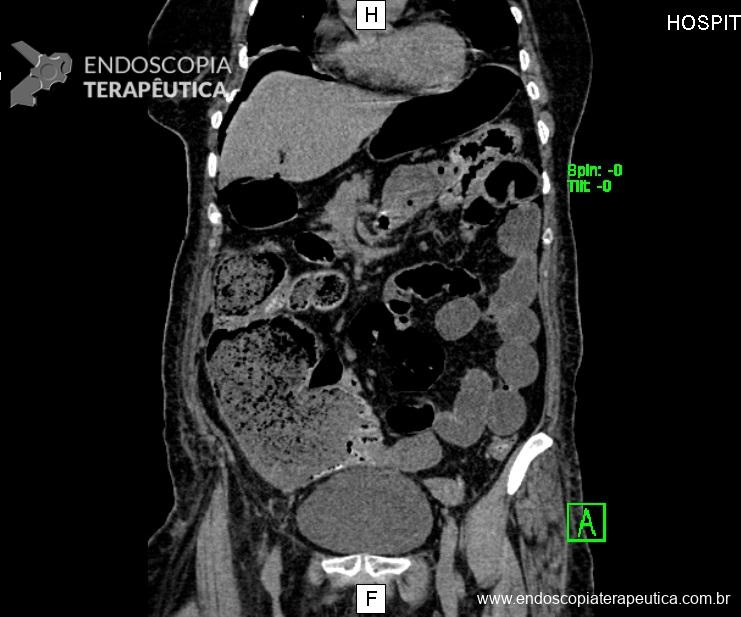
Realizou tomografia de abdome total com os seguintes achados:
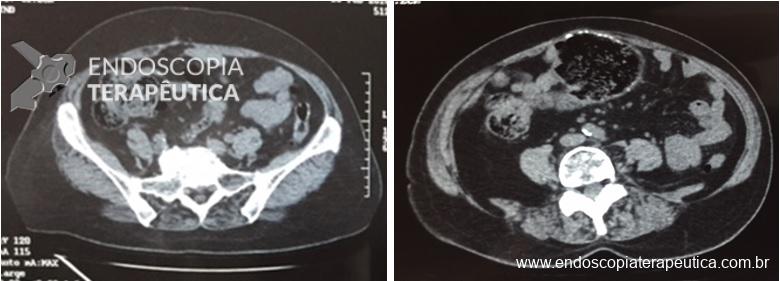
Ausência de líquido livre ou sinais de pneumoperitônio. Estômago e intestino delgado sem distensão. Volumosa coprostase no cólon direito e cólon transverso sem se identificar ponto de obstrução evidente.
Com este achado foi iniciado o uso de laxativos via oral, ingestão aumentada de líquidos e lavagem retal com glicerina 12 %. Mesmo após várias lavagens retais e uso de laxativos orais a paciente evoluiu com piora da dor e distensão abdominal.
Neste momento foi indicada a realização de uma colonoscopia (preparo exclusivamente retrógrado) para descartar a presença de um fator obstrutivo não identificado na tomografia e tentar descomprimir o cólon.
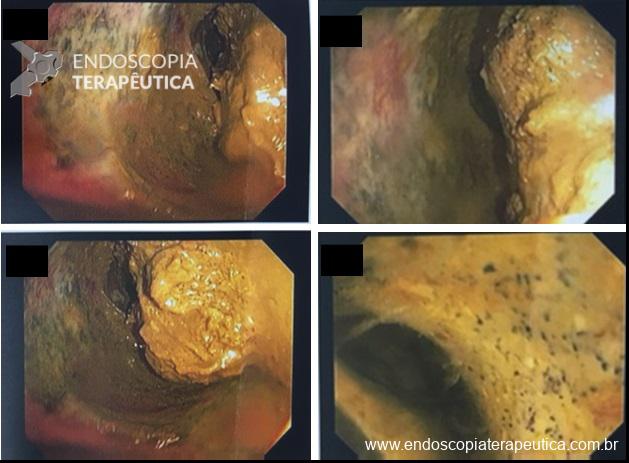
Colonoscopia: Volumoso fecaloma impactado no cólon transverso. Foi realizada infusão lenta de 1000 ml de soro fisiológico morno com amolecimento do fecaloma, permitindo a passagem do aparelho através da área de obstrução e descompressão do cólon direito que também apresentava grande quantidade de resíduos fecais. O local de impactação apresentava sinais de isquemia e necrose da mucosa. O cólon direito apresentava grande quantidade de resíduos fecais aderidos às paredes, impedindo a avaliação da mucosa.
Após a colonoscopia descompressiva a paciente apresentou melhora significativa da dor e distensão abdominal e estava em ótimo estado geral. Foi mantida internada com antibióticos, dieta líquida sem resíduos e laxativos via oral. Apresentou eliminação de gases e evacuações no mesmo dia da colonoscopia.
No dia seguinte a paciente voltou a apresentar distensão abdominal e evoluiu com taquicardia, taquipnéia e alteração do nível de consciência.
Realizou nova tomografia de abdome que demonstrou grande distensão do ceco e presença de pneumoperitônio. Ausência de líquido livre. Neste momento foi indicada abordagem cirúrgica. Devido à distensão abdominal foi optado por laparotomia convencional.
No intra-operatório foi identificada grande área de necrose no ceco, ainda sem perfuração e outro ponto de necrose no cólon transverso. Não havia perfuração evidente e nem contaminação da cavidade. Foi realizada uma colectomia direita ampliada (ceco, ascendente, transverso residual e descendente). Como a paciente estava estável hemodinamicamente, sem anemia, o intestino delgado e o sigmóide não estavam distendidos e não havia contaminação da cavidade foi realizada anastomose primária íleo-sigmóide.
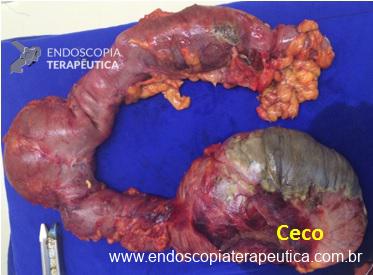
Colectomia direita ampliada. Nota-se grande área de necrose no ceco e outra pequena no transverso. Também é possível identificar a área de anastomose da ressecção prévia.
A paciente apresentou uma boa evolução no pós operatório, recebendo alta da UTI no 5º pós operatório com evacuações presentes e recebendo dieta via SNE.
Revisão
A impactação fecal é uma patologia comum e potencialmente fatal que pode ocorrer em todos os grupos etários. Crianças, pacientes acamados e idosos são as populações que estão sob maior risco. A impactação geralmente ocorre na presença de constipação severa, anormalidades anorretais e nas disfunções neurogênicas e funcionais gastrointestinais1.
O reconhecimento precoce desta doença é importante devido à sua alta morbidade, mortalidade e grande custo ao sistema de saúde. O tratamento minimiza o risco de complicações que incluem obstrução intestinal levando à úlcera estercoral, perfuração, peritonite e sepse1.
Uma revisão incluindo 188 artigos, analisou 280 casos de obstrução por fecaloma. Destes 43,5% pacientes tinham mais do que 65 anos, 49% apresentavam história de constipação severa, 29% eram portadores de doenças neuropsiquiátricas e 15% estavam institucionalizados. Um total de 346 complicações médicas secundárias à impactação fecal foram identificadas incluindo perfuração, obstrução, fístulas para órgãos adjacentes e complicações clínicas como pneumonia aspirativa e sepse2.
Não há diferença na distribuição por sexo mas a idade avançada aumenta a incidência desta patologia. No exame físico a distensão e a dor abdominal são os achados mais frequentes. No exame retal, a presença de fezes tocáveis é encontrada em menos da metade dos casos, pois a impactação pode ocorrer em qualquer local, desde o cólon direito até o reto. Os achados laboratoriais são inespecíficos mas a leucocitose e alterações eletrolíticas são comuns. A radiografia de abdome costuma mostrar dilatações difusas do delgado e do cólon além de grande quantidade de fezes acumuladas. A tomografia de abdome é o melhor exame pois pode identificar o local preciso da impactação, descartar complicações e outras causas de obstrução3.
A sigmoidoscopia e a colonoscopia podem ser utilizadas para descartar a presença de obstrução mecânica de outra etiologia e também para ajudar na fragmentação e irrigação da massa fecal impactada, porém, devem ser realizadas com cuidado devido ao risco de perfuração iatrogênica3.
A perfuração intestinal causada por impactação fecal é rara e quando ocorre apenas 10-20 % dos casos tem o diagnóstico confirmado antes da operação. Neste cenário é importante a realização de ressecção do segmento colônico acometido (já que a área isquêmica costuma ser grande) e a realização de uma ostomia. A sutura da perfuração ou a simples derivação estão associadas à um maior risco de complicações e mortalidade4.
Referências
- Hussain ZH, Whitehead DA, Lacy BE. Curr Gastroenterol Rep. 2014 Sep;16(9):404.
- Serrano Falcón B, Barceló López M, Mateos Muñoz B, Álvarez Sánchez A, Rey E. Fecal impaction: a systematic review of its medical complications. BMC Geriatr. 2016 Jan 11;16(1):4.
- Byun YH, Park YS, Myung SJ, Eom WY, Choi WW, Kim TH, Jo YJ, Kim SH, Song MH. Transient intestinal obstruction due to stool impaction in the elderly. Korean J Gastroenterol. 2005 Sep;46(3):211-7.
- Serpell JW, Nicholls RJ. Stercoral perforation of the colon. Br J Surg. 1990 Dec;77(12):1325-9.
Conceitos em Carcinogênese Colorretal
O câncer colorretal (CCR) é o quarto tumor mais frequente e a segunda causa de morte por câncer nos EUA. Estima-se para o ano de 2016 mais de 140 mil novos casos de câncer de cólon e reto nos EUA com aproximadamente 50 mil mortes, correspondendo a aproximadamente 9% das causas de morte por câncer. No Brasil, segundo os dados do INCA, estima-se mais de 34 mil novos casos de CCR para 2016. Apesar dos elevados números a incidência e a mortalidade nos pacientes acima de 50 anos vem diminuindo desde a década de 90 devido aos programas de rastreamento e melhora da assistência oncológica clínica e cirúrgica.
Entretanto, o diagnóstico de CCR nos pacientes abaixo de 50 anos tem aumentado por fatores ainda não esclarecidos. Segundo a OMS, estima-se que nos pacientes abaixo de 34 anos a incidência deve aumentar em até 125% até 2030.
O câncer colorretal é uma doença heterogênea no que se refere ao desenvolvimento e ao comportamento biológico e causada pela interação entre fatores genéticos herdados ou não e ambientais. A doença pode se apresentar de forma esporádica, herdada ou familiar.
Forma esporádica: a apresentação esporádica, sem história familiar, corresponde a aproximadamente 70% dos casos. A idade acima de 50 anos é o fator de risco mais importante além da dieta e de outros fatores ambientais.
Herdada: uma pequena proporção dos casos se deve às formas herdadas, relacionadas à mutações germinativas específicas, divididas pela presença ou não de polipose associada.
- O CCR com polipose inclui a Polipose Adenomatosa Familiar (PAF) em 1% dos casos, a Polipose associada ao gene MYH em menos de 1% e as síndromes de poliposes hamartomatosas como Peutz-Jeghers e a Polipose Juvenil.
- As formas não relacionadas à polipose correspondem a 2 a 5% dos casos e se referem ao HNPCC e a Síndrome de Lynch. Todas estas condições apresentam um risco muito significativo de transformação maligna e na maioria das vezes a mutação genética pode ser identificada.
Familiar: Aproximadamente 20 a 25% dos casos se relacionam a um componente hereditário não tão bem estabelecido como as formas descritas acima e são denominados “câncer colorretal familiar”. As alterações genéticas são até o momento menos conhecidas que as das formas herdadas e o risco de desenvolvimento de câncer em um indivíduo deste grupo é 1,7 vezes maior que o da população geral quando existe um parente de primeiro com CCR.
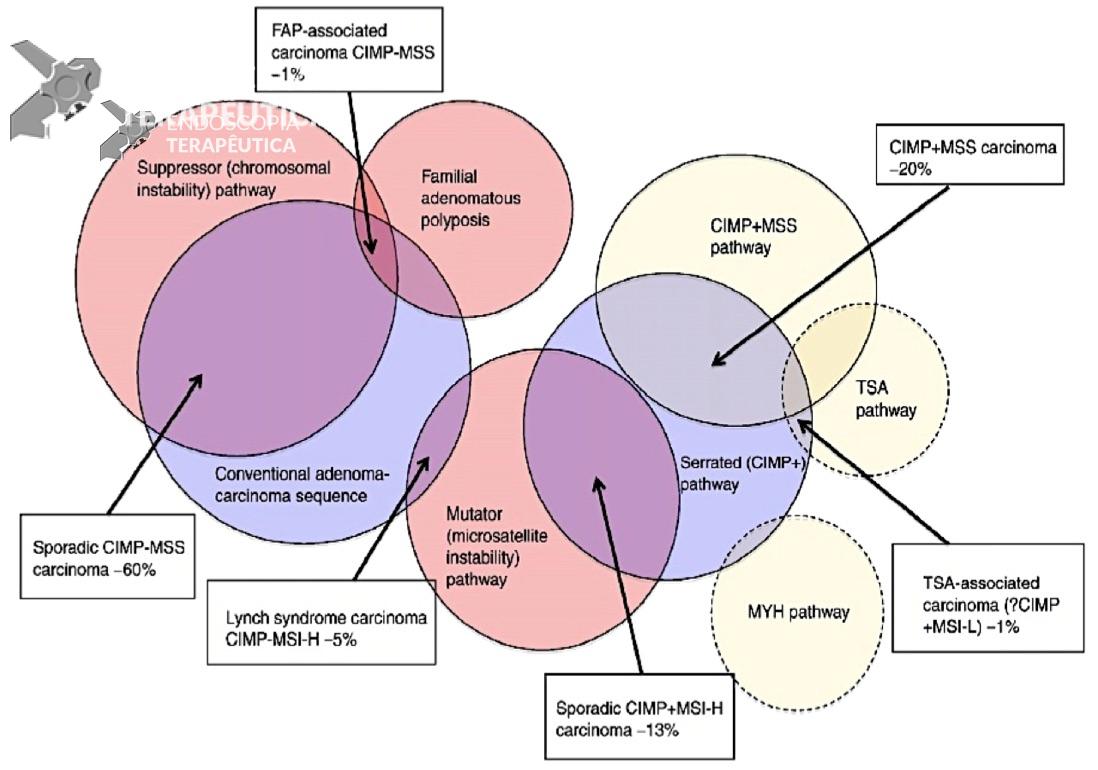
A carcinogênese pode ser entendida como um desequilíbrio entre o desenvolvimento de mutações e os mecanismos de controle do ciclo celular. As vias mais estabelecidas para o câncer colorretal são a via supressora ou instabilidade cromossômica (CIN), a via de instabilidade de microssatélites (MSI) e a via do fenótipo metilador da ilhas CPG (CIMP). A figura 1 demonstra de forma esquemática a sobreposição das vias de carcinogênese colorretal.
Figura 1. Representação esquemática e interação entre as diferentes vias de carcinogênese colorretal.
Referência: Snover DC. Human Pathology 2011;42:1-10.
1. CIN – Via Supressora ou Instabilidade Cromossômica.
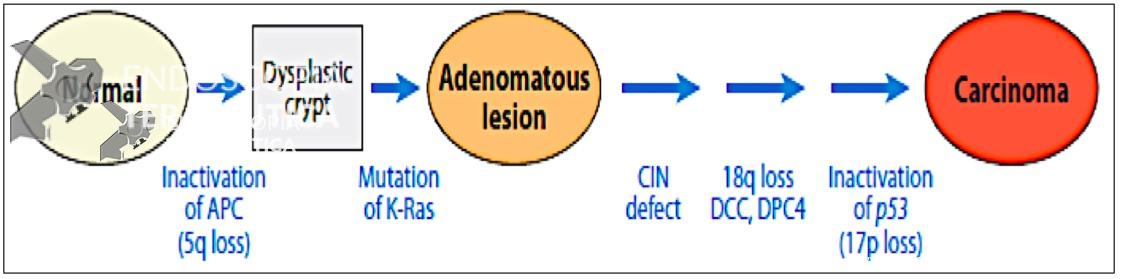
A via denominada supressora contempla a via adenoma-carcinoma descrita em 1990 por Fearon e Vogelstein e se caracteriza por um acumulo gradual de mutações que levam a ativação de oncogenes (KRAS) e inativação de genes supressores de tumor (DCC, APC, SMAD4 e TP53). CIN se refere a alterações das estruturas cromossômicas com ganhos e perdas parciais ou totais que resultam em variabilidade do cariótipo, aneuploidia e perda da heterozigoze (LOH). Trata-se da via mais bem estudada de carcinogênese colorretal e se relaciona à PAF e aos tumores esporádicos, correspondendo a aproximadamente 70% dos casos de CCR. As lesões precursoras da via supressora (CIN) são os adenomas. Os tumores são mais frequentemente encontrados no cólon distal e são sensíveis ao 5-FU, droga chave no tratamento sistêmico, quando indicado antes ou depois do tratamento cirúrgico. A figura 2 ilustra de uma forma simplificada os passos principais do desenvolvimento do carcinoma colorretal de acordo com a via CIN.
Figura 2. Via adenoma carcinoma (CIN).
Referência: Fearon ER. Annu. Rev. Pathol. Mech. Dis 2011; 6:479-507.
2. MSI – Instabilidade de Microssatélites.
A segunda via de carcinogênese colorretal é denominada Instabilidade de Microssatélites ou MSI. Descrita inicialmente em 1993, envolve o acumulo de erros durante a replicação do DNA devido a presença de mutações herdadas ou adquiridas em genes responsáveis pelo seu reparo (MMR). Estes erros se acumulam predominantemente em fragmentos de DNA com padrão de repetições de 1 a 5 nucleotídeos denominados Microssatélites. Os cinco genes que têm particular interesse por sua relação com o câncer hereditário não polipóide (HNPCC/Síndrome de Lynch) e suas respectivas frequências de mutação são: MLH1 (49%), MSH2 (38%), MSH6 (9%), PSM2 (2%) e PMS1 (0,3%). Os tumores colorretais podem ser divididos em MSI alto se dois ou mais genes MMR estiverem mutados, MSI baixo se apenas uma mutação for encontrada ou MSS (estáveis). MSI é encontrado na Síndrome de Lynch (MSI alto) e em aproximadamente 15% dos CCR esporádicos.
Pelo menos dois mecanismos resultam num defeito das proteínas de reparo (MMR). Uma mutação germinativa de um gene MMR (MLH1, MSH2, MSH6 e PMS2) resultando no funcionamento inadequado da proteína de reparo como acontece no HNPCC/Síndrome de Lynch ou um silenciamento do gene MMR por hipermetilação, usualmente MLH1, mais frequentemente observado no câncer esporádico (evento epigenético).
A lesão precursora da via MSI também é o adenoma e velocidade de transformação para o cancer invasivo é mais rápida quando comparada à via CIN e estimada em aproximadamente 5 anos. Os tumores esporádicos relacionados à Instabilidade de Microssatélites são mais frequentemente encontrados em mulheres, localizados no cólon proximal, com padrão mucinoso pouco diferenciado e acentuada infiltração linfocítica. Apesar da resistência ao 5-FU, os tumores MSI altos têm melhor prognóstico, menor probabilidade de metástases à distância e maior sobrevida quando comparados aos tumores MSI estáveis.
3. CIMP – Fenótipo Metilador das Ilhas CPGs.
Historicamente os pólipos do cólon eram classificados em adenomas neoplásicos e pólipos hiperplásicos não neoplásicos. Em 1990, Longacre e Fenoglio-Preiser descreveram o primeiro caso de “serrated adenoma”. Em 1996, Torlakovic e Snover publicaram uma série de casos de polipose hiperplásica sugerindo que os até então benignos pólipos hiperplásicos poderiam se transformar. Outras estudos vieram até que na edição de 2010 a OMS publicou a nova classificação das lesões serrilhadas que foram divididas em pólipos hiperplásicos (PH, 75%), com seus subtipos microvesicular (PHMV), pobre em mucina (PHPM) e células caliciformes (PHCC), pólipo ou adenoma sessil serrilhado (ASS, 15-25%) com ou sem displasia e pólipo ou adenoma serrilhado tradicional (AST, 1%) com ou sem displasia.
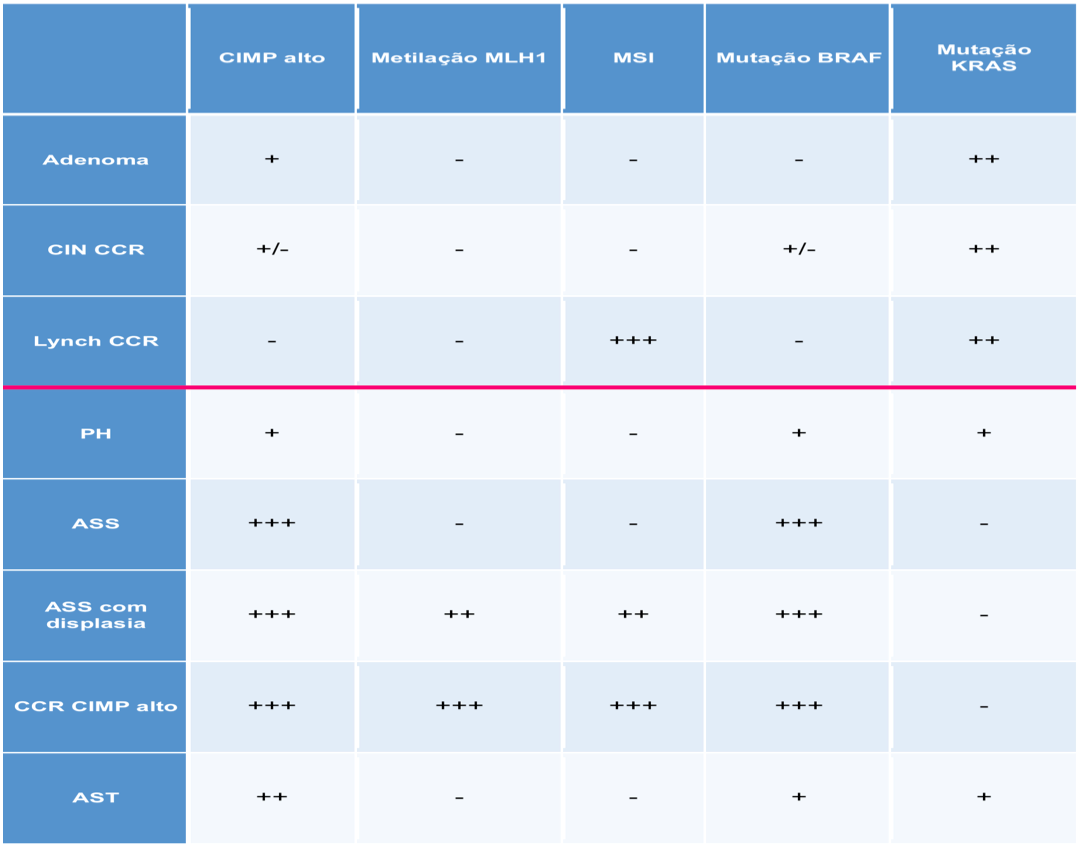
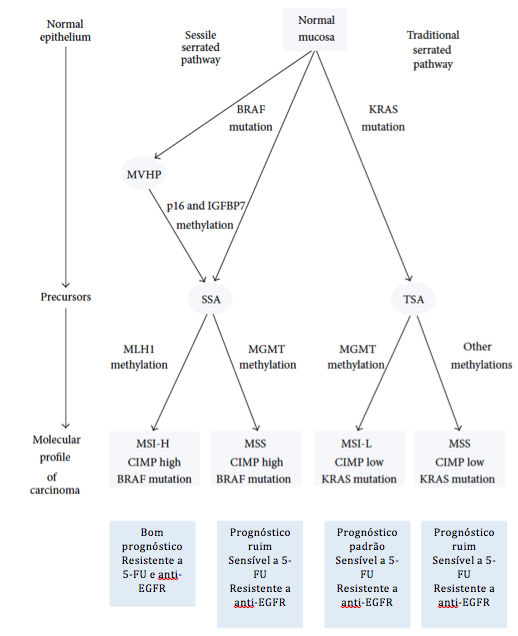
A chamada via alternativa de carcinogênese colorretal ou via serrilhada, responsável por aproximadamente 20 a 30% dos casos de CCR, foi descrita há pouco mais de 15 anos e é caracterizada pela hipermetilação das chamadas ilhas CpG (regiões do genoma ricas em CpG ou Citosina – Phosfato – Guanina) nas regiões promotoras de genes supressores de tumor (CIMP) com consequente silenciamento dos genes envolvidos e mutação do oncogene BRAF. CIMP pode ser expresso em alto, baixo ou ausente. O fenótipo de CIMP alto pode ser encontrado em até 25% dos PH, 65% dos ASS e menos de 1% dos adenomas. Assim, a via serrilhada é também conhecida como via CIMP. O tempo de progressão das lesões serrilhadas para o cancer invasivo é controverso e parece ser de aproximadamente 15 anos, podendo se tornar significativamente mais rápido quando a lesão exibe displasia e fenômenos de metilação. As lesões serrilhadas possuem uma íntima relação com o câncer de intervalo. Os tumores desta via se encontram mais frequentemente no cólon proximal e em geral apresentam um prognóstico ruim com exceção dos MSI altos. As características moleculares dos pólipos e do CCR e as outras variações moleculares da via serrilhada são descritas respectivamente na tabela 1 e na figura 3 abaixo.
Tabela 1. Características moleculares dos pólipos e do câncer colorretal.
Referência: Rex et al. Am J Gastroenterol 2012; 107:1315-1329.
Figura 3: Via de carcinogênese serrilhada.
Referência: Szylberg L et al. Gastroenterol Res Pract 2015; 2015:573814.
Implicações clínicas e considerações finais
- O CCR é uma doença comum e heterogênea envolvendo diversos aspectos moleculares e manifestações clinicopatológicas.
- A colonoscopia associada à polipectomia se relaciona à uma redução significativa da incidência e da mortalidade do CCR. O aperfeiçoamento no diagnostico endoscópico, o melhor tratamento e o adequado seguimento dos pacientes portadores de lesões precursoras do CCR deve ser o objetivo do endoscopista nos programas de rastreamento.
- Recomenda-se a ressecção de todos os adenomas e pólipos serrilhados proximais ao sigmoide além daqueles maiores que 5 mm no cólon distal e no reto.
- Os avanços na biologia molecular e na classificação genética do CCR são essenciais para o tratamento sistêmico mais personalizado e efetivo dos pacientes com doença metastática.
Referências Bibliográficas
- IJspeert JEG, Medema JP, Dekker E. Colorectal Neoplasia Pathways: State of the Art. Gastrointest Endoscopy Clin N AM. 2015; 25: 169-182.
- Kanthan R, Senger JL, Kanthan SC. Molecular Events in Primary and Metastatic Colorectal Carcinoma: A Review. Patholog Res Int. 2012; 2012:597497.
- Snover DC. Update on the serrated pathway to colorectal carcinoma. Human Pathology 2011;42:1-10.
- Bettington M, Walker N, Clouston A, Brown I, Leggett B, Whitehall V. The serrated pathway to colorectal carcinoma: current concepts and challenges. Histopathology 2013; 62: 67-386.
- Rex DK, Ahnen DJ, Baron JA, Batts KP, Burke CA, Burt RW, Goldblum JR, Guillem JG, Kahi CJ, Kalady MF, O’Brien MJ, Odze RD, Ogino S, Parry S, Snover DC, Torlakovic EE, Wise PE, Young J, Church J. Serrated lesions of the colorectum: review and recommendations from an expert panel. Am J Gastroenterol 2012; 107:1315-1329.
- Szylberg L, Janiczek M, Popiel A, Marszalek A. Serrated polyps and Their Alternative Pathway to the Colorectal Cancer: A Systematic Review. Gastroenterol Res Pract 2015; 2015:573814.
- Raskov H, Pommergaard HC, Burcharth J, Rosenberg J. Colorectal carcinogenesis-update and perspectives. World J Gastroenterol. 2014; 48: 18151-18164.
Ressecções endoscópicas
O plano terapêutico, a técnica a ser utilizada, os materiais a serem usados e a forma de realização das ressecções endoscópicas estão diretamente ligados ao tipo de lesão a ser ressecada.
Definições das lesões do trato gastrointestinal
- Pólipos (séssil, subpediculado, pediculado)
- Lesões planas (plano-elevadas, planas, plano-deprimidas)
- Lesão plana maior que 10 mm de circunferência = Lesão de crescimento lateral (LST)
Ver mais em: Classificação de Yamada e Classificação Japonesa das lesões do trato gastrointestinal
O primeiro aspecto a ser avaliado antes de uma ressecção é o tamanho da lesão, sendo que quando menores que 5 mm podem ser ressecadas com pinça de biópsia. Lesões de até 7 mm, em casos selecionados, podem ser ressecadas com alça sem corrente de coagulação (“a frio”). Clique aqui para ver mais sobre o assunto
Lesões maiores que 7 mm geralmente são tratadas com corrente de coagualação e conforme a característica de cada lesão:
Pólipos pediculados
Do ponto de vista terapêutico, os pólipos pediculados são tratados com ressecção com alça diatérmica. Geralmente usa-se corrente mais de coagulação do que de corte, solicitando que o auxiliar feche a alça com calma e algumas vezes deixando esta fechada por um bom tempo para estrangular o pedículo e assim prevenir sangramento pós-polipectomia.
Quanto maior e mais grosso o pedículo maior a chance de sangramento e por isto algumas medidas podem ser realizadas, como a utilização somente de corrente de coagulação, colocação de endoloop previamente, clipagem com endoclipe antes ou depois da polipectomia e até mesmo a injeção de solução de adrenalina no pedículo. Todas estas técnicas tem suas vantagens e desvantagens sendo a decisão tomada conforme cada situação.
A colocação de endoloop às vezes é inviável em pólipo muito grande principalmente pelo fato do laço ser muito maleável o que dificulta a laçada. Nestes casos pode-se optar por clipar o pedículo, antes ou após a polipectomia. Se for optado pela clipagem prévia deve-se ter cuidado para que alça não entre em contato com o clipe e assim transmita corrente podendo causar danos ao tecido normal. Se a opção for a clipagem após ressecção, o clipe já deve estar montado e rapidamente acessível pra uso caso ocorra um sangramento imediatamente após a ressecção. Uma opção para evitar, ou ao menos diminuir, o sagramento pós-polipectomia é a injeção solução de adrenalina no pedículo, e após a ressecção pode-se ou não realizar a colocação do clipe. Alguns autores argumentam que o efeito da adrenalina na contenção do sangramento é efêmero, podendo resultar em sangramento tardio e contra-indicam o seu uso isolado como método de prevenção de sangramento.
Pólipos subpediculados
Nos pólipos subpediculados a base da lesão deve ser avaliada. Se o componente que forma o “subpediculo” tiver a mesma característica que a lesão, sugere-se a realização de injeção submucosa antes da ressecção. Isto garante que todo o componente adenomatoso ou anormal seja ressecado. Se a base da lesão tiver a mesma caracterísca do cólon normal a polipectomia simples sem injeção na submucosa pode ser realizada.
Lesões planas
As lesões planas devem ser ressecadas sempre após a injeção submucosa de alguma solução (mucosectomia), para afastar a lesão da muscular própria do órgão e assim evitar uma perfuração. Como nas lesões planas o risco de perfuração é maior do que o de sangramento, geralmente usa-se mais corrente de corte do que de coagulação. Deve-se sempre que possível tentar a ressecção da peça em monobloco. Lesões até 2 cm podem ser ressecadas em fragmentos (piecemeal). Segundo a classificação de Gotoda, lesões planas maiores que 2 cm não devem ser ressecadas com alça, sendo estes casos reservados para dissecção endoscópica da submucosa (ESD).
Para a realização de ressecções com sucesso, além do conhecimento teórico e habilidade técnica deve-se possuir e conhecer os instrumentos de trabalho.
Eletrocautério
- Dispositivo que usa alta frequência (300-1000Hz) para não estimular os tecidos neuromusculares do organismo.
- Voltagem é a força de “empurrar” a corrente. Corrente pode ser contínua ou oscilar.
- Potência (watts) é o trabalho realizado pela corrente elétrica em um determinado intervalo de tempo. Fixada pelo operador e constante no cautérios tradicionais.
- Corte puro: alta temperatura em curto espaço de tempo, com corrente contínua, o que leva a explosão celular e “efeito corte”.
- Coagulação: a corrente oscila, com tempo para o tecido não esquentar tão rapidamente, assim desidrata as células, produz dano tecidual mais profundo e “efeito coagulação”.
A passagem da corrente depende:
- Área de tecido a ser seccionada (maior área = maior voltagem ou maior tempo necessário)
- Impedância do tecido (maior impedância = maior voltagem ou maior tempo necessário)
Eletrocautérios que oscilam sua potência conforme a impedância do tecido são conhecidos como tendo a função endocut:
- Ajuste é feito da potência máxima do ciclo que oscila, por isto recomenda-se usar o dobro da potência usada nos eletrocautérios de potência fixa
- Deve-se manter o pedal pisado constantemente durante todo o procedimento para que o aparelho consiga ir ajustando a potência ideal
Ver mais em: Corte ou Coagulação? Que corrente utilizar?
Alças de polipectomia
- Multifilamentar: alça padrão, com tamanho e formatos diferentes para cada caso específico.
- Monofilamentar: alça de um único filamento rígido que por isto tem mais força pra pressionar a mucosa e realizar ressecções mais profundas. Possui também um corte muito rápido, tipo “navalha”, dessa forma o auxiliar deve fechá-la mais lentamente. Usa-se geralmente apenas corrente de coaugulação tendo em vista que o efeito de corte da-se pela própria alça.
Técnicas de ressecção profunda
Usadas em casos específicos onde é necessária a ressecção da mucosa e da submucosa, geralmente em lesões que se originam da mucosa profunda, que são denominadas subepiteliais, porém não submucosas (ex: tumores neuroendócrinos, tumor de células granulares).
As três principais técnicas de ressecção endoscópica profunda são:
- Ressecção com alça monofilamentar
- Ligadura elástica da lesão seguida de resseção com alça
- Dissecção endoscópica da submucosa (ESD). Clique aqui para ver mais sobre o assunto
Ressecção underwater
- Estudos com ecoendoscopia comprovam que após preencher o órgão com água ocorre um afastamento da mucosa em relação a muscular própria. Assim através deste método algumas lesões podem ser ressecadas com segurança sem a necessidade de injeção submucosa.
ASSISTA ALGUNS VÍDEOS DE RESSECÇÕES ENDOSCÓPICAS
Polipectomia com profilaxia primária com endoloop
[ddownload id=”4964″]
Mucosectomia
[ddownload id=”4963″]
Ressecção em piecemeal e profilaxia secundária com endoclipe
[ddownload id=”5577″]
Ressecção underwater
[ddownload id=”4954″]
Ressecção profunda com alça monofilamentar
[ddownload id=”4960″]
Ressecção profunda com ligadura
[ddownload id=”4957″]
Ressecção profunda com alça monofilamentar underwater
[ddownload id=”4971″]
Qual o melhor forma de ressecção para os pólipos subcentimétricos do cólon e reto?
A polipectomia é o procedimento terapêutico endoscópico mais comum e todos os colonoscopistas devem estar aptos à realizar este procedimento de forma segura e efetiva. A prática evoluiu consideravelmente nos últimos anos e atualmente dispomos de várias técnicas e equipamentos para diferentes cenários clínicos.
O endoscopista deve considerar o tamanho, características morfológicas e localização do pólipo no cólon antes de escolher a técnica apropriada. Para pólipos pequenos existem várias técnicas que podem ser utilizadas, mas são poucos os estudos disponíveis para nos guiarem entre qual a mais indicada para cada caso.
Os pólipos devem ser divididos entre sésseis ou pediculados, e também de acordo com o tamanho da lesão (até 3 mm, 3-7 mm e 7-9 mm). Em relação à localização, a maioria dos estudos considera cólon direito do ceco ao ângulo esplênico, e esquerdo os segmentos distais à esta região.
PÓLIPOS PEDICULADOS
- Melhor tratamento sugerido pela maioria dos estudos e guias é a polipectomia com alça diatérmica, não importando se é no cólon direito ou esquerdo.
- Pólipos com pedículos maiores do que 1 cm sugere-se o uso de clipe ou endoloop para prevenção do sangramento.
PÓLIPOS SÉSSEIS
O tratamento varia de acordo com o tamanho e localização.
Existe um certo consenso no tratamento das seguintes lesões:
- Pólipos sésseis até 3 mm podem ser tratados por pinça de biópsia fria.
- Lesões sésseis com 1 cm ou mais, em qualquer lugar do cólon, devem ser sempre tratadas por mucosectomia.
- Lesões planas ou deprimidas maiores do que 3-4 mm (que não podem ser ressecadas adequadamente por pinça fria/hot/jumbo) são tratadas por mucosectomia.
Lesões de tamanho intermediário
Para as lesões de 3-7 mm e 7-9 mm as condutas variam bastante.
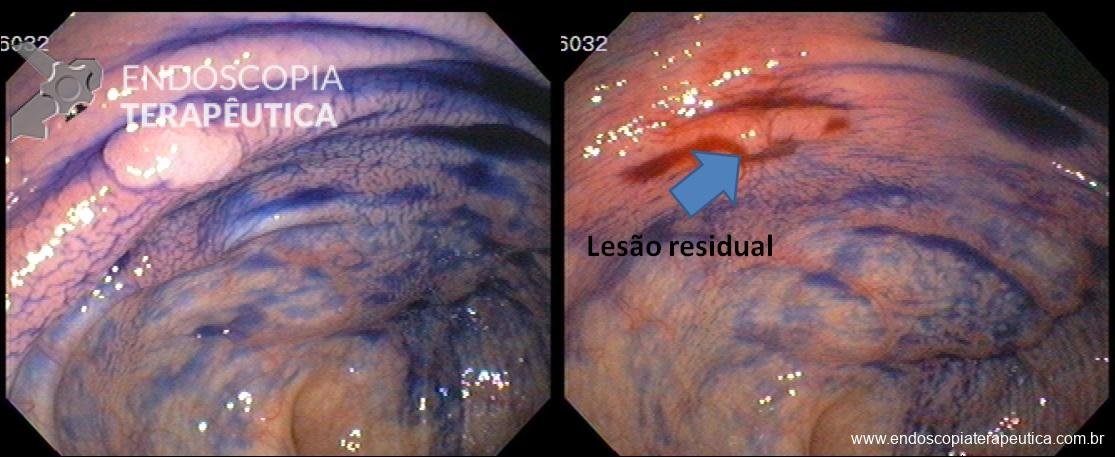
- Lesões de 3-7 mm: Boa parte dos estudos considera segura a ressecção das lesões de 3-7 mm com alça fria. Não se recomenda ressecção com pinça de biópsia devido à alta frequência de ressecção incompleta. Hot biopsy pode ser usada no cólon esquerdo mas é contra indicada no cólon direito devido ao risco de perfuração (cada vez menos usada). Alça diatérmica pode ser usada com relativa segurança no cólon esquerdo mas tem um risco de perfuração maior quando utilizada no cólon direito. A mucosectomia se mostra segura, efetiva, com baixo risco de perfuração e maiores taxas de ressecções completas destas lesões. Estudos demonstram que a aplicação da mucosectomia nas ressecções de lesões maiores do que 5 mm no cólon direito tem aumentado e é sugerida como a melhor opção por alguns autores.
(Clique para aumentar) Lesão plana de 6 mm no ceco. Tentativa de ressecção com pinça de biópsia fria. Após a primeira mordida foi observada lesão residual com necessidade de ressecção adicional. Este tipo de tratamento deve ser evitado pois quanto maior o número de fragmentos em que a lesão for ressecada, maior a incidência de recidiva.
- Lesões de 7-9 mm: Não se deve usar pinça de biópsia fria. Hot biopsy é contra indicada no cólon direito e tem grande taxa de ressecção incompleta em lesões maiores do que 5 mm. A alça fria é uma opção possível, porém, as técnicas mais utilizadas e sugeridas nos artigos para este tipo de lesão são a ressecção com alça diatérmica e a mucosectomia. O uso de terapia térmica (alça) sem injeção submucosa no cólon direito tem uma maior incidência de perfuração e síndrome pós polipectomia, levando à uma tendência em se indicar mucosectomia para estas lesões quando localizadas nesta região. No cólon esquerdo a ressecção com alça diatérmica é mais segura do que no cólon direito mas a mucosectomia também é uma opção que deve ser considerada. Em um estudo multicêntrico prospectivo (6) realizado em 11 instituições japonesas incluindo 624 pacientes, foi avaliado a aplicação da mucosectomia em lesões menores do que 2 cm. O tamanho médio das lesões era de 8,3 mm + 3,2 (5-20 mm). A ressecção em bloco foi obtida em 93,3% dos pacientes com 78,3% de ressecções completas. A taxa de perfuração foi 0 (zero) e a taxa de sangramento 1,1%. Este estudo demonstra que a mucosectomia é uma técnica simples, rápida, segura e com altas taxas de ressecção completa de lesões menores do que 1 cm.
Como medir as lesões?
Outra dificuldade na decisão terapêutica dos pólipos subcentimétricos é como estimar o tamanho da lesão. Infelizmente não exite um método 100% preciso. O tamanho é estimado, na maioria das vezes, comparando-se a lesão com algum dos instrumentos endoscópicos, geralmente uma pinça. Para isso o endoscopista deve conhecer o material que utiliza. A concha da pinça de colonoscopia padrão mede em torno de 5 mm de comprimento e quando aberta tem aproximadamente 8 mm.
(Clique para aumentar). A) Comparação da pinça aberta (visão endoscópica) com área arredondada de 5 mm. B) Medida da pinça aberta (aproximadamente 8 mm).
(Clique para aumentar). A) Pólipo pequeno no cólon descendente. B) Comparação do pólipo com uma das conchas da pinça de colonoscopia que mede 5 mm de comprimento.
Referências
- Riley SA. Colonoscopic polypectomy and endoscopic mucosal resection: A pratical Guide. Britihs Society of Gastroenterology. 2008. Disponível no endereço: http://www.bsg.org.uk/pdf_word_docs/polypectomy_08.pdf
- Saunders B. “HOW I DO IT” Removing large or sessile colonic polyps. World Endoscopy Organization. Disponível no endereço: http://www.worldendo.org/assets/downloads/pdf/publications/how_i_doit/2007/omed_hid_removing_large_or_sessile_colonic_polyps.pdf
- Lee TJ, Rutter MD, Blanks RG, Moss SM, Goddard AF, Chilton A, Nickerson C, McNally RJ, Patnick J, Rees CJ.Colonoscopy quality measures: experience from the NHS Bowel Cancer Screening Programme. Gut 2012;61:1050e1057. doi:10.1136/gutjnl-2011-300651
- Ross WA, Thirumurthi S, Lynch PM, Rashid A, Pande M, Shafi MA,
Lee JH, Raju GS. Detection rates of premalignant polyps during screening colonoscopy: time to
revise quality standards? GASTROINTESTINAL ENDOSCOPY Volume 81, No. 3 : 2015 - Lee TJ, Blanks RG, Rees CJ, Wright KC, Nickerson C, Moss SM, Chilton A, Goddard AF, Patnick J, McNally RJ, Rutter MD. Longer mean colonoscopy withdrawal time is associated with increased adenoma detection: evidence from the Bowel Cancer Screening Programme in England. Endoscopy 2013; 45: 20–26
- Yoshida N(1), Naito Y, Inada Y, Kugai M, Yagi N, Inoue K, Okuda T, Hasegawa D, Kanemasa K, Kyoichi K, Matsuyama K, Ando T, Takemura T, Shimizu S, Wakabayashi N, Yanagisawa A, Yoshikawa T. Multicenter study of endoscopic mucosal resection using 0.13% hyaluronic acid solution of colorectal polyps less than 20 mm in size. Int J Colorectal Dis (2013) 28:985–991.
Confira também: Lesões sésseis serrilhadas | vídeo sobre: Ressecção de pólipo pediculado gástrico com auxílio de endoloop
Doença linfoproliferativa pós-transplante
CASO CLÍNICO
Feminina, 4 anos, há 1 semana com diarréia aquosa volumosa, com náuseas e febre (37,9°C), evolui há 3 dias com enterorragia. Tem antecedente de transplante renal (intervivos) há 6 meses, e faz uso de medicações imussupressoras: prednisona, everolimus e tacrolimus. Ao exame apresenta-se descorada e com sinais de desidratação. Abdômen globoso, flácido, RHA+.
Solicitada colonoscopia que evidenciou múltiplas úlceras ativas, profundas, recobertas por fibrina, com bordas bem delimitadas e elevadas, medindo de 10 a 30 mm, distribuídas por todo o cólon (ver imagens abaixo):
Resultado das biópsias (estudo anatomopatológico + imuno-histoquímica):
Úlceras com infiltrado linfoide atípico associadas ao Epstein-Barr vírus, ver nota:
- Presença de moderado infiltrado linfoide, com alguns linfócitos maiores de padrão imunoblástico de permeio.
- Identificada positividade para o antígeno do vírus Epstein-Barr em algumas destas células linfoides pelo estudo imuno-histoquímico.
Conclusão: Deve ser considerada como hipótese diagnóstica uma doença linfoproliferativa pós-transplante (DLPT), forma precoce do tipo polimórfica.
PET-CT demonstrou:
Aumento focal do metabolismo em linfonodomegalias retroperitoneais, cervicais, axilares e inguinal à direita. Focos de captação também são observados no baço e fígado. O conjunto dos aspectos pode estar associado a suspeita clínica de doença linfoproliferativa pós-transplante.
Neste caso foi iniciado tratamento com Rituximab.
REVISÃO
A doença linfoproliferativa pós-transplante (DLPT) é uma complicação da imunossupressão após o transplante de órgão. A incidência da DLPT varia de 2% a 20%, porém sabe-se que ela é maior em crianças. A maior freqüência da DLPT na população pediátrica ocorre pois grande parte destes não haviam sido expostos ao Epstein-Barr vírus (EBV) antes do transplante, sendo, portanto, a soroconversão pós-transplante um fator de risco significativo para o desenvolvimento da doença.
Acredita-se que o EBV desempenhe um papel central na patogênese da DLPT, sendo reportado que cerca de 80% dos casos estão associados a esse vírus.
As manifestações clínicas da DLPT ocorrem mais frequentemente no primeiro ano após o transplante, e podem afetar virtualmente qualquer órgão do corpo, focal ou difusamente. O trato gastrointestinal é acometido em até 20% dos casos. Sendo que o intestino delgado distal é o mais comumente afetado.
Endoscopicamente pode-se observar desde mucosa com leves alterações, como edema, enantema difuso ou focal, erosões, e até formação de úlceras (como no caso apresentado). Por se tratar de uma condição que pode ser agressiva e fatal, a endoscopia precoce com biópsias, mesmo em casos com sintomas/achados leves e inespecíficos, é aconselhável.
As modalidades de tratamento da DLPT são variadas, incluindo redução da terapia de imunossupressão, controle da replicação do EBV, terapia antineoplásica convencional (radioterapia, quimioterapia e cirurgia) e imunoterapia (anticorpos anti-células-B: rituximab).
Referências:
- Badham K, Mirchandani A, Arumainayagam N, West DR. Epstein-Barr virus associated with a post–transplant lymphoproliferative disorder presenting as isolatedgastrointestinal tract bleeding. Endoscopy. 2007;39(Suppl 1):E64-5.
- Fernandes PM, Azeka E, Odoni V, Junqueira JJ, Bento GP, Aiello V, Barbero-Marcial M. Post-transplantation lymphoproliferative disorder in pediatric patient. Arq Bras Cardiol. 2006;87(4):e108-11.
- Bitencourt AGV, Pinto PNV, Almeida MFA, Cerqueira WS, Assis AM, Rodrigues AMST, Chojniak R. Incidence and imaging findings of lymphoma after liver transplantation in children. Radiol Bras. 2012;45(1):7–11.
Dieta pobre em resíduos vs dieta líquida antes da colonoscopia: uma metanálise de trabalhos randomizados e controlados
Realizar revisão sistemática e metanálise de estudos comparativos onde dois grupos de pacientes foram submetidos a colonoscopia e consumiram uma dieta líquida (DL) versus dieta pobre em resíduos (DPR), na véspera do exame.
Métodos: Pesquisa nos bancos de dados: Scopus, PubMed / MEDLINE, Cochrane, e CINAHL.
A análise foi realizada usando os modelos DerSimonian e Laird Mantel-Haenszel, ou com o odds ratio (OR). Sendo os desfechos: qualidade do preparo, tolerabilidade, vontade de repetir a dieta e efeitos adversos.
Resultados: Nove estudos (1686 pacientes) foram incluídos.
O grupo de pacientes que consomem uma DPR comparado ao grupo da DL apresentou taxas significativamente maiores de tolerabilidade (OR 1,92; IC 95%, 1,36-2,70; P <0,01) e vontade de repetir o preparo (OR 1,86; IC 95%, 1,34-2,59; P < 0,01), sem diferenças em relação a qualidade do preparo (OR 1,21; 95% CI, 0.64-2.28; PZ 0,58) ou efeitos adversos (OR 0,88; IC 95%, 0,58-1,35; PZ 0,57).
Conclusão: Uma DPR antes da colonoscopia resultou em melhor tolerabilidade pelos pacientes e uma maior vontade de repetir o preparo. Não houve diferenças quanto aos efeitos adversos ou qualidade do preparo. Esse resultado sugere que a dieta líquida deva ser substituída pela dieta pobre em resíduos.
Comentário:
O resultado desse estudo é no mínimo questionável devido ao grande número de vieses, sendo um dos principais a ausência de dados sobre o nível de instrução e compreensão dos pacientes. Esse tipo de viés tende a ser maior em países em desenvolvimento. Nessa metanálise, 200 pacientes do Líbano estão incluídos. Não que esse seja um fator determinante para dizer que o resultado desse estudo está completamente equivocado, mas não há dúvidas que isso deva ser levado em consideração. Explico o porquê. Notem; no Brasil todos sabemos que há diferenças brutais entre os sistemas público e privado, não só em relação a qualidade do atendimento e a infraestrutura, mas também em relação ao grau de instrução e compreensão dos pacientes, portanto esse fato não pode ser menosprezado, e obviamente isso influencia no resultado final do presente trabalho. Sabemos que a orientação dos pacientes para a realização do preparo da colonoscopia (dieta e as medidas a serem adotadas na véspera) é fundamental para que a preparação intestinal tenha sucesso. Não é raro em nossa prática clínica, observarmos algumas situações que contradizem o resultado desse estudo. Diversas vezes quando adotamos uma dieta líquida restrita conseguimos um preparo de melhor qualidade em comparação com a dieta pobre em resíduos; isso se torna mais evidente quando os pacientes apresentam níveis socioculturais mais baixos.
Apesar dessa metanálise ser composta por trabalhos randomizados, há outros vieses que também contribuem para diminuir a relevância do seu resultado, são eles:
- A metanálise é composta de estudos de baixa qualidade: dos 9 estudos selecionados, 5 apresentam pontuação 3 na escala de Jaddad (moderada qualidade) e 4 apresentam pontuação 2 (baixa qualidade).
- A substituição das dietas pobres em resíduos variou: alguns permitiram essa dieta somente pela manhã, outros em duas refeições, e alguns substituíram as três refeições.
- Foram adotados diferentes tipos de soluções para o preparo.
- Alguns estudos usaram dietas pré-fabricadas e outros dietas baseadas em protocolos próprios.
- As escalas de avaliação do preparo não foram as mesmas.
- Os estudos incluídos nessa metanálise foram baseados em “abstracts”.
E como discutido anteriormente, algumas questões essenciais que precisavam ser respondidas:
- Como foi feita a orientação do preparo (email, telefone, internet, pessoalmente)?
- O nível de escolaridade dos pacientes?
- Foram preparos domiciliares ou hospitalares?
Em resumo, o resultado do presente estudo deve ser visto com parcimônia. Estudos com menos vieses são necessários para se chegar à uma conclusão mais precisa sobre esse tema.
Como aumentar sua taxa de detecção de adenomas?
A Taxa de Detecção de Adenoma (TDA) atualmente é o principal indicador de qualidade de colonoscopia. Dentre os vários indicadores propostos, este é o único que comprovadamente se correlaciona com a incidência de câncer de intervalo. Quanto maior a TDA de um colonoscopista (ou de um serviço de colonoscopia), menor a chance do paciente apresentar um câncer de intervalo.
Na população assintomática acima de 50 anos submetida a screening, a TDA deve ser
- ≥ 30% nos homens
- ≥ 20% nas mulheres
Portanto, medidas que possam melhorar nossa TDA são bem-vindas e benéficas para os pacientes. Nesse artigo vamos discorrer sobre as principais medidas estudadas, variando desde medidas simples e sem custos, até modernas tecnologias desenvolvidas para este fim.
Qualidade do preparo: este é um indicador de qualidade ressaltado por quase todas as sociedades internacionais. A qualidade do preparo está diretamente relacionada com o tempo de chegada ao ceco e com a detecção de pólipos. É importante cada serviço estar habituado com a solução de preparo de cólon padrão, bem como saber individualizar o preparo de cólon para situares especiais.
Mudança de posição: visam melhorar a distensão dos segmentos do cólon, melhorando sua inspeção. O cólon direito pode ser melhor inspecionado no DLE, o transverso em DDH e o cólon esquerdo em DLD. Em dezembro de 2015 tivemos um artigo comentado estudando essa técnica que demonstrou aumento na detecção de pólipos apenas no cólon direito. Dois outros estudos também foram favoráveis à mudança de decúbito. No entanto, devido ao desenho destes estudos (examinava uma vez numa posição, depois examinava uma segunda vez em outra posição), o aumento da TDA pode ser explicados pelo simples second-look, ou seja, não seria necessário mudar o decúbito, apenas examinar pela segunda vez.1 De fato, um RCT publicado em 2014 em que a mudança de decúbito programada e proposital foi comparada com mudança apenas quando encontrava-se uma dificuldade, falhou em demonstrar aumento na TDA.2
Segundo observador: a participação da enfermagem como um segundo observador durante a retirada do aparelho mostrou aumento na detecção de pólipos e adenomas em ao menos dois estudos. Uma medida simples e sem custo.3
Horário do exame: a fadiga do endoscopista vai aumentando ao longo do dia e pode afetar a TDA. Sanaka et al foram os primeiros a mostrar que a TDA foi significativamente maior nas colonoscopias agendadas pela manhã do que nas agendadas a tarde. Vários outros estudos também chegaram a mesma conclusão. Gurudu et al4 mostraram que quando os exames eram divididos em blocos de meio-dia, não havia diferença entre a TDA dos exames realizados pela manhã ou à tarde.
Water-imersion/ Water-exchange: a colono sob imersão foi idealizada para facilitar a chegada ao ceco. A colono com troca de água almeja a aspiração de todo o resíduo líquido do cólon e instilação de grandes volumes de água que é mantida durante a retirada do aparelho. Seus defensores relatam melhor visualização dos pólipos devido um efeito de lente de aumento da água e visto que os pólipos tendem a boiar na água em vez de permanecerem achatados. Um estudo demonstrou aumento na TDA (25% vs 19%) e outro demonstrou tendência a maior detecção, porém sem poder estatístico (56.7% vs 43.3%).5,6
Visualização do cólon direito: a maioria dos adenomas não detectados (missed adenomas) ocorrem no cólon direito. Vários fatores contribuem para esse fato, como o preparo de cólon que tende a ser um pouco pior no cólon direito, a maior taxa de adenomas sésseis serrilhados, que por sua natureza plana são mais difíceis de detectar, as haustrações pronunciadas, etc. Portanto, vários autores advogam a necessidade de se examinar com maiores detalhes o cólon direito, utilizando-se manobras como retroflexão, direita e esquerda, mudança de decúbito, etc. Hewett e Rex 7 mostraram uma taxa adicional de 10% de adenomas detectados com a manobra de retrovisão, mas esta taxa também pode ser obtida com uma segunda inspeção com visão frontal. A retrovisão, portanto, não é imperativa.
Tempo de retirada do aparelho: esse é um assunto polêmico e que talvez mereça outro post. Embora vários estudos tenham demonstrado uma correlação entre tempo de retirada e detecção de pólipos, os achados não são unânimes. Um estudo da Universidade John Hopkins 8, por exemplo, falhou em demonstrar aumento da TDA com a política de obrigar os endoscopistas a gastarem 7 min ou mais para retirar o aparelho. Outro estudo ressaltou a importância da qualidade técnica do exame em detrimento ao tempo de retirada 9. Controvérsias a parte, fazer o exame com calma, “gastando” o tempo necessário, é importante, e o guideline da ASGE 2015 recomenda no mínimo 6 minutos dedicados à retirada do aparelho. 10
Antiespasmódicos: hioscina, escopolamina e outros agentes antiespasmódicos já foram testados em ensaios randomizados, mas os resultados não foram satisfatórios. Apesar de um RCT demonstrar uma tendência a maior detecção de pólipos com uso de hioscina (sem significância estatística), uma meta-análise destes estudos mostrou que não há benefício. Recentemente, Inoue e col demonstraram aumento da TDA com uso de L-mentol, também um agente antiespasmódico (60.2% vs 42.6%). Este achado ainda precisa ser confirmado com futuros estudos. 11-13
Cromoendoscopia: vários estudos avaliaram o impacto da cromoendoscopia com índigo-carmin na TDA. Os resultados não são unânimes. Um estudo prospectivo randomizado mostrou aumento da TDA com índigo (46% vs 36%). Uma metanálise que compilou 42 estudos comparando diferentes métodos (autofluorescência, FICE, NBI, i-Scan, cap e cromoendoscopia) mostrou que apenas a cromoendoscopia esteve relacionada com maior TDA. Por outro lado, um estudo prospectivo não evidenciou diferença. Neste estudo, os pacientes realizavam um primeiro exame sem cromoscopia e um segundo exame era realizado imediatamente após. Os pacientes foram então randomizados: 60 com índigo vs 70 convencional (luz branca). Adenomas adicionais foram detectados em 27 vs 33%, respectivamente. O segundo exame era limitado aos segmentos distais à flexura esplênica, o que pode ter limitado o impacto da cromoendoscopia na detecção de lesões planas serrilhadas do cólon direito.
Uso de cap (cap-assisted colonoscopy): o uso de um cap transparente na extremidade do aparelho é advogado por alguns autores pois facilita a inspeção atrás das haustrações. No entanto, em uma meta-análise incluindo 8991 pacientes, o uso de cap teve um impacto muito pequeno na TDA (RR 1.08 – IC 1.00-1.17). O tempo de inserção foi significativamente menor com o uso de cap, tanto para experts quanto para os trainees. 14
Aparelhos de alta resolução: esse é um tema ainda polêmico. Não há dúvidas que os aparelhos de alta resolução (HD-WL) ofereçam melhor qualidade de imagem do que os aparelhos convencionais (SD-WL), mas as evidências em relação a TDA não são tão contundentes quanto se esperava. Um RCT mostrou que os aparelho HD-WL aumentaram o número total de adenomas detectados e aumentaram a detecção de lesões planas no cólon direito. No entanto, não houve diferença estatística na quantidade de paciente com ao menos 1 adenoma (38.6% vs 45.7%, P = 0.17). Em uma meta-análise de 5 estudos (2 RCTs e 3 não-RCTs) o uso da alta resolução aumentou em apenas 3,5% a TDA (NNT de 28) e não houve impacto na taxa de detecção de adenomas de alto risco (maiores que 10 mm, componente viloso ou displasia de alto grau). Os autores alertam para a interpretação cuidados desses dados devido a heterogeneidade dos estudos (estudos não RCTs e TDA variando de 23-65%). 15 Atualmente, a ESGE recomenda o uso de aparelhos de alta resolução no screening da população de médio risco.
Cromoscopia óptica ou virtual: o uso de tecnologias como FICE, NBI e i-Scan foi testado por diversos estudos, sendo que a maioria não mostrou benefício na detecção de adenomas. Existem inclusive duas meta-análises mostrando que seu uso não melhor a TDA. Estes estudos compararam estas tecnologias com a luz branca de alta definição. 16, 17
NOVAS TECNOLOGIAS
Third-eye Retroscope: consiste em um fino cateter que é passado pelo canal do colonoscópio convencional e faz retrovisão de 180, permitindo melhor visualização atrás das pregas. Um estudo randomizado multicêntrico mostrou aumento de 29.8% na detecção de pólipos e 23.2% na detecção de adenomas, comparado com a colonoscopia convencional 18. No entanto, o cateter ocupa o canal de trabalho e necessita ser retirado para fazer biópsia ou polipectomia, além de ser descartável, agregando um custo considerável ao exame. Sua produção foi descontinuada e a segunda geração deste aparelho vem sendo testada: Third-eye panoramic device, que consiste em um cateter acoplado externamente ao aparelho, provido de uma luz de LED e uma microcâmera de cada lado do cateter, fornecendo visão de 330°, e com proposta de ser reutilizável.
Full Spectrum Endoscopy (FUSE): os colonoscópios convencionais permitem uma visão de 140-170°. O FUSE possui câmeras laterais na extremidade do aparelho, permitindo uma visão de 330°. No entanto, esta visão não é contínua, mas separada em 3 telas, exigindo um novo treinamento visual do endoscopista. Em um estudo com 185 pacientes, a taxa de adenomas que passaram despercebidos com o FUSE foi de 7% contra 41% com o uso dos aparelhos convencionais 19. O que chama a atenção neste estudo é a alta taxa de adenomas perdidos no grupo convencional (41%!). Não há dúvidas que novos estudos são necessários para comprovar o benefício desta tecnologia.
Endocuff: consiste em uma especie de borracha acoplada à extremidade do aparelho, com asas flexíveis que ajudam a esticar a mucosa, reduzindo as haustrações. O endocuff foi aprovado pelo FDA em 2012. Em um estudo com 498 pacientes, a taxa de detecção pólipos e de adenoma foi significativamente maior com o uso do Endocuff vs sem Endocuff: 56% vs 42% e 36% vs 28%, respectivamente. 20
G-Eye: consiste em um balão inflável alguns centímetros antes da extremidade do aparelho. Durante a fase de retirada do aparelho o balão é inflado com o acionamento de um pedal. Sua pressão é controlada pelo sistema, permitindo que o balão se acople ao diâmetro da luz do cólon. Conforme o aparelho vai sendo retirado, o balão estica as haustrações, permitindo uma excelente visualização de toda a mucosa. RCT multicêntrico demonstrou TDA de 59% vs 39% com aparelho convencional 21. Tive a oportunidade de assistir o uso deste aparelho e sem dúvida aparenta ser uma tecnologia promissora.

Colonoscópio FUSE
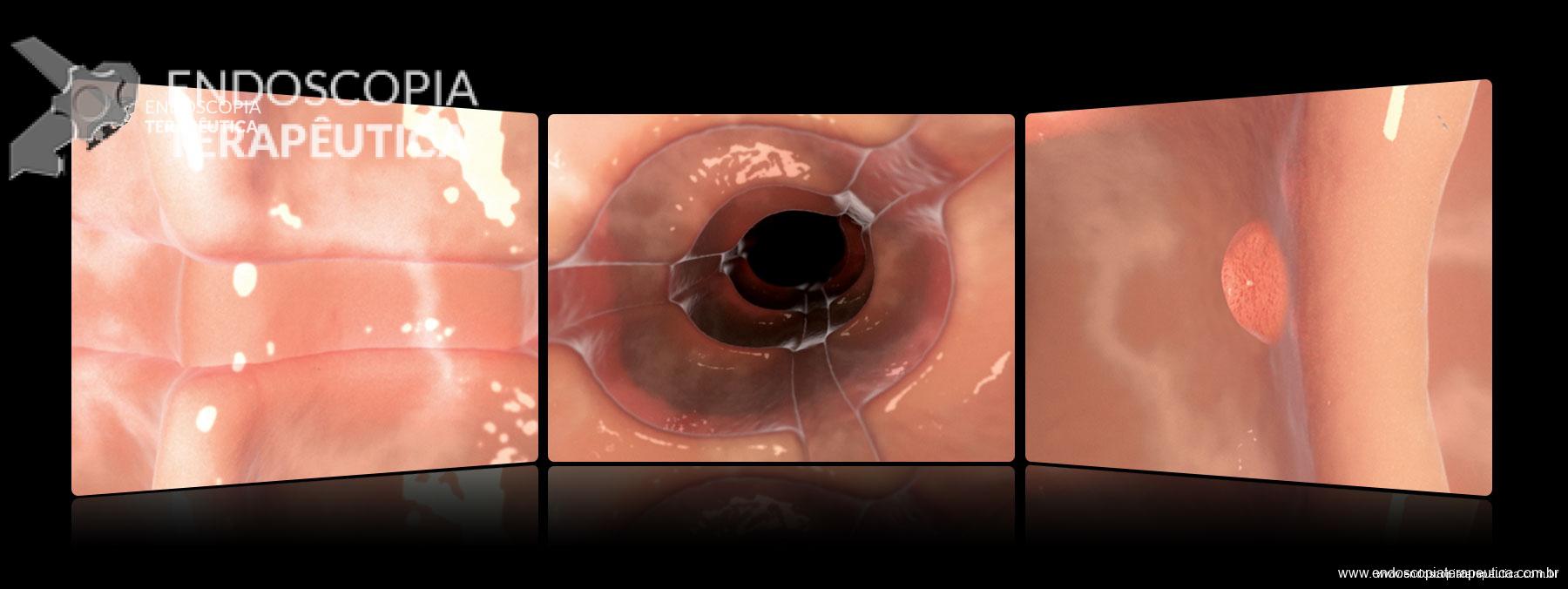
Colonoscópio FUSE projeta imagens em 3 monitores, ampliando o campo de visão
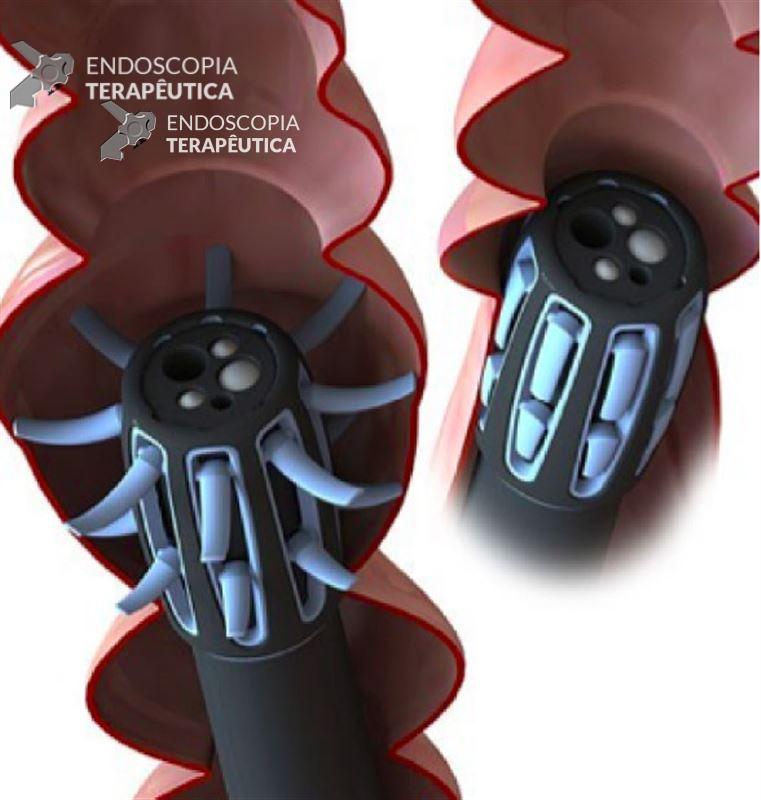
Endocuff

Colonoscópio G-Eye
SUMÁRIO
Técnicas com melhores evidências para aumentar a TDA:
- Preparo adequado
- Tempo de retirada
- Repetir o exame do cólon direito (com retrovisão ou não)
- Segundo observador
- Endoscopia de alta definição
- AM procedures
- Water-Exchange
Técnicas com evidências limitadas que favorecem maior TDA
- G-eye
- Endocuff
- FUSE
- L-Menthol
- Indigo-carmin
- Mudanças de decúbito
Técnicas que parecem não aumentar a TDA
- NBI, FICE e i-Scan
- Hioscina, escopolamina
- Cap
Referências:
- Dynamic patient position changes during colonoscope withdrawal increase adenoma detection: a randomized, crossover trial. Gastrointest Endosc 2011; 73: 456-463
- Ou G, et al. A randomized controlled trial assessing the effect of prescribed patient position changes during colonoscope withdrawal on adenoma detection. Gastrointest Endosc 2014; 80: 277-283
- Pullens and Siersema. Quality indicators for colonoscopy: Current insights and Caveats. World J Gastrointest Endosc 2014 December 16; 6(12): 571-583
- Gurudu SR, et al. Adenoma detection rate is not influenced by the timing of colonoscopy when performed in half-day blocks. Am J Gastroenterol 2011
- Cadoni S, et al. A two-center randomized controlled trial of water-aided colonoscopy versus air insufflation colonoscopy. Endoscopy 2014; 46: 212-218
- Hsieh YH, Koo M, Leung FW. A patient-blinded randomized, controlled trial comparing air insufflation, water immersion, and water exchange during minimally sedated colonoscopy. Am J Gastroenterol 2014; 109: 1390-1400
- Hewett DG, Rex DK. Miss rate of right-sided colon examination during colonoscopy defined by retroflexion: an observational study. Gastrointest Endosc 2011; 74: 246-252
- SAWHNEY MS, et al. GASTROENTEROLOGY 2008;135:1892–1898
- Lee RH. Quality of colonoscopy withdrawal technique. Gastrointest Endosc 2011.
- Quality indicators for colonoscopy. Gastrointest Endosc 2015; 81:1
- Corte C, et al. Hyoscine butylbromide administered at the cecum increases polyp detection: a randomized double-blind placebo controlled trial. Endoscopy 2012; 44: 917-922
- Rondonotti E, et al. The impact of hyoscine-N-butylbromide on adenoma detection during colonoscopy: meta-analysis of randomized, controlled studies. Gastrointest Endosc 2014;
- Inoue K, et al. L-menthol improves adenoma detection rate during colonoscopy: a randomized trial. Endoscopy 2014; 46: 196-202
- Ng SC, et al. The efficacy of cap-assisted colonoscopy in polyp detection and cecal intubation: a meta-analysis of randomized controlled trials. Am J Gastroenterol 2012
- Subramanian V, Mannath J, Hawkey CJ, Ragunath K. High definition colonoscopy vs. standard video endoscopy for the detection of colonic polyps: a meta-analysis. Endoscopy 2011; 43: 499-505
- Pasha SF, et al. Comparison of the yield and miss rate of narrow band imaging and white light endoscopy in patients undergoing screening or surveillance colonoscopy: a meta-analysis. Am J Gastroenterol 2012
- Chung SJ, et al. Comparison of detection and miss rates of narrow band imaging, flexible spectral imaging chromoendoscopy and white light at screening colonoscopy:a randomised controlled back-to-back study. Gut 2014; 63:785-791
- Leufkens AM, et al. Effect of a retrograde-viewing device on adenoma detection rate during colonoscopy: the TERRACE study. Gastrointest Endosc 2011; 73: 480-489
- Gralnek IM, et al. Standard forward viewing colonoscopy versus full-spectrum endoscopy: an international, multicentre, randomised, tandem colonoscopy trial. Lancet Oncol 2014; 15: 353-360
- Biecker E, et al. Novel endocuff-assisted colonoscopy significantly increases the polyp detection rate: a randomized controlled trial. J Clin Gastroenterol 2015; 49: 413-418
- Hendel J, et al. 435 Prospective Randomized Multicenter Trial to Compare Adenoma Detection Rate of HD Colonoscopy With Standard HD Colonoscopy – Intermediate Results. Gastrointest Endosc 2015; 81: AB145-AB146
Artigos de cromoendoscopia
- Hashimoto K, et al. Hepatogastroenterology. 2010 Nov-Dec;57(104):1399-404.
- Omata F, et al. Scand J Gastroenterol. 2014 Feb;49(2):222-37.
- Pohl J, et al. Gut. 2011 Apr;60(4):485-90.