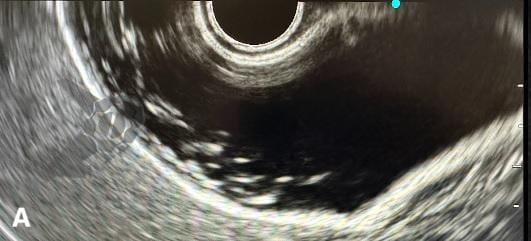
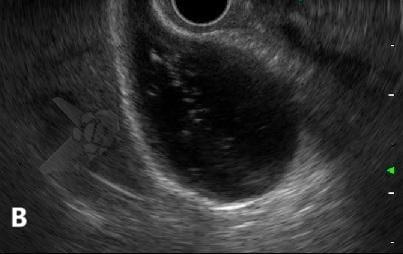
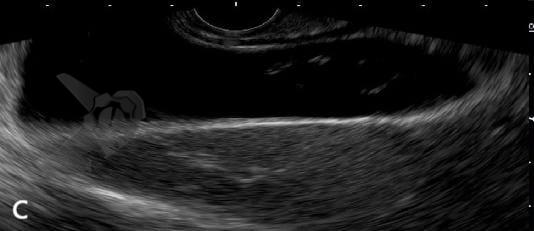
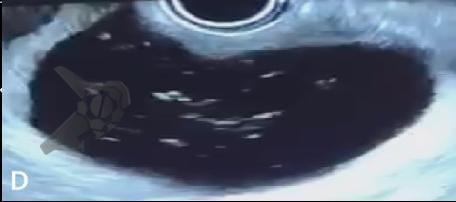
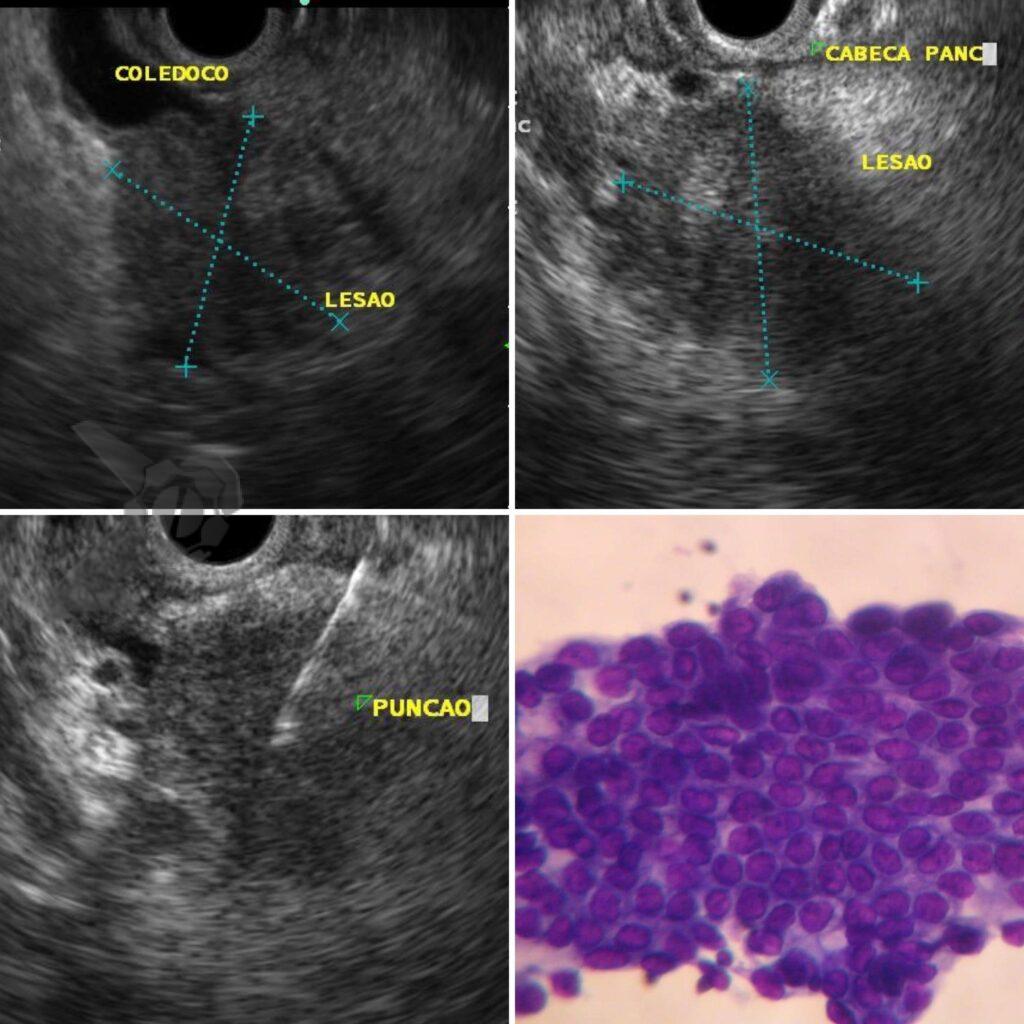
Endoscopic ultrasound-guided gallbladder versus bile duct drainage for first-line therapy of malignant biliary obstruction: international multicenter trial
Publicado na Endoscopy em janeiro 2026
Autores: Benedetto Mangiavillano, Daryl Ramai, Alessandro Fugazza, Gianluca Franchellucci, Marco Spadaccini, Carmelo Barbera, Paolo Giorgio Arcidiacono, Germana De Nucci, Belén Martínez-Moreno, Roberto Di Mitri, Francesco Di Matteo, Alberto Larghi, Carlos Robles Medranda, Andrea Anderloni, Luca De Luca, Anthony Y. B. Teoh, Jorge Vargas-Madrigal, Edoardo Forti, Michiel Bronswijk, Helga Bertani, Sundeep Lakhtakia , Khanh Do-Cong Pham, Stefano Francesco Crinò, Alessandro Repici, Antonio Facciorusso, Biliary Therapeutic EUS Study Group.
Introdução
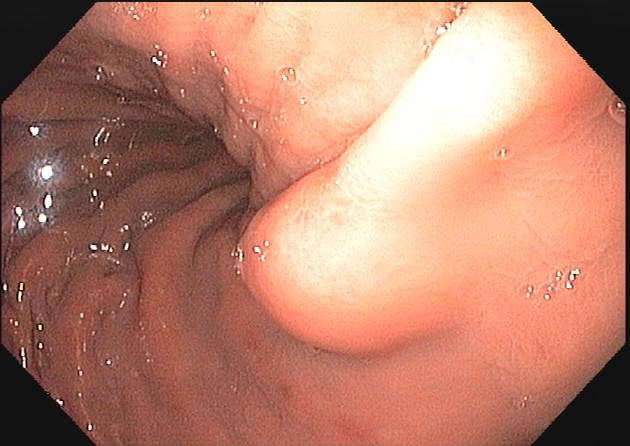
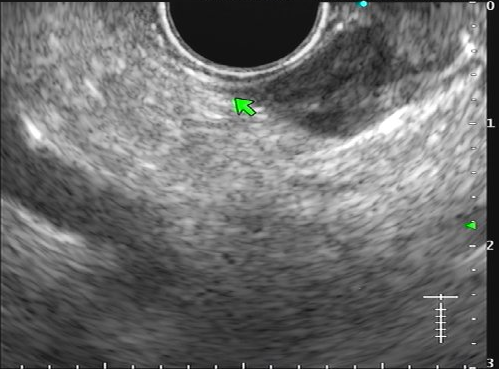
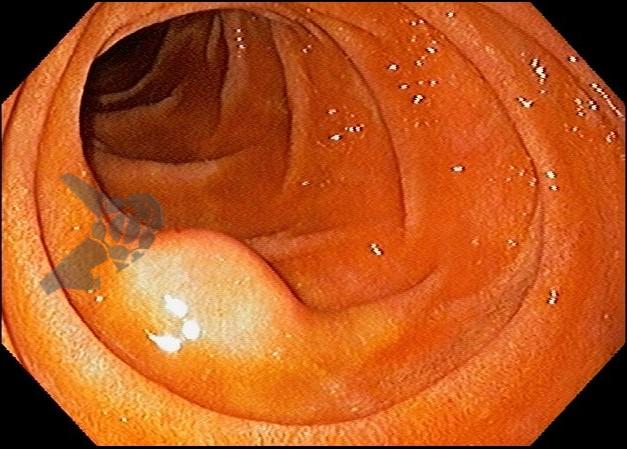
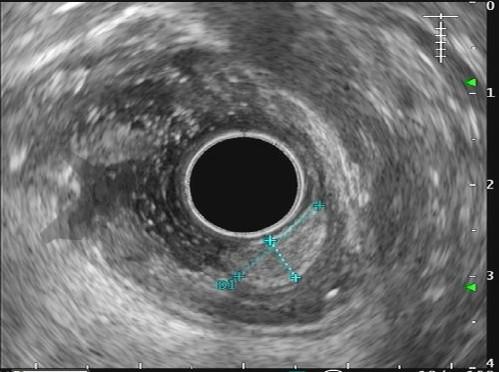
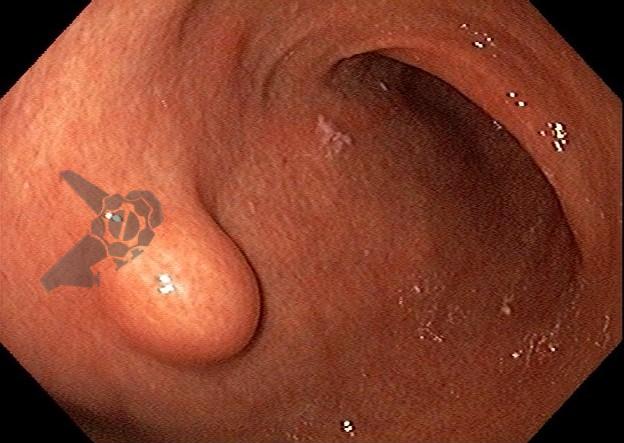
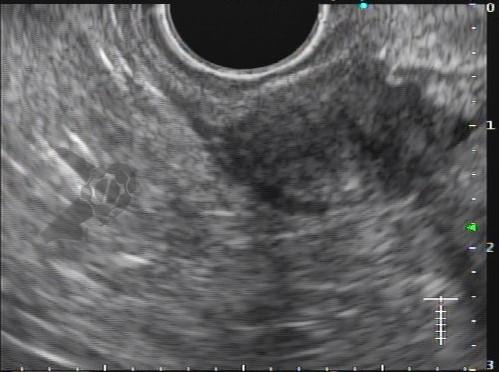
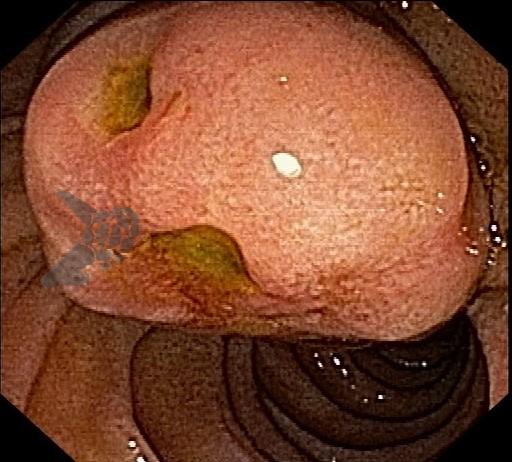
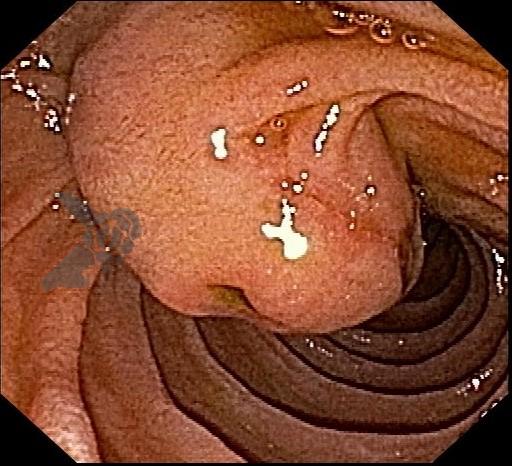
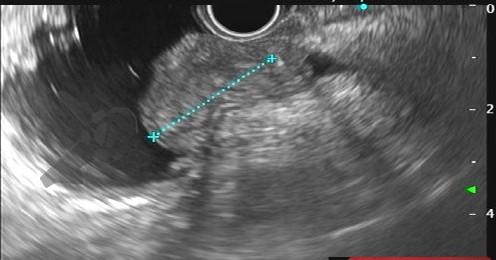
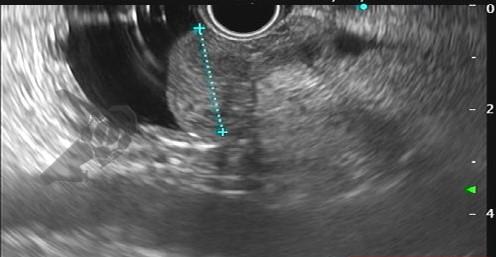
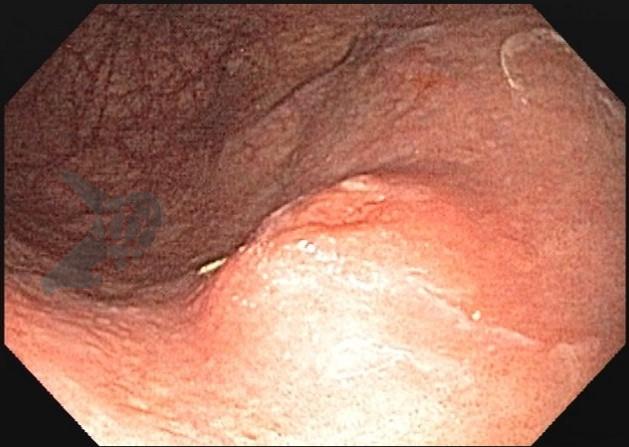
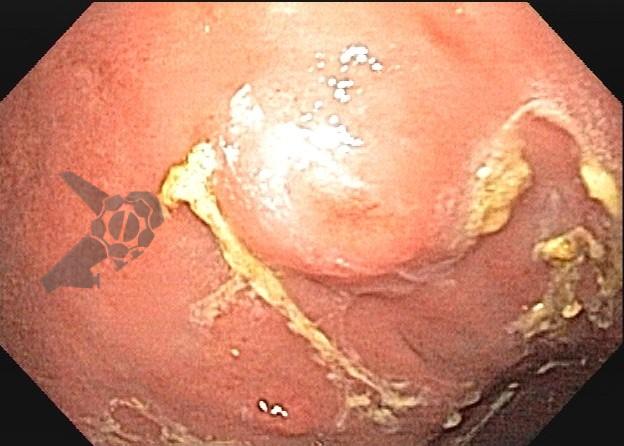
O principal método de drenagem biliar para obstruções malignas distais é a CPRE. Nos casos de impossibilidade/falha, a coledocoduodenostomia ecoguiada (EUS-choledoduodenostomy – CDS) surge como uma das principais opções, porém pode ser desafiadora devido fatores anatômicos, como colédoco < 12 mm, posição do colédoco distante do probe, além da possibilidade de disfunção do stent a longo prazo (1 – 3). Considerando um ducto cístico patente, a drenagem ecoguiada da vesícula (EUS-gallblader drainage – GBD) é uma alternativa interessante, pela técnica em geral mais fácil (alvo/vesícula de maiores proporções). Uma vez que os resultados são bons (100% de sucesso técnico e 10,8% de eventos adversos em um estudo), os autores optaram por investigar estas opções como primeira linha na paliação endoscópica da obstrução maligna distal (4, 5).
Métodos
Trata-se de um estudo retrospectivo multicêntrico que incluiu casos de EUS-CDS e GBD como tratamento de primeira linha para drenagem biliar (sem tentativa de drenagem por CPRE). Foram incluídos pacientes com ducto cístico patente (avaliação prévia por RNM e/ou TC e durante a ecoendoscopia terapêutica), ambos métodos factíveis no procedimento inicial, colédoco > 12 mm e não candidatos a cirurgia.
O desfecho primário foi o sucesso clínico, definido como > 15% de queda de bilirrubina em 24h e > 50% em 14 dias. Desfechos secundários: sucesso técnico (drenagem de bile após o procedimento), eventos adversos e sobrevida.
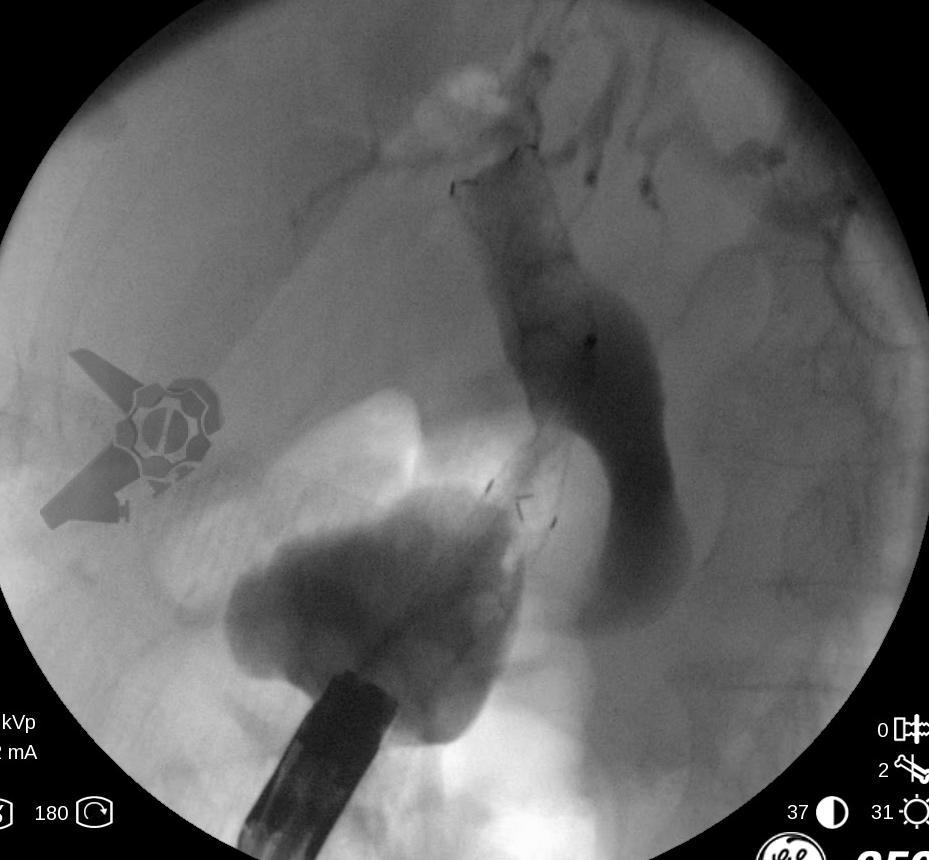
Resultados
Após a análise retrospectiva de 291 pacientes, 77 em cada grupo (total de 154 pacientes) foram incluídos. Não houve diferença nas características de base dos pacientes.
A hot AXIOS foi utilizada em 87% dos casos de EUS-GBD e 92% das CDS. Nos demais casos, a hot Spaxus foi o stent empregado.
A mediana de sobrevida em ambos os grupos foi de 5 meses. Os dados sobre recorrência de obstrução biliar só estavam disponíveis em 95 pacientes (48 EUS-CDS e 47 GBD). Não houve diferença entre os grupos para recorrência (CDS 10/48 = 21% e GBD 8/47 = 17%), sucesso técnico e clínico e eventos adversos (tabela 1).
| Desfechos, n (%) [95 %CI] | EUS-GBD (n = 77) | EUS-CDS (n = 77) | P |
|---|---|---|---|
| Sucesso técnico | 74 (96) [89–99] | 76 (99) [92–99] | 0.36 |
| Sucesso clínico | 66 (86) [75–92] | 71 (92) [83–97] | 0.17 |
| Eventos adversos | 11 (14) [7–24] | 11 (14) [7–24] | > 0.99 |
| Sangramento | 2 (3) [0.3–9] | 2 (3) [0.3–9] | > 0.99 |
| Perfuração | 1 (1) [0.1–7] | 0 (0) [0–0.4] | 0.54 |
| Oclusão do stent | 3 (4) [0.8–10] | 2 (3) [0.3–9] | 0.61 |
| Migração do stent | 1 (1) [0.1–7] | 0 (0) [0–0.4] | 0.54 |
| Falha na liberação do stent | 0 (0) [0–0.4] | 4 (5) [1–12] | 0.12 |
| Pancreatite aguda | 3 (4) [0.8–10] | 0 (0) [0–0.4] | 0.09 |
| Colangite | 1 (1) [0.1–7] | 3 (4) [0.8–10] | 0.29 |
| Eventos adversos graves | 6 (8) [2–16] | 6 (8) [2–16] | > 0.99 |
Discussão
Implicações clínicas
Os guidelines atuais recomendam a drenagem ecoguiada ao invés da percutânea para falha da CPRE em casos de obstrução biliar distal maligna (1, 6). A EUS-CDS pode ser tecnicamente desafiadora ou até inviável por uma dilatação biliar discreta e/ou distância do probe para o colédoco. Assim, a EUS-GBD apresenta-se como opção factível quando o ducto cístico é patente e não há histórico de colecistectomia.
EUS-GBD versus EUS-CDS como primeira linha
Trabalhos prévios demonstraram resultados similares entre os métodos após falha da CPRE, porém este é o primeiro estudo colocando estas opções como primeira linha na drenagem das vias biliares.
Os resultados para os entusiastas das drenagens ecoguiadas são muito positivos: 96% de sucesso técnico, 86% de sucesso clínico e 11% de eventos adversos, todos sem diferença estatística quando comparados a EUS-CDS. Vale lembrar que estudos prévios já nos fornecem evidência para empregar a EUS-CDS no tratamento da estenose biliar maligna distal mesmo sem tentar realizar a CPRE (7). Quando comparada à CDS, a GBD apresenta a vantagem de ser tecnicamente mais fácil, podendo ainda, ser factível com maior frequência.
Outro ponto que deve ser sempre mantido em mente para a GBD é a necessidade de uma boa avaliação da patência do ducto cístico tanto por exame de imagem seccional prévio (RNM e/ou TC) e na ecoendoscopia terapêutica.
Como escolher a abordagem
A literatura atual, portanto, nos permite considerar três opções de primeira linha na obstrução biliar maligna distal: (1) CPRE, (2) EUS-CDS e (3) EUS GBD.
Considerando a otimização de recursos e o sentido de priorizar abordagens “mais fisiológicas”, faz sentido manter a CPRE como opção inicial. Talvez os bons resultados das opções ecoguiadas apresentem essa opção diante de preditores de dificuldade e/ou maior incidência de eventos adversos na CPRE. Ainda não existem guidelines ou fluxogramas baseados em evidências para indicar qual contexto favorece um tipo dessas 3 abordagens em relação aos demais. Faz sentido considerar fatores do paciente como patência do ducto cístico, invasão tumoral do duodeno, morfologia da papila e outros fatores anatômicos que possam dificultar a CPRE, além da expertise local para as drenagens ecoguiadas. Outra coisa a se considerar, almejando o sucesso endoscópico técnico em quase todos os casos, é iniciar a CPRE com a possibilidade de uma baixo limiar de conversão para uma drenagem ecoguiada no mesmo tempo anestésico.
Perspectivas futuras
Fica evidente o avanço da ecoendoscopia terapêutica com bons resultados na drenagem biliar. Os próximos passos, que devem ser elucidados com novos estudos, envolvem compreender melhor o tipo de situação clínica em que cada opção se aplica.
Quer saber mais sobre drenagem biliar ecoguiada? Acesse o link.
Referências
- van der Merwe SW, van Wanrooij RLJ, Bronswijk M, Everett S, Lakhtakia S, Rimbas M, Hucl T, Kunda R, Badaoui A, Law R, Arcidiacono PG, Larghi A, Giovannini M, Khashab MA, Binmoeller KF, Barthet M, Perez-Miranda M, van Hooft JE. Therapeutic endoscopic ultrasound: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2022;54(2):185-205. doi:10.1055/a-1717-1391.
- Bang JY, Varadarajulu S. Lumen-apposing metal stents for endoscopic ultrasonography-guided interventions. Dig Endosc. 2019;31(6):619-626. doi:10.1111/den.13428.
- Chen YI, Long C, Sahai AV, Napoleon B, Donatelli G, Kunda R, Martel M, Chan SM, Arcidiacono PG, Lam E, Kongkam P, Forbes N, Larghi A, Mosko JD, Van der Merwe S, Gan SI, Jacques J, Kenshil S, Ratanachu-Ek T, Miller C, Saxena P, Desilets E, Sandha G, Alrifae Y, Teoh AYB; ELEMENT and DRA-MBO working groups. Stent misdeployment and factors associated with failure in endoscopic ultrasound-guided choledochoduodenostomy: analysis of the combined datasets from two randomized trials. Endoscopy. 2025;57(4):330-338. doi:10.1055/a-2463-1601.
- Issa D, Irani S, Law R, Shah S, Bhalla S, Mahadev S, Hajifathalian K, Sampath K, Mukewar S, Carr-Locke DL, Khashab MA, Sharaiha RZ. Endoscopic ultrasound-guided gallbladder drainage as a rescue therapy for unresectable malignant biliary obstruction: a multicenter experience. Endoscopy. 2021;53(8):827-831. doi:10.1055/a-1259-0349.
- Mangiavillano B, Moon JH, Facciorusso A, et al. Endoscopic ultrasound-guided gallbladder drainage as a first approach for jaundice palliation in unresectable malignant distal biliary obstruction: prospective study. Dig Endosc. 2024;36:351-358.
- Marya NB, Pawa S; American Society for Gastrointestinal Endoscopy Standards of Practice Committee, et al. American Society for Gastrointestinal Endoscopy guideline on the role of therapeutic EUS in the management of biliary tract disorders: methodology and review of evidence. Gastrointest Endosc. 2024;100:e79-e135.
- Khoury T, Sbeit W, Fumex F, et al. Endoscopic ultrasound- versus ERCP-guided primary drainage of inoperable malignant distal biliary obstruction: systematic review and meta-analysis of randomized controlled trials. Endoscopy. 2024;56(12):955-963. doi:10.1055/a-2340-0697.
Como citar este artigo
Funari MP. Endoscopic ultrasound-guided gallbladder versus bile duct drainage for first-line therapy of malignant biliary obstruction: international multicenter trial Endoscopia Terapeutica 2026 Vol I. Disponível em: https://endoscopiaterapeutica.net/pt/artigoscomentados/endoscopic-ultrasound-guided-gallbladder-versus-bile-duct-drainage-for-first-line-therapy-of-malignant-biliary-obstruction-international-multicenter-trial/