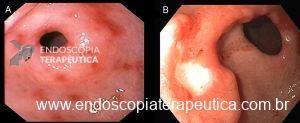
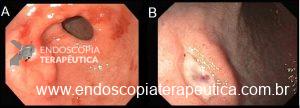
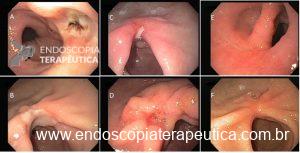
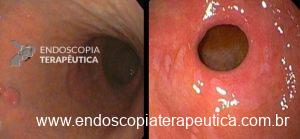
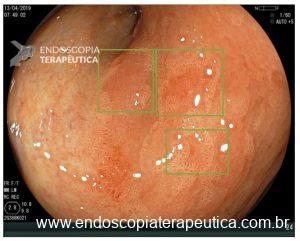
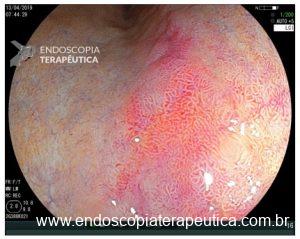
Onde coletar as biópsias gástricas para o estadiamento OLGA?
O protocolo OLGA para estadiamento da atrofia gástrica ficou muito popular no nosso meio. Cada vez mais os endoscopistas estão recebendo pedidos dos gastroenterologistas solicitando coleta de biópsias conforme o protocolo OLGA.
Mas existe uma dúvida persistente: de que locais devemos coletar essas biópsias?
O Sistema Sidney
Primeiramente, devemos revisitar um artigo importantíssimo acerca do assunto: O update do sistema Sydney, escrito pelo Dr. Michael Dixon, pelo famoso Dr. Pelayo Correa além de outros autores (Dixon M, 1996). Destaco esse trecho:

Sistema OLGA
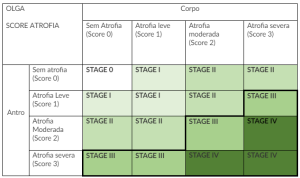
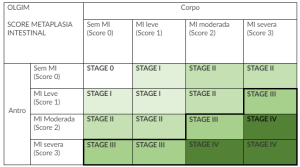
Em abril de 2005, um grupo internacional de gastroenterologistas e patologistas (Operative Link for Gastritis Assessment [OLGA]) reuniu-se em Parma, Itália, com o objetivo de reavaliar criticamente as diretrizes atualizadas do Sistema de Sydney e determinar se seria possível adicionar alguma espécie de estadiamento da gastrite crônica.
Como o risco do CaG esta relacionado a extensão da atrofia gástrica, um sistema que envolvesse o status da atrofia poderia fornecer informações importantes para o prognostico e seguimento desses pacientes. Nasce então o sistema OLGA.

Nesse artigo, os autores escrevem o seguinte paragrafo:
“…the Sydney Systems took into account the topographical distribution of the elementary lesions in the different gastric compartments and recommended that multiple endoscopic biopsy samples be taken from predefined sites of the stomach [8]. Five main sites were considered necessary: (1) greater and lesser curvature of the distal antrum (mucus-secreting mucosa), (2) greater and lesser curvature of the proximal corpus (oxyntic mucosa), and (3) lesser curvature at the incisura angularis, where the earliest atrophic-metaplastic changes tend to occur.” [Rugge M. Hum Pathol. 2005]
Ou seja, eles se baseiam nas recomendações do sistema Sidney e recomendam biópsias da pequena e grande curvatura tanto de corpo quanto de antro, além da incisura.
Em 2007 surge uma nova publicação do protocolo OLGA

Notem que aqui ele já não fala nada a respeito da parede gástrica, se pequena curvatura, grande, anterior ou posterior.
Um ano depois, em 2008, sai a seguinte publicação

Aqui ele já muda para parede anterior e posterior de corpo, porém cita a mesma referência de Dixon M et al, do updated Sydney System de 1994, que recomendava PC e GC 🧐. Esse novo artigo do Dr. Massimo Rugge tem ilustrações bonitinhas e que foram bastante reproduzidas nas aulas de congressos, publicações, etc. Talvez um dos motivos da maioria das pessoas entenderem que o local correto é a parede anterior e posterior de corpo.
Teria sido um erro da publicação?
A princípio parece que não, pois em publicações posteriores, Massimo Rugge e colaboradores reiteram a coleta na parede anterior e posterior de corpo, mas em outras publicações voltam para pequena e grande curvatura e em algumas citam apenas corpo, antro e incisura, sem especificar a parede. Explicado então porque existe tanta confusão a esse respeito.
MAPS II
Mais recentemente, a ESGE, em conjunto com outras sociedades europeias (European Helicobacter and Microbiota Study Group (EHMSG), European Society of Pathology (ESP), and Sociedade Portuguesa de Endoscopia Digestiva (SPED) publicaram o consenso MAPS (Management of epithelial precancerous conditions and lesions in the stomach). Nesse consenso a preferência é pela pequena e grande curvatura.
“Biopsies of at least two topographic sites (from both the antrum and the corpus, at the lesser and greater curvature of each) should be taken and clearly labelled in two separate vials.”
Nesse consenso a preferência é pela pequena e grande curvatura, mas sumiu a incisura angularis! 😫
Incisura angularis: to biopsy or not biopsy?
Mais biópsias permitirão um melhor estadiamento. No entanto, na prática clínica, mais biópsias significam mais tempo e mais custos.
O racional para a biópsia da incisura vem das recomendações do sistema Sydney atualizado. O sistema Sydney original recomendava duas biópsias de antro e duas de corpo. Já o sistema Sydney atualizado recomenda incluir a incisura, visto ser o local onde mais precocemente ocorre as alterações atróficas e metaplásicas “….lesser curvature at the incisura angularis, where the earliest atrophic-metaplastic changes tend to occur”. No entanto, essa recomendação foi baseada em conceitos, e não havia evidências cientificas sugerindo um benefício clínico.
Estudos sobre o benefício da amostragem de biópsia da incisura:
- Um grande estudo com mais de 400 mil biópsias mostrou que a aderência ao sistema original de Sydney proporcionou a mais alta eficácia diagnóstica para infecção por H. pylori e IM. A inclusão de uma biópsia da incisura resultou em ganhos diagnósticos marginais a um custo adicional. [Lash JG, 2013]
- Dois estudos europeu mostraram que sem a biópsia da incisura, 14/1048 pacientes mudariam a categoria de alto risco (III/IV) para baixo risco (I/II) do estadiamento OLGA. [Isajevs S, 2014 e Varbanova M, 2016]
- Isso se traduziu em um número necessário para tratar de 75 – 80, o que significa que um em cada 75 – 80 pacientes não seria corretamente incluído em um grupo de alto risco se a biópsia da incisura não fosse realizada.
- Outro estudo europeu, incluindo população de alto risco (parentes de primeiro grau de pacientes com câncer gástrico de início precoce) avaliou o sistema OLGA sem a biópsia da incisura e demonstrou um downgrade geral de 15% e 30% em comparação com o sistema OLGA original. No entanto, para pacientes em estágios de alto risco (OLGA III/IV), o rebaixamento foi menor (apenas 5% dos pacientes). [Marcos-Pinto R, 2012]
- Um estudo coreano (Kim YI, 2017) incluindo 247 pcts de alto risco testou vários protocolos de biópsias e mostrou que incluir a incisura angularis e obter biópsias da pequena e grande curvaturas de corpo (PC + GC) ao invés da parede anterior e posterior (AP) identificavam mais pacientes no grupo de alto risco de OLGA e OLGIM
- Corpo (PC + GC), incisura, antro (PC + GC) = 64,4%
- Corpo (PC + GC) + antro (PC + GC) = 59,5% (p= .031)
- Corpo (AP), incisura, antro (PC + GC) = 55,5% (P< .001)
- Corpo (AP) + antro (PC + GC) = 47,8% (P< .001)
Em resumo, existe um pequeno rendimento adicional de uma biópsia da incisura o qual precisa ser equilibrado em relação aos custos e tempo, tempo e trabalho. O consenso MAPS II recomenda um mínimo de duas biópsias do antro e duas biópsias do corpo, observando que pode ser considerado adicionar uma biópsia da incisura para maximizar a detecção de pacientes com condições pré-neoplásicas, especialmente quando a cromoendoscopia não está disponível.
Onde colher então?
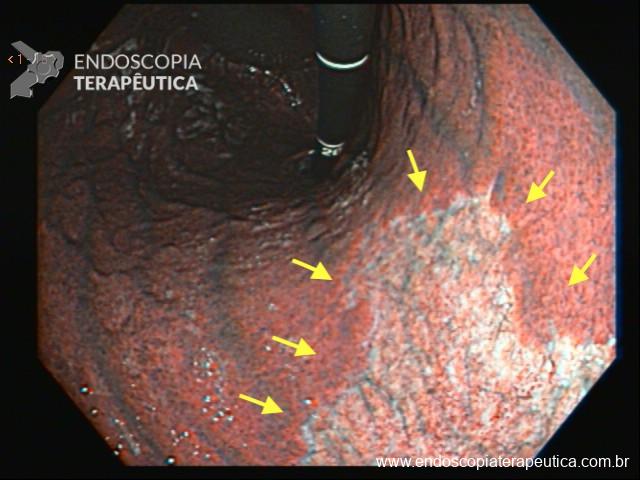
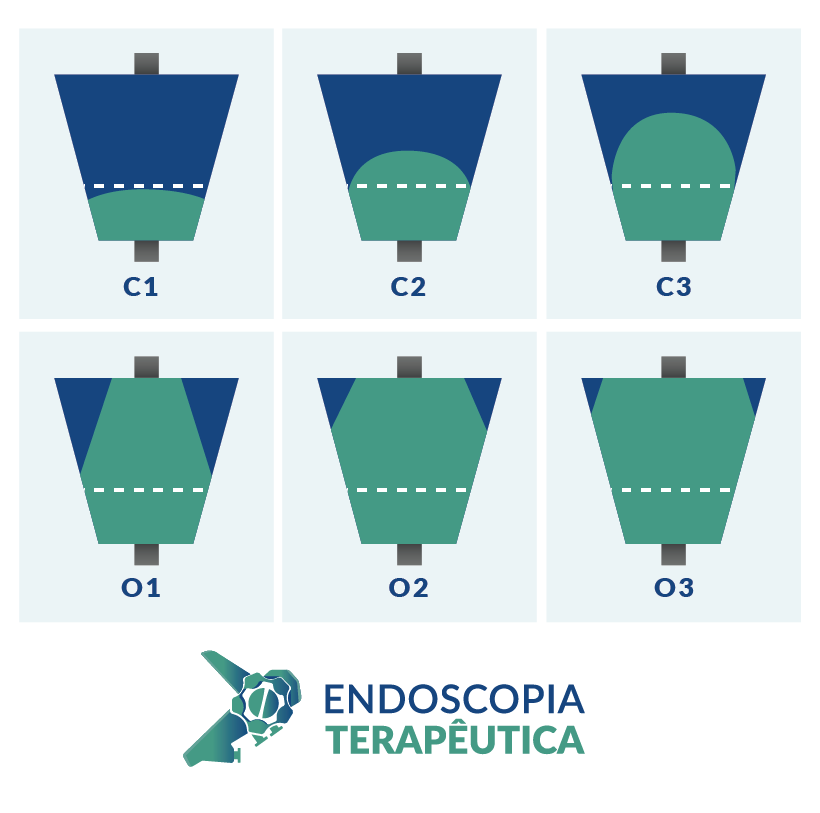
Minha preferência é pela pequena e grande curvatura. Além dos motivos já expostos, devemos lembrar da linha F, que é a linha de progressão da atrofia no estômago. Segundo a classificação de Kimura, a linha F se estende pela pequena curvatura do corpo em direção à cárdia. Ou seja: maior chance de pegar uma amostra com sinais de atrofia se incluirmos a PC nas amostras.
Referências
- Dixon MF, Genta RM, Yardley JH, Correa P. Classification and grading of gastritis. The updated Sydney System. International Workshop on the Histopathology of Gastritis, Houston 1994. Am J Surg Pathol. 1996 Oct;20(10):1161-81. doi: 10.1097/00000478-199610000-00001. PMID: 8827022.
- Rugge M, Genta RM. Staging and grading of chronic gastritis. Hum Pathol. 2005 Mar;36(3):228-33. doi: 10.1016/j.humpath.2004.12.008. PMID: 15791566.
- Rugge M, Meggio A, Pennelli G, Piscioli F, Giacomelli L, De Pretis G, Graham DY. Gastritis staging in clinical practice: the OLGA staging system. Gut. 2007 May;56(5):631-6. doi: 10.1136/gut.2006.106666. Epub 2006 Dec 1. PMID: 17142647; PMCID: PMC1942143.
- Rugge M, Correa P, Di Mario F, El-Omar E, Fiocca R, Geboes K, Genta RM, Graham DY, Hattori T, Malfertheiner P, Nakajima S, Sipponen P, Sung J, Weinstein W, Vieth M. OLGA staging for gastritis: a tutorial. Dig Liver Dis. 2008 Aug;40(8):650-8. doi: 10.1016/j.dld.2008.02.030. PMID: 18424244.
- Pimentel-Nunes P, Libânio D, Marcos-Pinto R, Areia M, Leja M, Esposito G, Garrido M, Kikuste I, Megraud F, Matysiak-Budnik T, Annibale B, Dumonceau JM, Barros R, Fléjou JF, Carneiro F, van Hooft JE, Kuipers EJ, Dinis-Ribeiro M. Management of epithelial precancerous conditions and lesions in the stomach (MAPS II): guideline update 2019. Endoscopy. 2019 Apr;51(4):365-388. doi: 10.1055/a-0859-1883. Epub 2019 Mar 6. PMID: 30841008.
- Misiewicz JJ. The Sydney System: a new classification of gastritis. Introduction. J Gastroenterol Hepatol 1991; 6: 207 – 208
- Isajevs S, Liepniece-Karele I, Janciauskas D et al. The effect of incisura angularis biopsy sampling on the assessment of gastritis stage. Eur J Gastroenterol Hepatol 2014; 26: 510 – 513
- Lash JG, Genta RM. Adherence to the Sydney System guidelines increases the detection of Helicobacter gastritis and intestinal metaplasia in 400738 sets of gastric biopsies. Aliment Pharmacol Ther 2013; 38: 424 – 431
- Varbanova M, Wex T, Jechorek D et al. Impact of the angulus biopsy for the detection of gastric preneoplastic conditions and gastric cancer risk assessment. J Clin Pathol 2016; 69: 19 – 25
- Marcos-Pinto R, Carneiro F, Dinis-Ribeiro M et al. First-degree relatives of patients with early-onset gastric carcinoma show even at young ages a high prevalence of advanced OLGA/OLGIM stages and dysplasia. Aliment Pharmacol Ther 2012; 35: 1451 – 1459
- Kim YI, Kook MC, Cho SJ, Lee JY, Kim CG, Joo J, Choi IJ. Effect of biopsy site on detection of gastric cancer high-risk groups by OLGA and OLGIM stages. Helicobacter. 2017 Dec;22(6). doi: 10.1111/hel.12442. Epub 2017 Sep 22. PMID: 28940945.
Como citar este artigo
Martins BC. Onde coletar as biópsias gástricas para o estadiamento OLGA? Endoscopia Terapeutica 2023, vol 2. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/onde-coletar-as-biopsias-gastricas-para-o-estadiamento-olga