Caso clínico – Melanoma metástatico e Gastrite
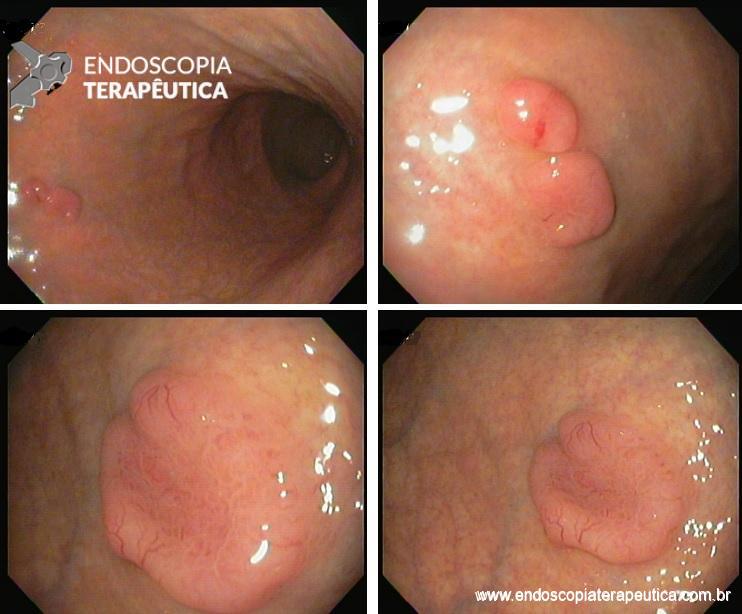
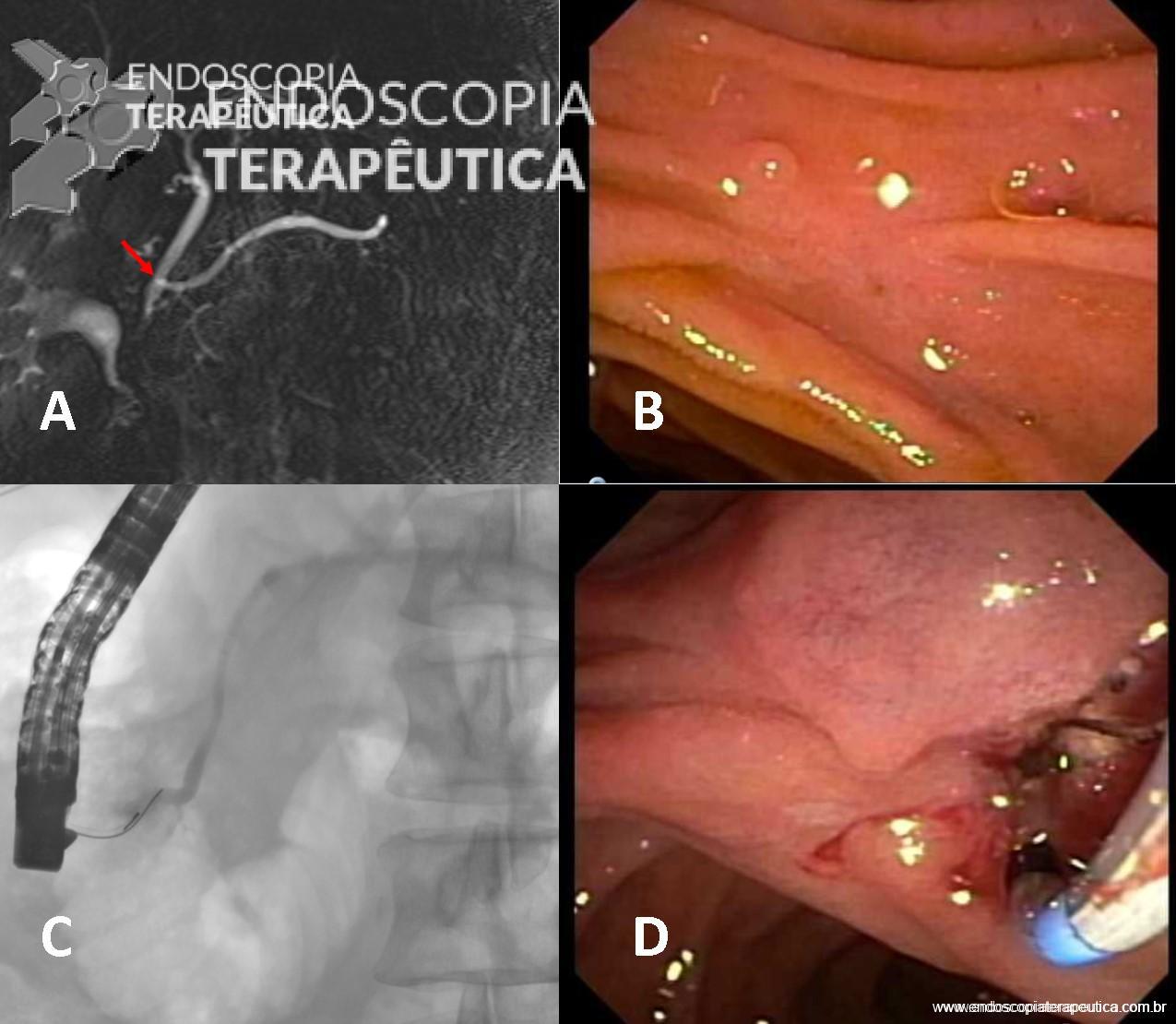
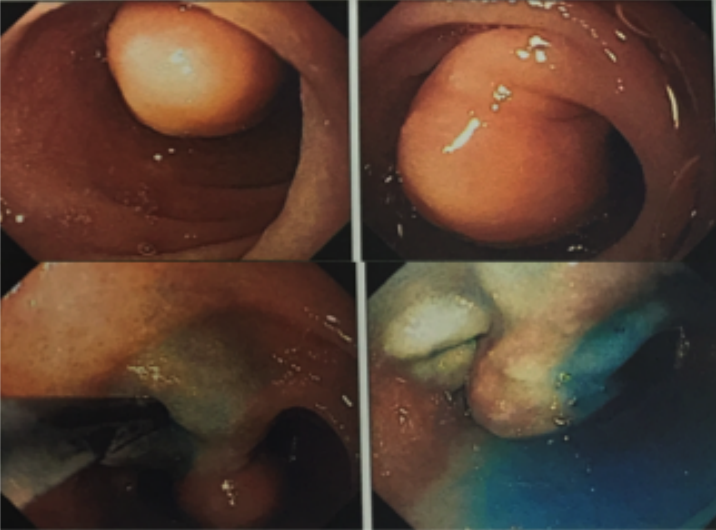
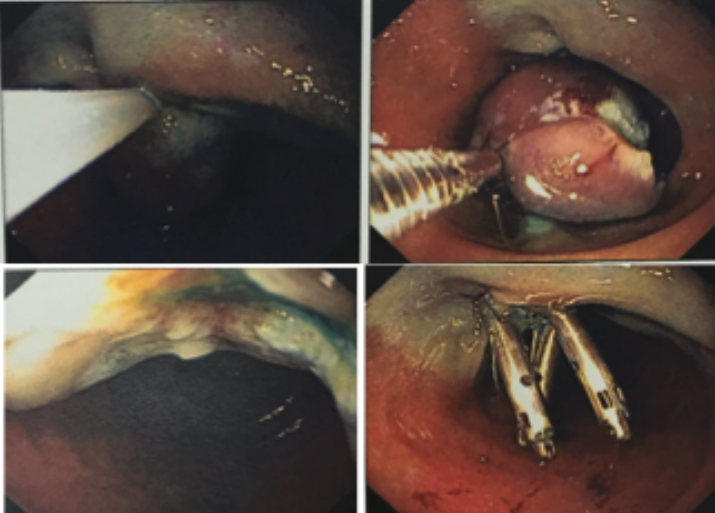
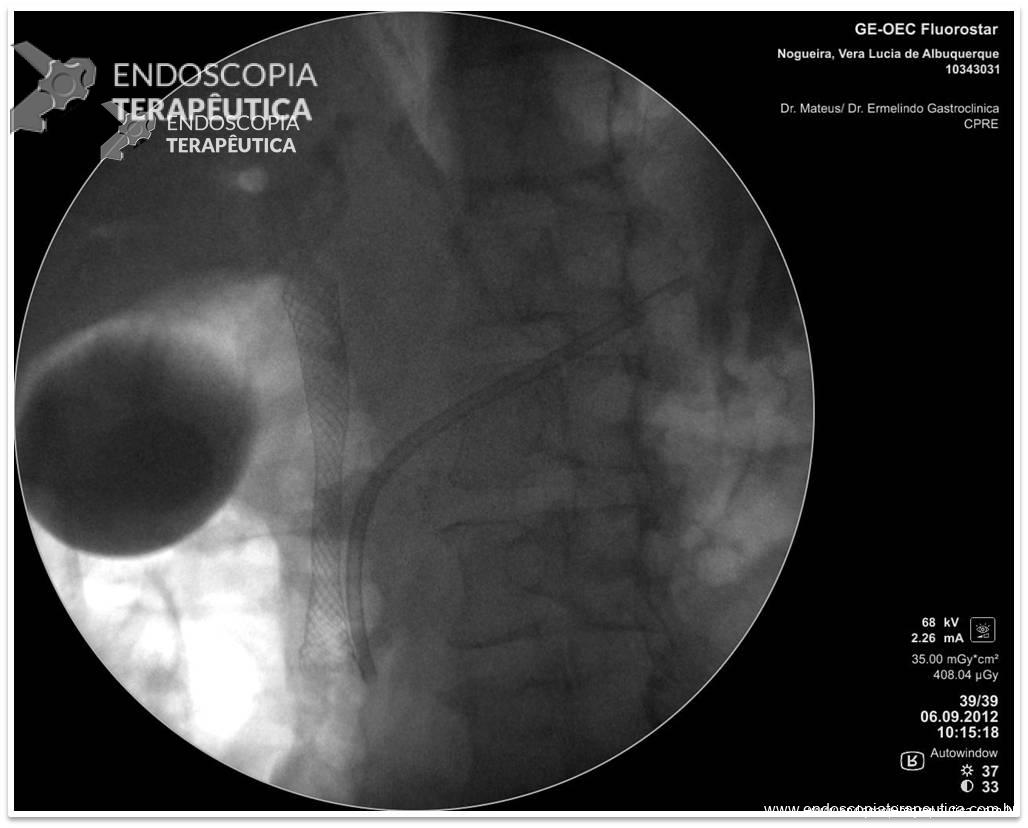
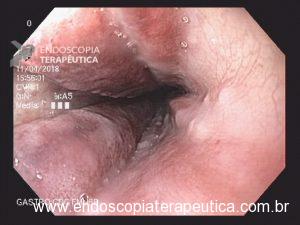
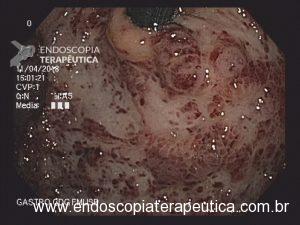
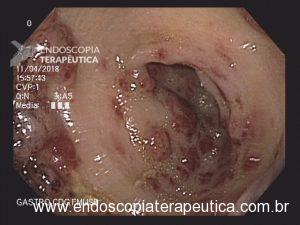
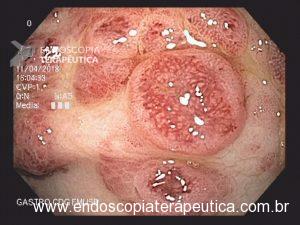
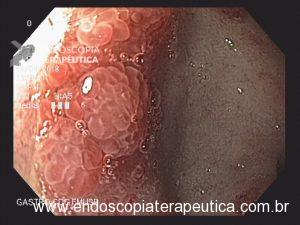
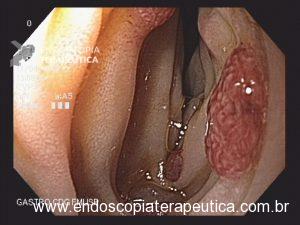
Paciente do sexo masculino, 27 anos, portador de melanoma metastático, tendo realizado 03 doses de Ipilimumabe (imunoterápico), evolui com náuseas, vômitos, dor epigástrica e perda ponderal de cerca de 08 Kg em 10 dias. Na admissão, estável do ponto de vista hemodinâmico. Ao exame, abdome plano, RHA presentes, flácido, doloroso a palpação em região epigástrica, sem sinais de irritação peritoneal. Realizou EDA: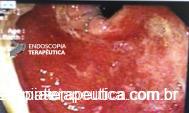
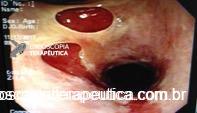
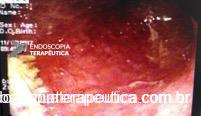
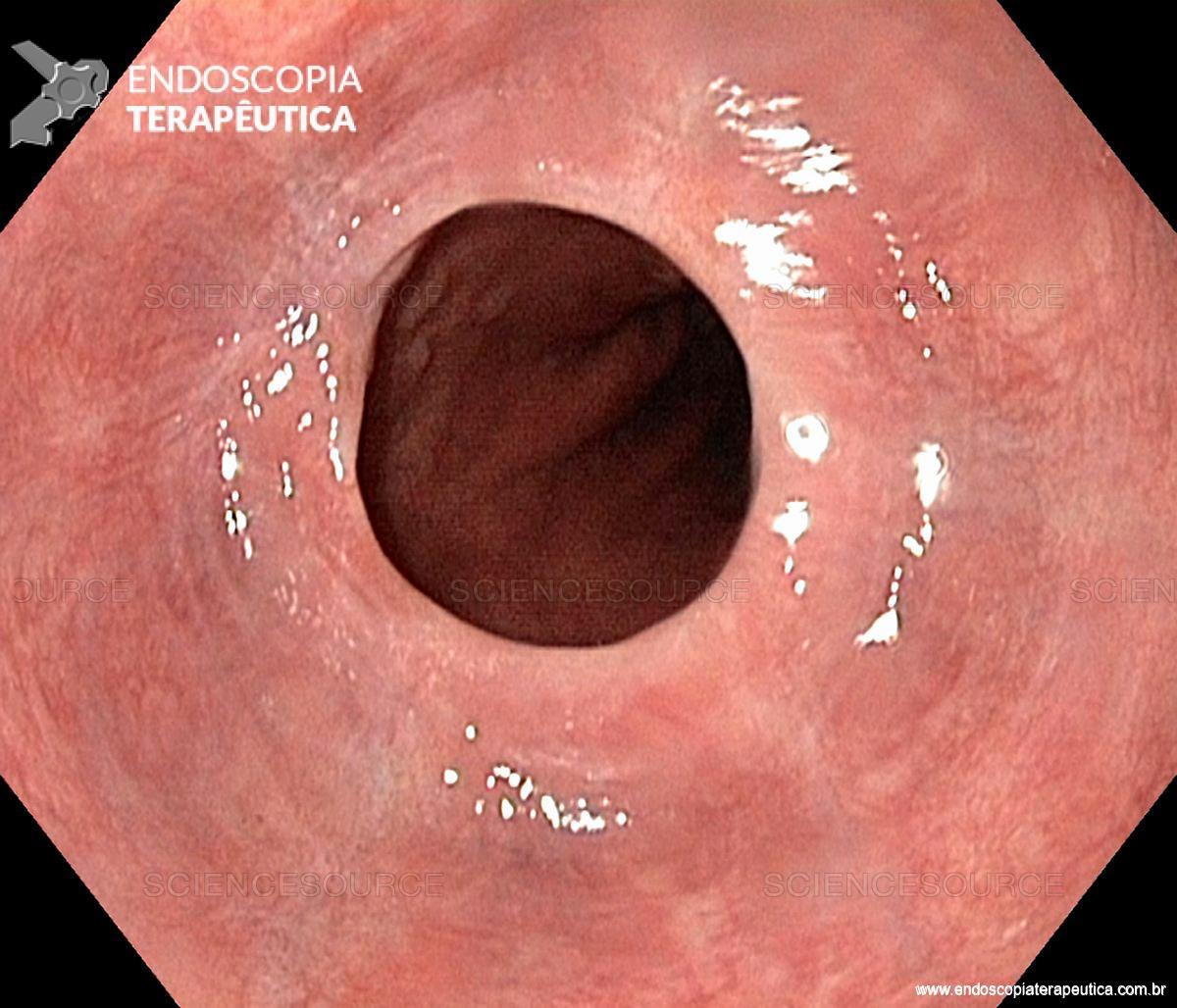
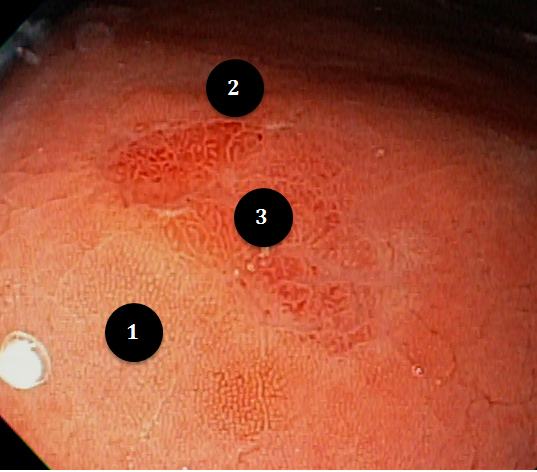
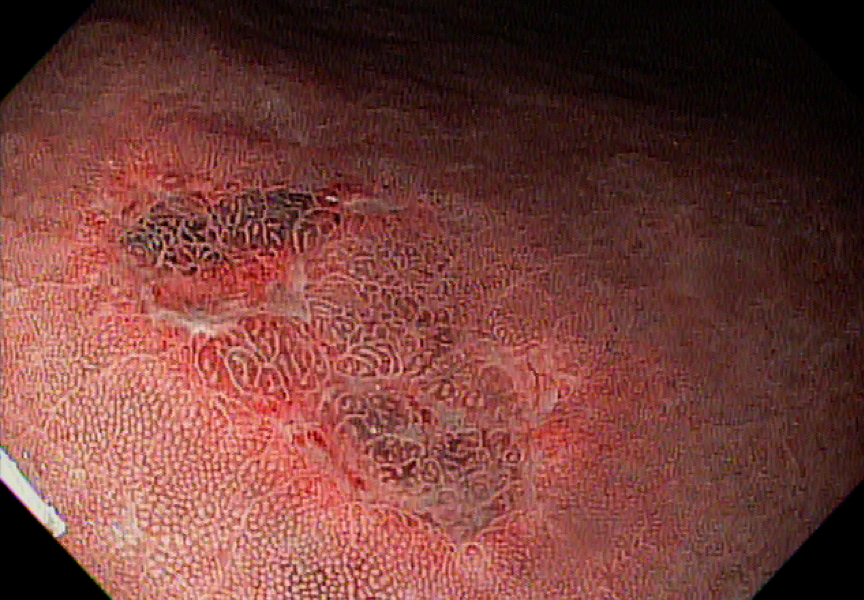
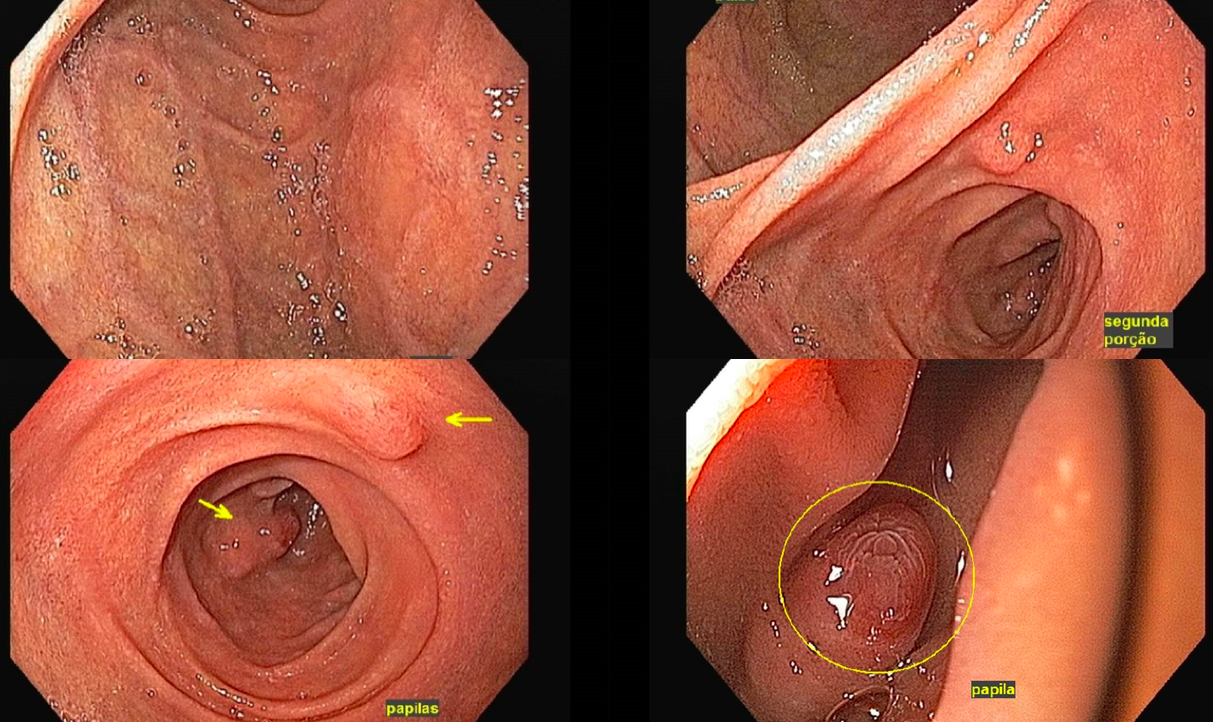
Foi realizada inicialmente a pesquisa imunohistoquimica para CMV e pesquisa para outras bactérias (ex: Streptococcus), sendo negativa, além de se afastar melanoma metástatico (não seria também a característica endoscópica esperada). Anatomopatológico inicial apenas com importante infiltrado linfocítico e neutrofílico inespecífico. Foi aventada a possibilidade de gastropatia relacionada ao Ipililumabe e diante da gravidade do aspecto endoscópico e urgente necessidade de iniciar terapêutica, após discussão entre gastroenterologia e oncologia, foi optado por iniciar Metilprednisolona 02 mg/Kg/dia. Além de iniciar corticoterapia, foi realizada passagem de SNE pós pilórica, IBP endovenoso e sucralfato. O paciente apresentou significativa melhora clínica em 48 horas e após 01 semana da internação hospitalar, obteve alta hospitalar para desmame ambulatorial do corticoide. Durante acompanhamento ambulatorial, paciente trouxe revisão de lâmina do primeiro anatomopatológico (AP do diagnóstico) sendo evidenciado que 04 células endoteliais estavam acometidas pelo CMV e a pesquisa para H. pylori positiva (paucibacilar). Em discussão multidisciplinar entre oncologista, gastroenterologista e patologista, a gastropatia foi atribuída a imunoterapia. Dentre os aspectos considerados, tem-se: aspecto endoscópico não é típico para CMV (principalmente pelo fato que o antro encontrava-se completamente recoberto por camada de fibrina) assim como também não era típico para H. pylori, além do acometimento paucibacilar pelo H. pylori e apenas 04 células endoteliais acometidas pelo CMV, o que não justificaria a gravidade do aspecto endoscópico e o fato da lesão endotelial identificada na histologia não ser típica do CMV. Fora isso, tem-se a resposta terapêutica e rápida com uso da metilprednisolona (02 mg/kg/dia). Segue a última EDA realizada ambulatorialmente:
Os imunoterápicos correspondem a nova classe de quimioterápicos cujas indicações tem-se ampliado. São drogas que estimulam as células T a atuarem contra as células neoplásicas. Os eventos adversos gastrointestinais mais comumente relacionados são a colite e hepatotoxidade. Para tratamento dos eventos adversos, a corticoterapia exerce papel importante. Apesar de não existirem relatos de caso relacionando o uso do ipililumabe com a gastropatia medicamentosa, na literatura existem dois relatos de casos relacionando o uso do Nivolumabe (outro tipo de imonuterápico) com gastropatia. A característica clínica, endoscópica e histológica é muito semelhante ao caso apresentado acima. Seguem os dois relatos de caso na referência abaixo do texto. Dessa forma, os gastroenterologistas e endoscopistas tem que ficar atentos quanto a gastropatia medicamentosa mediada por imunoterápicos (classe nova de quimioterápicos) vir a ser encontrada com maior frequência em futuro próximo em função do aumento da prescrição desta classe de imunoterápicos não somente para o melanoma como também para outras neoplasias.
Referências:
- Boyke J, Dejulio T. Severe esophagitis and gastritis from NivolumabTherapy. ACG Case Rep J 2017
- Kobayashi M, Yamaguchi O, Nagata K, Nonaka K, Ryozawa S, Acute hemorrhagic gastritis after nivolumab treatment, Gastrointestinal Endoscopy (2017)
Elaborado em colaboração com:
Dr. Rodrigo Antônio Vieira Guedes (oncologista)
Dr. Nathanael de Freitas Pinheiro Junior (patologista)