Caso clínico – Biópsia hepática por ecoendoscopia
Paciente sexo feminino, 54 anos, com antecedentes de transtorno depressivo e dislipidemia, iniciou em novembro de 2019 quadro de icterícia, colúria e hipocolia fecal, sem dor abdominal, febre ou perda de peso. Etilista de 5 doses/semana e tabagista com baixa carga tabágica (2 anos/maço). Fazia uso de sertralina há 2 anos e havia iniciado o uso de sinvastatina em outubro de 2019, tendo interrompido o uso quando ficou ictérica.
- Exames laboratoriais (janeiro/2020): AST: 70/ ALT: 24/ Fosfatase alcalina: 552 (referência: <110)/ Gama-GT: 706/ Bilirrubinas: 4,9 (Direta: 3,3)/ Alb: 3,1/ INR: 1,0.
- Sorologias virais e autoanticorpos negativos, incluindo anti-mitocôndria.
- Colangiorressonância (dezembro/2019): fígado com redistribuição volumétrica e sinal heterogêneo, com vesícula e vias biliares sem alterações.
Feita hipótese de lesão hepática induzida por sinvastatina e optado por seguimento clínico-laboratorial.
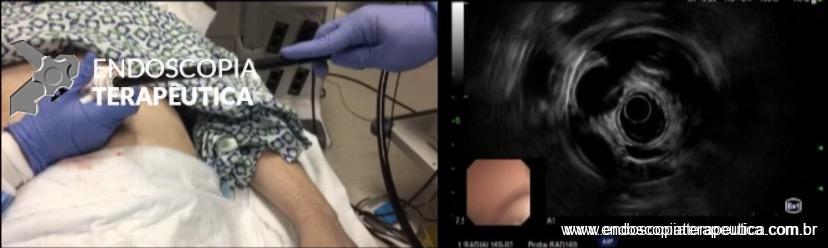
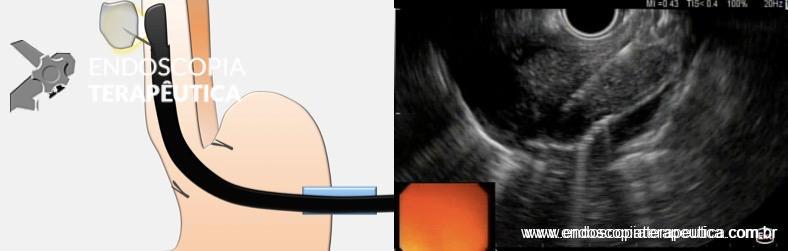
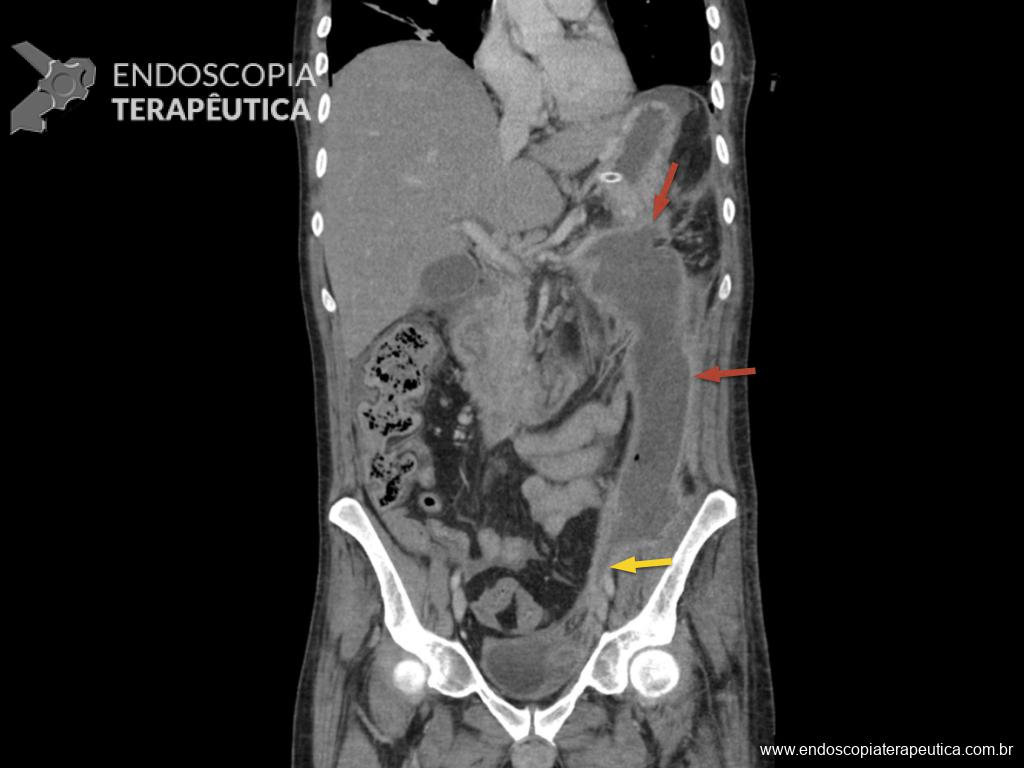
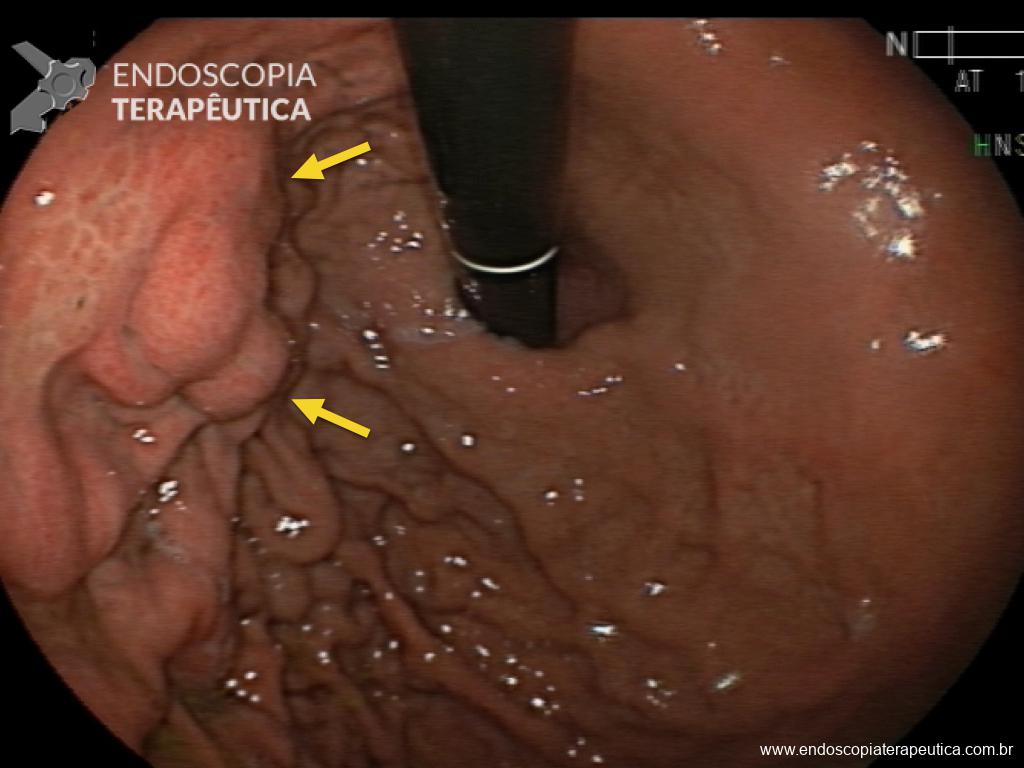
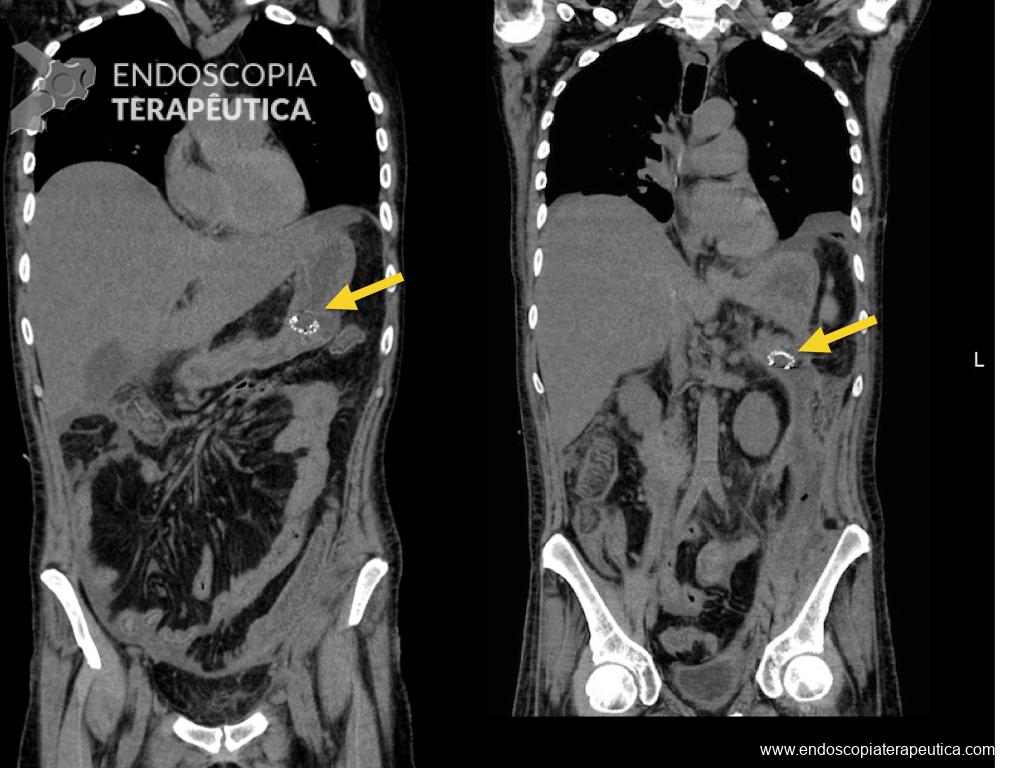
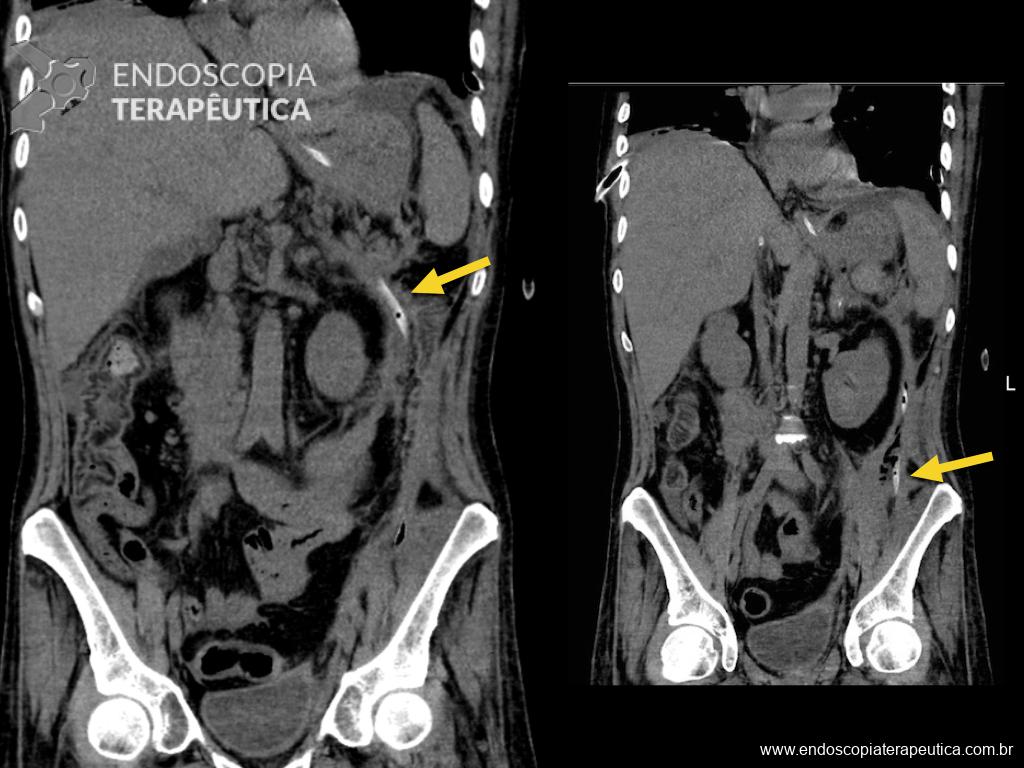
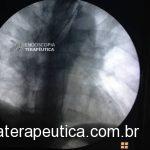
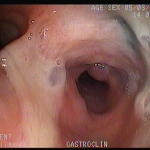
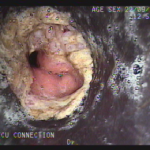
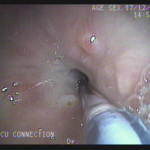
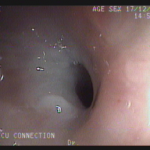
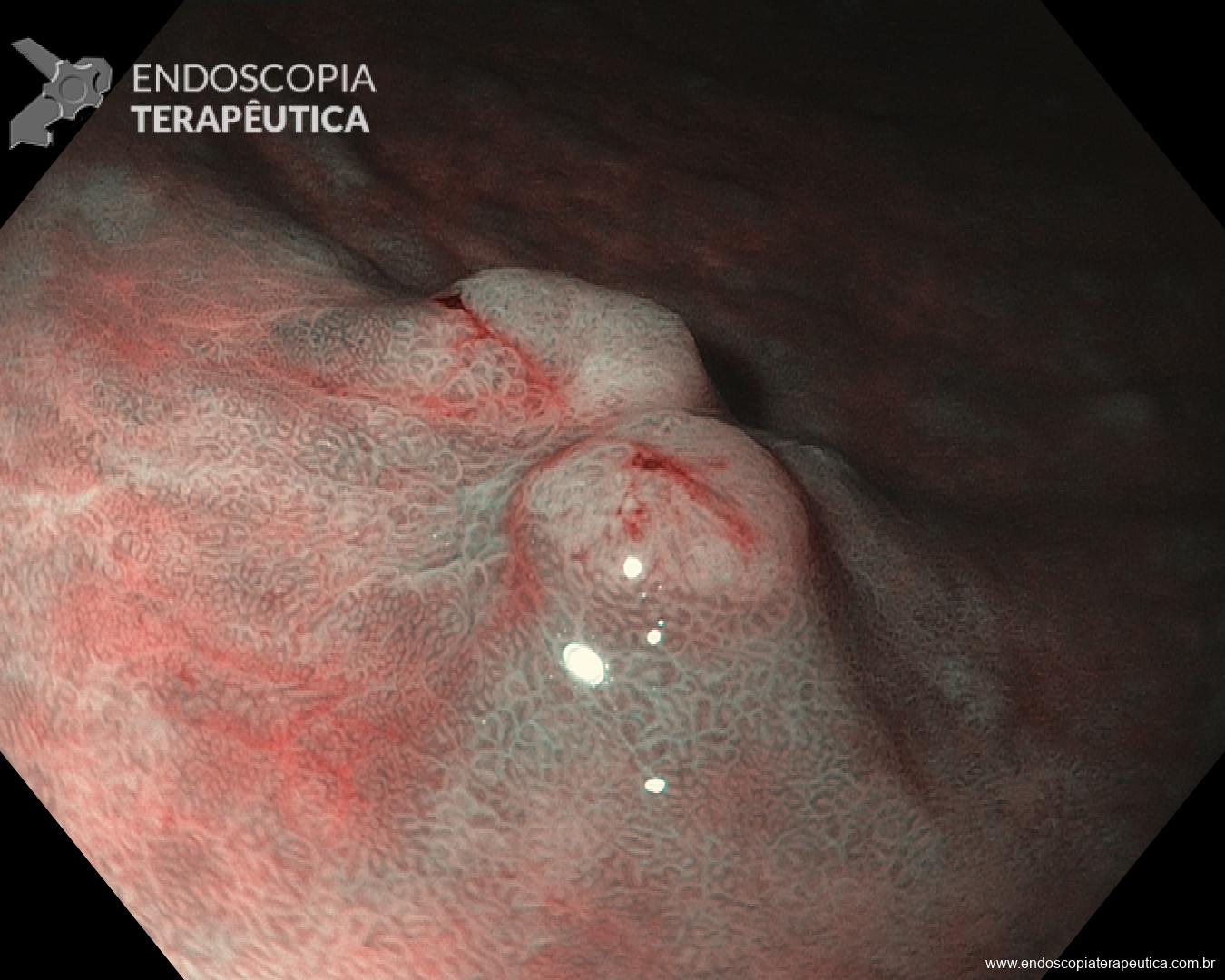
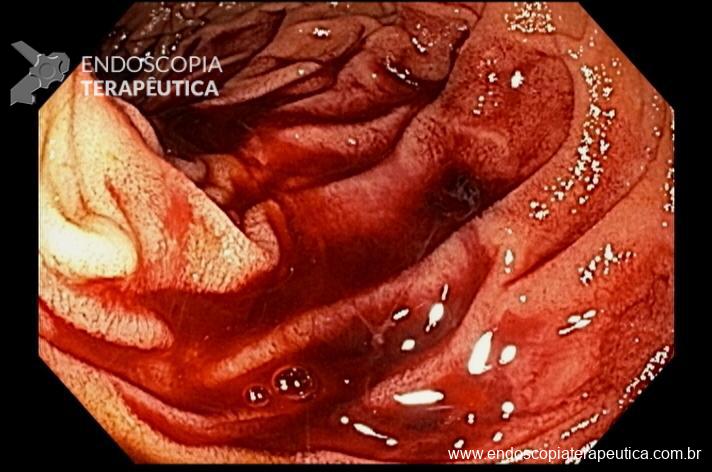
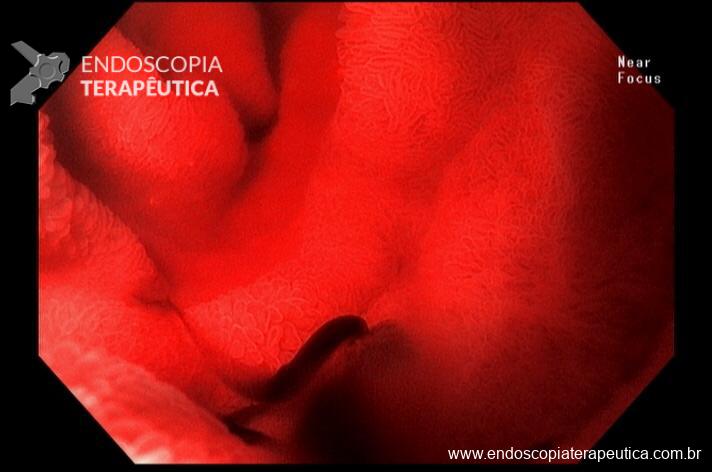
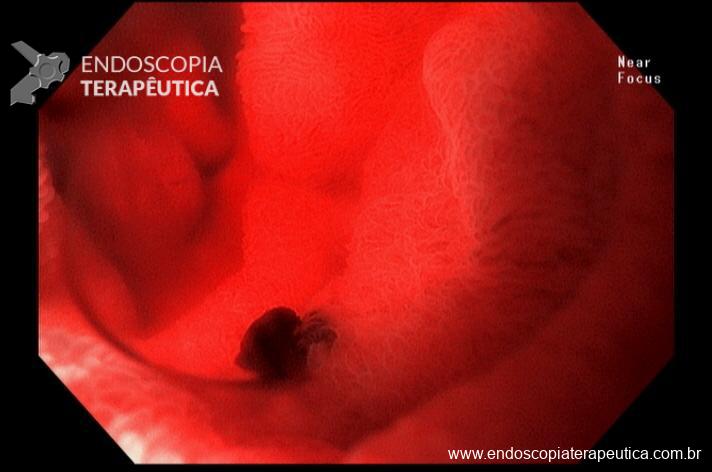
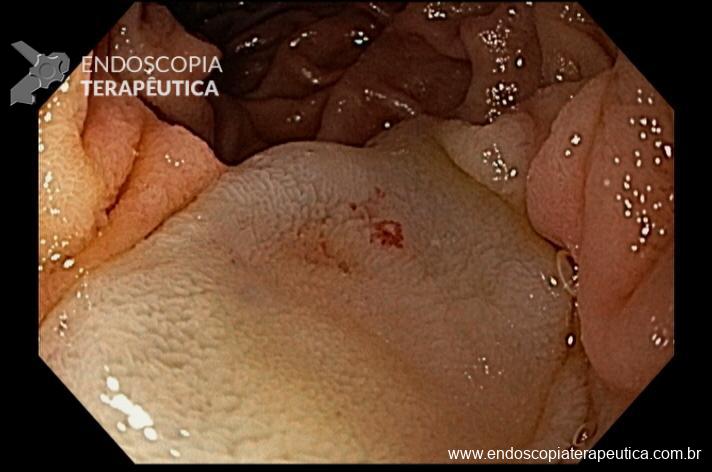
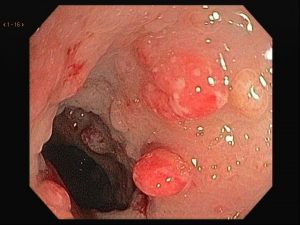
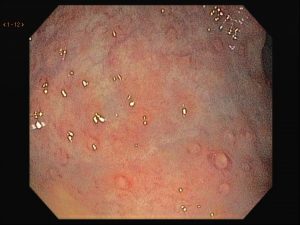
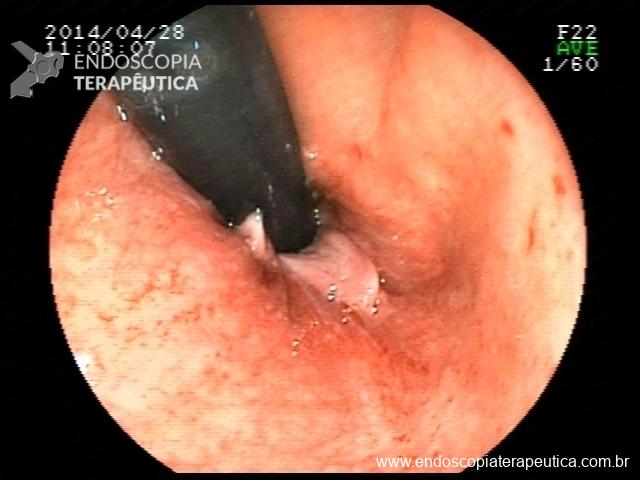
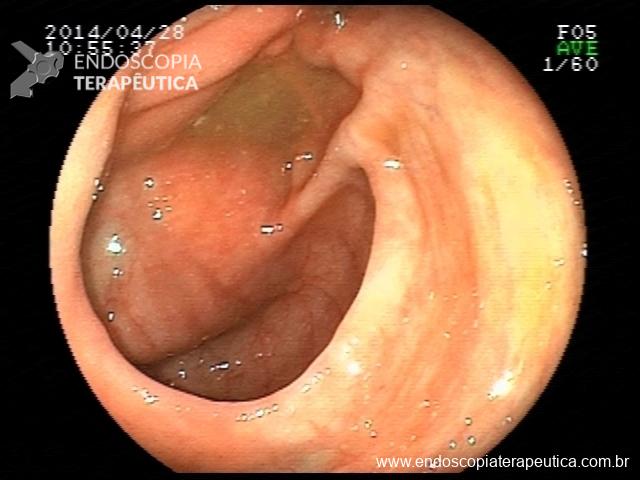
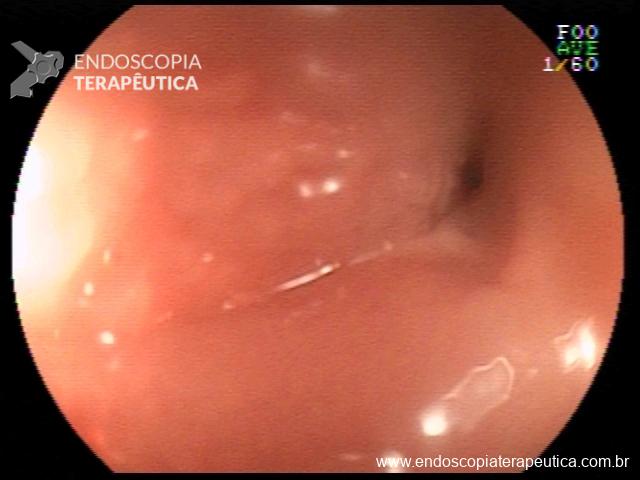
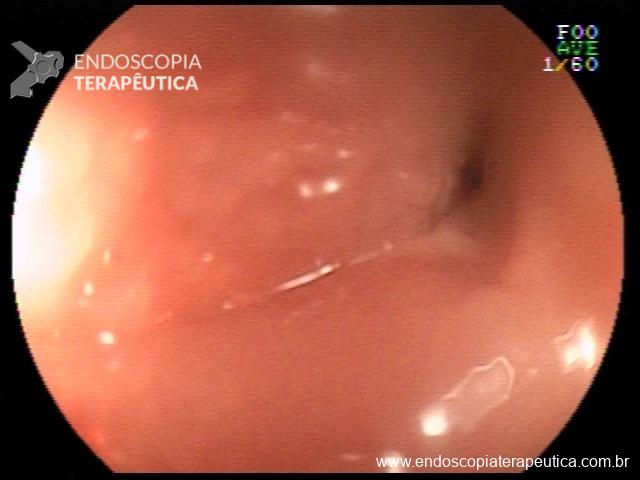
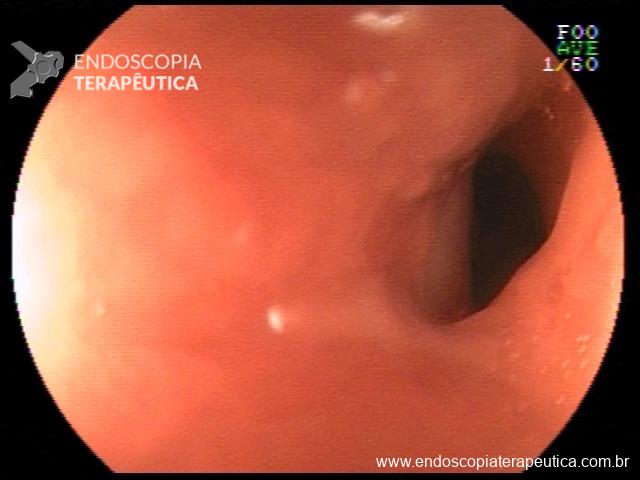
Houve persistência do quadro, sendo realizada ecoendoscopia em julho de 2020 para afastar causas obstrutivas, com achado de região hipoecogênica, heterogênea, limites irregulares, medindo 2,5 x 1,5 cm na cabeça pancreática (Figura 1), sem dilatação de colédoco à montante (5,8 mm).
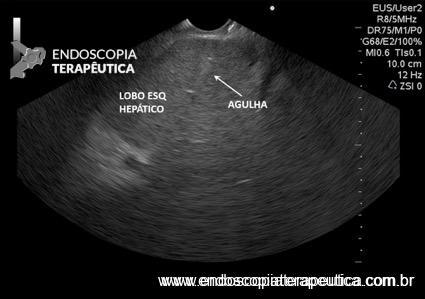
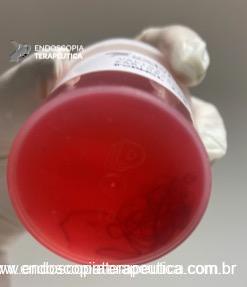
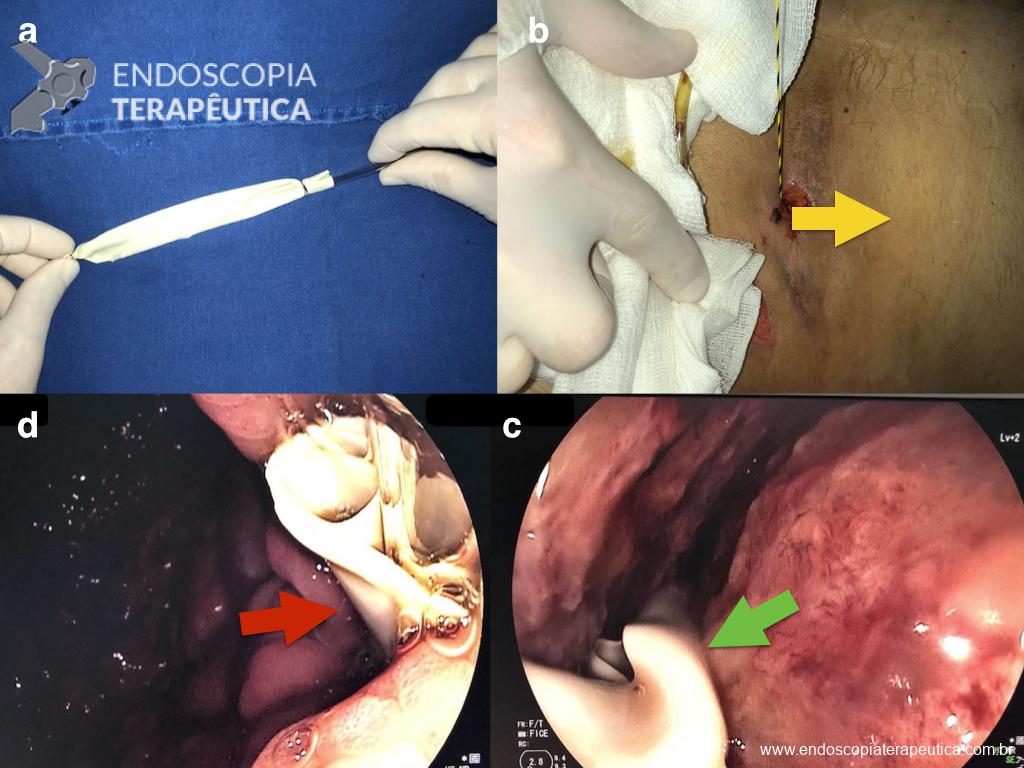
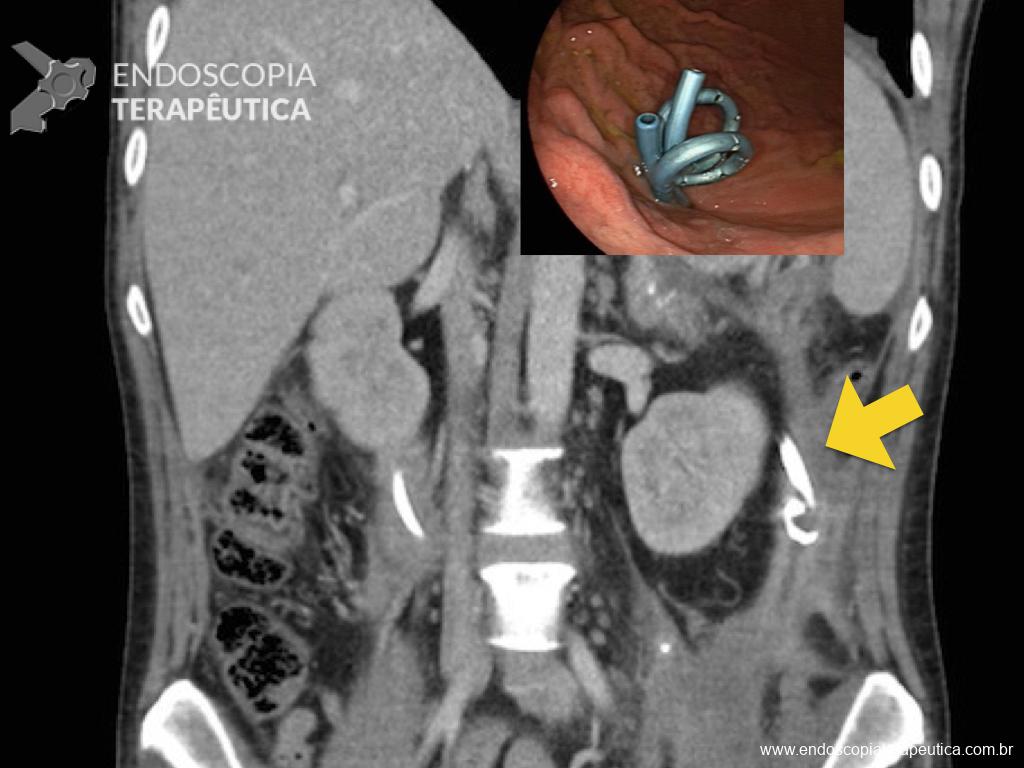
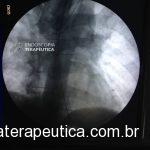
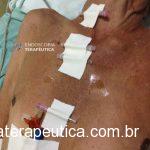
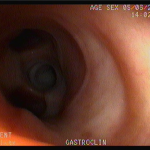
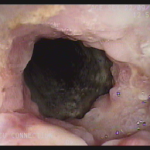
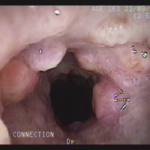
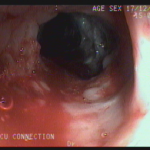
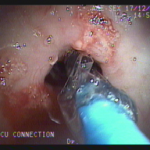
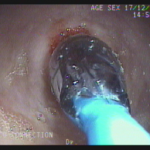
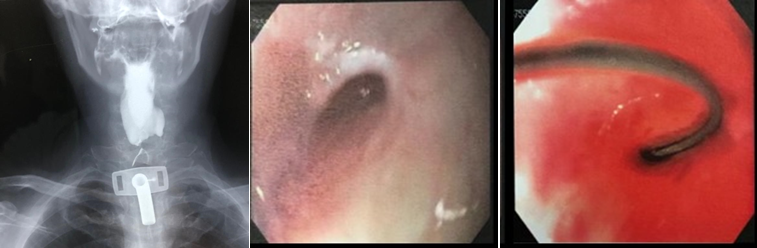
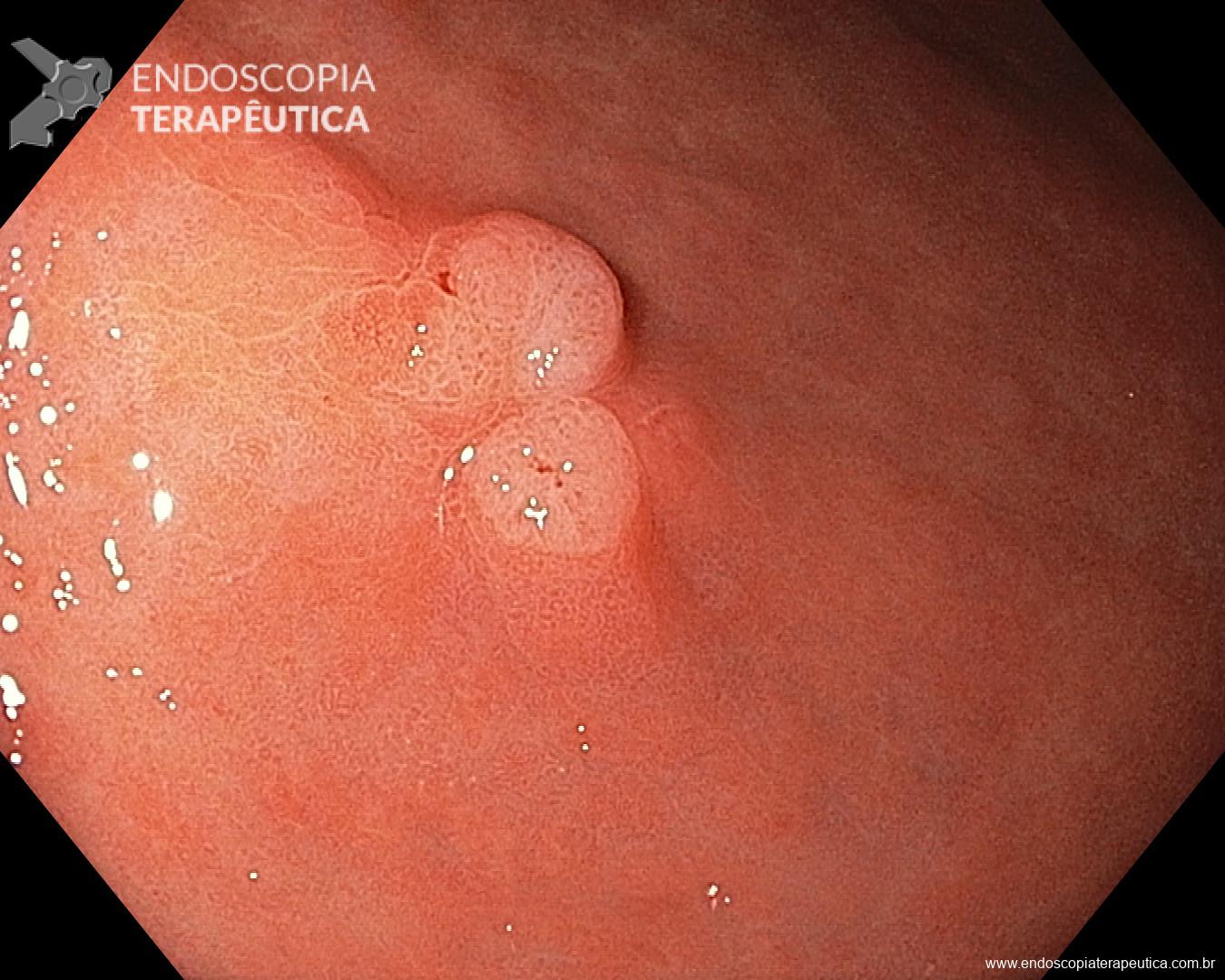
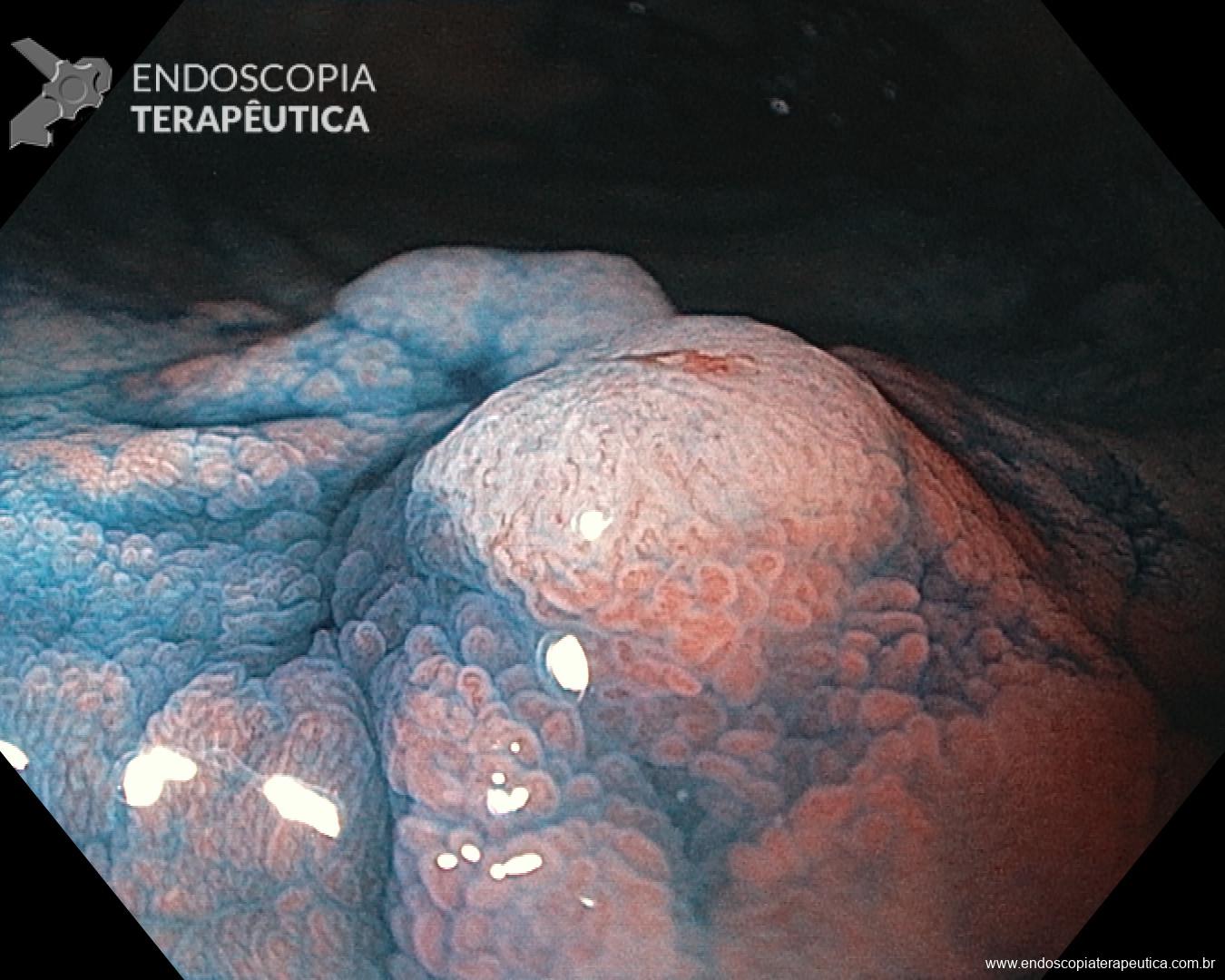
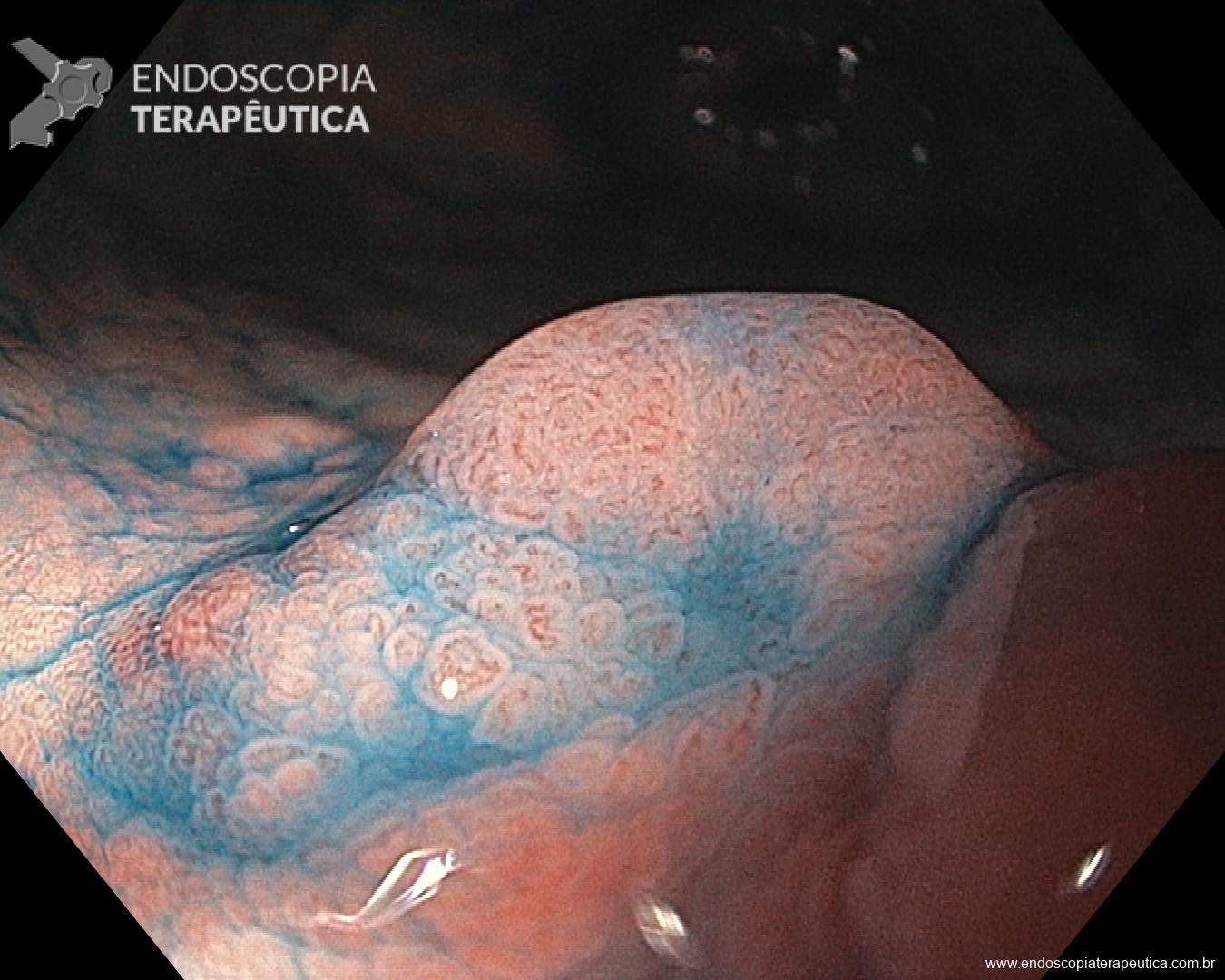
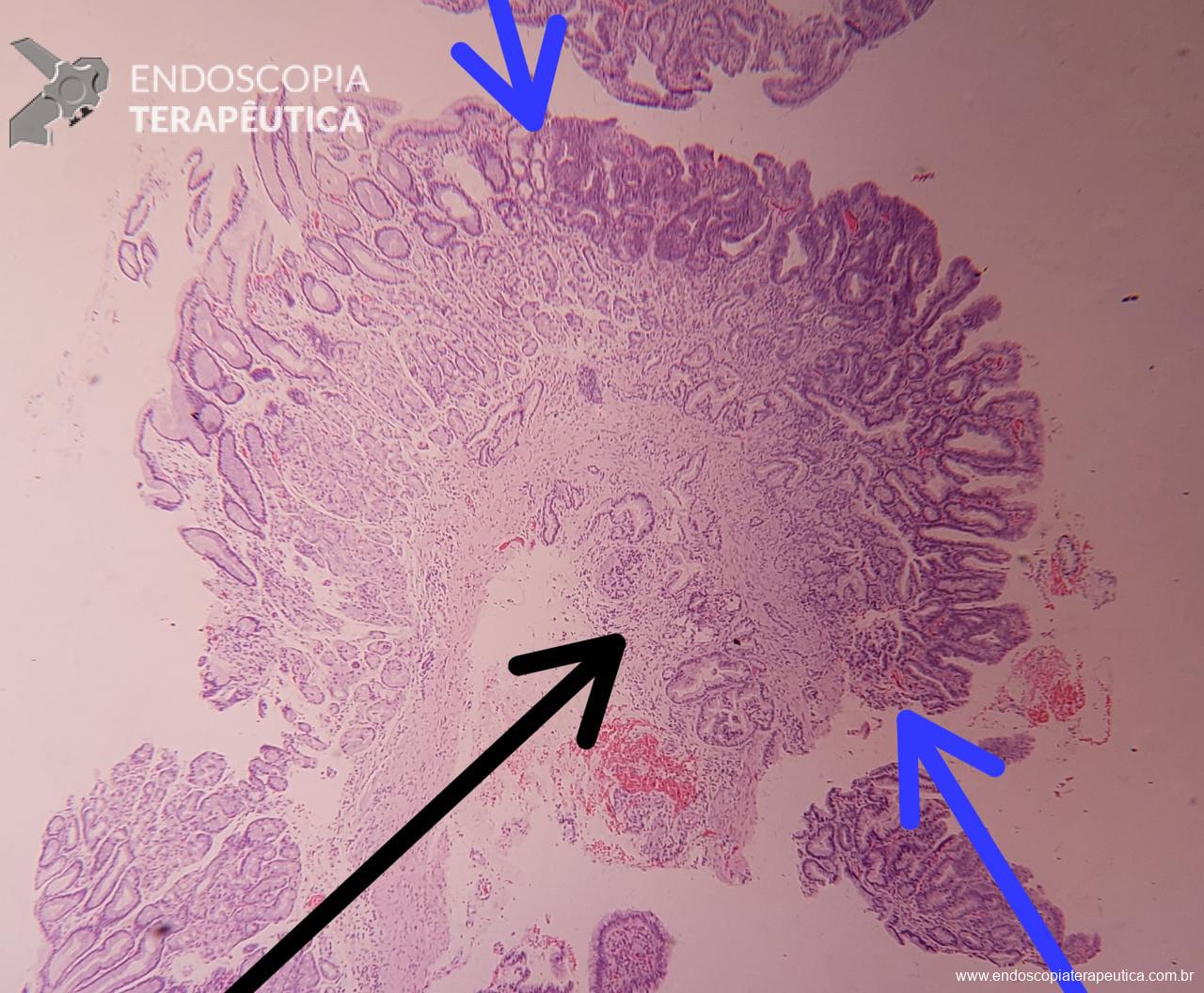
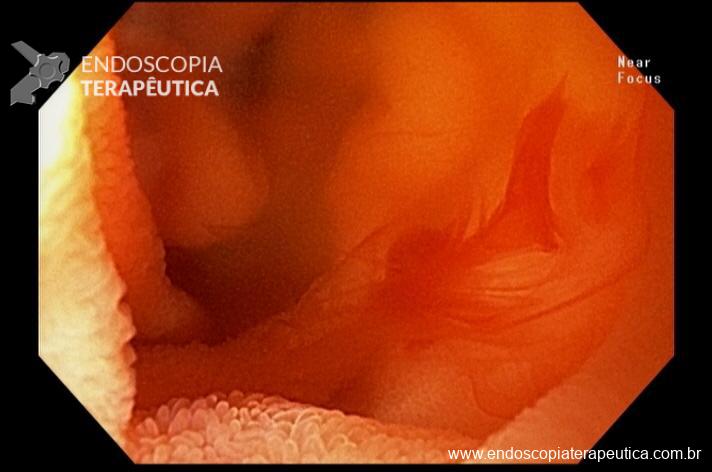
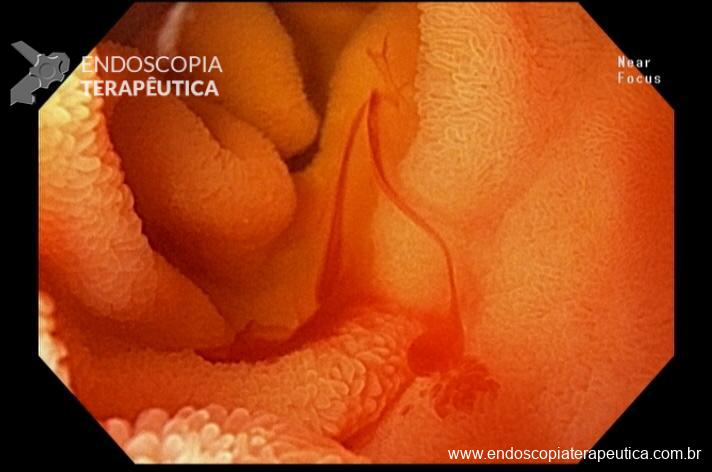
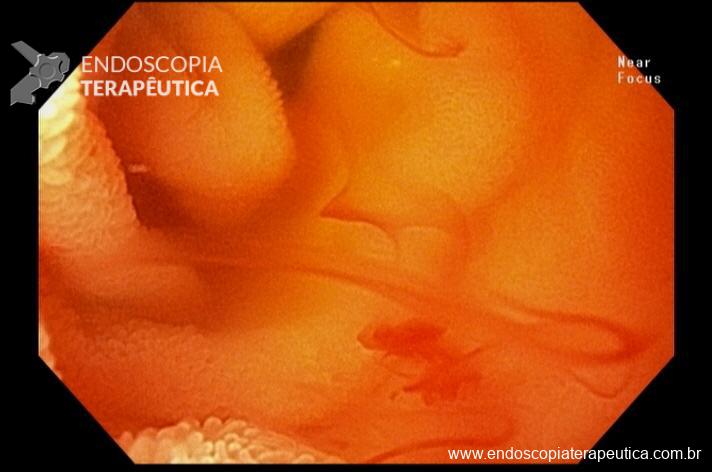
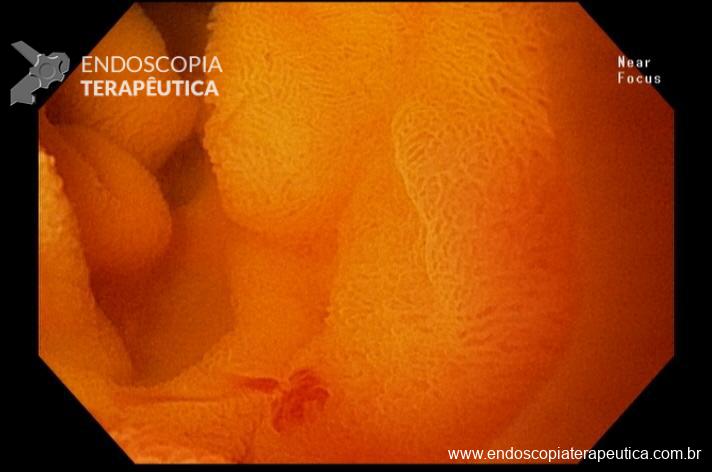
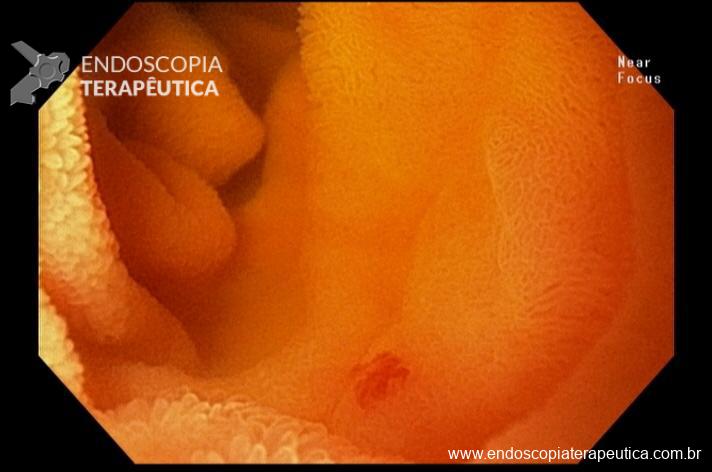
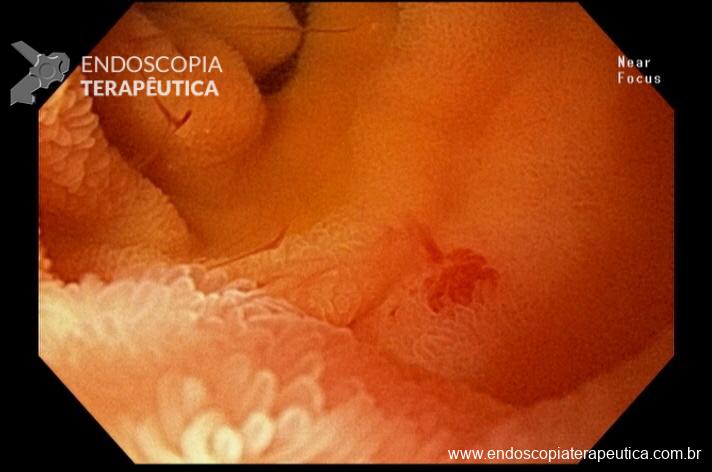
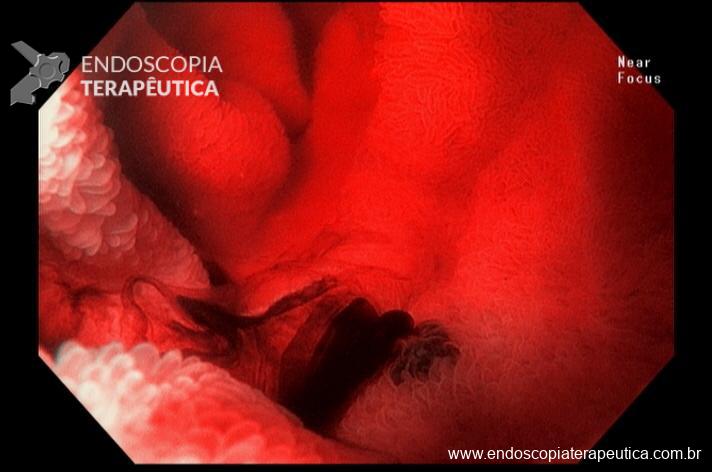
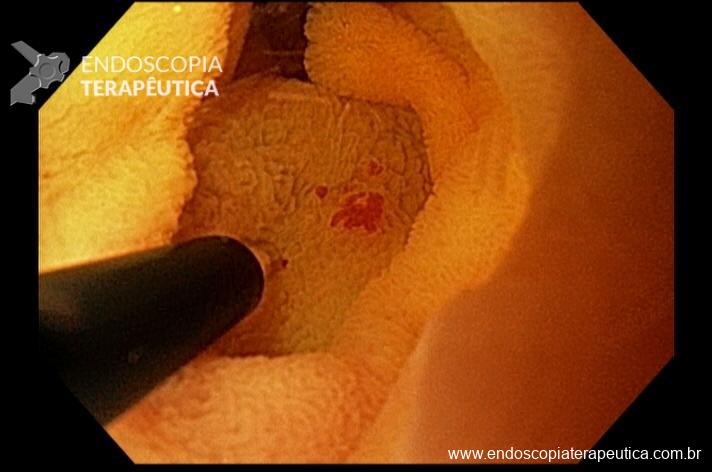
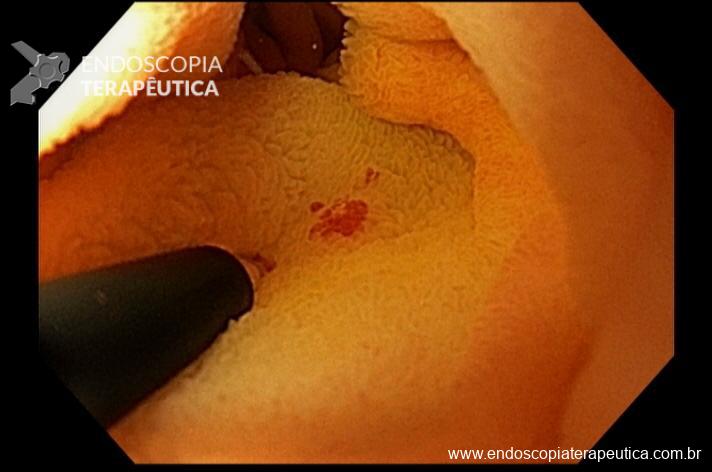
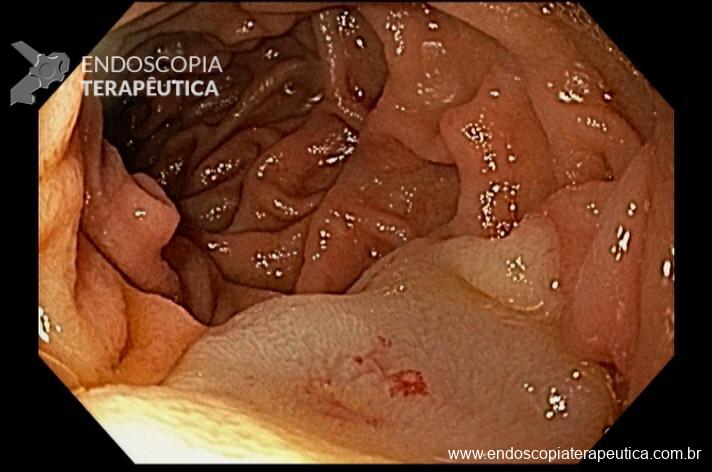
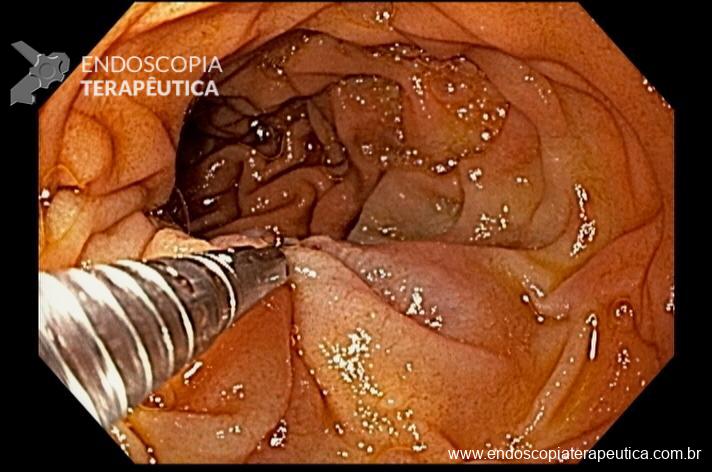
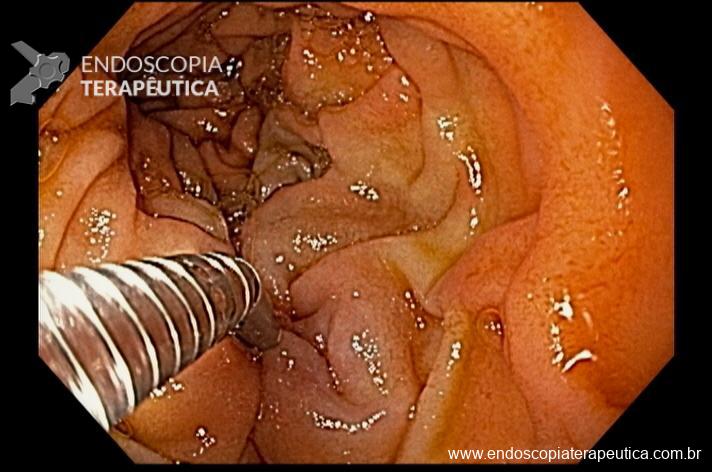
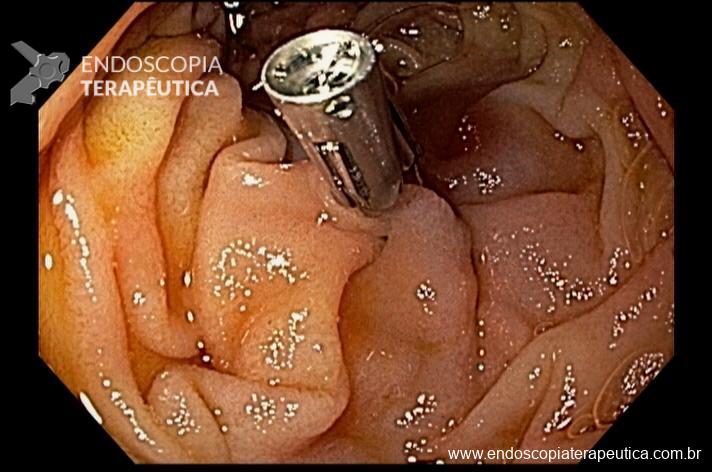
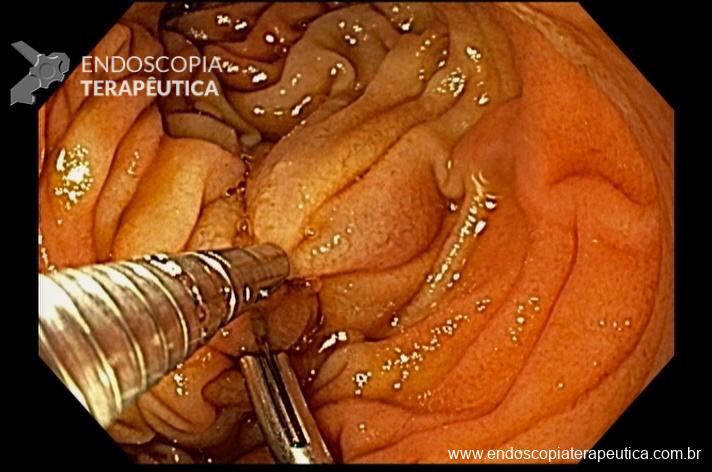
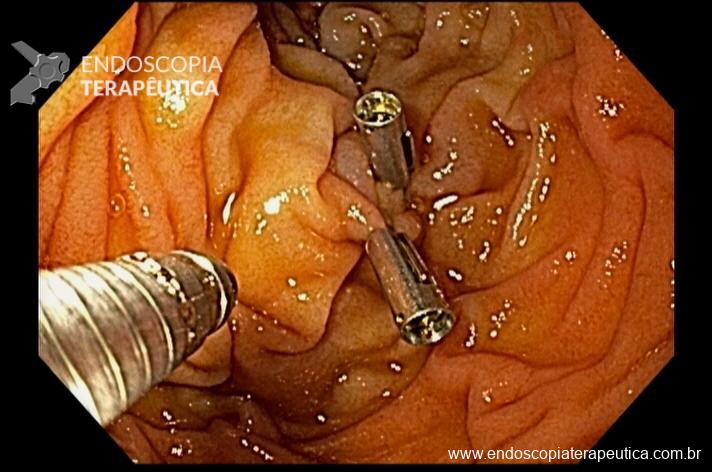
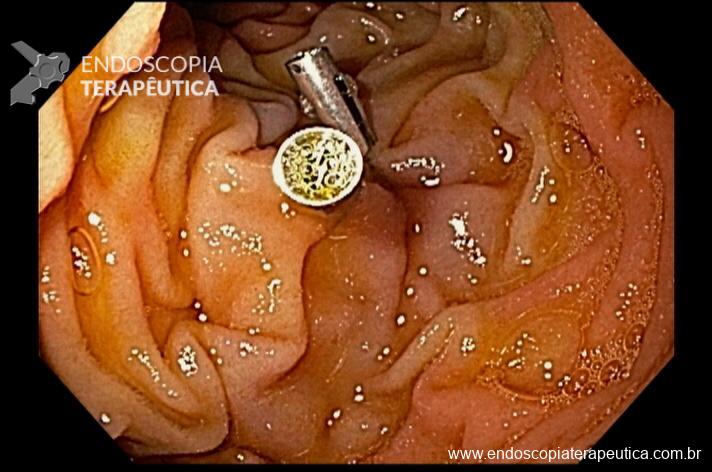
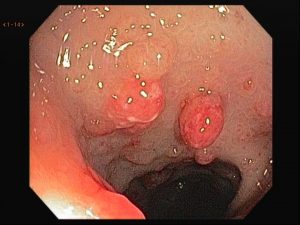
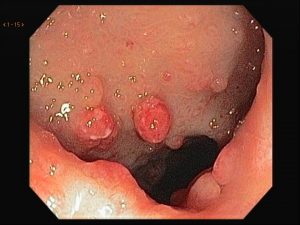
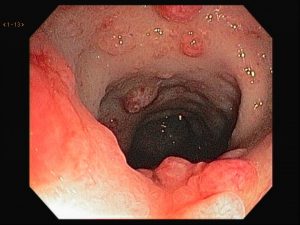
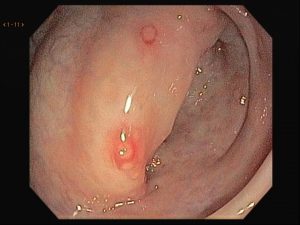
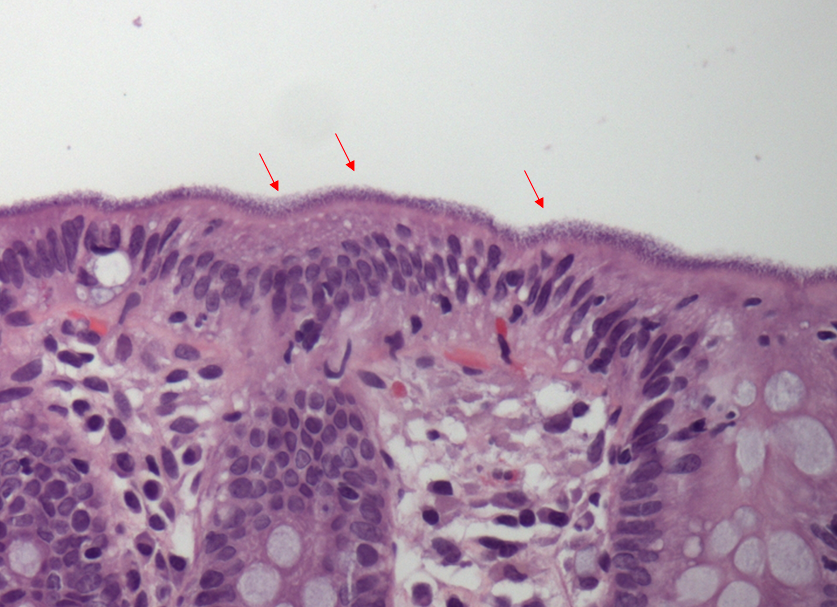
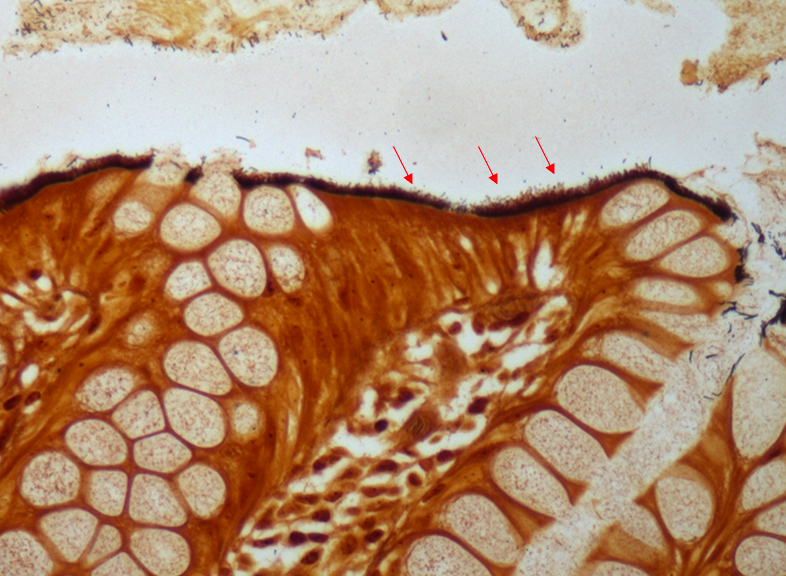
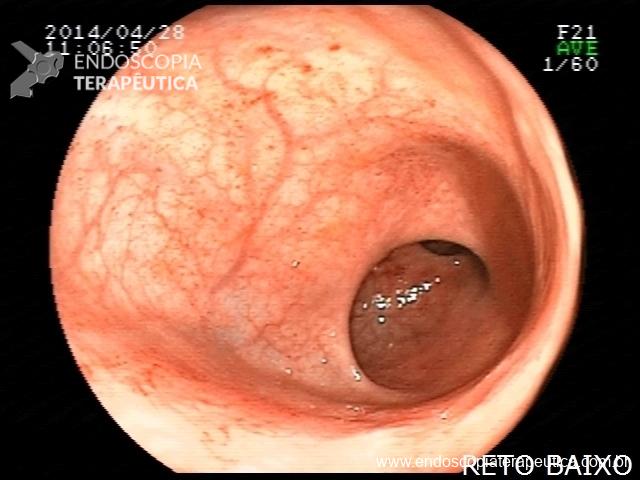
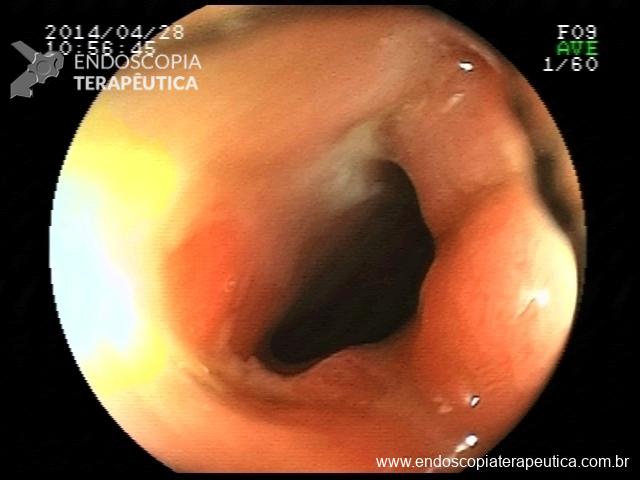
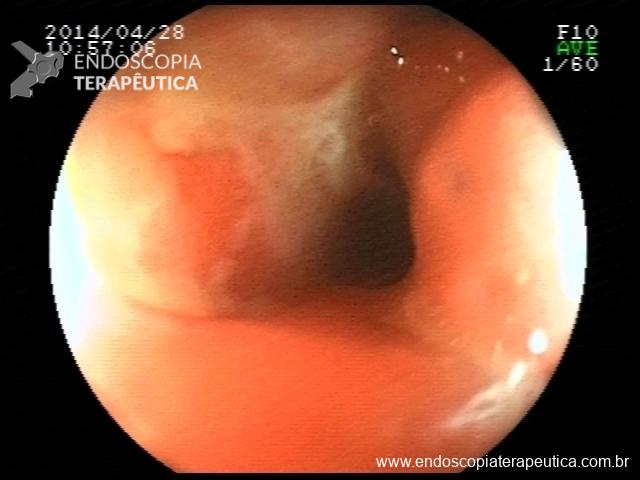
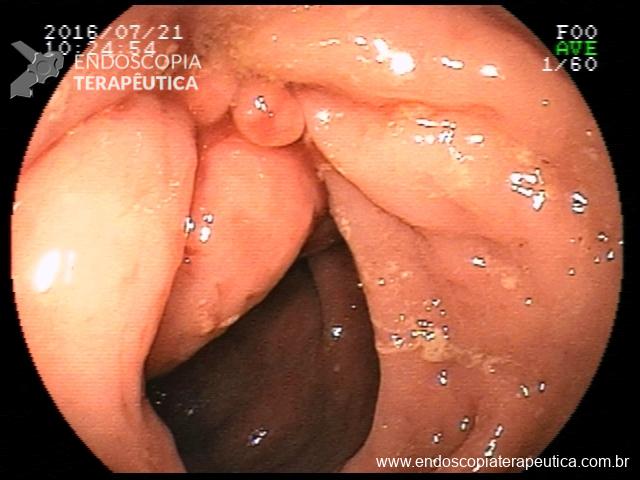
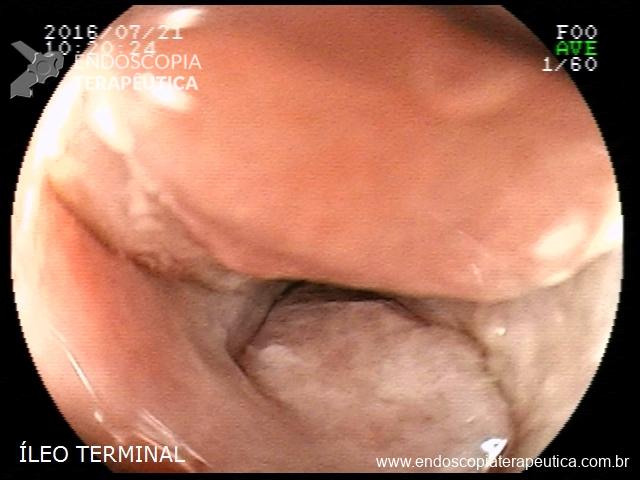
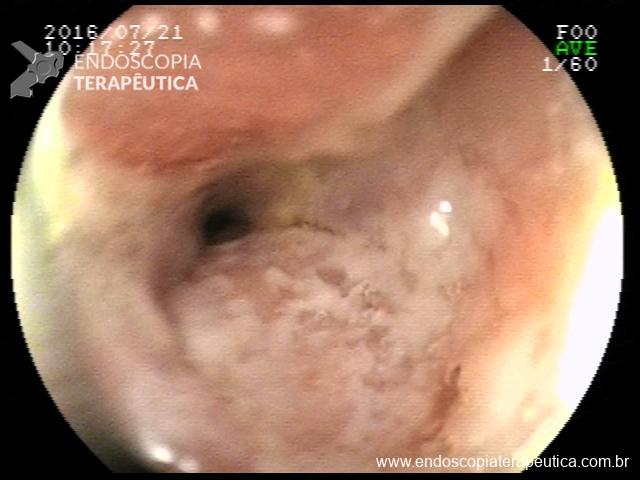
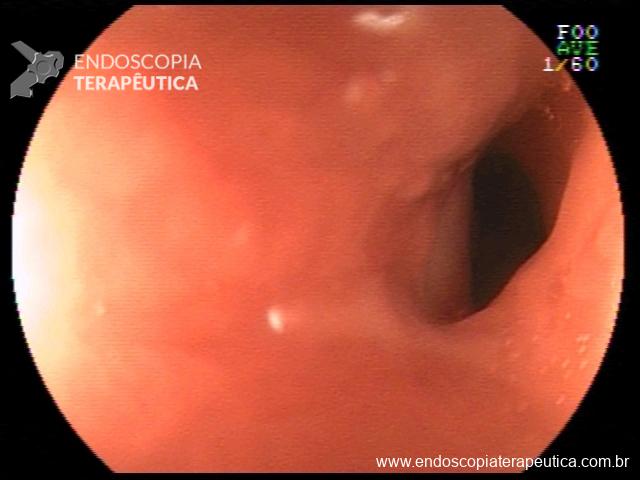
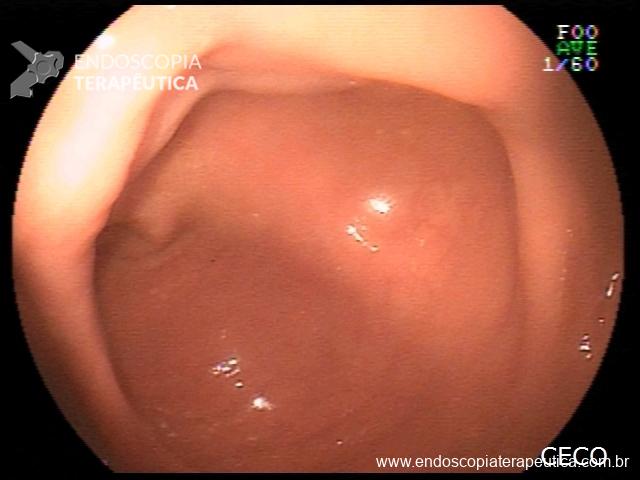
Realizada punção com agulha de biópsia (FNB) de 20G da lesão pancreática e, no mesmo procedimento, biópsia de lobo esquerdo hepático (Figura 2). Para a biópsia hepática, foi utilizada também uma agulha de FNB de 20G, 2 passagens, com 3 oscilações lentas em cada, sem uso de vácuo. Obtida quantidade satisfatória de material (Figura 3). Não houve intercorrências durante ou após o procedimento.
Anatomopatológico da lesão pancreática revelou tecido acinar pancreático sem atipias e do fígado hepatopatia crônica colestática padrão biliar, com fibrose grau 2 e colestase moderada/acentuada, compatível com ação medicamentosa.
Iniciado uso de ácido ursodesoxicólico, com melhora inicial do quadro clínico-laboratorial.
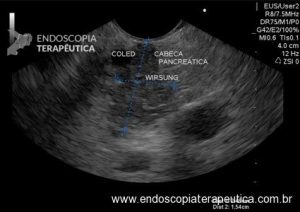
Figura 1. Região hipoecogênica, heterogênea, limites irregulares, medindo 2,5 x 1,5 cm, localizada na cabeça pancreática.
Discussão
A biópsia hepática é ferramenta útil no diagnóstico e estadiamento de doenças do fígado como hepatites virais, doença hepática gordurosa associada a disfunção metabólica e hepatopatias autoimunes. Apesar do avanço de técnicas não invasivas como a elastografia hepática, estas permitem o estadiamento apenas do grau de fibrose, não fornecendo dados importantes para confirmação etiológica a avaliação do grau de atividade inflamatória, por exemplo.
As vias mais utilizadas para biópsia hepática são a percutânea, cirúrgica e transjugular. Cada uma delas possui limitações e riscos importantes como dor abdominal, sangramento, complicações da anestesia geral (biópsia cirúrgica) e alto custo (biópsia transjugular).
A biópsia hepática por ecoendoscopia vem ganhando espaço nos últimos anos, com publicações recentes de séries de casos com mais de 200 pacientes e metanálises incluindo mais de 400 pacientes. Tem como potenciais vantagens:
- Maior conforto para o paciente.
- Maior facilidade técnica em pacientes obesos (comparada com a via percutânea).
- Possibilidade de avaliação endoscópica simultânea para rastreamento de varizes.
- Realização simultânea de medida do gradiente de pressão venosa hepática por ecoendoscopia.
A eficácia em se obter material adequado para análise histológica na biópsia hepática por ecoendoscopia é de 93,9 a 100%. O comprimento médio total dos fragmentos obtidos nos diferentes estudos é de 2,4 a 5,5 cm (com fragmentos únicos de 0,4 a 1,1 cm) e o número médio de espaços porta obtidos de 21 a 42. A biópsia dos dois lobos hepáticos está associada a maior comprimento da amostra e maior número de espaços porta.
Em relação às complicações
- O índice médio dos estudos é de 2,3%, que é comparável àquele descrito para os outros métodos de biópsia hepática.
- O evento adverso mais comum é a dor abdominal (2 a 15%), na quase totalidade dos casos leve e de resolução espontânea.
- Há descrição de sangramento em cerca de 1,2% dos pacientes e raros casos de febre e sangramento fatal (este último ocorrido em um paciente crítico).
A biópsia hepática por ecoendoscopia pode ser feita com agulhas de punção aspirativa (FNA) de 19G, bem como agulhas de FNB de 19G e 22G, com índice de sucesso semelhante. A punção pode ser feita no lobo hepático esquerdo (via transgástrica) e/ou direito (via transduodenal) geralmente sem vácuo, 1 a 3 passagens, 3 a 4 oscilações, utilizando-se o Doppler para evitar vasos no trajeto. A retirada do fragmento da agulha pode ser feita com estilete ou flush com heparina, com cuidado para não curvar a agulha e fragmentar a amostra, que deve ser colocada em formalina 10%.
A principal limitação para a maior utilização da biópsia hepática por ecoendoscopia no Brasil é seu maior custo comparado à via mais utilizada (percutânea). Porém, em casos em que a ecoendoscopia está indicada por outros motivos (como o caso em questão) ou quando outras vias não são possíveis (obesidade grau 3, por exemplo), esta via parece ser factível e segura.
Para saber mais sobre este tema e outros relacionados, acesse o site Gastropedia clicando aqui!
Referências
- Dellatore P, Sarkar A, Rustgi VK et al. REVIEW OF ENDOSCOPIC ULTRASOUND GUIDED LIVER BIOPSY: A MULTICENTER EXPERIENCE. Pôster, DDW 2020.
- Hasan MK, Kadkhodayan K, Idrisov E et al. Endoscopic ultrasound-guided liver biopsy using a 22-G fine needle biopsy needle: a prospective study. Endoscopy 2019;51:818-824.
- Mohan BP, Shakhatreh M, Garg R et al. Efficacy and safety of EUS-guided liver biopsy: a systematic review and meta-analysis. Gastrointest Endosc 2019;89:238-46
- Bazerbachi F, Vargas EJ, Matar R et al. EUS-guided core liver biopsy sampling using a 22-gauge fork-tip needle: a prospective blinded trial for histologic and lipidomic evaluation in nonalcoholic fatty liver disease. Gastrointest Endosc 2019;90:926-32.