Pólipo hamartomatoso juvenil solitário pediátrico: relato de caso e revisão de literatura.
Paciente do sexo feminino, 4 anos de idade, apresentando episódios recorrentes de sangramento retal (hematoquezia) há 11 meses, sem instabilidade hemodinâmica ou necessidade de hemotransfusão. Histórico atual de intolerância à lactose, sem outras doenças crônicas ou cirurgias. Apesar da exclusão de lacticínios e derivados da dieta, os episódios de sangramento persistiram.
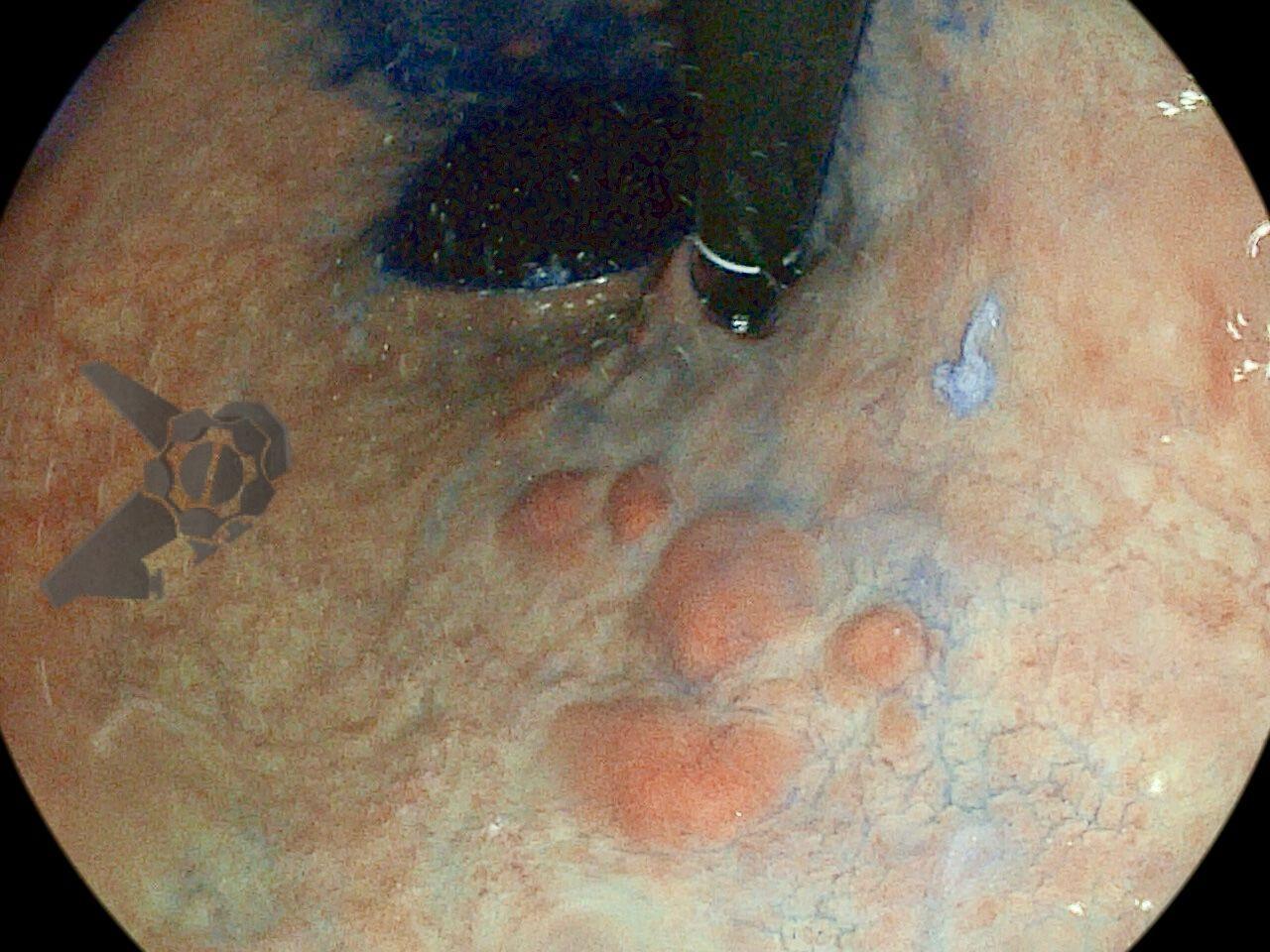
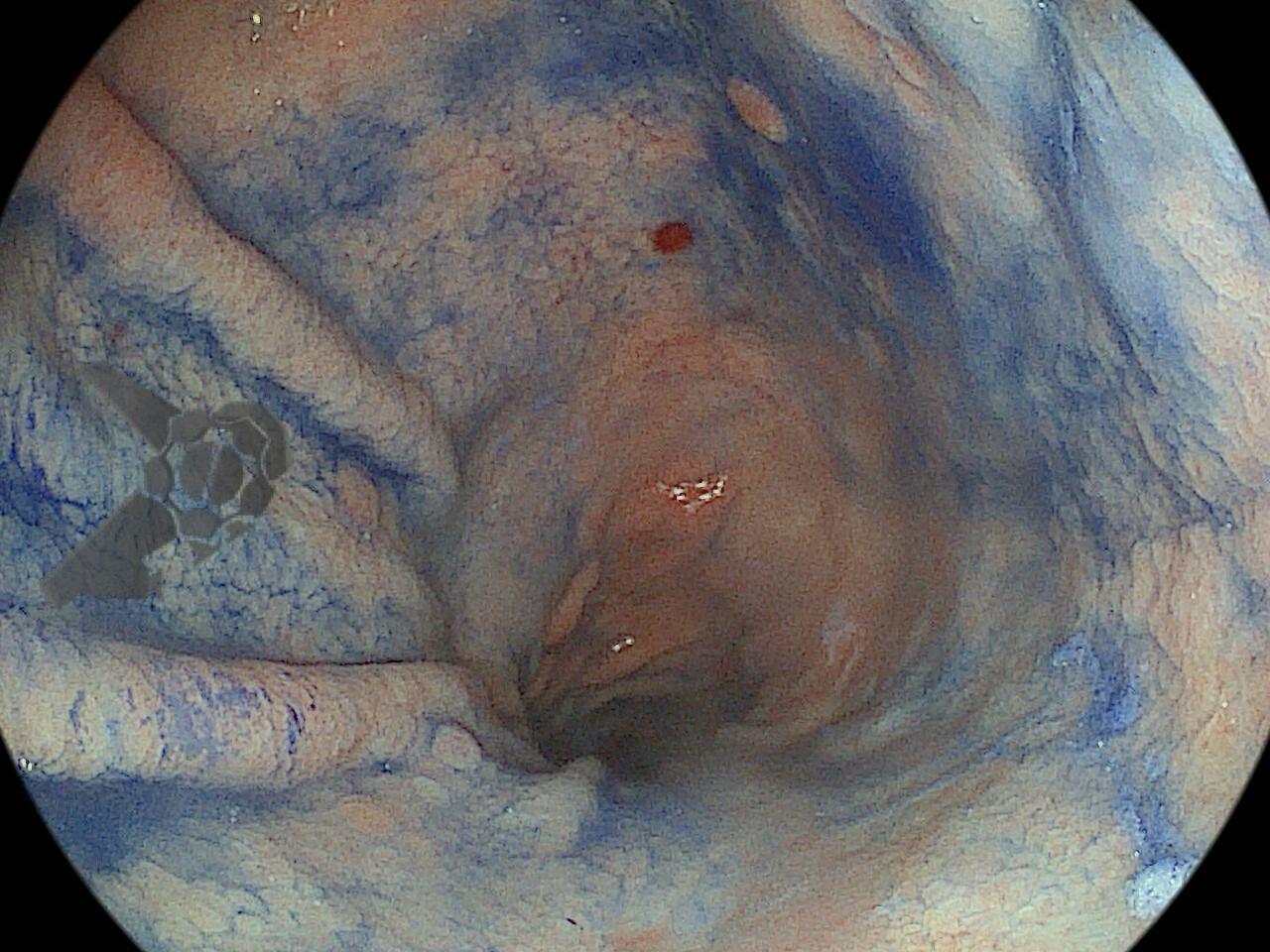
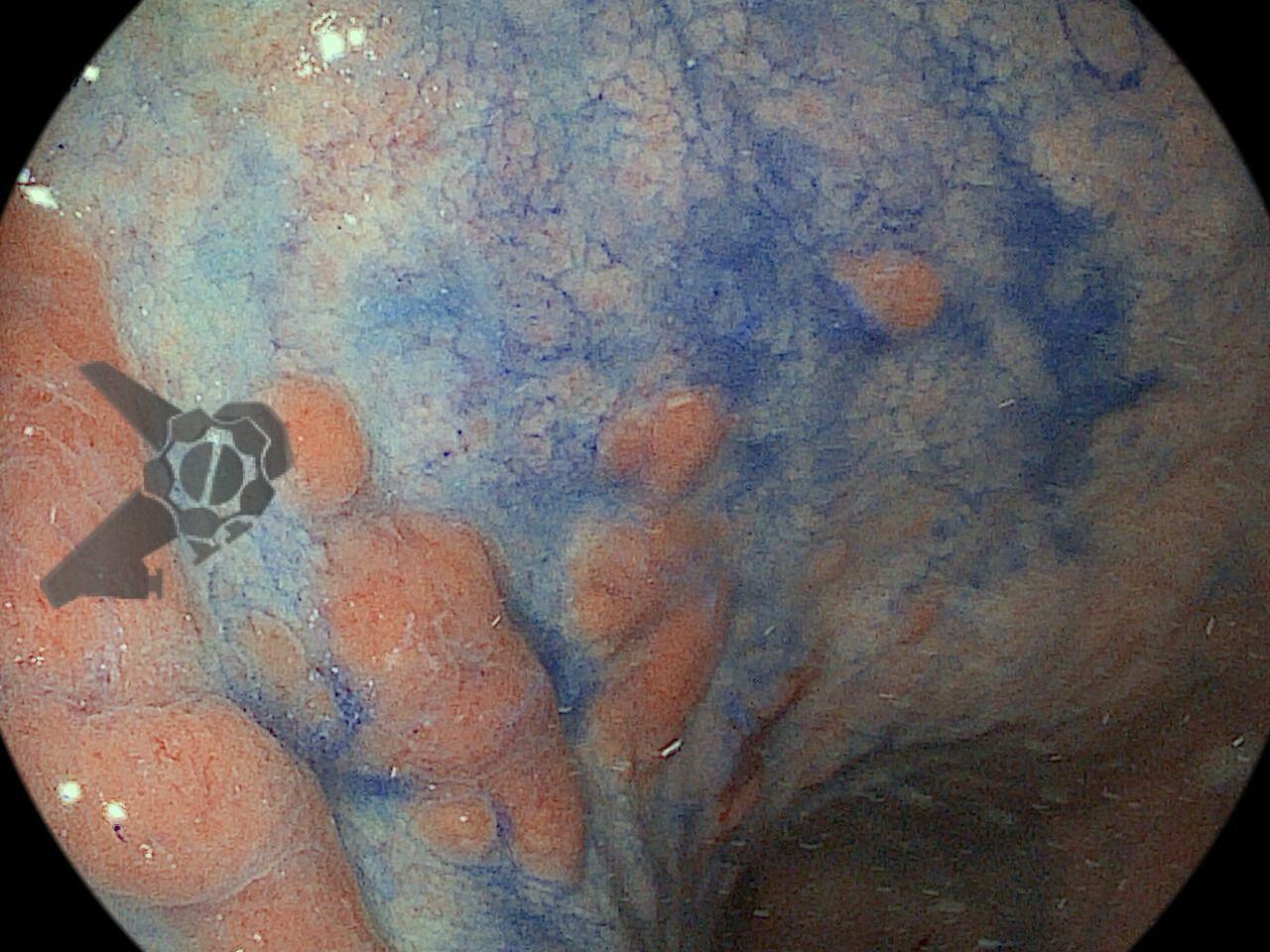
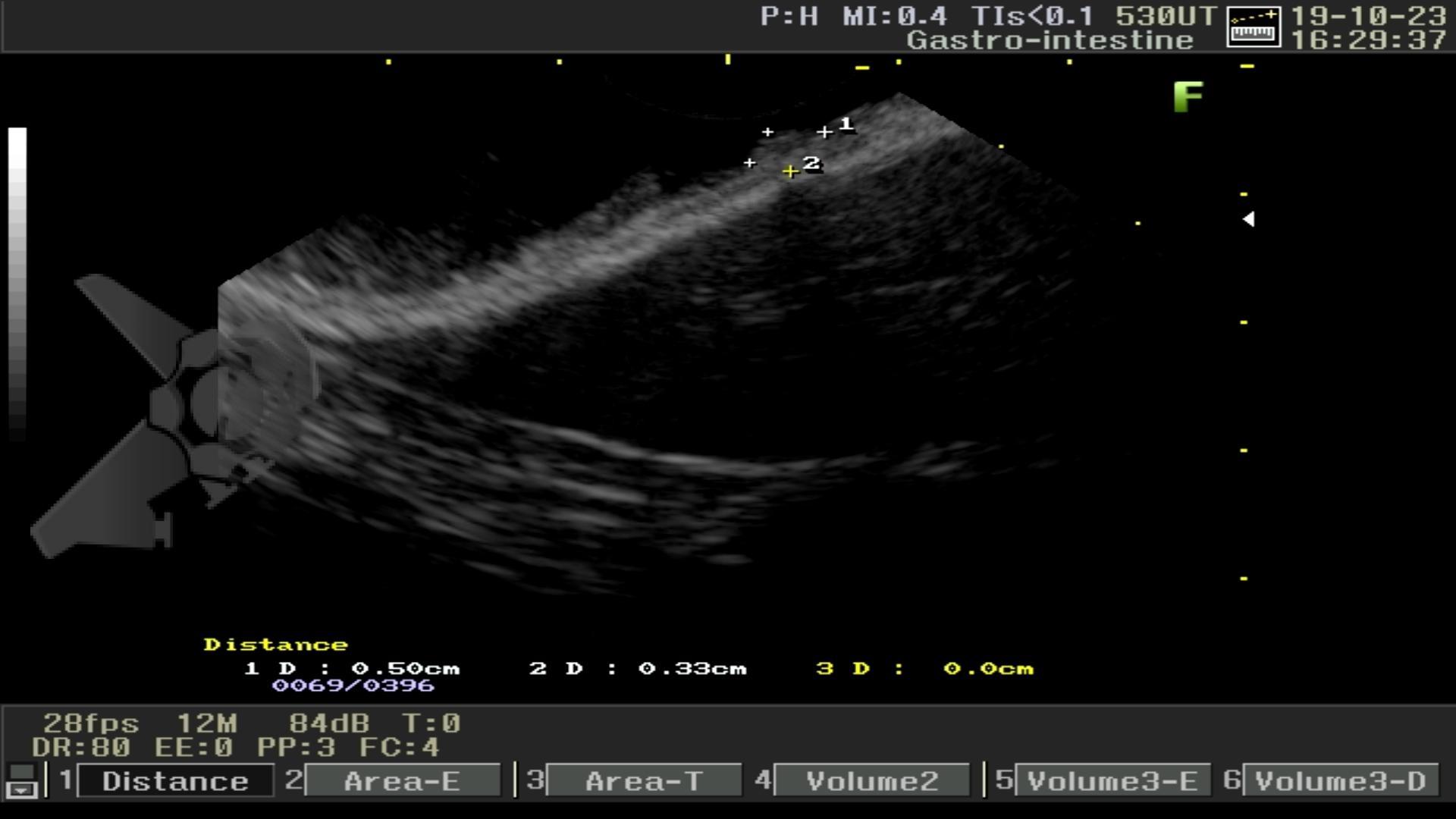
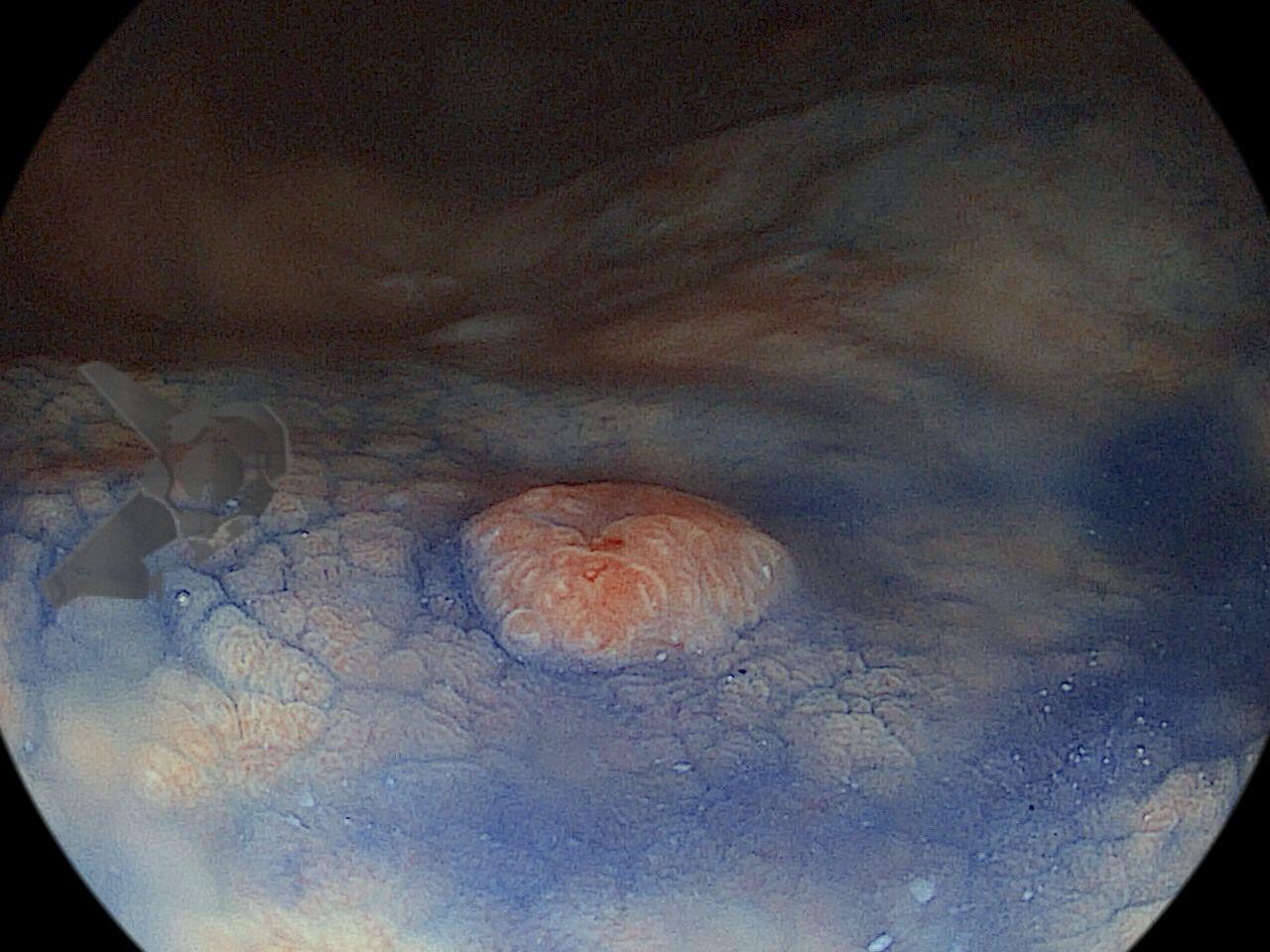
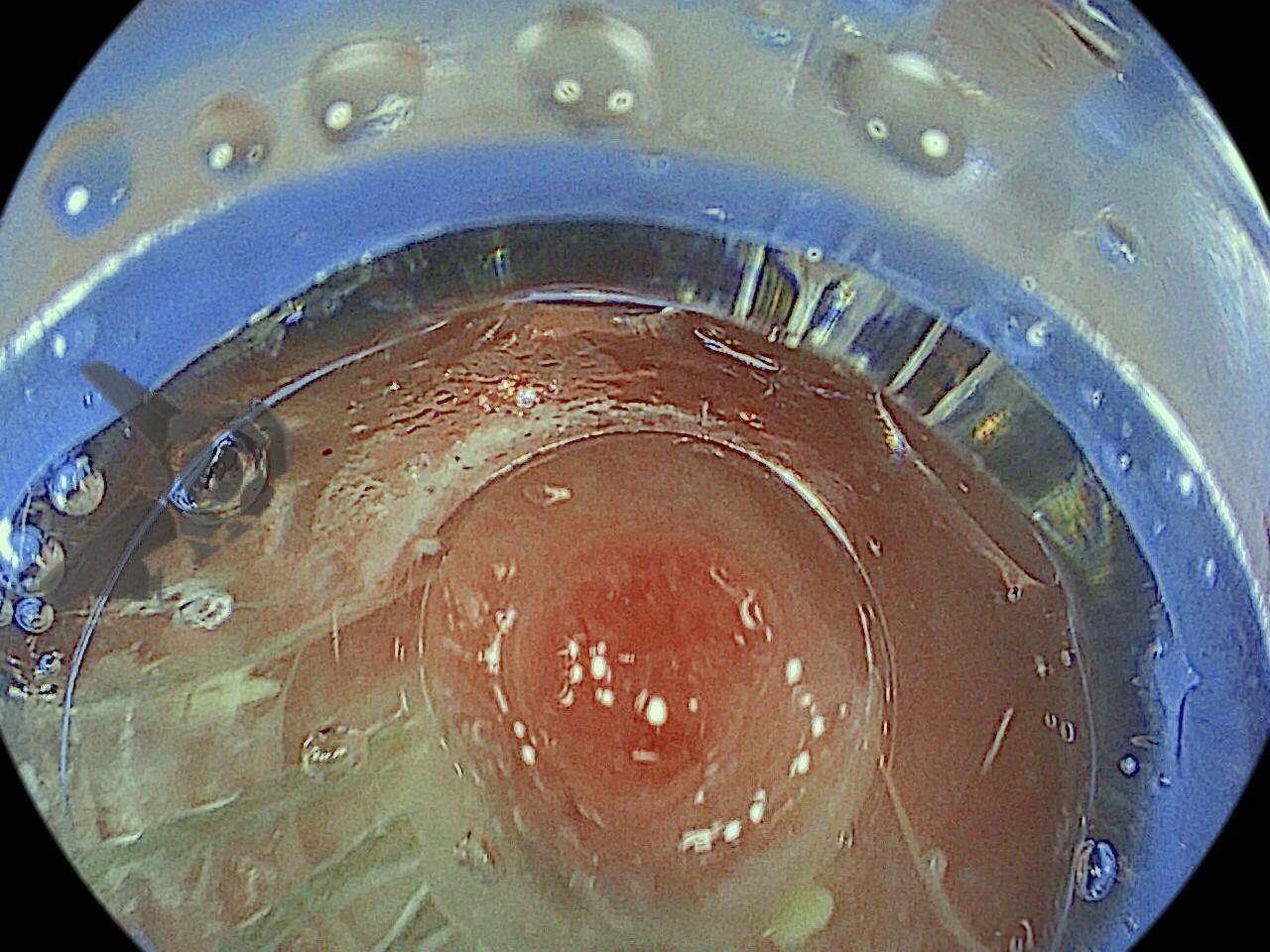
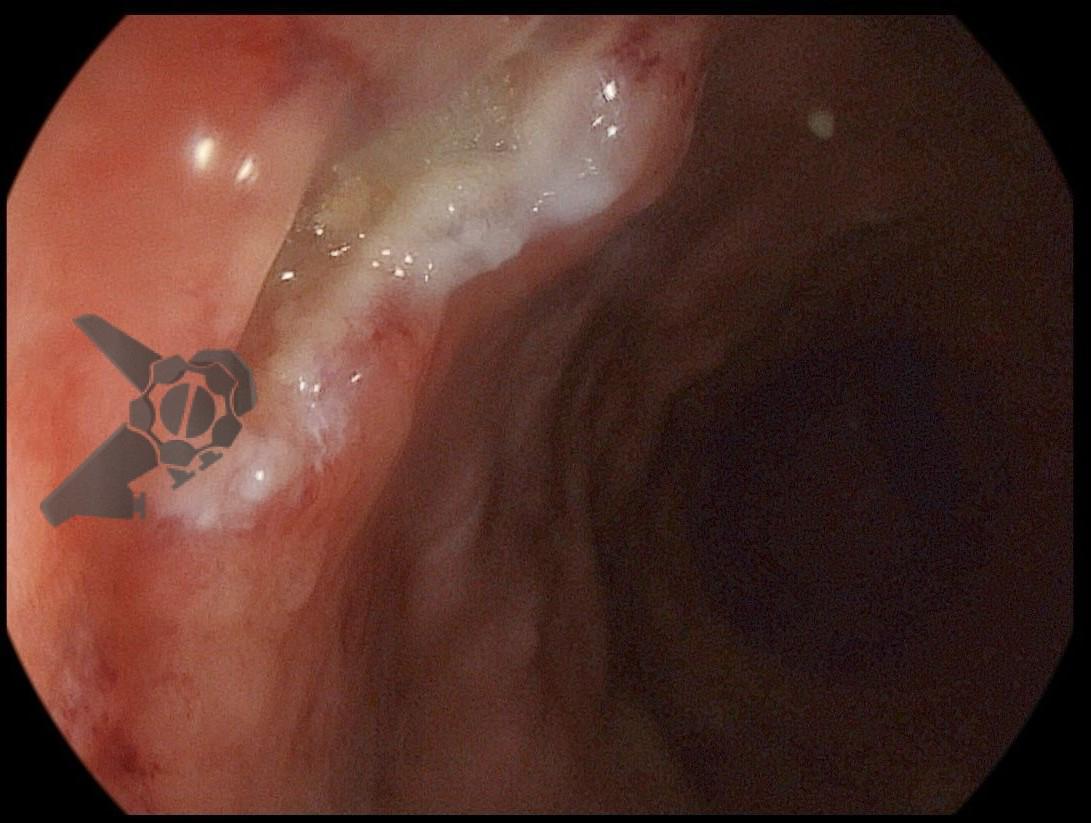
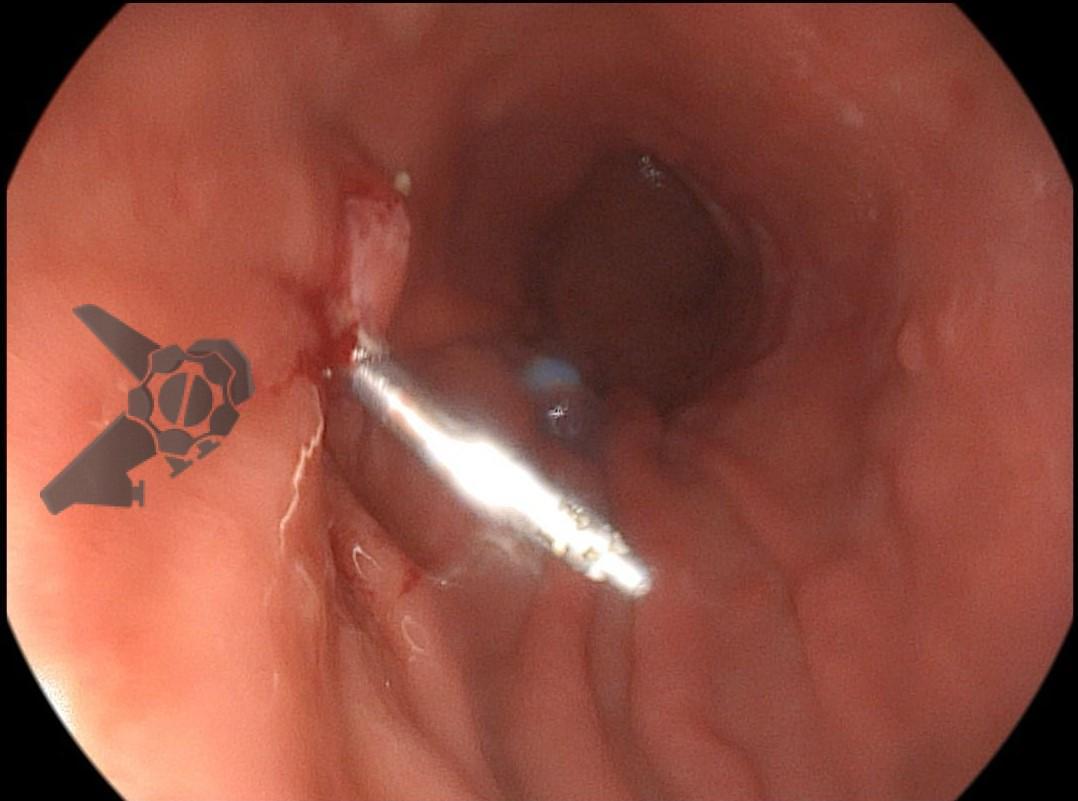
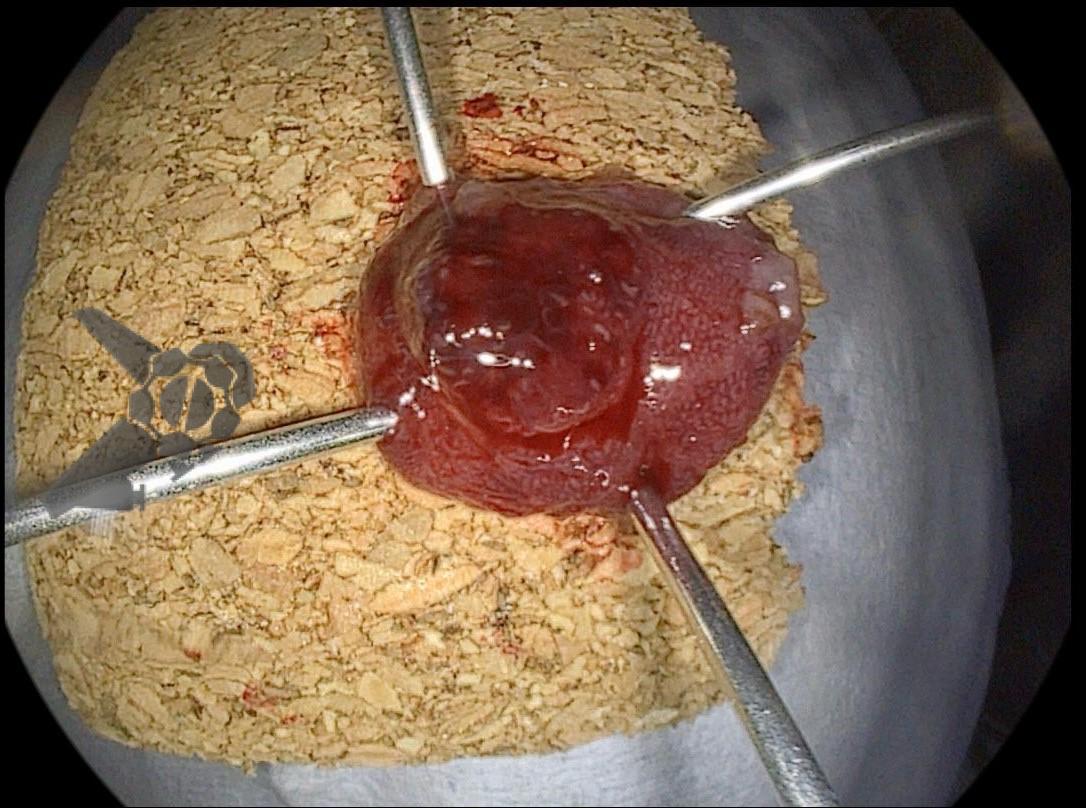
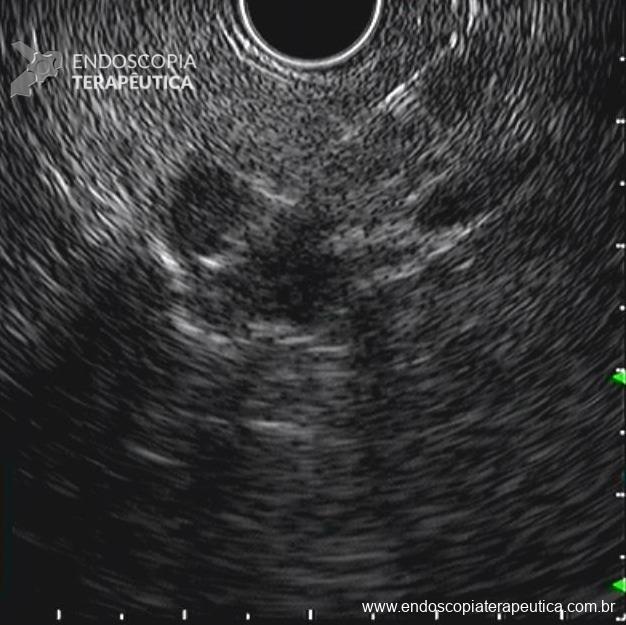
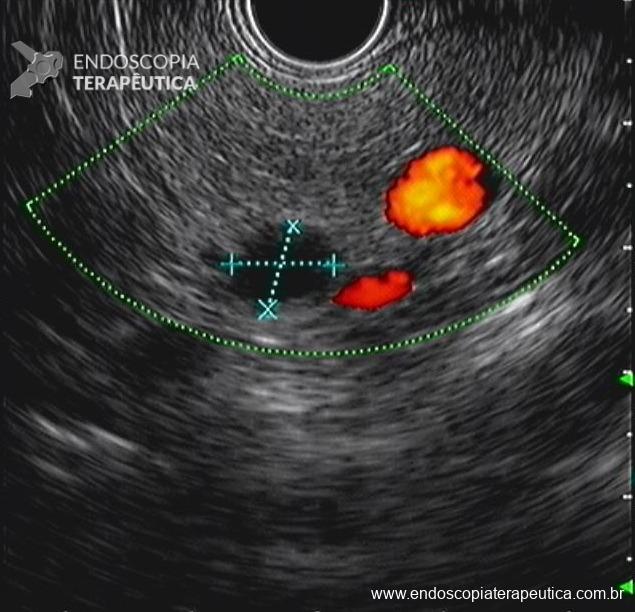
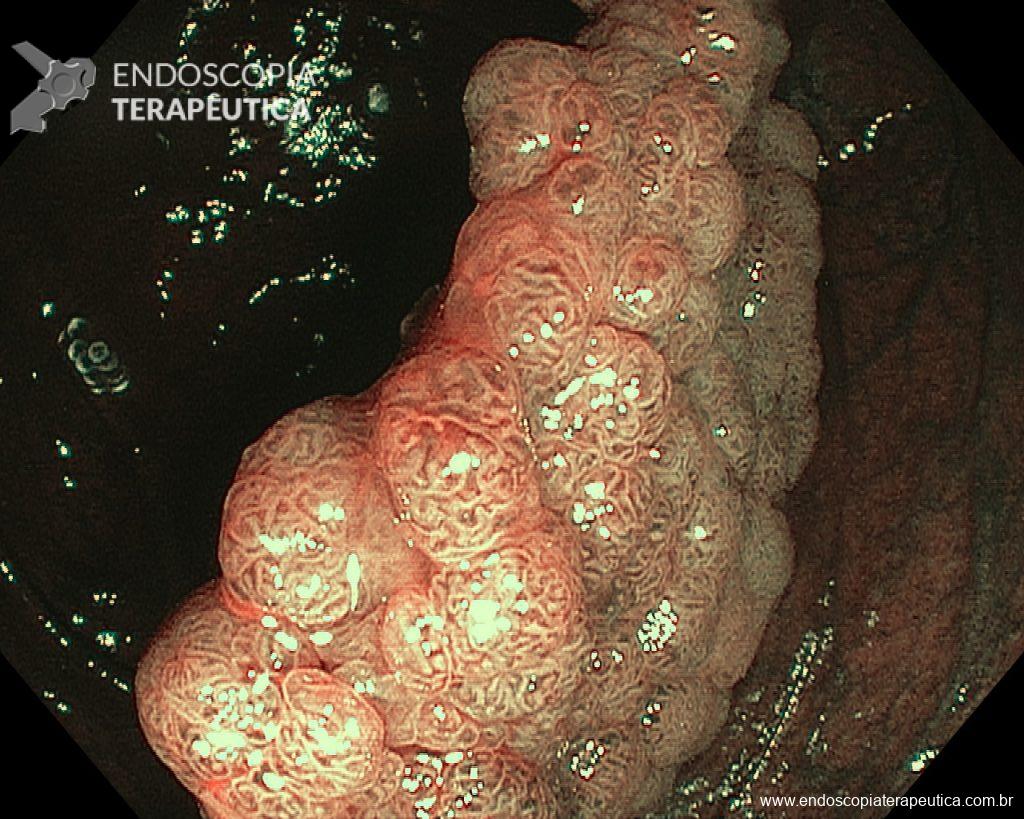
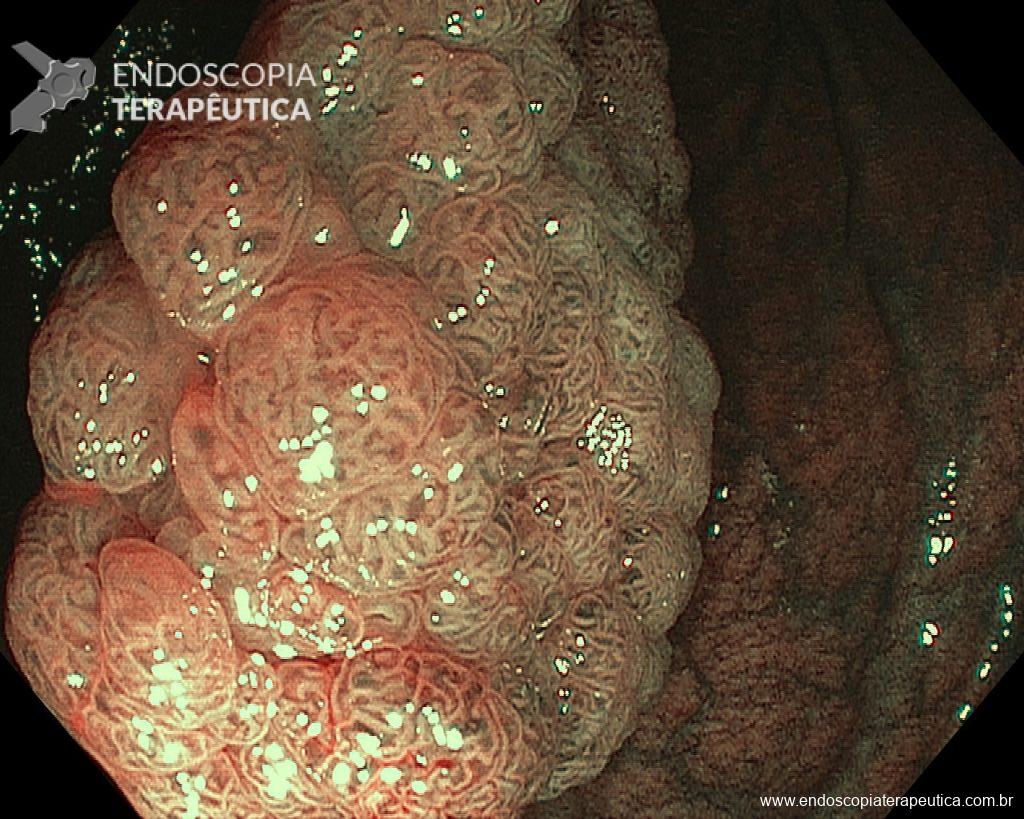
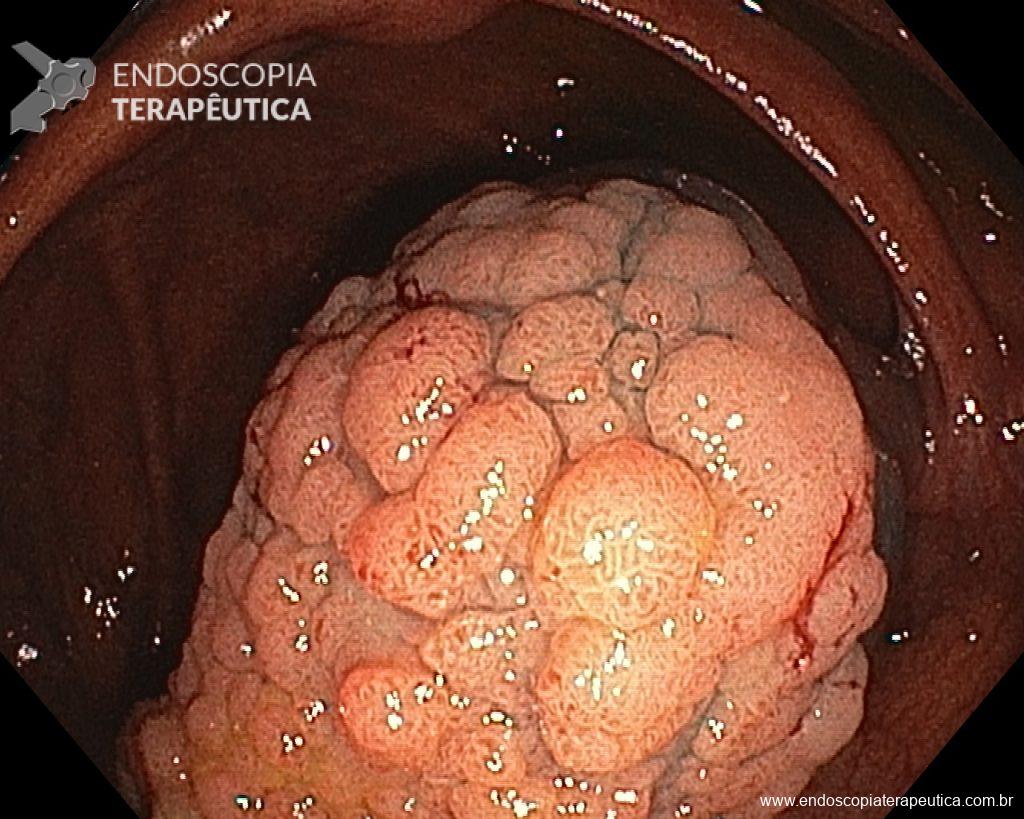
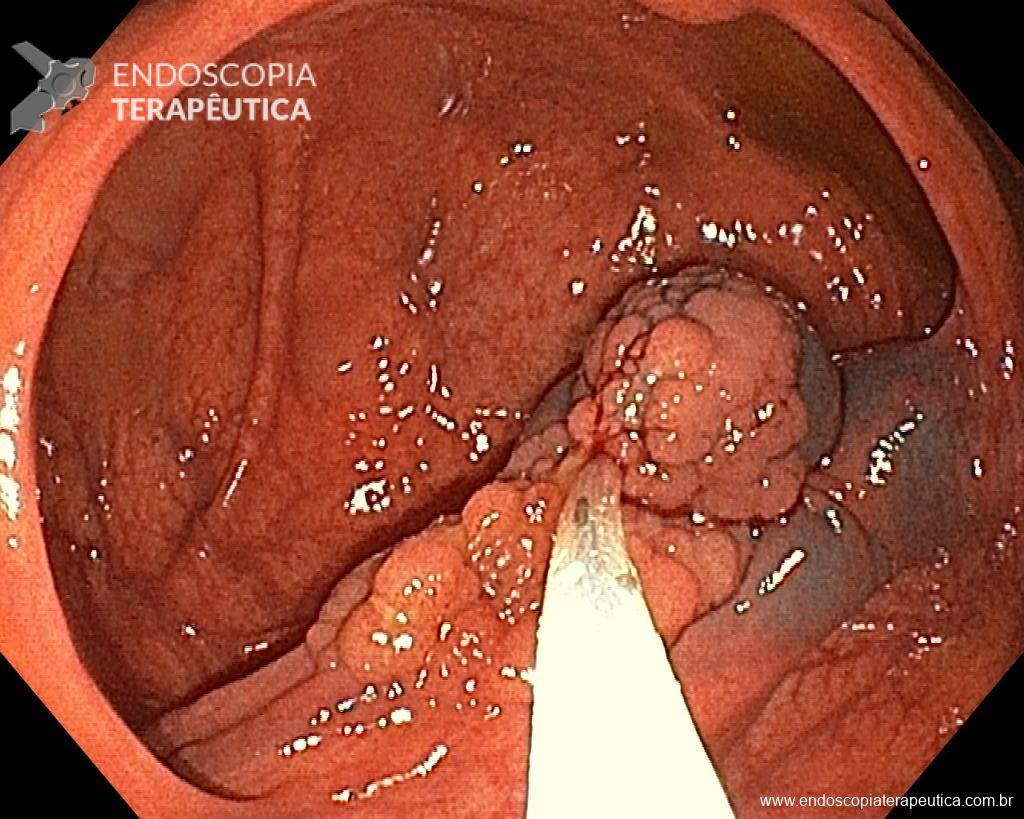
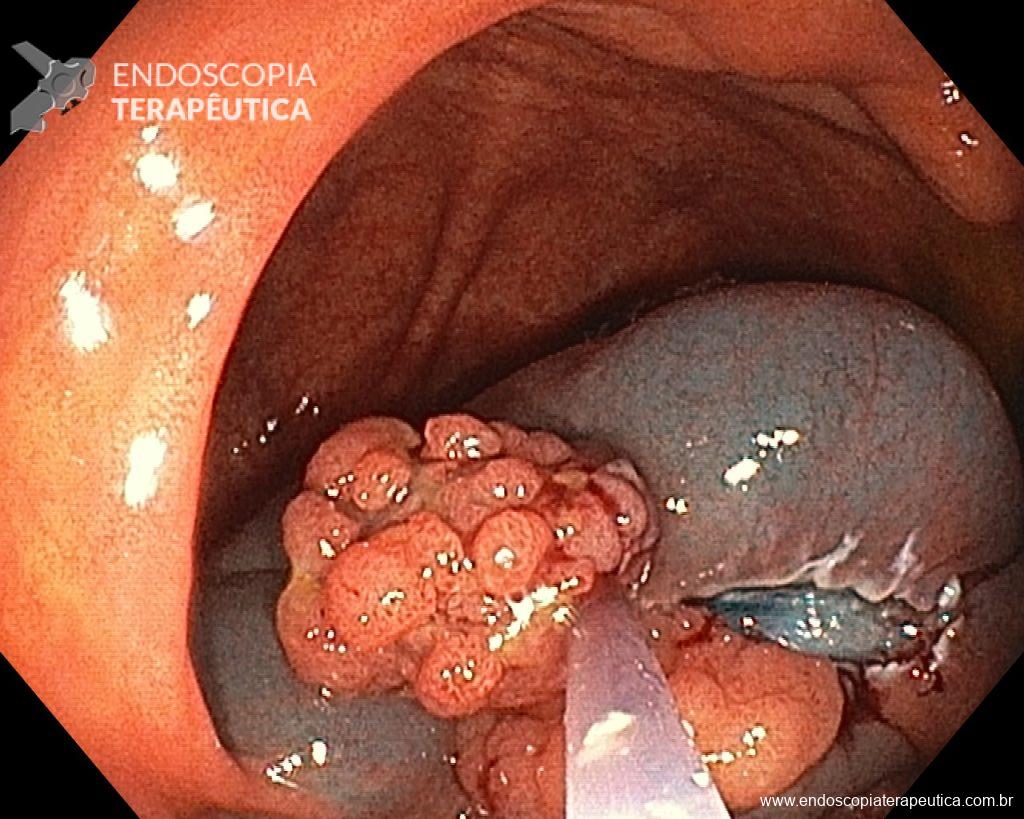
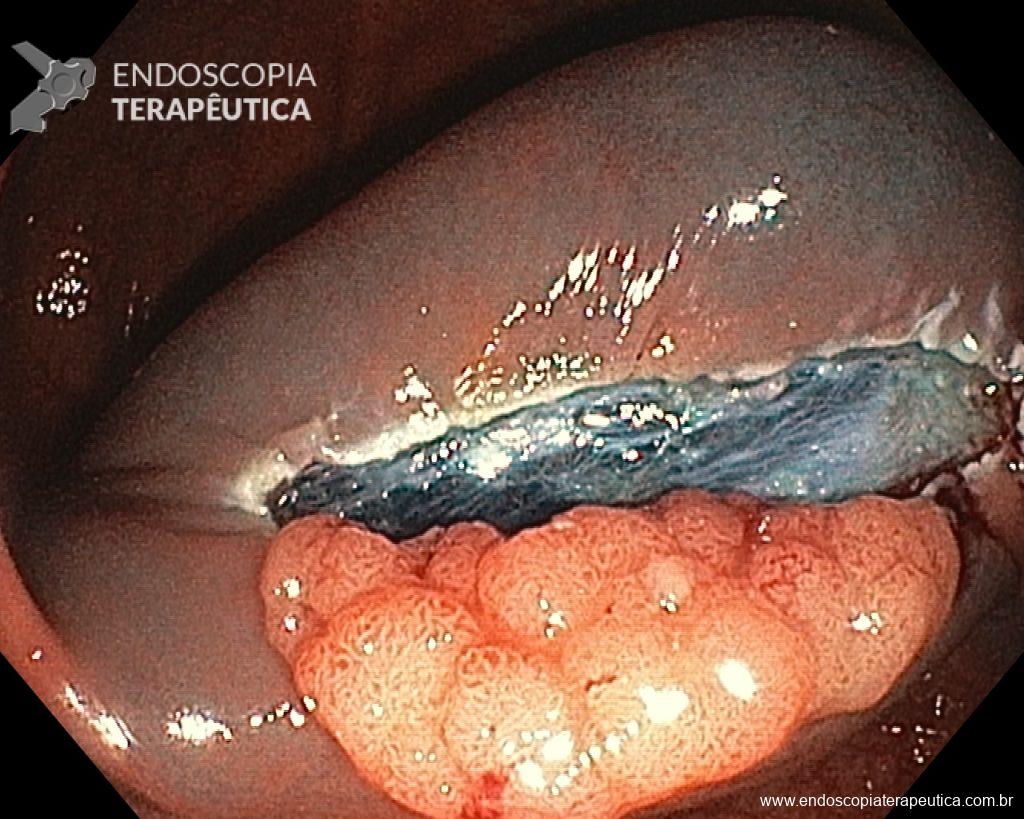
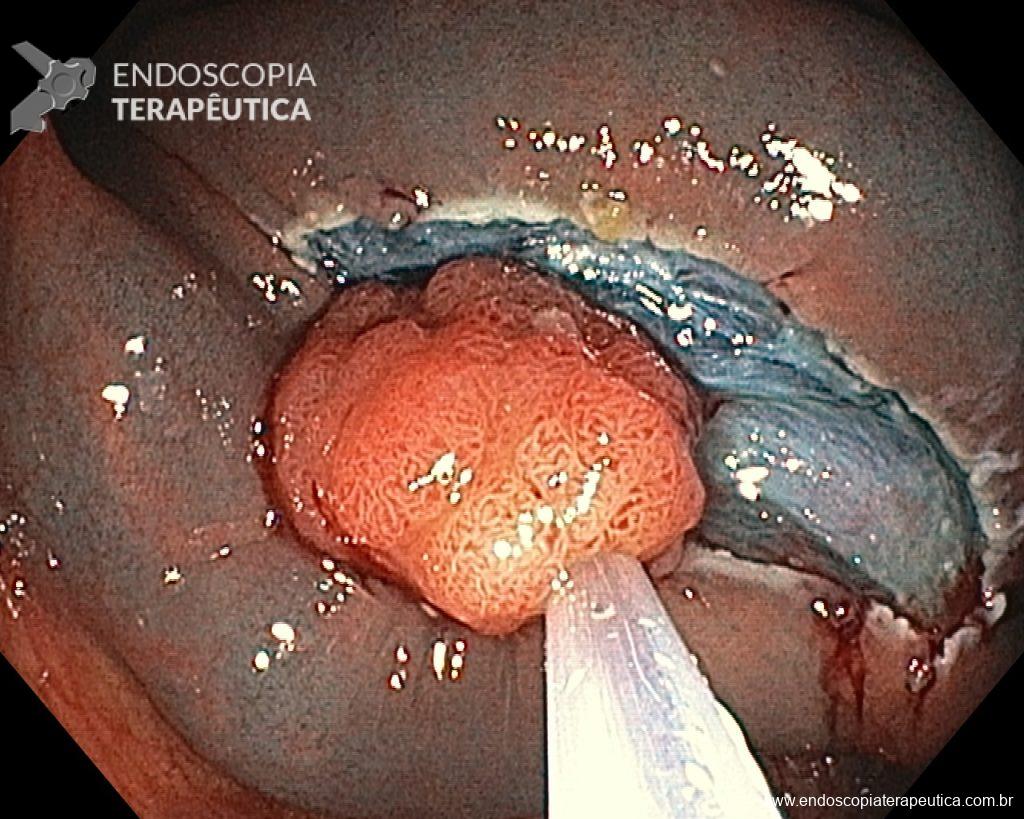
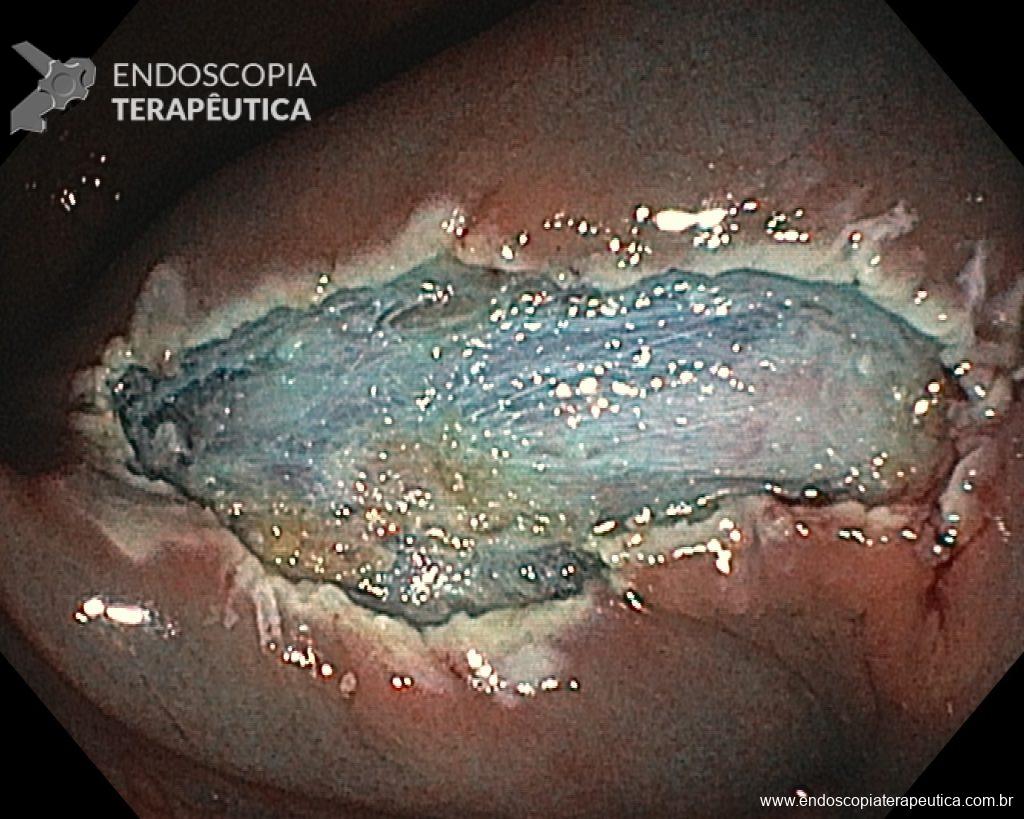
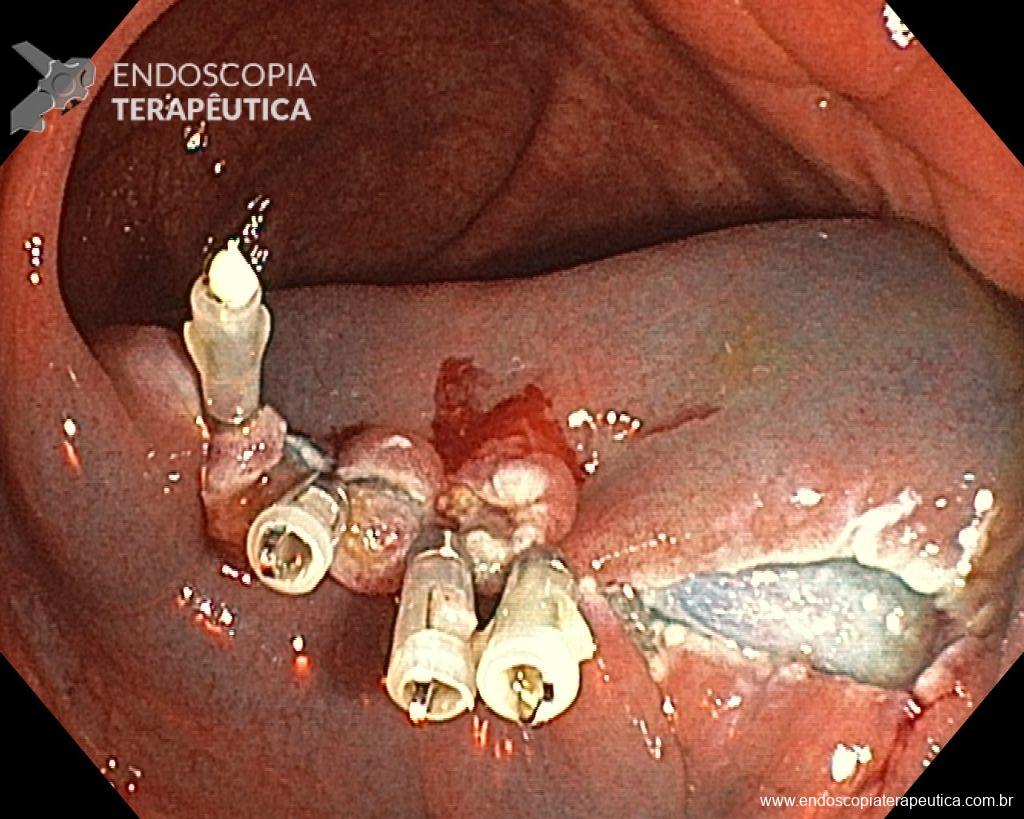
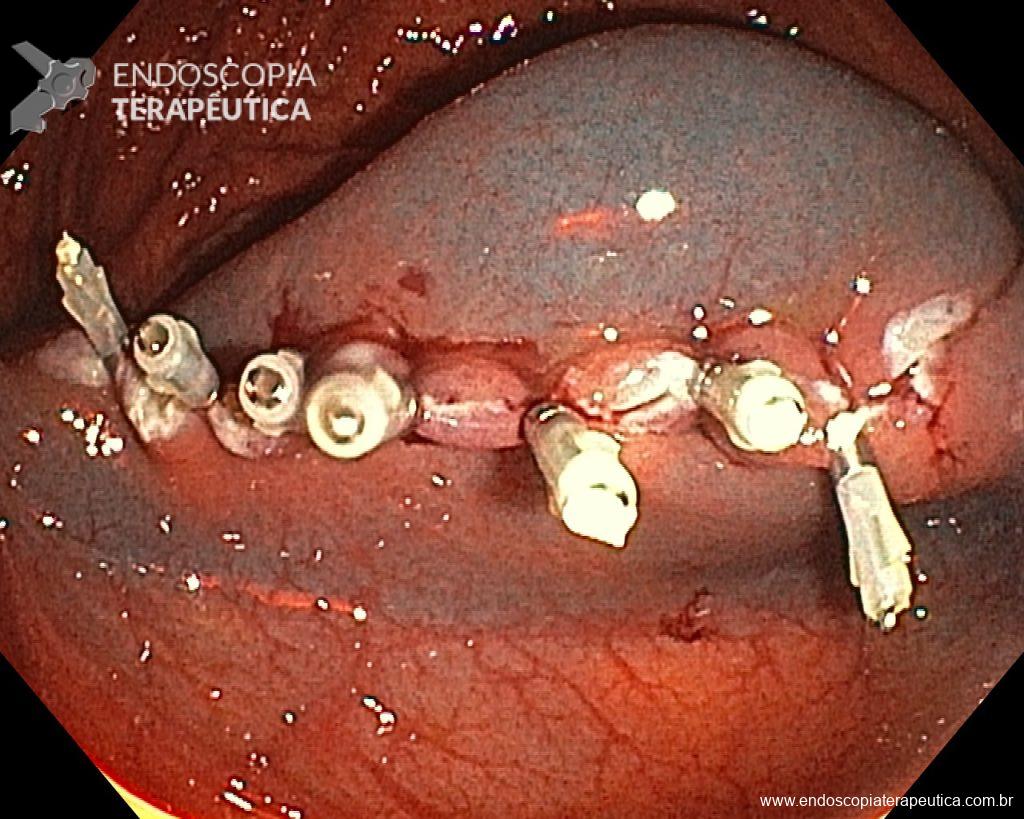
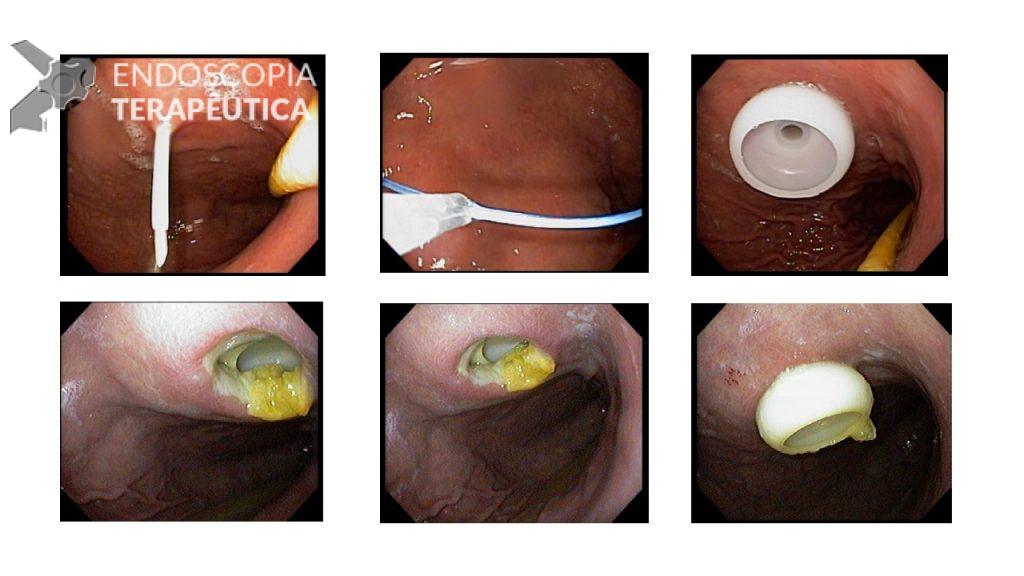
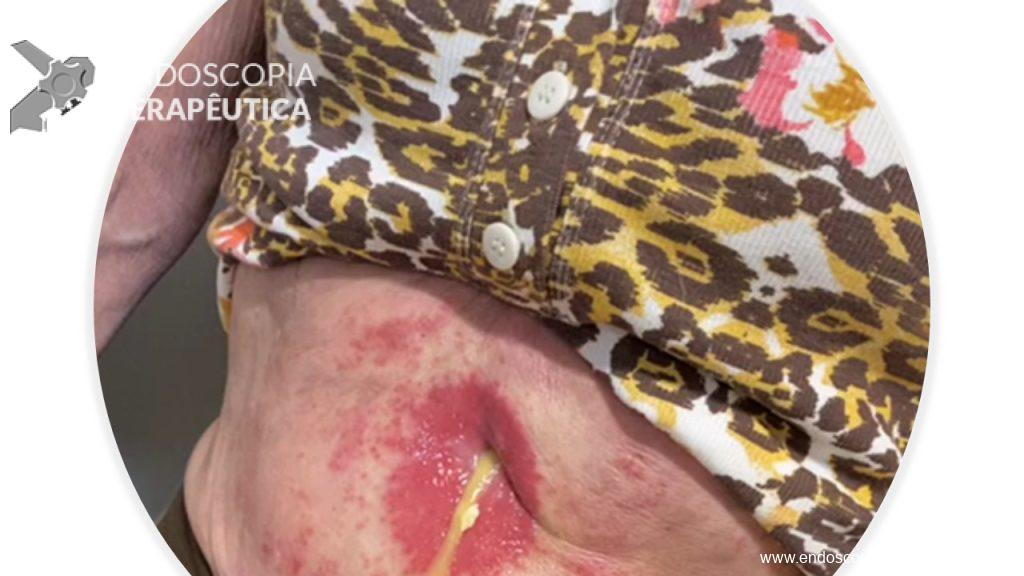
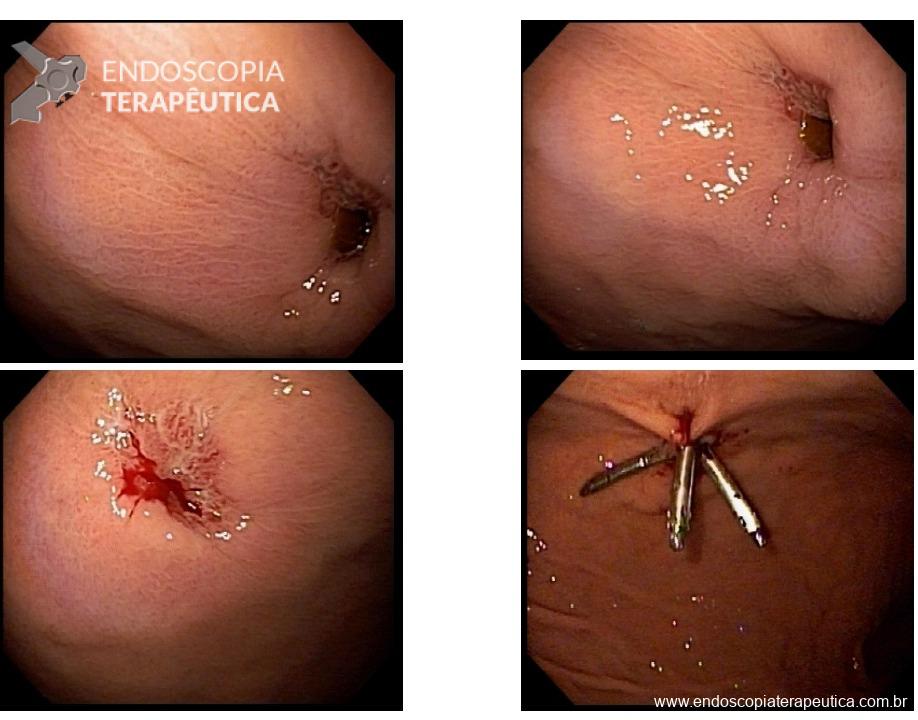
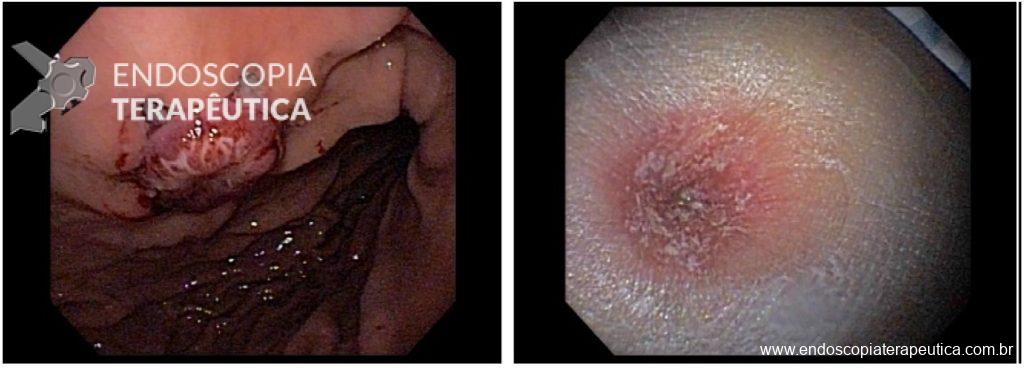
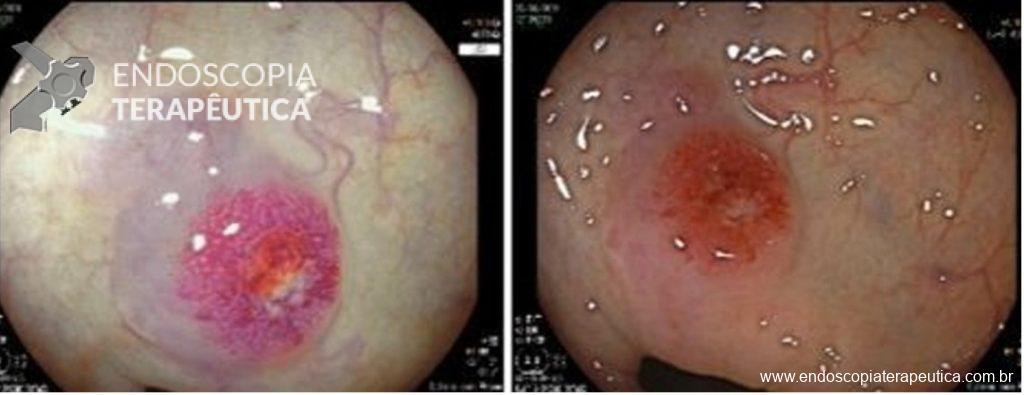
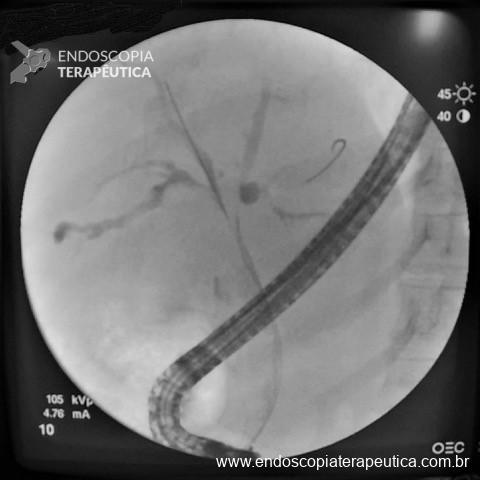
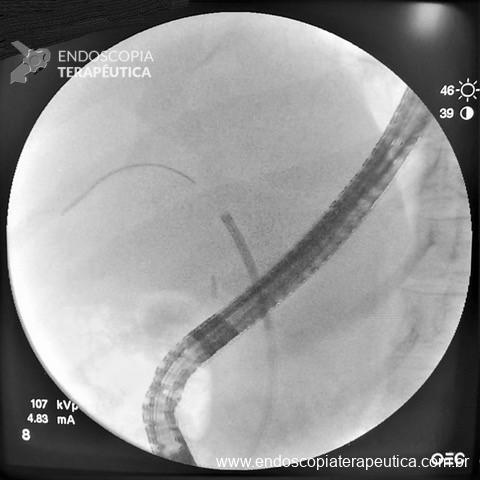
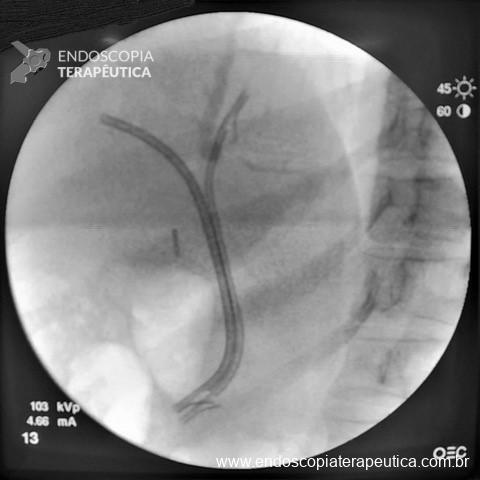
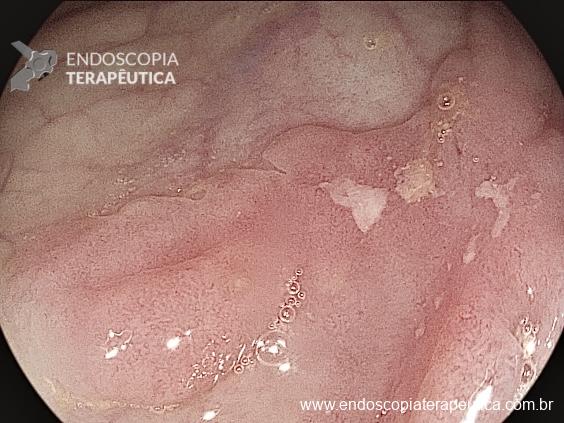
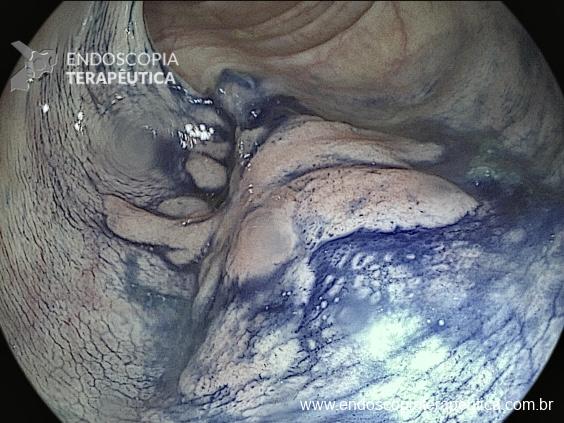
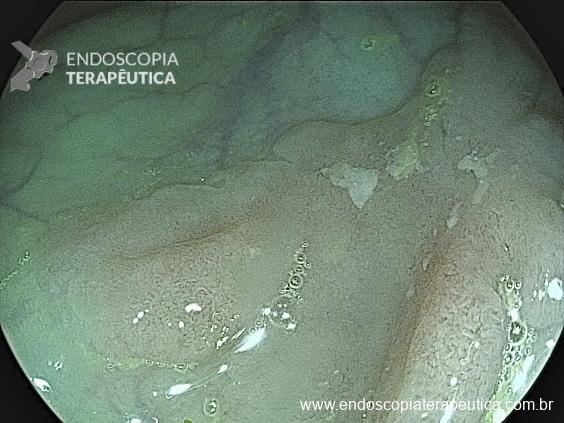
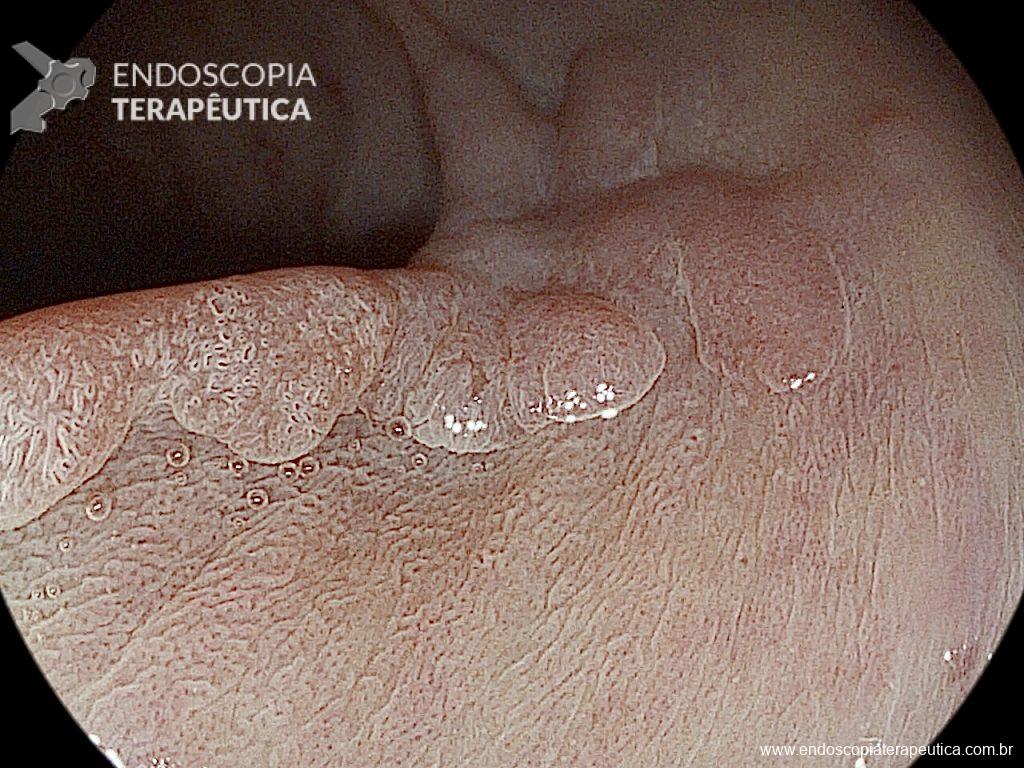
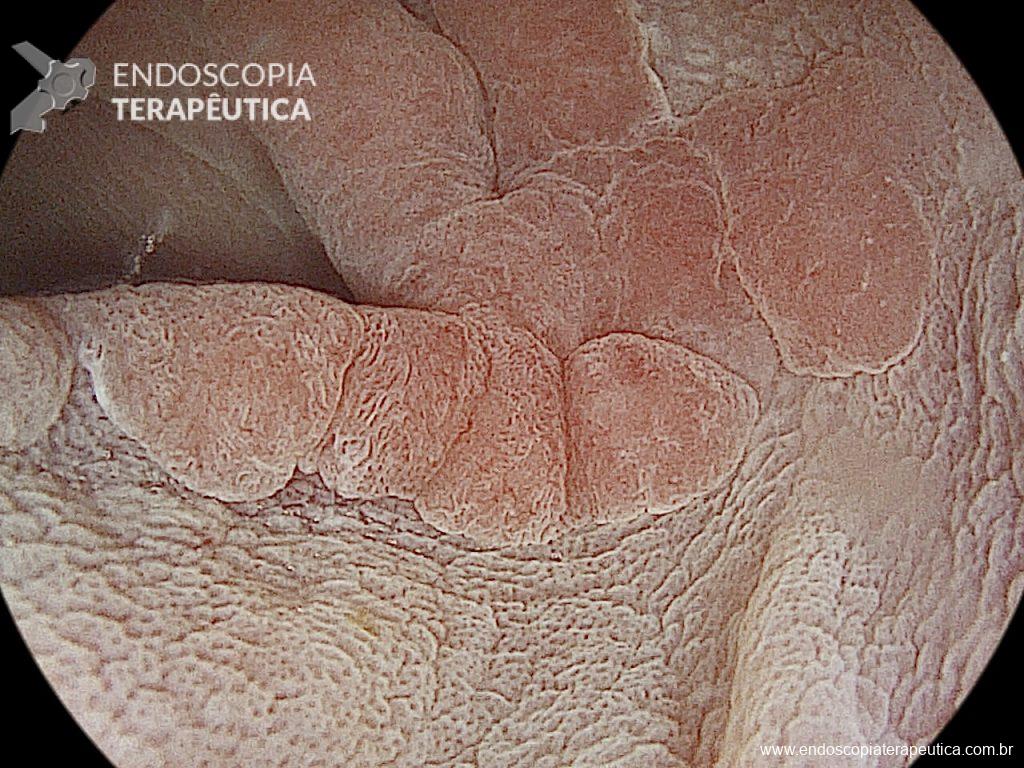
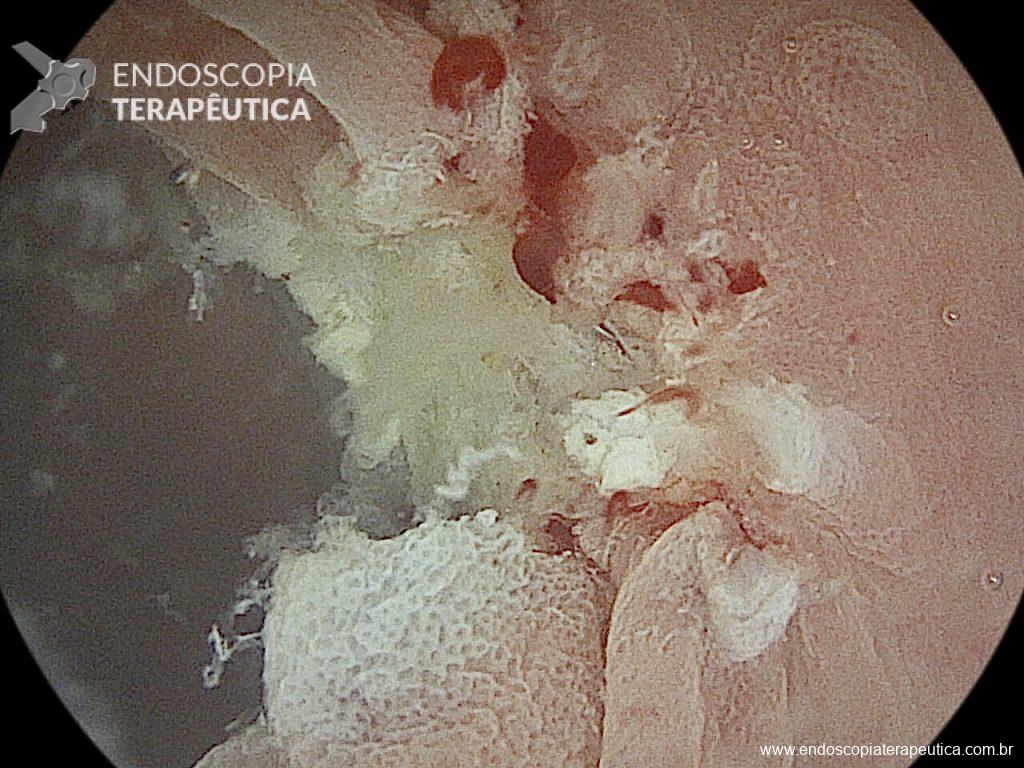
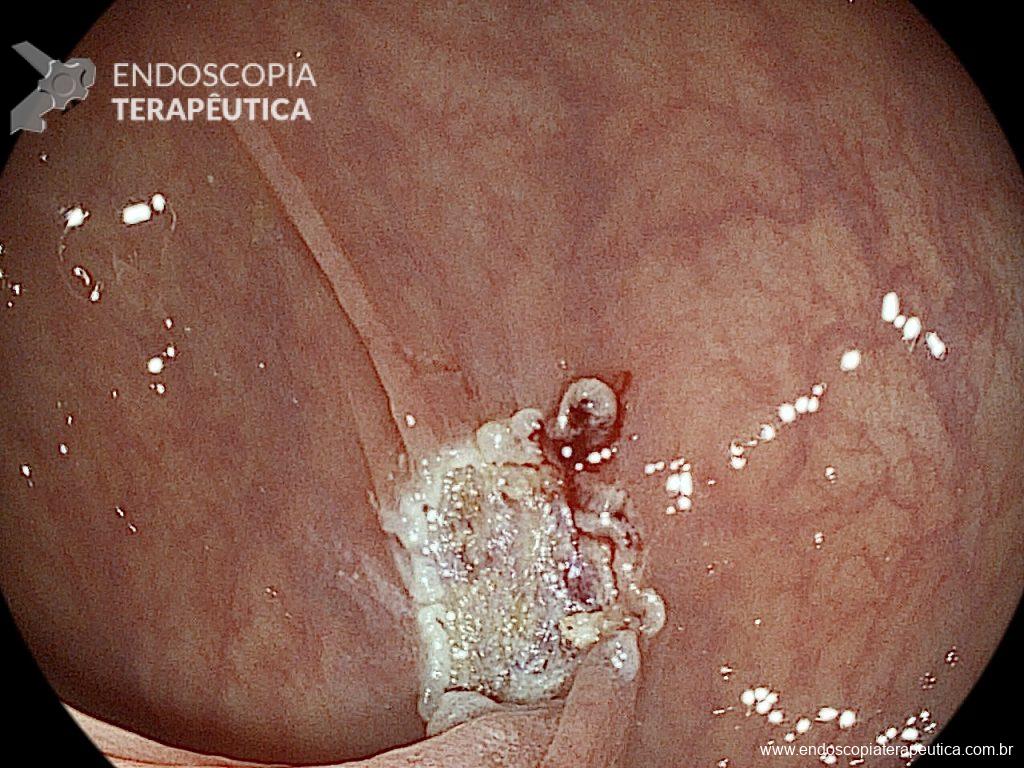
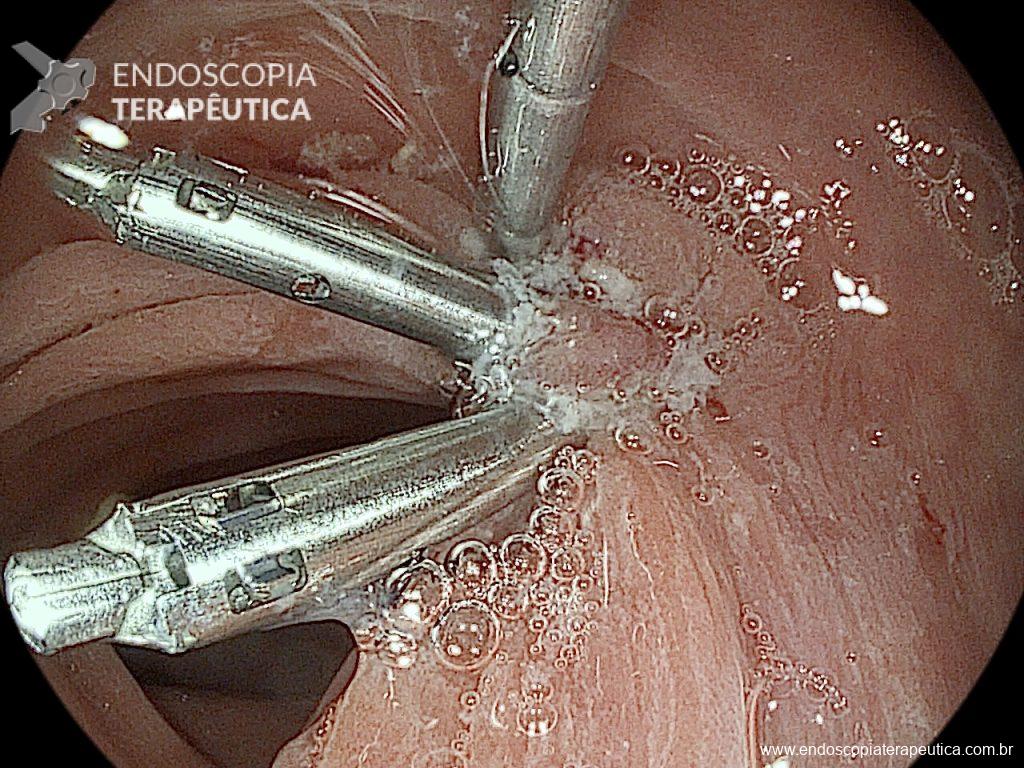
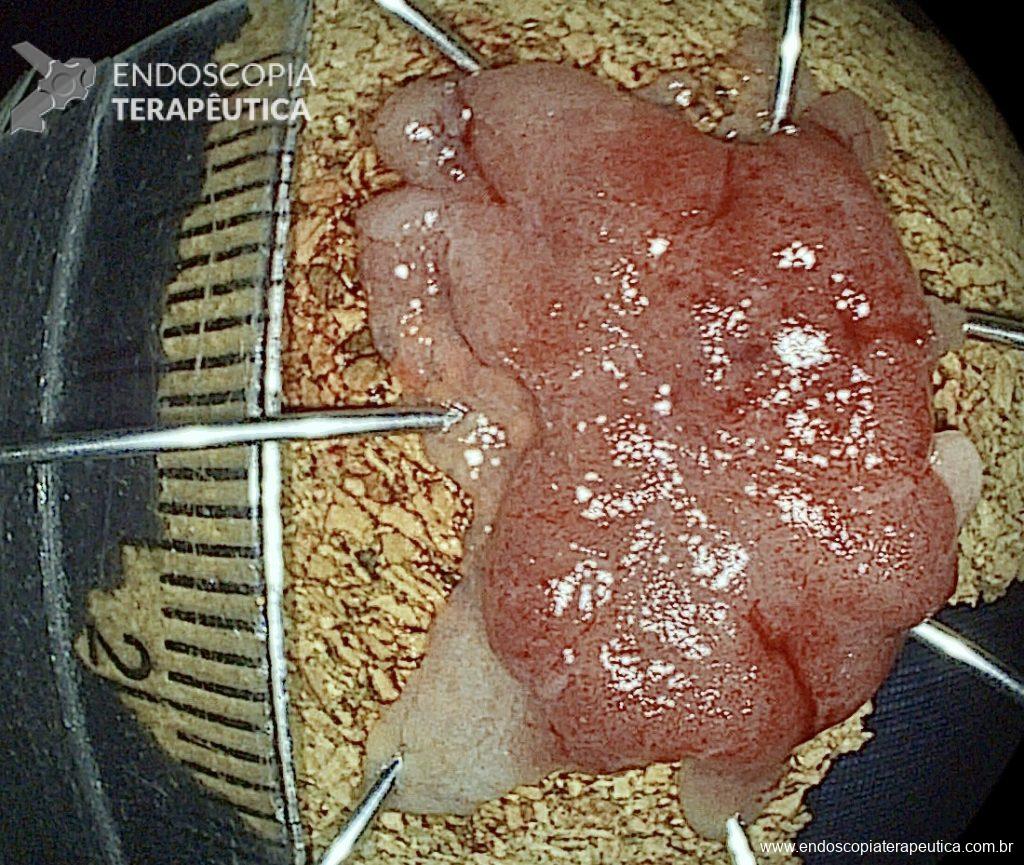
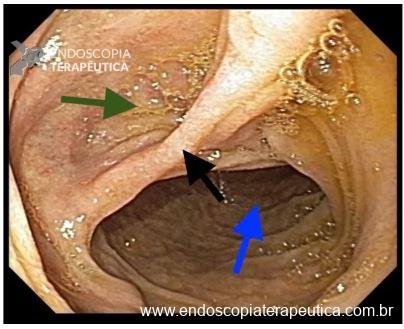
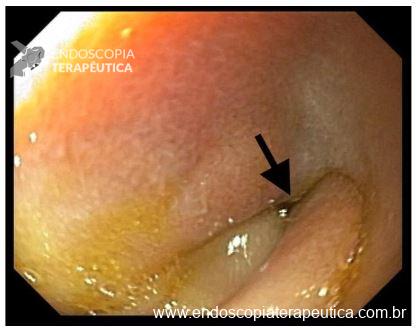
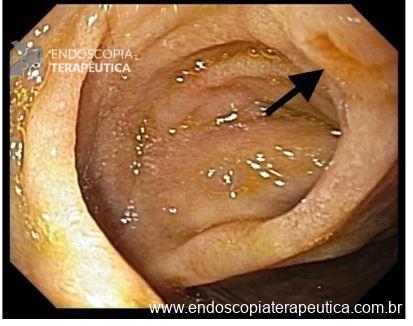
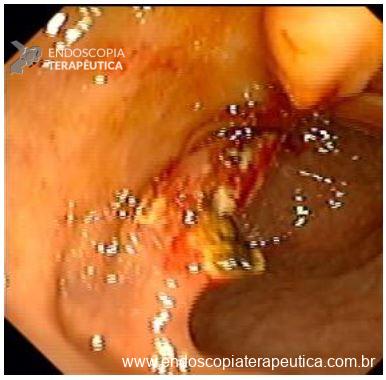
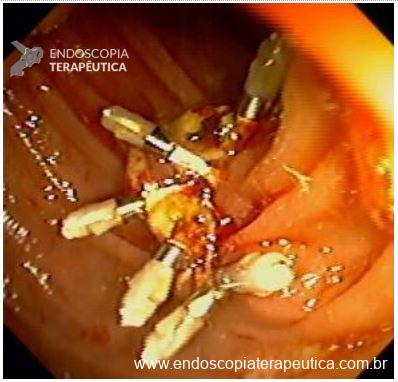
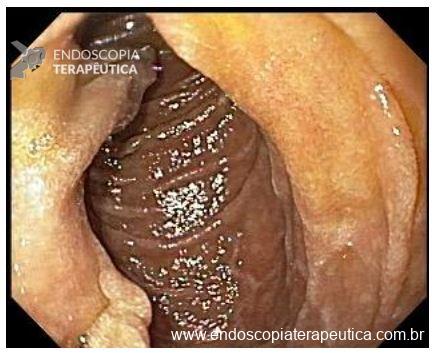
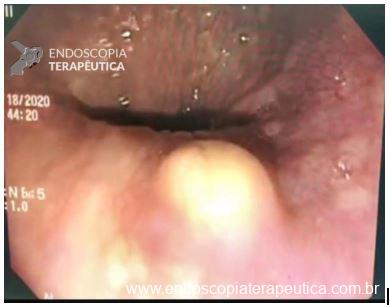
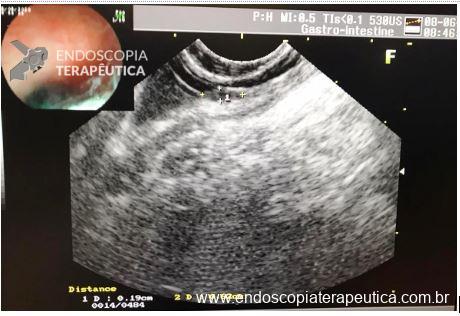
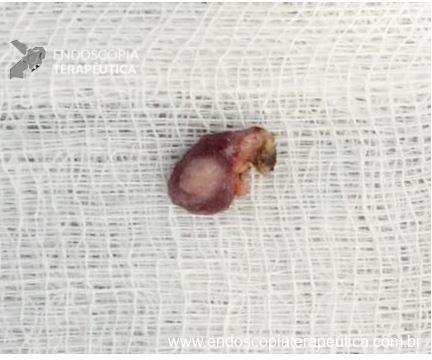
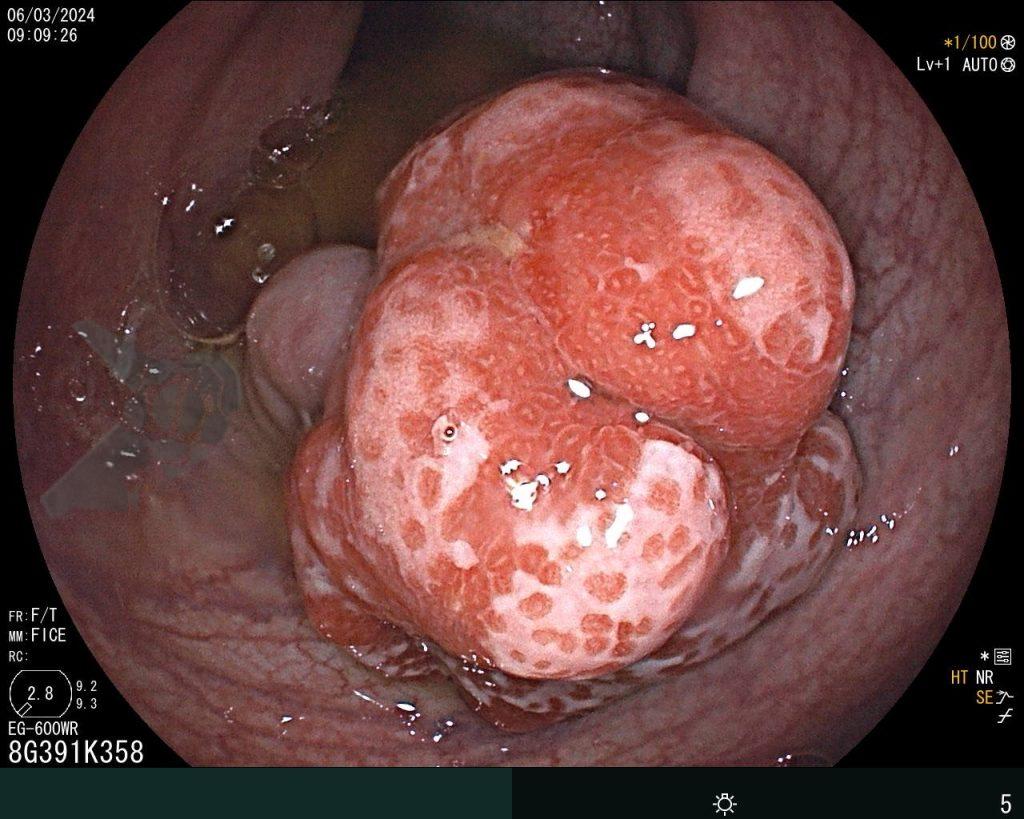
Realizou colonoscopia, ambulatorialmente, onde foi identificado um pólipo pediculado lobulado no cólon descendente distal, com mucosa congesta e edematosa, coberta por fibrina e áreas hiperêmicas, com padrão de criptas tipo II de Kudo (Fig.1-2). O pólo cefálico tinha aproximadamente 3 cm de diâmetro, com um pedículo longo e largo (Fig.3-4). Foi realizada a polipectomia utilizando alça diatérmica, com ressecção completa em monobloco (Fig.5-6). Optou-se pelo fechamento do sítio da excisão com um endoclipe, sem complicações (Fig.7-8). Não houve achados adicionais nos demais segmentos estudados. O procedimento teve duração de 30 minutos, com alta da paciente após sua conclusão.
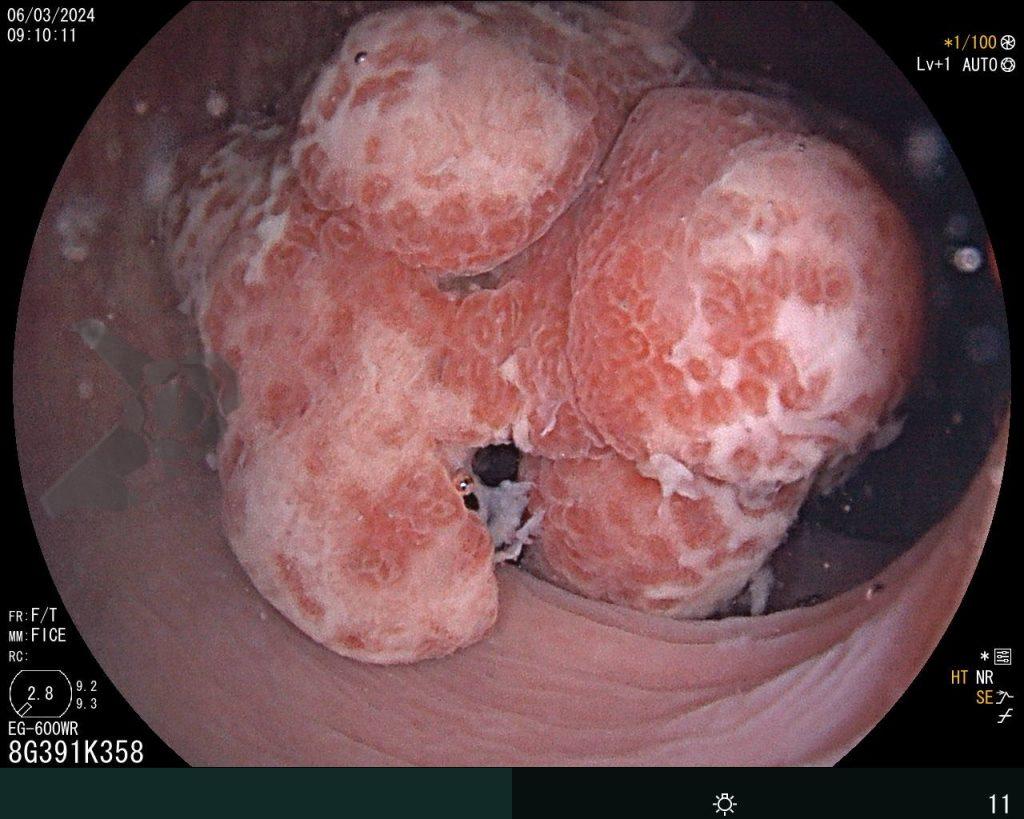
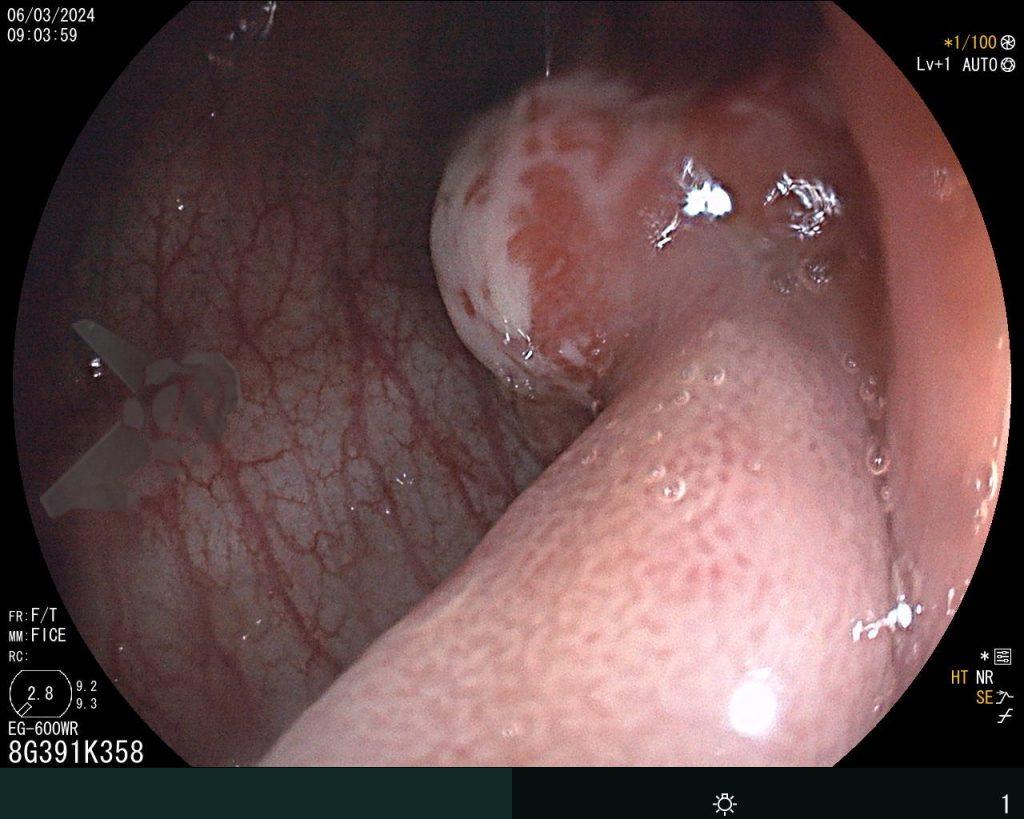
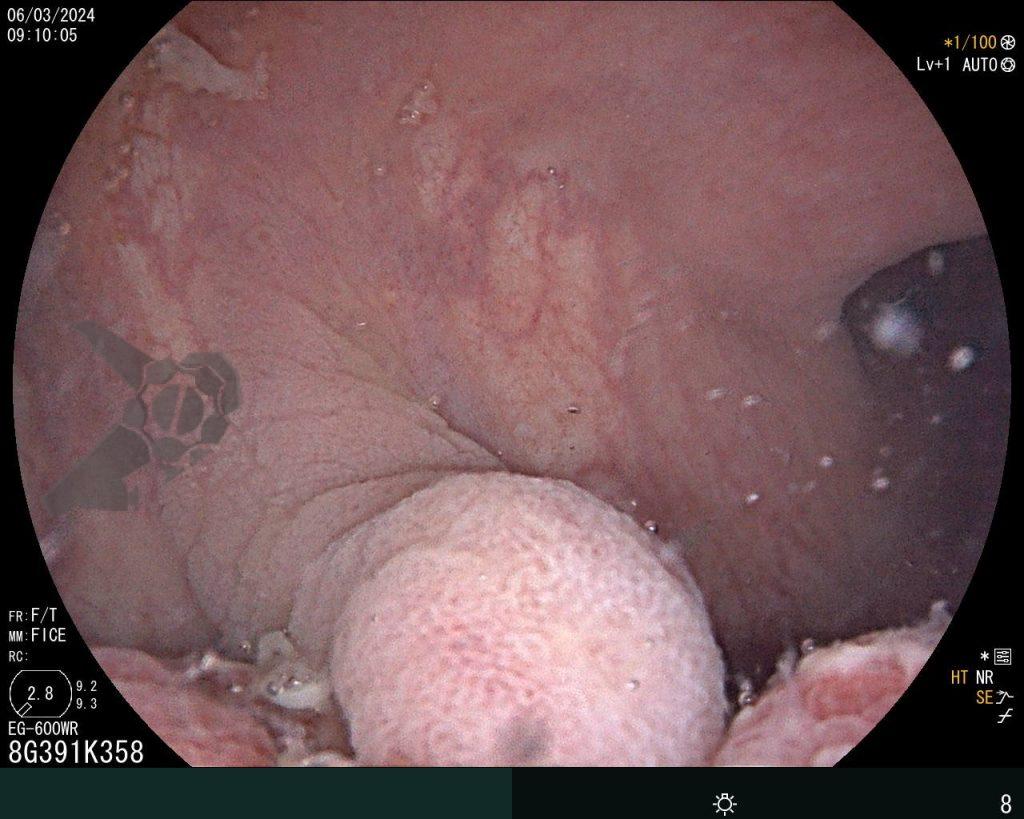
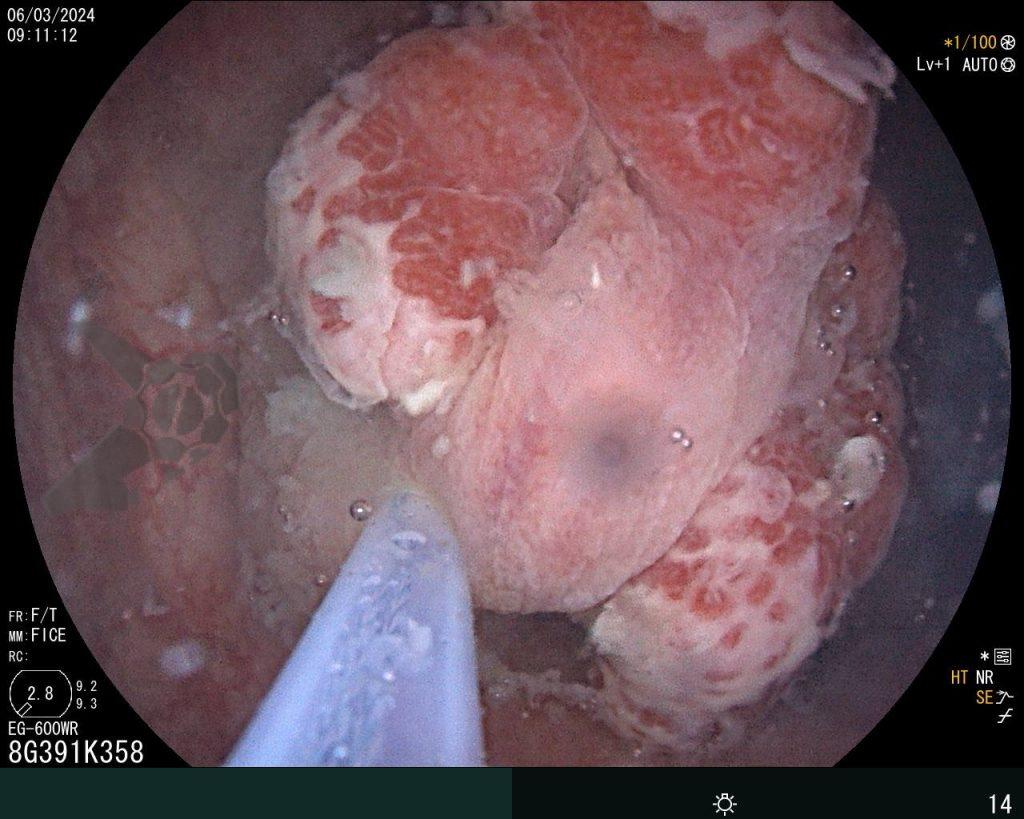
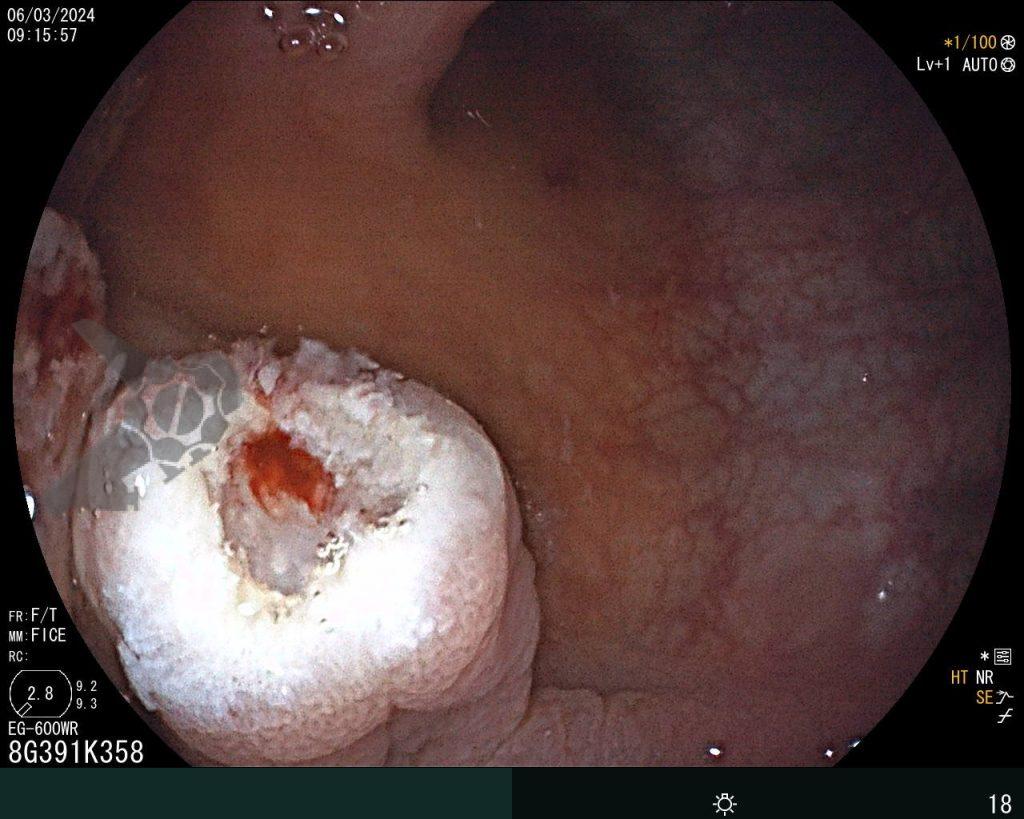
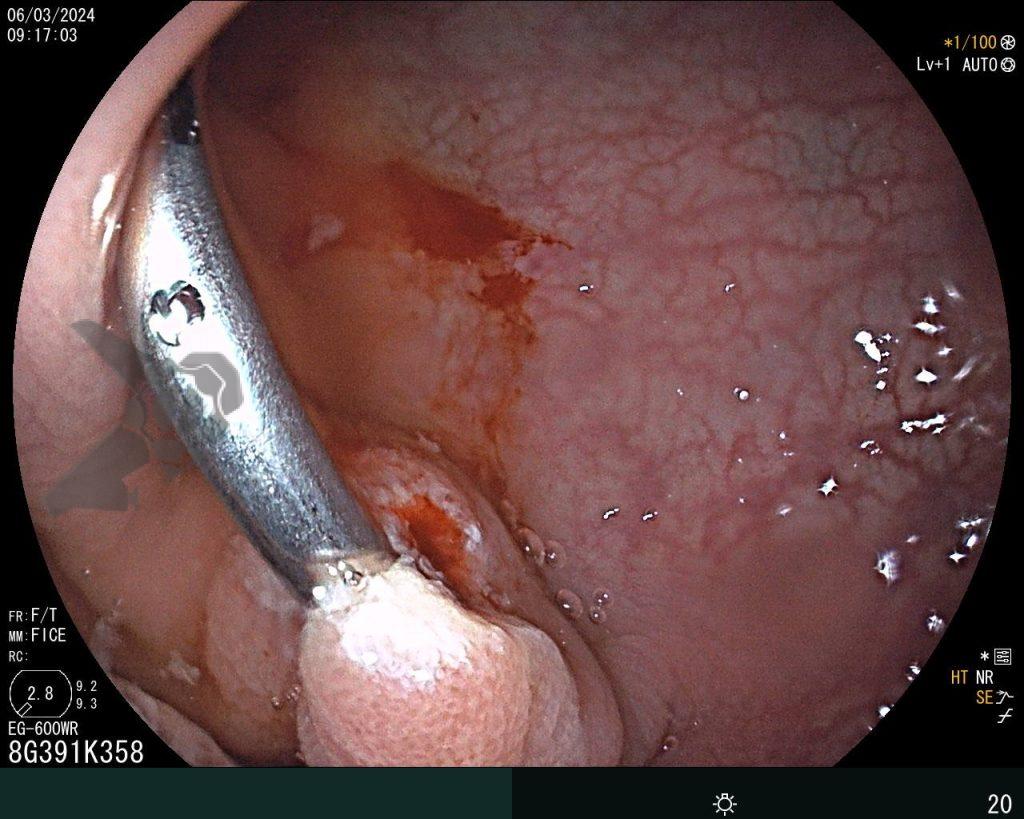
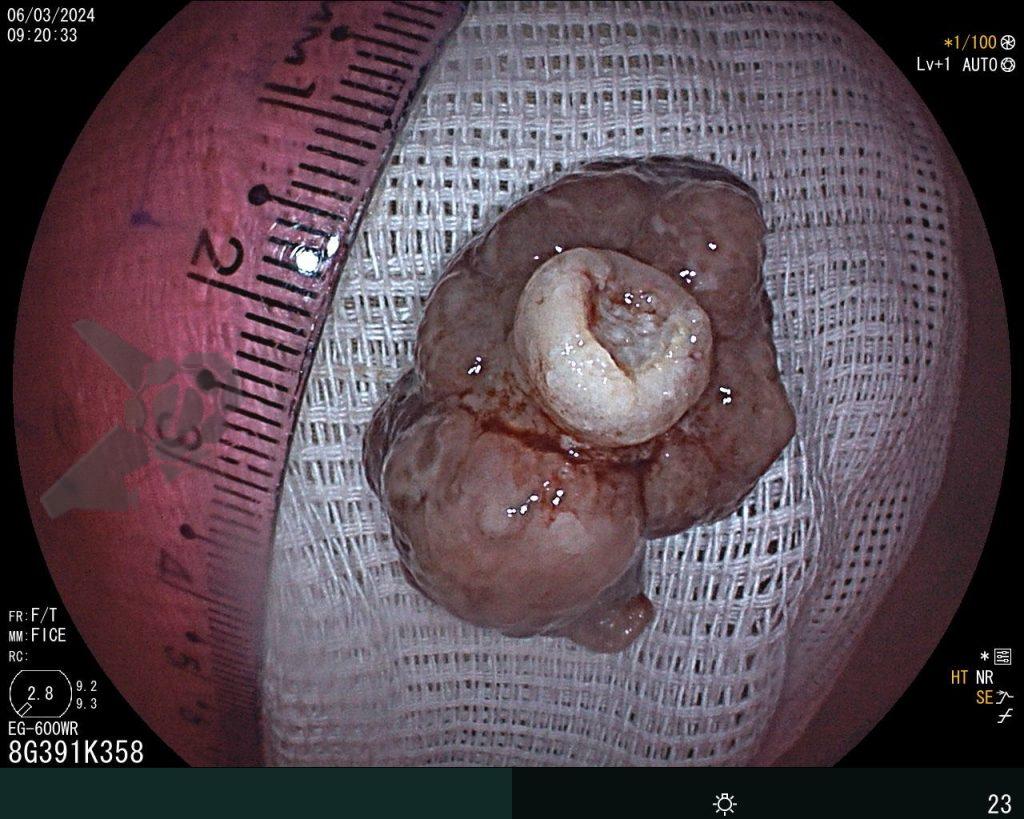
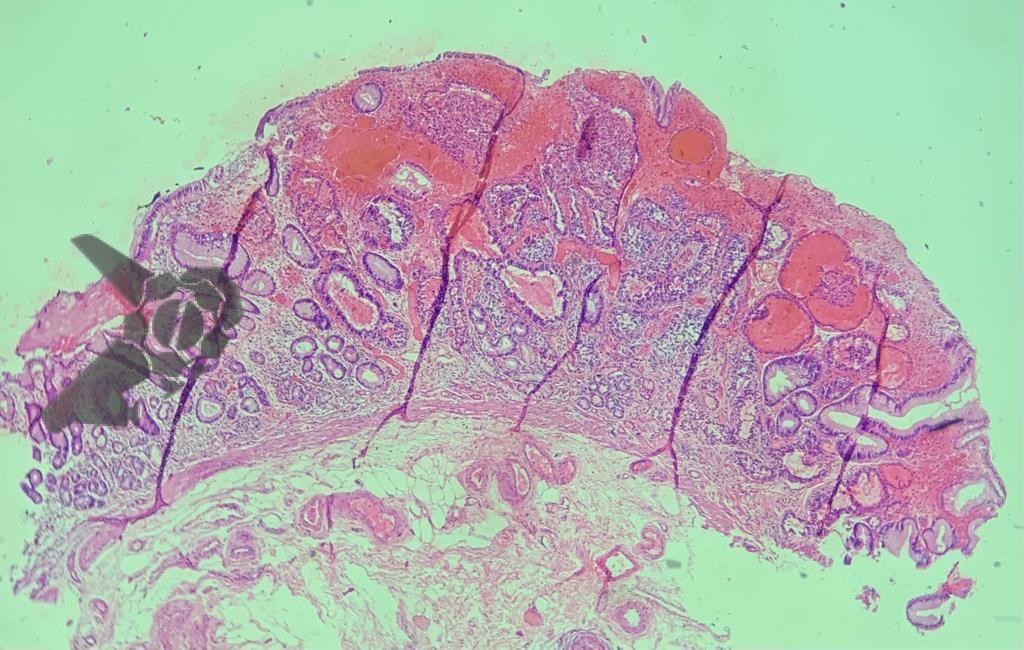
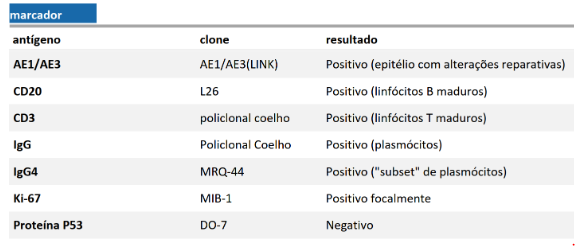
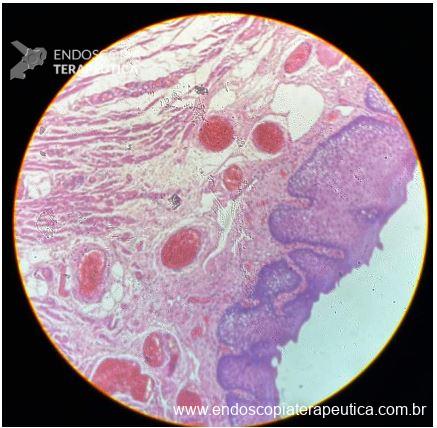
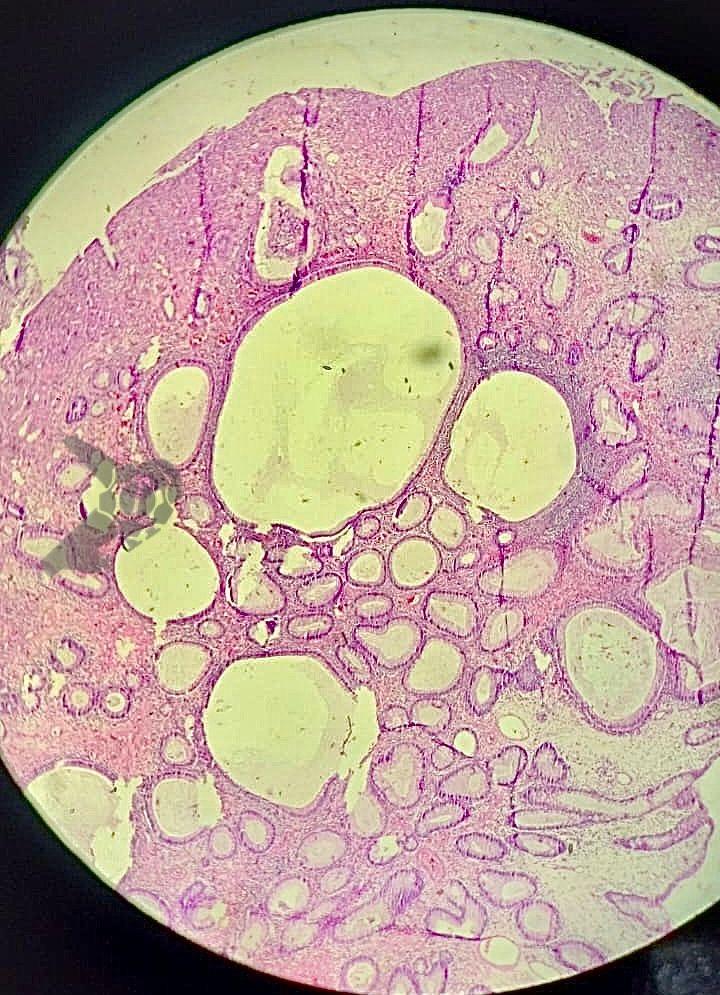
O exame anatomopatológico revelou tratar-se de uma lesão polipóide hiperplásica benigna, com estroma frouxo (Fig.9-10). As estruturas glandulares estavam hiperplásicas, variando de tamanho e ocasionalmente dilatadas cisticamente, sem apresentar atipias. O diagnóstico é compatível com pólipo hamartomatoso juvenil.
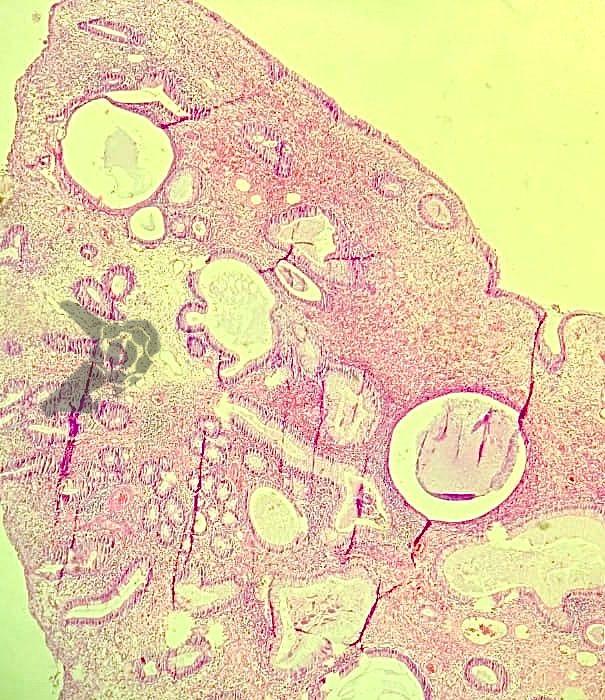
Revisão de literatura
As principais causas de hemorragia digestiva baixa, em crianças de 2 a 12 anos, incluem fissura anal, pólipo juvenil, enterocolite infecciosa e DII (Doença Inflamatória Intestinal). Mais raramente, podem estar relacionadas à úlcera retal solitária, duplicação intestinal, púrpura de Henoch-Schönlein, síndrome hemolítico-urêmica e malformação vascular colônica.
A presença de pólipo hamartomatoso juvenil solitário (esporádico), em crianças com menos de 10 anos de idade, tem incidência de até 2%. O termo “juvenil” refere-se ao tipo anatomopatológico do pólipo e não à idade de aparecimento. Apesar de serem infrequentes, também são descritos casos em adultos. Esses pólipos não são neoplásicos, apresentando histologicamente espaços císticos dilatados, inflamação, aumento da vascularização e áreas de destruição epitelial.
Distribuem-se por qualquer segmento colônico, com predileção pelo hemicólon esquerdo, sendo a topografia retossigmoidea a mais comum. O tipo pediculado é o mais frequente. Apesar da denominação “pólipos juvenis solitários”, eles podem ser únicos ou ocorrer em até 5 pólipos, sendo que 50% das crianças com essa condição apresentam mais de um pólipo. A verdadeira incidência de pólipos juvenis solitários é subestimada devido à sua apresentação clínica discreta e, geralmente, indolor, além da dificuldade do acesso a exame confirmatório.
O tipo pediculado é o mais frequente. Eventualmente, pode ocorrer torção no próprio eixo e autoamputação do pólipo, com consequente hemorragia, que pode ser volumosa.
Ao exame, o tamanho varia de 1 a 3 cm de diâmetro, com friabilidade associada, o que leva ao sangramento retal. Pode haver prolapso do pólipo através do ânus e, raramente, dor abdominal. Um terço das crianças apresenta-se com anemia microcítica em consequência do sangramento crônico, fato que pode induzir erroneamente o diagnóstico de doença inflamatória intestinal e postergar a solicitação da colonoscopia.
É essencial frisar que o pólipo hamartomatoso juvenil solitário difere da síndrome da polipose juvenil familiar (SPJ). A SPJ também é caracterizada pela presença de pólipos hamartomatosos contudo trata-se de uma doença genética autossômica dominante, causada por mutações nos genes SMAD4 e BMPR1A, que confere um risco aumentado de desenvolver câncer no trato gastrointestinal ao longo da vida. A SPJ abrange a Síndrome da Polipose Juvenil, a Síndrome de Peutz-Jeghers e a Síndrome do Tumor Hamartomatoso PTEN. O diagnóstico da SPJ requer o preenchimento de um dos seguintes critérios:
- 1) mais de 5 pólipos juvenis no cólon e/ou no reto;
- 2) múltiplos pólipos juvenis ao longo do trato gastrointestinal;
- 3) qualquer número de pólipos com história familiar presente.
A SPJ familiar é uma condição pré-neoplásica, distinguindo-se do pólipo hamartomatoso solitário, que é esporádico, benigno e apresenta baixo risco de malignização.
A colonoscopia é uma ferramenta amplamente utilizada em todo o mundo para diagnosticar sangramentos gastrointestinais baixos e, frequentemente, serve como método terapêutico em muitos desses casos. No entanto, os exames endoscópicos pediátricos apresentam particularidades que exigem cuidados mínimos essenciais, devendo ser realizados em hospitais que possuam serviços de pediatria e anestesia preparados, tendo assegurado o apoio multiespecialidades indispensáveis ao tratamento de possíveis complicações, sobretudo quando se pratica endoscopia terapêutica. Além disso, o preparo adequado dos cólons é outro aspecto crucial, que pode representar um desafio, podendo atrasar ou adiar o acesso ao exame, diagnóstico e tratamento.
Como tratamento padrão, preconiza-se a remoção desses pólipos por via endoscópica, utilizando a técnica e os recursos adequados.
Conclusão
A investigação do sangramento corretal persistente em crianças com menos de 10 anos deve incluir a realização de colonoscopia. Na presença de um pólipo hamartomatoso juvenil esporádico, após a completa remoção, dado o baixo risco de transformação maligna, não há indicação de repetir a colonoscopia rotineiramente ou encaminhamento para aconselhamento genético, eliminando a necessidade de qualquer acompanhamento posterior adicional.
Referências
- Yachha SK, Khanduri A, Sharma BC, Kumar M. Gastrointestinal bleeding in children. Journal of Gastroenteroly and Hepatology. 1996;11:903–907.
- Colonoscopic finding in children with lower gastrointestinal complaints. Journal of Gastroenteroly and Hepatology. 2023 Nov 8;7(12):863-868.
- Current role of colonoscopy in infants and young children: a multicenter study. BMC Gastroenterology. 2019; 19: 149.
- A solitary rectal juvenile polyp with chicken skin-like changes in the surrounding mucosa in an adult: A case report. Experimental and Therapeutic Medicine. 2023 Apr; 25(4): 185.
- Cancer risk and mortality in patients with solitary juvenile polyps—A nationwide cohort study with matched controls. United European Gastroenterology Journal. jul, 2023.
- Figueiredo LZ, Martins BC. Síndrome da Polipose Juvenil. Endoscopia Terapêutica. 2022; vol 1. Disponível em: endoscopiaterapeutica.net/pt/assuntosgerais/sindrome-da-polipose-juvenil.
Como citar este artigo
Vieira BB. Pólipo hamartomatoso juvenil solitário pediátrico: relato de caso e revisão de literatura. Endoscopia Terapeutica 2024, Vol I. disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/polipo-hamartomatoso-juvenil-solitario-pediatrico-relato-de-caso-e-revisao-de-literatura/