Tratamento do Volvo de Cólon e da Pseudo-Obstrução Aguda do Cólon (Síndrome de Ogilvie)
As obstruções de cólon podem ser mecânicas ou não mecânicas e constituem cerca de 25% de todas as obstruções intestinais. Entre as causas mecânicas, as mais comuns são:
- tumor obstrutivo no cólon ou reto (60%);
- estenose cicatricial por diverticulites prévias (10%);
- volvo do cólon (15 a 20%).
O volvo do cólon é a torção de um segmento redundante do cólon em seu mesentério que pode levar à oclusão luminal do segmento torcido e isquemia por rotação do mesocólon e, consequentemente, à perfuração.
Embora o volvo do cólon possa ocorrer em qualquer segmento redundante, envolve mais comumente o sigmóide (60%–75% de todos os casos) e ceco (25%–40% de todos os casos).
O volvo de sigmóide ocorre principalmente durante a 6ª a 8ª décadas de vida, sendo mais comum em homens, pacientes institucionalizados, pacientes com constipação crônica, comprometimento neuropsicológico ou comorbidades descompensadas. Por outro lado, o volvo de ceco, geralmente se apresenta em pacientes mais jovens e tem predominância do sexo feminino.
Já a pseudo-obstrução aguda do cólon, ou síndrome de Ogilvie, é uma causa funcional não mecânica de obstrução que se acredita ser uma consequência da desregulação dos impulsos autônomos da inervação do cólon. Há grande distensão do cólon sem fator obstrutivo, mas que também pode evoluir para isquemia e perfuração. As apresentações clínicas variam de acordo com o grau de distensão, se a válvula ileocecal é competente ou não e a condição clínica do paciente. Mais comumente, a síndrome de Ogilvie afeta pacientes idosos ou pacientes internados por motivos não relacionados, incluindo cirurgia eletiva, trauma ou tratamento de uma condição médica aguda.
Aqui apresentamos algumas recomendações das diretrizes da Sociedade Americana de Cirurgia Colorretal para a condução desses casos.
Volvo de Cólon
- Avaliação inicial com história, exame físico e exames laboratoriais básicos. Os sintomas podem incluir cólicas, náuseas, vômitos, desconforto abdominal. O volvo de sigmóide geralmente tem apresentação mais indolente, enquanto o volvo de ceco costuma ter apresentação mais aguda. No exame físico, em geral há distensão abdominal com diferentes graus de dor à palpação, até peritonite. O toque retal revela uma ampola retal vazia. Apresentação na emergência com peritonite e sinais de choque acontecem em 25 a 35% dos casos.
- Em pacientes hemodinamicamente estáveis, uma radiografia de abdome auxilia na avaliação inicial (achado de “grão de café” e, em pacientes com válvula ileocecal incompetente, distensão de delgado). Tomografia é usada para confirmar o diagnóstico.
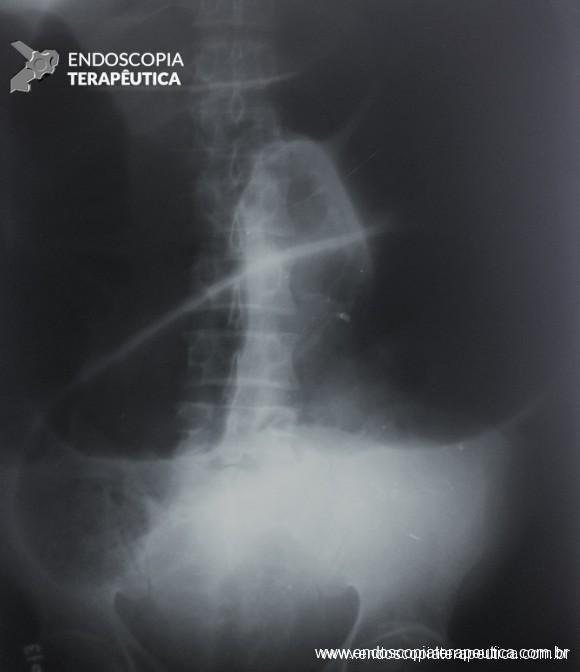
Volvo de Sigmóide
- Pacientes hemodinamicamente estáveis, sem sinais de peritonite ou evidência de perfuração devem ser submetidos a retossigmoidoscopia para avaliar a viabilidade do sigmoide, desfazer a torção e descomprimir o cólon, terapia efetiva em 60 a 95% dos casos. É possível manter uma sonda para descompressão após a retossigmoidoscopia. A taxa de recorrência é de 43 a 75% nos casos que não são submetidos a intervenção cirúrgica posterior.
- Sigmoidectomia de urgência é indicada quando a distorção endoscópica não é bem-sucedida e nos casos de sofrimento do cólon ou perfuração, assim como em pacientes com sinais de peritonite ou choque séptico. Após a ressecção do segmento torcido, a decisão de realizar uma anastomose primária, colostomia terminal ou anastomose com derivação deve ser individualizada considerando o contexto clínico do paciente no momento da cirurgia, as condições do cólon remanescente e as comorbidades.
- Pacientes submetidos à distorção endoscópica bem-sucedida são candidatos à colectomia segmentar durante a mesma internação hospitalar para evitar volvo recorrente e suas complicações. As operações sem ressecção, incluindo apenas distorção, sigmoidopexia e mesosigmoidoplastia, são inferiores à colectomia para a prevenção de volvo recorrente.
- A fixação endoscópica do sigmóide pode ser considerada em pacientes selecionados nos quais a intervenção cirúrgica tem risco proibitivo.

Volvo de Ceco
- Tentativas de redução endoscópica do volvo de ceco não são recomendadas.
- Ressecção segmentar é o tratamento de escolha para pacientes com volvo de ceco. Ceco inviável ou isquêmico está presente em 18% a 44% dos pacientes com volvo de ceco e está associado a uma taxa de mortalidade significativa.
- No caso de volvo de ceco com intestino viável, o uso de procedimentos cirúrgicos sem ressecção deve ser limitado a pacientes sem condições clínicas para ressecção.
Pseudo-Obstrução Aguda do Cólon (Síndrome de Ogilvie)
- A avaliação inicial deve incluir história e exame físico, exames laboratoriais e diagnóstico por imagem.
Na ausência de febre, leucocitose, peritonite, pneumoperitôneo ou diâmetro do ceco > 12 cm, a terapia inicial consiste na correção de distúrbios hidroeletrolíticos, reposição volêmica, evitar ou minimizar uso de opióides, evitar medicamentos anticolinérgicos e identificar e tratar infecções concomitantes. Também é recomendável deambulação, jejum, manobras de posicionamento (genu-peitoral ou prona) para promover a motilidade intestinal e descompressão com sondas nasogástricas e retais. Laxantes osmóticos orais devem ser evitados porque podem piorar a dilatação do cólon. Radiografias de abdome fazem parte da avaliação diária, acompanhado do exame físico.
- O tratamento inicial é de suporte clínico e inclui a exclusão ou correção de condições que predispõem os pacientes ao quadro ou prolongam seu curso.
- O tratamento farmacológico com neostigmina é indicado quando o quadro não se resolve com terapia de suporte.
- A descompressão endoscópica do cólon deve ser considerada em pacientes com Ogilvie nos quais a terapia com neostigmina é contraindicada ou ineficaz.
- O tratamento cirúrgico é recomendado nos casos complicados por isquemia ou perfuração do cólon ou refratários a terapias farmacológicas e endoscópicas.
Teste seus conhecimentos respondendo esses QUIZ!
Referências:
- Alavi K, Poylin V, Davids JS, Patel SV, Felder S, Valente MA, Paquette IM, Feingold DL; Prepared on behalf of the Clinical Practice Guidelines Committee of the American Society of Colon and Rectal Surgeons. The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Management of Colonic Volvulus and Acute Colonic Pseudo-Obstruction. Dis Colon Rectum. 2021 Sep 1;64(9):1046-1057. doi: 10.1097/DCR.0000000000002159. PMID: 34016826.
- Yeo HL, Lee SW. Colorectal emergencies: review and controversies in the management of large bowel obstruction. J Gastrointest Surg. 2013;17:2007–2012.
- Bauman ZM, Evans CH. Volvulus. Surg Clin North Am. 2018;98:973–993.
- Quénéhervé L, Dagouat C, Le Rhun M, et al. Outcomes of first-line endoscopic management for patients with sigmoid volvulus. Dig Liver Dis. 2019;51:386–390.