Tratamento de estenose benigna gastrointestinal com prótese de aposição de lúmen
O artigo publicado na edição de Junho de 2017 da revista Gastrointestinal Endoscopy testa uma alternativa ao tratamento convencional da estenose benigna do trato gastrointestinal.
Essas estenoses são tradicionalmente tratadas com dilatação, estenotomias ou injeção de corticosteroides. Stents metálicos auto-expansíveis são raramente usados nessas situações e geralmente são reservados para casos refratários. Cabe destacar, ainda, a elevada taxa de migração desses stents que pode atingir 30 a 40%.
O stent metálico com aposição de lúmen tem um design diferente e foi aprovado para uso nos EUA inicialmente para a drenagem de coleções pancreáticas (Axios stent, Boston Scientific). Esse stent tem extensão longitudinal curta (limitada em apenas 10 mm) com extremidades amplas (23 a 28 mm) e com diâmetros que variam de 10 a 15 mm. O artigo trata de um estudo multicêntrico que avalia o uso desse stent para o tratamento de estenoses benignas do TGI.
MÉTODO
No período de Agosto de 2014 a Novembro de 2015, 25 pacientes de 2 hospitais terciários foram tratados. A programação era que os pacientes permanecessem com os stents por cerca de 90 dias.
O Sucesso técnico foi definido como a colocação adequada dos stents, confirmada endoscopicamente e radiologicamente. Sucesso clínico foi definido como a melhora clínica dos sintomas por pelo menos 6 meses após a colocação dos stents.
Foram realizadas 28 colocações de stents (3 pacientes colocaram stents com diâmetro de 10 mm que imediatamente foram removidos para recolocarem um de 15 mm) para tratar diferentes estenoses benignas com extensão menor do que 1 cm.
A localização das estenoses variou incluindo anastomoses esofagogástricas (n=4), anastomoses gastrojejunais (n=13), estenoses pilóricas (n=6), estenose pós gastroplastia vertical (n=1) e anastomose ileocolócia (n=1).
Vinte pacientes haviam sido previamente tratados com dilatação isolada, 11 pacientes com dilatação e injeção de corticosteroides, 2 pacientes com estenotomia e 1 paciente com colocação de um stent metálico auto-expansível totalmente recoberto convencional, que migrou precocemente.
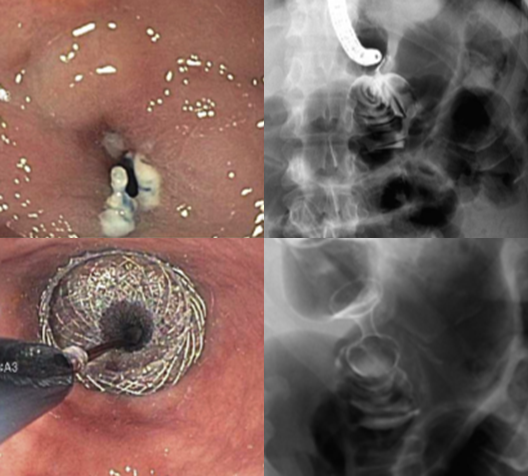
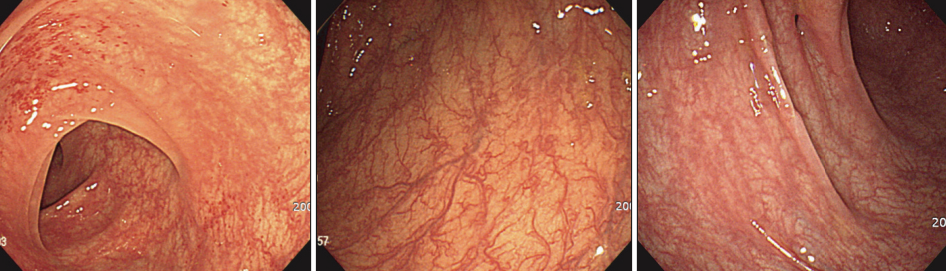
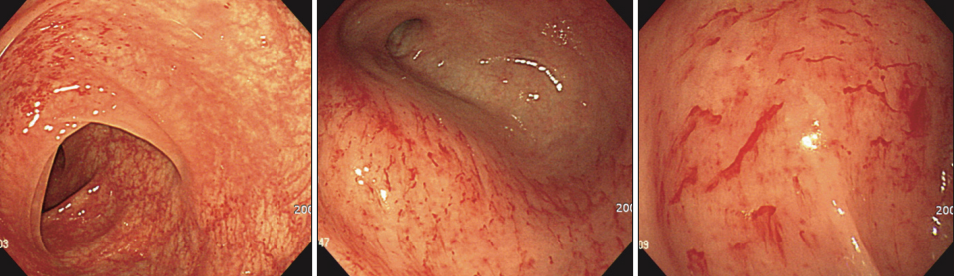
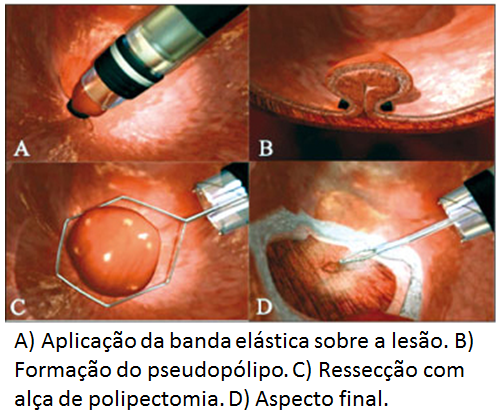
Prótese metálica de aposição de lúmen. Tratamento de estenose de anastomose. Adaptado de Shayan et al. http://dx.doi.org/10.1016/j.gie.2016.08.028
RESULTADOS
- Média de idade de 54 anos. Foram tratados 7 pacientes do sexo masculino e 18 do sexo feminino.
- Sucesso técnico foi alcançado em todos os pacientes,
- Sucesso clínico foi alcançado em 15 dos 25 pacientes (60%).
- Tempo médio de permanência do stent de 92 dias com seguimento médio de 301 dias para as diferentes causas de estenose.
- As estenoses de anastomoses gastrojejunais e estenoses pilóricas apresentaram as respostas mais favoráveis.
Complicações
- Migração de stent foi observada em 2 de 28 procedimentos (7%)
- 5 eventos adversos: Dor que necessitou remoção do stent em 2 pacientes, formação de nova estenose em 2 pacientes e sangramento em 1 paciente.
DISCUSSÃO
Estenose benigna não constitui indicação precisa para o uso de stent. Próteses parcialmente recobertas são de difícil manejo e remoção. As próteses totalmente recobertas migram com facilidade e mesmo quando são utilizados dispositivos para evitar a migração como clipes ou sutura endoscópica as taxas podem atingir 15%. O estudo apresentado mostrou uma taxa de migração baixa, de 7%, provavelmente devido ao design do stent utilizado.
Outro fato a ser destacado é que as próteses tradicionais são muito longas em relação à extensão das estenoses e podem provocar lesões teciduais adicionais. Neste estudo, dois pacientes desenvolveram estenoses proximais aos stents, associadas a tecido de granulação. Isso pode ter ocorrido, também, devido ao design do stent (curta extensão e extremidades amplas), os mesmos atributos que resultam em menores taxas de migração.
O pequeno número de pacientes e o curto acompanhamento limitam as conclusões, bem como seu desenho retrospectivo, abordagem de causas diversas de estenose e a falta de um braço de tratamento de controle.
Os autores concluem que a colocação desses stents é tecnicamente fácil e relativamente segura. No entanto, algumas questões permanecem: apesar do sucesso técnico ter sido obtido em todos os pacientes, a resposta clínica global foi de 60%. Não se sabe qual é o diâmetro ideal do stent, não há estudos de custo-efetividade e a comparação entre as diferentes técnicas é difícil.
A abordagem algorítmica usual para estenoses GI benignas permanece a mesma. Deve-se começar com a dilatação endoscópica, aumentando até atingir 14 a 15 mm. Estenotomia pode ser realizada para estenoses curtas e semelhantes a anéis. Injeções de corticosteroides podem ser tentadas após falha na dilatação isolada e progredindo para colocação de stent em casos selecionados, apenas após sucessivas falhas das intervenções acima.
REFERÊNCIA
Use of a lumen-apposing metal stent to treat GI stricture. Gastrointestinal endoscopy Vol 85 N.06, 2017. Link para o artigo – clique aqui
Nota: O artigo contém um vídeo muito didático demonstrando a técnica, porém, é necessário login e senha para acessar o conteúdo restrito do Jornal Gastrointestinal Endoscopy.