CPRE em pacientes com Y-de-Roux
A realização de colangiopancreatografia retrógrada endoscópica (CPRE) em pacientes com anatomia em Y de Roux representa um grande desafio para os endoscopistas.
Na era da epidemia de obesidade, essa situação é encontrada com frequência crescente devido à popularidade da cirurgia de bypass gástrico em Y-de-Roux e à alta prevalência de cálculos biliares nesses pacientes.
Frequentemente, é impossível acessar a papila usando um duodenoscópio padrão devido ao comprimento da alça intestinal que deve ser percorrida. Para superar esses problemas, abordagens não padronizadas, técnicas inovadoras e acessórios especializados foram desenvolvidos para realizar CPRE nesses casos.
Considerações gerais
Antes de realizar a CPRE em pacientes submetidos à reconstrução em Y de Roux, o endoscopista deve obter detalhes sobre a ressecção anatômica, o tipo de reconstrução, o comprimento das alças, os tipos de anastomoses e a presença ou ausência de uma papilotomia prévia.
É importante ainda estar ciente do intervalo de tempo após a cirurgia. No período pós-operatório imediato, devem-se pesar os riscos em relação à ruptura da anastomose contra os benefícios potenciais da CPRE.
Escolhendo a melhor abordagem
Existem várias técnicas disponíveis para realizar CPRE em pacientes com anatomia em Y-de-Roux, cada uma com vantagens e desvantagens Nenhuma abordagem foi identificada como a melhor para todos os pacientes, portanto, o endoscopista deve selecionar a abordagem caso a caso, levando em consideração os seguintes fatores:
- Comprimento da alça do Y (longa versus curta);
- Se o paciente tem uma papila virgem ou uma anastomose biliodigestiva, por exemplo;
- A indicação de CPRE, incluindo a probabilidade de repetir procedimentos e a necessidade de manobras terapêuticas;
- A experiência do serviço (enteroscopia profunda, radiologia intervencionista, cirurgia);
- O risco cirúrgico do paciente.
Técnicas
As abordagens transorais envolvem o uso de duodenoscópios, colonoscópios pediátricos ou enteroscópios.
CPRE usando duodenoscópio padrão: o duodenoscópio de visão lateral é o endoscópio ideal para realizar CPRE, particularmente para a canulação de uma papila virgem. Infelizmente, a abordagem apenas com duodenoscópio é frequentemente malsucedida. Portanto, reservamos a abordagem transoral usando um duodenoscópio padrão para pacientes com um alça curta do Y-de-Roux.
CPRE usando um enteroscópio ou colonoscópio pediátrico: um enteroscópio ou colonoscópio pediátrico pode ser uma opção para realizar uma CPRE quando o uso de um duodenoscópio não for viável.
Uma desvantagem dessa abordagem é que a perspectiva de visão frontal e a falta do “elevador” no aparelho tornam a canulação seletiva mais difícil. Além disso, a capacidade de manobra do enteroscópio longo ou colonoscópio pode ser muito limitada devido à formação de alça. A falta de eixo devido à visão frontal desses aparelhos também pode dificultar ou impossibilitar a canulação.
CPRE usando técnicas de enteroscopia profunda: há uma experiência crescente com o desempenho de CPREs usando técnicas de enteroscopia profunda, incluindo enteroscopia de balão duplo (DBE), enteroscopia de balão único (SBE) e espiral enteroscopia.
Embora as técnicas de enteroscopia profunda representem um avanço significativo para a realização de CPRE em pacientes com anatomia alterada cirurgicamente, elas ainda não são amplamente realizadas fora de centros especializados. Além disso, elas têm as mesmas limitações supracitadas inerentes ao uso de enteroscópios para CPRE, incluindo capacidade de manobra restrita, orientação desfavorável da papila, falta de um elevador de instrumento e relativa escassez de acessórios compatíveis com enteroscópio.
CPRE assistida por enteroscópio de duplo balão: relatos de casos e algumas séries mostram que a papila pode ser alcançada em mais de 90% das vezes e a canulação seletiva em mais de 80% dos casos usando a técnica de CPRE assistida por enteroscópio de duplo balão.
Tal como acontece nos casos que usam endoscópios de visualização frontal, a canulação da papila pode ser difícil por essa técnica. Um problema adicional é que há um número limitado de acessórios que são compatíveis com um enteroscópio.
CPRE assistida por enteroscópio de balão único: desempenho de CPREs assistidas por enteroscópio de balão único em pacientes com Y de Roux foi associada a taxas de sucesso de diagnóstico que variam de 60 a 80%.
CPRE assistida por enteroscopia em espiral: a enteroscopia em espiral utiliza um overtube rotativo que permite o avanço profundo do aparelho. As vantagens potenciais da CPRE assistida por uma enteroscopia espiral sobre a duplo balão ou balão único incluem relativa facilidade de uso, melhor controle do endoscópio e, talvez, uma curva de aprendizado mais curta.
Abordagens transorais menos comuns: foi desenvolvida uma técnica que usa a colocação guiada por ecoendoscopia de um stent metálico (LAMS) entre o “pouch” e o estômago excluso para facilitar uma CPRE anterógrada transoral usando um duodenoscópio. A experiência preliminar com essa abordagem em pacientes com anatomia de bypass gástrico em Y de Roux tem sido promissora, com sucesso técnico semelhante e taxas de eventos adversos em comparação com CPRE assistida por laparoscopia e CPRE assistida por enteroscopia.
Como citar este artigo
Ruiz R. CPRE em pacientes com Y-de-Roux. Endoscopia Terapêutica; 2021. Disponível em: https://endoscopiaterapeutica.net/pt/assuntosgerais/cpre-em-pacientes-com-y-de-roux
Referências bibliográficas
- Nguyen NT, Root J, Zainabadi K, et al. Accelerated growth of bariatric surgery with the introduction of minimally invasive surgery. Arch Surg 2005; 140:1198.
- Pories WJ. Bariatric surgery: risks and rewards. J Clin Endocrinol Metab 2008; 93:S89.
- Shiffman ML, Sugerman HJ, Kellum JH, et al. Gallstones in patients with morbid obesity. Relationship to body weight, weight loss and gallbladder bile cholesterol solubility. Int J Obes Relat Metab Disord 1993; 17:153.
- Lopes TL, Wilcox CM. Endoscopic retrograde cholangiopancreatography in patients with Roux-en-Y anatomy. Gastroenterol Clin North Am 2010; 39:99.
- Hintze RE, Adler A, Veltzke W, Abou-Rebyeh H. Endoscopic access to the papilla of Vater for endoscopic retrograde cholangiopancreatography in patients with billroth II or Roux-en-Y gastrojejunostomy. Endoscopy 1997; 29:69.
- Elton E, Hanson BL, Qaseem T, Howell DA. Diagnostic and therapeutic ERCP using an enteroscope and a pediatric colonoscope in long-limb surgical bypass patients. Gastrointest Endosc 1998; 47:62.
- Wright BE, Cass OW, Freeman ML. ERCP in patients with long-limb Roux-en-Y gastrojejunostomy and intact papilla. Gastrointest Endosc 2002; 56:225.
- Aabakken L, Bretthauer M, Line PD. Double-balloon enteroscopy for endoscopic retrograde cholangiography in patients with a Roux-en-Y anastomosis. Endoscopy 2007; 39:1068.
- Emmett DS, Mallat DB. Double-balloon ERCP in patients who have undergone Roux-en-Y surgery: a case series. Gastrointest Endosc 2007; 66:1038.
- Itoi T, Ishii K, Sofuni A, et al. Long- and short-type double-balloon enteroscopy-assisted therapeutic ERCP for intact papilla in patients with a Roux-en-Y anastomosis. Surg Endosc 2011; 25:713.
- Thomas J. Wang, Christopher C. Thompson, Marvin RyouGastric access temporary for endoscopy (GATE): a proposed algorithm for EUS-directed transgastric ERCP in gastric bypass patients Surg Endosc 2019
Confira também: CPRE em pacientes com gastrectomia a Billroth II
Paciente jovem, diarreia crônica, distensão abdominal e as imagens abaixo. Será que você acerta essa?
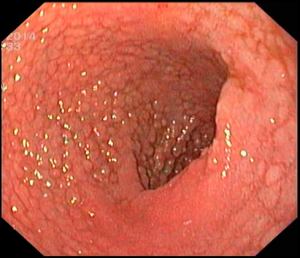

Paciente do sexo feminino, 17 anos de idade, relata queixa de diarreia há cerca de dois meses acompanhada por sintomas dispépticos e distensão abdominal, além de perda de 5 kg no período. Ao exame físico, apresenta-se pouco desidratada, com abdome levemente distendido e doloroso à palpação.
Acesse o Endoscopia Terapêutica para tomar contato com mais artigos comentados, assuntos gerais, casos clínicos, quizzes, classificações e mais!
Deparamo-nos frequentemente com essa situação. Será que você acerta essa questão?
Acesse o Endoscopia Terapêutica para tomar contato com mais artigos comentados, assuntos gerais, casos clínicos, quizzes, classificações e mais!
Achados Ecográficos na Pancreatite Crônica
As pancreatites crônicas (PC) se caracterizam, do ponto de vista anátomo-patológico, pela fibrose progressiva do parênquima glandular, inicialmente focal e, a seguir, difusa por todo o pâncreas. Do ponto de vista evolutivo, geralmente, há persistência das lesões, mesmo com a retirada do fator causal, determinando alterações pancreáticas residuais anatômicas e funcionais.
A ecoendoscopia tem um papel importante no diagnóstico dessa patologia, sobretudo das formas mais leves e iniciais da doença, que não são identificadas pelos métodos de imagem convencionais e para as quais os testes funcionais pancreáticos apresentam uma sensibilidade relativamente baixa.
O último consenso relativo aos critérios necessários para estabelecer o diagnóstico ultrassonográfico de pancreatite crônica foi designado de Critérios de Rosemont. Essa classificação baseou-se na experiência de autoridades na matéria. Foram estabelecidos critérios maiores (A e B) e menores.
Critérios maiores A:
- Focos hiperecoicos com cone de sombra;
- Cálculos do ducto pancreático principal.
Critério maior B:
- Lobularidade contígua do parênquima.
Critérios menores:
- Cistos;
- Ducto pancreático principal com contorno irregular;
- Ducto pancreático principal dilatado;
- Ramos secundários dilatados;
- Parede ductal hiperecoica;
- Faixas hiperecoicas;
- Focos hiperecoicos sem cone de sombra;
- Lobularidade não contígua do parênquima.
Apesar dessa classificação ser muito complexa, ainda é a mais utilizada na prática. E para que o diagnóstico de pancreatite crônica seja estabelecido, os critérios ultrassonográficos são analisados da seguinte forma:
Diagnóstico de certeza:
- presença de dois critérios maiores A;
- presença de um critério maior A + um critério maior B;
- presença de um critério maior A + pelo menos três critérios menores.
Os achados são sugestivos de PC quando há:
- presença de, pelo menos, 5 critérios menores;
- presença de um critério maior B + pelo menos 3 critérios menores;
- presença de um critério maior A + menos três critérios menores.
Os achados são indeterminados para PC quando há pelo menos:
- presença de 3 a 4 critérios menores e nenhum critério maior;
- presença apenas de um critério maior B ou com menos três critérios menores.
Os achados são NEGATIVOS para PC quando há:
- presença de apenas 2 critérios menores e nenhum critério maior.
O achados ultrassonográficos usualmente encontrados nos casos de PC são:














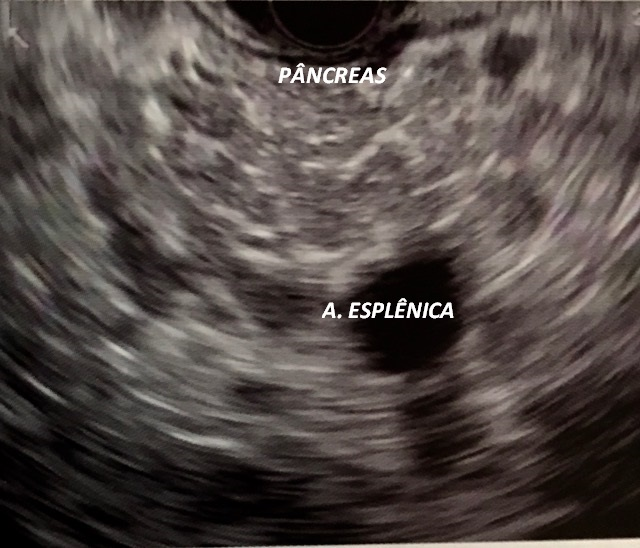
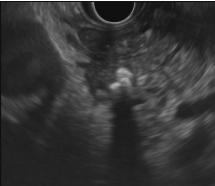
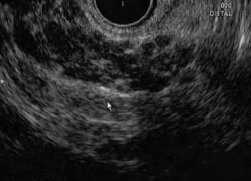
As imagens ultrassonográficas abaixo são de um paciente com pancreatite crônica. Nas imagens, notamos alguns critérios que corroboram com esse diagnóstico.
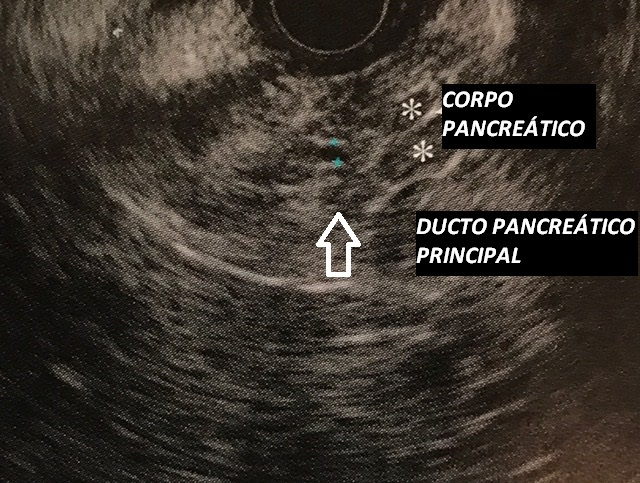
Ecoendoscopia setorial exibindo lobularidade difusa do corpo pancreático associada a estrias longitudinais hiperecoicas.
Clique nos links abaixo e assista aos vídeos de alguns pacientes com pancreatite crônica submetidos à EUS:
Para saber mais sobre este tema e outros relacionados, acesse o site Gastropedia clicando aqui!
QUIZ ! Vamos ver se você acerta essa ?
QUIZ !!! Vamos ver se você acerta as três questões na sequência ?
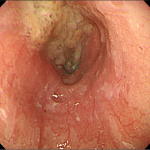
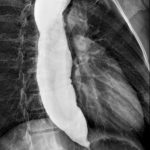
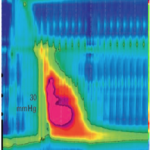
Paciente, feminino, 78 anos, com diagnóstico de megaesôfago chagásico e insuficiência cardíaca congestiva classe III. Refere disfagia progressiva de longa data que vem piorando nos últimos anos com escore atual de Eckardt de 11.
Dilatação da papila duodenal maior com balão para remoção de cálculos difíceis
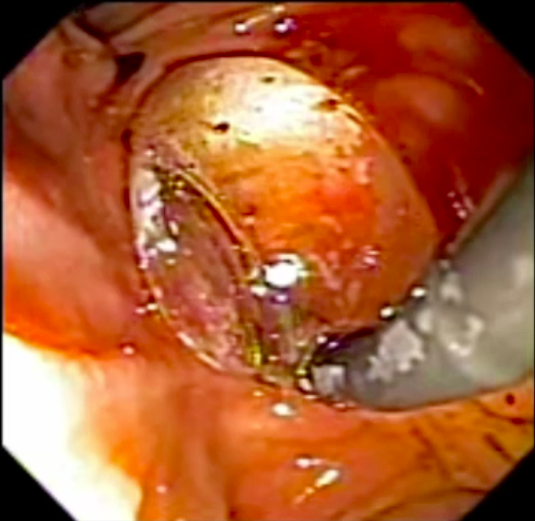
Colelitíase está presente em cerca de 10-20 % da população americana, sendo que 10-15 % destes pacientes irão cursar com coledocolitíase (1).
Mais de 90% dos cálculos de colédoco são extraídos apenas com papilotomia e varredura. Porém 10 % das coledocolitíases são representadas por cálculos gigantes (> 15 mm), que geralmente necessitam de procedimentos adicionais à papilotomia para sua extração.
Vários trabalhos na literatura comprovam que a dilatação da papila com balão após papilotomia é uma técnica simples, segura e eficaz no tratamento dos cálculos gigantes de colédoco, substituindo na maioria dos casos a tradicional litotripsia mecânica. Acrescenta-se que é uma técnica mais rápida, fato que diminui a quantidade de radiação a qual o paciente é exposto durante o procedimento(2,3).
Indicações:
Presença de cálculos de colédoco gigantes ou não, quando a papilotomia não foi suficiente para permitir a retirada do cálculo.
Contraindicação:
A principal contraindicação deste procedimento é a presença de desproporção acentuada entre o cálculo e o colédoco distal, seja pela presença de estenose ou não.
Técnica
A técnica consiste na realização da papilotomia seguido da passagem do balão dilatador transpapilar, mantendo-o 80% da sua extensão dentro do colédoco, e 20% na luz duodenal.
A escolha do diâmetro do balão depende do tamanho do cálculo e da via biliar distal:
- Cálculo/ colédoco distal 12-14 mm: balão 12-15 mm
- Cálculo/ colédoco distal 15-17 mm: balão 15-18 mm
- Cálculo/ colédoco distal 18-20 mm: balão 18-20 mm
O balão é preenchido com contraste para avaliação da cintura radiológica e insuflado até o diâmetro desejado de acordo com a pressão indicada no balão. O desaparecimento da cintura indica a ruptura do esfíncter, sendo fundamental para permitir a passagem do cálculo.
O tempo de permanência do balão insuflado não está padronizado na literatura, podendo ficar entre 30 seg a 3 minutos. A intenção de não desinsuflar o balão precocemente é somente por fins hemostáticos, visto que após o rompimento da “cintura”, ou seja, das fibras musculares do esfíncter, não há necessidade de manter o balão insuflado; não é isso que fará a dilatação mais efetiva, ao contrário do que muitos colegas ainda acreditam !
Após a dilatação da papila retira-se o balão e realiza-se a varredura com balão extrator ou basket.
Importante ressaltar que a dilatação deve ser precedida pela papilotomia, pois diversos estudos mostram que apenas a dilatação, sem uma esfincterotomia prévia, aumenta muito o índice de pancreatite.
Comentário
Pessoal, apesar do post ser sobre dilatação balonada da papila maior, vou me permitir comentar uma situação que vejo ocorrer com frequência mesmo com colegas experientes. É sobre a impactação do basket (cesto de Dormia) na papila.
Eu NÃO uso basket, a não ser que tenha um litotriptor de emergência disponível durante o procedimento ou que o basket seja do tipo Trapezoid RX, o qual permite a destruição dos cálculos através do acoplamento a uma pistola de pressão.
Já vi diversos colegas em situações difíceis quando o basket fica preso na papila e não é possível nem empurrá-lo e nem tracioná-lo, fazendo com que na maioria das vezes a resolução do caso seja através de uma cirurgia (já vi colegas conseguirem passar um balão dilatador em paralelo ao basket impactado e resolver a situação, mas isso não é o habitual). Nesses casos, quando a cirurgia não pode ser realizada de imediato, o paciente por vezes recebe alta com um fio de aço exteriorizado por uma das narinas ou o protegem com um acessório de silicone e o mesmo permanece no estômago até que a cirurgia possa ser realizada. Em casos de cálculos grande o risco dessa complicação é ainda maior ! Minha conduta nessas situações é a passagem de uma prótese plástica e agendamento de uma segunda abordagem em 6 semanas. Diversas vezes me surpreendi com a grande diminuição do tamanho do cálculo causado pelo atrito com a prótese após esse período, o que tornou a extração muito mais fácil e segura.
Recentemente com a introdução em nossa prática diária do SpyGlass, o qual possibilita a fragmentação e remoção desses cálculos sem maiores problemas, não vejo o porquê correr o risco de uma impactação com o uso do basket. De qualquer forma, essas situações citadas anteriormente são exceções, e taxa de sucesso na remoção dos cálculos gigantes através de uma esfíncterotomia associada à dilatação atinge cifras de 95% com índice de complicações não superiores a pacientes que realizam apenas a esficterotomia (4).
Referências
- Everhart JE, Khare M, Hill M, Maurer KR. Prevalence and ethnic differences in gallbladder disease in the United States. 1999 Sep;117(3):632-9.
- Itoi T, Itokawa F, Sofuni A et al. Endoscopic sphincterotomy combined with large balloon dilation can reduce the procedure time and fluoroscopy time for removal of large bile duct stones. Am J Gastroenterol 2009;104:560–5.
- Stefanidis G, Viazis N, Pleskow D, Manolakopoulos S, Theocharis L, Christodoulou C, et al. Large balloon dilation vs. mechanical lithotripsy for the management of large bile duct stones: a prospective randomized study. Am J Gastroenterol. 2011 Feb;106(2):278-85.
- Shim C, Kim JW, Lee TY, Cheon YK .Is Endoscopic Papillary Large Balloon Dilation Safe for Treating Large CBD Stones? Saudi Gastroenterol 2016;22(4):251-9
Qual agulha é melhor para punção ecoguiada do fígado ? FNA ou FNB ? Leia o ARTIGO COMENTADO !
Endoscopy. 2019 Jul 23. doi: 10.1055/a-0956-6922.
19 G aspiration needle versus 19 G core biopsy needle for endoscopic ultrasound-guided liver biopsy: a prospective randomized trial.
Ching-Companioni RA1, Diehl DL1, Johal AS1, Confer BD1, Khara HS1.
Department of Gastroenterology and Nutrition, Geisinger Medical Center, Danville, Pennsylvania, United States.
Introdução
A doença hepática crônica tem várias causas e é um importante fator de morbimortalidade. Embora exames laboratoriais e de imagem sejam úteis na avaliação hepatica, eles podem não ser capazes de determinar sua etiologia e, em alguns casos, podem não conseguir estimar com precisão o grau de fibrose hepática. A biópsia continua sendo uma ferramenta importante no diagnóstico e tratamento de algumas doenças crônicas do fígado. A biópsia percutânea ou pela via transjugular continuam sendo o padrão ouro utilizado para obtenção de fragmentos hepáticos, porém as biópsias guiadas por ultrassonografia endoscópica (EUS-LB) estão sendo cada vez mais utilizadas. Um benefício das biópsias ecoguiadas é a capacidade de executar com rapidez e segurança a obtenção de fragmentos de ambos os lobos hepáticos sob controle ultrassonográfico em tempo real durante todo o procedimento, minimizando o risco de punção inadvertida de um vaso ou mesmo outro órgão. Outros benefícios potenciais incluem o conforto do paciente durante o procedimento, pois habitualmente o mesmo encontra-se sob sedação profunda, e maior eficiência e conveniência para pacientes que necessitam de um biópsia hepática, uma esofagogastroduodenoscopia e/ou uma ecoendoscopia. Vários estudos usando a punção ecoguiada com aspiração com agulha fina (FNA) de 19 G mostraram a viabilidade e precisão do dessa técnica, com rendimento superior a 90%. Um estudo retrospectivo comparando biópsia hepática guiada por ecoendoscopia com biópsias adquiridas pela via percutânea ou transjugular mostrou que os diferentes métodos eram comparáveis em termos de quantidade de tecido obtido. Pesquisas em andamento se concentram em como melhorar as amostras obtidas com esta técnica (EUS-LB). Os estudos iniciais com EUS-LB utilizaram uma agulha 19 G FNA ou a agulha TruCut 19 G (Merit Medical, South Jordan, Utah, EUA). Desde o desenvolvimento de agulhas para biópsia guiada por EUS, esses dispositivos foram testados para EUS-LB, com resultados encorajadores. No entanto, nenhuma comparação prospectiva in vivo dessas agulhas tinha sido realizada. Neste estudo, objetivamos comparar o rendimento tecidual de uma agulha de EUS de 19 G (FNB) com o de uma agulha 19 G EUS (FNA) em um estudo prospectivo randomizado. A hipótese do nosso estudo foi que as agulhas de 19 G do tipo FNB proporcionaria melhores rendimentos teciduais do que a agulha FNA.
Métodos
Este foi um estudo prospectivo, paralelo, randomizado, comparando fragmentos de tecidos hepáticos obtidos por dois tipos diferentes de agulhas de 19 G, FNA versus FNB.
O desfecho primário obtido foi o comprimento do fragmento. Os desfechos secundários foram, comprimento agregado da amostra, número de tríades portais completas (CPTs) e eventos adversos.
Uma passagem transgástrica e uma transduodenal foram realizadas com a mesma agulha em cada paciente.
Os comprimentos das amostras foram medidos antes e após o processamento histológico.
Fragmentos obtidos logo após a punção. Foram peneirados com solução salina
Fragmentos posicionados ao lado de uma régua para aferição do comprimento das amostras
Resultados
Os 40 pacientes encaminhados para realização das biópsias guiadas por ecoendoscopia foram randomizados em dois grupos distintos.
Um grupo foi submetido a FNA (n = 20) e outro foi submetido a FNB (n = 20).
Todos os pacientes selecionados para o estudo eram portadores de alguma doença parenquimatosa crônica e foram submetidos a biópsias de ambos os lobos hepáticos.
As biópsias de FNB produziram amostras médias mais longas (média de pré-processamento de 2,09 cm vs. média 1,47 cm e pós-processamento médio de 1,78 cm vs. média 1,05 cm; (P <0,001), e um comprimento agregado da amostra maior (média de pré-processamento de 15,78 cm vs. 10,89 cm; (P = 0,003) e mais CPTs (média 42,6 vs 18,1; (P <0,001) em comparação com a agulha FNA. Não houve eventos adversos graves em nenhum dos grupos. A incidência de efeitos adversos foi semelhante entre ambos. A dor pós-biópsia foi observada em 30% dos que foram submetidos a FNB e 35% e a 30% no grupo da FNA, porém sem diferença estatisticamente significativa.
Conclusão
Os fragmentos obtidos através da punção ecoguiada por FNB foram maiores, mais longos, e com uma maior quantidade de tríade portais completas do que o tecido obtido através de FNA. Não houve diferença em relação a incidência de efeitos adversos entre os dois grupos estudados.
Comentário
A biópsia transjugular ou percutânea continuam sendo o padrão-ouro para a obtenção de fragmentos hepáticos na avaliação da fibrose nas doenças crônicas do fígado. Porém, com o advento das punções ecoguiadas isso tende a mudar, já que esse método apresenta diversas vantagens sobre os métodos atualmente utilizados. Para citar algumas :
- É uma abordagem tecnicamente reprodutível, independentemente do tipo corporal, pois a agulha necessita apenas atravessar a parede gástrica ou duodenal para alcançar o parênquima hepático;
- É teoricamente menos dolorosa que a abordagem percutânea, pois não requer punção na parede abdominal;
- É uma abordagem guiada por imagens em tempo real, que permite visualizar e evitar a punção de vasos de tamanho tão pequeno quanto 1 mm;
- Fornece acesso a uma área muito maior do parênquima hepático, pois todo o lobo esquerdo e a maioria do lobo direito podem ser avaliados para possíveis locais de punção da agulha;
- Além de obter tecido, a biópsia hepática guiada por ecoendoscopia também oferece o benefício de uma avaliação abrangente do trato digestivo alto, incluindo rastreio ou acompanhamento de varizes esofágicas.
Portanto, o atual artigo está entre tantos que corroboram a vantagem da punção guiada por ecoendoscopia sobre os demais métodos atualmente utilizados, e ainda, com o advento de novas agulhas (FNB) conseguimos com a mesma incidência de efeitos colaterais, uma precisão diagnóstica maior.
Clique aqui para acessar o artigo original !
Vídeo ilustrativo de um caso onde foram realizadas biópsias hepáticas por FNB.
Referências
[1] Rockey DC, Caldwell SH, Goodman ZD et al. Liver biopsy. Hepatology 2009; 49: 1017 – 1044
[2] Rockey DC, Bissell DM. Noninvasive measures of liver fibrosis. Hepatology 2006; 43: S113 – S120
[3] Rockey DC. Non-invasive assessment of liver fibrosis and portal hypertension with transient elastography. Gastroenterology 2008; 134: 8 – 14
[4] Ziol M, Handra-Luca A, Kettaneh A et al. Noninvasive assessment of liver fibrosis by measurement of stiffness in patients with chronic hepatitis C. Hepatology 2005; 41: 48 – 54
[5] Parekh PJ, Majithia R, Diehl DL et al. Endoscopic ultrasound-guided liver biopsy. Endosc Ultrasound 2015; 4: 85 – 91
[6] Stavropoulos SN, Im GY, Jlayer Z et al. High yield of same-session EUSguided liver biopsy by 19-gauge FNA needle in patients undergoing EUS to exclude biliary obstruction. Gastrointest Endosc 2012; 75: 310 – 318
[7] Diehl DL, Johal AS, Khara HS et al. Endoscopic ultrasound-guided liver biopsy: a multicenter experience. Endosc Int Open 2015; 3: E1 – 6
[8] Schulman AR, Thompson CC, Odze R et al. Optimizing EUS-guided liver biopsy sampling: comprehensive assessment of needle types and tissue acquisition techniques. Gastrointest Endosc 2017; 85: 419 – 426
[9] Dewitt J, McGreevy K, Cummings O et al. Initial experience with EUS guided Tru-cut biopsy of benign liver disease. Gastrointest Endosc 2009; 69: 535 – 542
[10] Gor N, Salem SB, Jakate S et al. Histological adequacy of EUS-guided liver biopsy when using a 19-gauge non-Tru-Cut FNA needle. Gastrointest Endosc 2014; 79: 170 – 172
[11] Rocken C, Meier H, Klauck S et al. Large-needle biopsy versus thinneedle biopsy in diagnostic pathology of liver diseases. Liver 2001; 21: 391 – 397
[12] Sey MSL, Al-Haddad M, Imperiale TF et al. EUS-guided liver biopsy for parenchymal disease: a comparison of diagnostic yield between two core biopsy needles. Gastrointest Endosc 2016; 83: 347 – 352
[13] Gleeson FC, Clayton AC, Zhang L et al. Adequacy of endoscopic ultrasound core needle biopsy specimen of nonmalignant hepatic parenchymal disease. Clin Gastroenterol Hepatol 2008; 6: 1437 – 1440
[14] Pineda JJ, Diehl DL, Miao CL et al. EUS-guided liver biopsy provides diagnostic samples comparable with those via the percutaneous or transjugular route. Gastrointestinal Endosc 2016; 83: 360 – 365
[15] Nieto J, Khaleel H, Challita Y. EUS-guided fine-needle core liver biopsy sampling using a novel 19-gauge needle with modified 1-pass, 1 actuation wet suction technique. Gastrointest Endosc 2018; 87: 469 – 475
[16] Mok SRS, Diehl DL, Johal AS et al. A prospective pilot comparison of wet and dry heparinized suction for EUS-guided liver biopsy (with videos). Gastrointest Endosc 2018; 88: 919 – 925
[17] Schindelin J, Rueden CT, Hiner MC et al. The ImageJ ecosystem: an open platform for biomedical image analysis. Mol Reprod Dev 2015; 82: 518 – 529
[18] Cotton PB, Eisen GM, Aabakken L et al. A lexicon for endoscopic adverse events: report of an ASGE workshop. Gastrointest Endosc 2010; 71: 446 – 454
[19] Mok SR, Diehl DL, Johal AS et al. Endoscopic ultrasound-guided biopsy in chronic liver disease: a randomized comparison of 19-G FNA and 22-G FNB needles. Endosc Int Open 2019; 7: E62 – 71
[20] Attam R, Arain MA, Bloechl SJ et al. “Wet suction technique (WEST)”: a novel way to enhance the quality of EUS-FNA aspirate. Results of a prospective, single-blind, randomized, controlled trial using a 22- gauge needle for EUS-FNA of solid lesions. Gastrointest Endosc 2015; 81: 1401 – 1407
[21] Diehl DL, Mok SRS, Khara HS et al. Heparin priming of EUS-FNA needles does not adversely affect tissue cytology or immunohistochemical staining. Endosc Int Open 2018; 6: E356 – E362
[22] DeWitt J, LeBlanc J, McHenry L et al. Endoscopic ultrasound-guided fine needle aspiration cytology of solid liver lesions: a large single center experience. Am J Gastroenterol 2003; 98: 1976 – 1981
[23] Hollerbach S, Willert J, Topalidis T et al. Endoscopic ultrasound-guided fine-needle aspiration biopsy of liver lesions: histological and cytological assessment. Endoscopy 2003; 35: 743 – 749
[24] tenBerge J, Hoffman BJ, Hawes RH et al. EUS-guided fine needle aspiration of the liver: indications, yield, and safety based on an international survey of 167 cases. Gastrointest Endosc 2002; 55: 859 – 862
[25] Early DS, Acosta RD, Chandrasekhara V et al. Adverse events associated with EUS and EUS with FNA. Gastrointest Endosc 2013; 77960: 839 – 843
[26] Eisenberg E, Konopniki M, Veitsman E et al. Prevalence and characteristics of pain induced by percutaneous liver biopsy. Anesth Analg 2003; 96: 1392 – 1396
[27] Procopet B, Bureau C, Métivier S et al. Tolerance of liver biopsy in a tertiary care center: comparison of the percutaneous and the transvenous route in 143 prospectively followed patients. Eur J Gastroenterol Hepatol 2012; 24: 1209 – 1213
Caso Clínico – Espiroquetose Intestinal
Paciente, masculino, 45 anos, HIV + há cerca de 20 anos, relata ter interrompido o uso de anti-retrovirais há 6 meses por conta própria.
Queixa-se de diarreia associada a episódios de enterorragia nos últimos 2 meses.
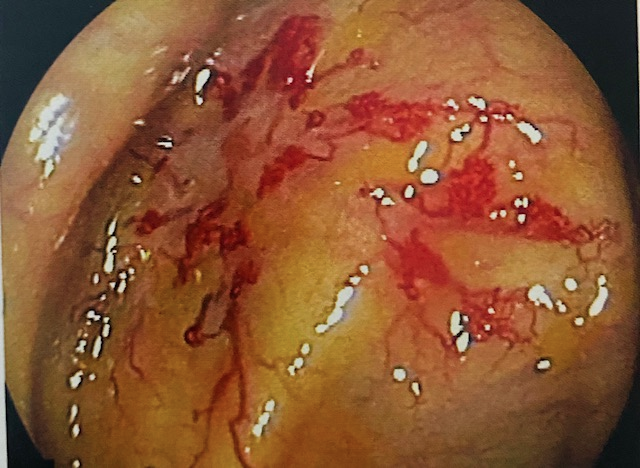
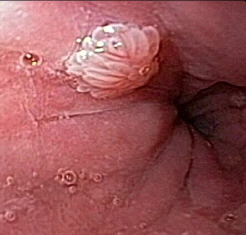
Foi encaminhado ao nosso serviço para realização de colonoscopia que evidenciou em cólon sigmoide, múltiplas erosões planas e desnudas esparsamente distribuídas sobre mucosa edemaciada e medindo entre 2-3 mm. Ainda em sigmoide notou-se a presença de lesões polipoides, com tamanhos em torno de 4-8 mm, avermelhadas e com erosões apicais.
Seguem as imagens:
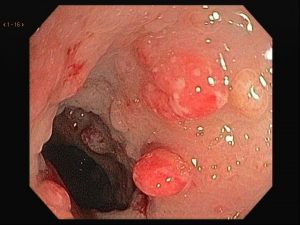
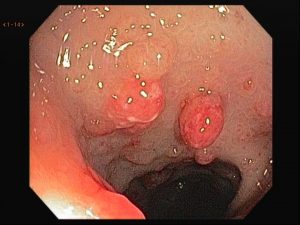
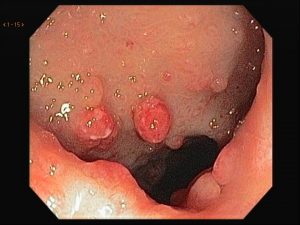
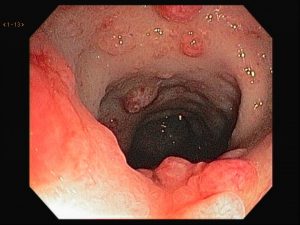
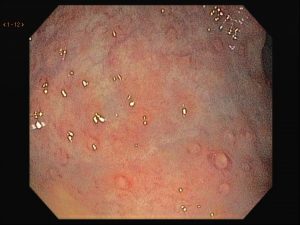
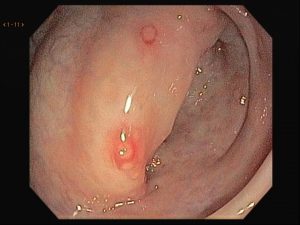
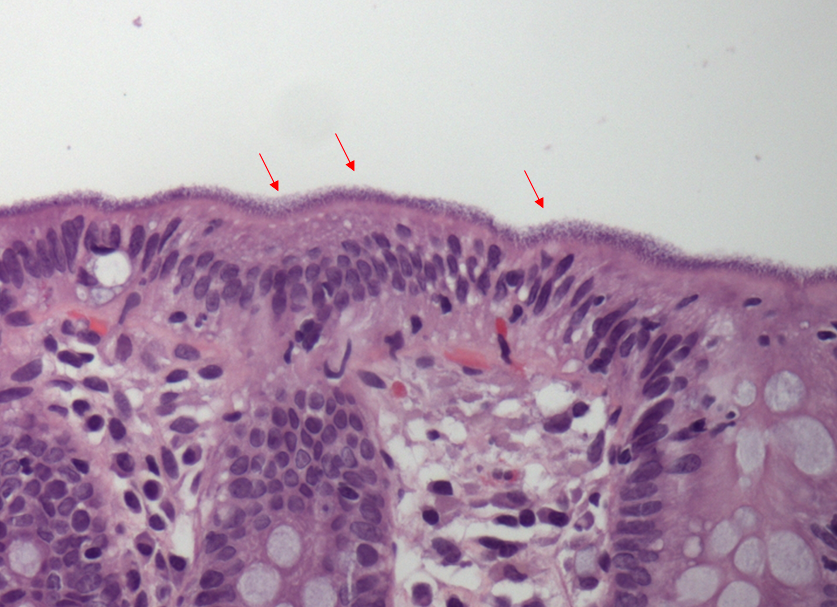
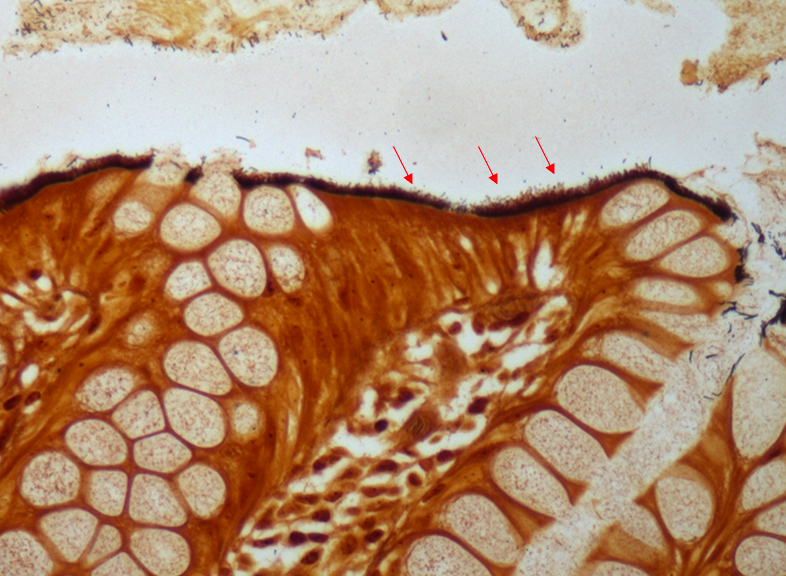
Realizamos múltiplas biópsias que mostraram colite crônica com componente erosivo e hiperplasia folicular linfóide com presença de estruturas consistentes com espiroquetose intestinal.
Revisão:
- A espiroquetose intestinal é definida histologicamente como a presença de microrganismos da família spirochetaceae ligadas ao ápice das células do epitélio cólico.
- A doença pode ser provocada por um grupo heterogêneo de bactérias. Em humanos, a Brachyspira aalborgi e a Brachyspira pilosicoli predominam.
- A incidência da colonização intestinal por espiroquetas varia de 1% nos países desenvolvidos a até 34% nas áreas mais pobres, atingindo taxas de colonização de 62,5% entre homossexuais e em pacientes portadores do vírus da imunodeficiência humana (HIV).
- O significado clínico dessa colonização ainda é incerto e a maioria dos infectados permanece assintomática.
- Quando há sintomas gastrointestinais, o tratamento mais utilizado e efetivo é feito com metronidazol na dose de 500 mg 3 vezes ao dia por 10 dias. Há relatos de séries de casos onde a clindamicina e macrolídeos foram utilizados com sucesso.
- Manifestação de sintomas é mais comum em pacientes imunodeprimidos.
- A infecção pelo Treponema pallidum deve ser excluída, pois os tratamentos são diferentes e as complicações por essa última são mais graves.
Referências
- Bechara C. S. et al. “ESPIROQUETOSE INTESTINAL ‐ RELATO DE CASO E REVISÃO DE LITERATURA.” Journal of Coloproctology vol. 38 (2018); 68. doi.org/10.1016/j.jcol.2018.08.144
2. Nadal, Luis Roberto Manzione, & Nadal, Sidney Roberto. (2011). Intestinal spirochetosis. Journal of Coloproctology (Rio de Janeiro), 31(4), 405-406.