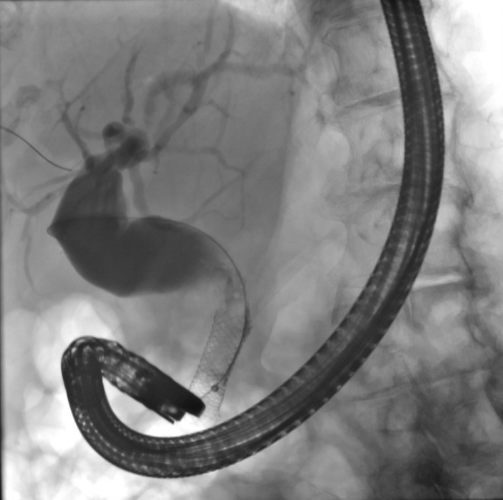
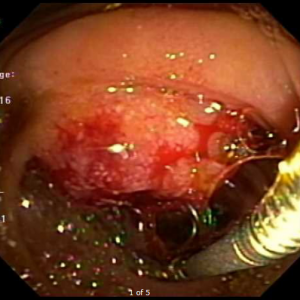
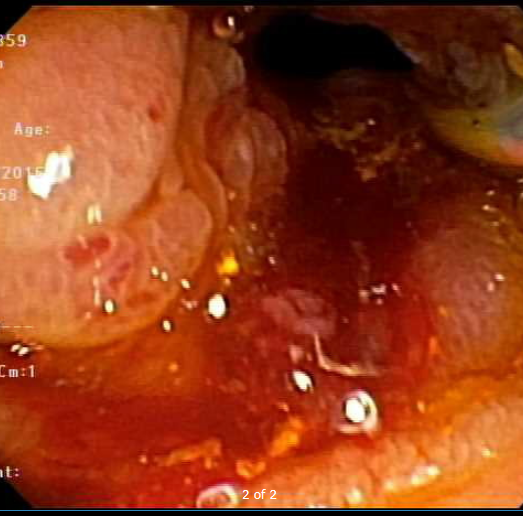
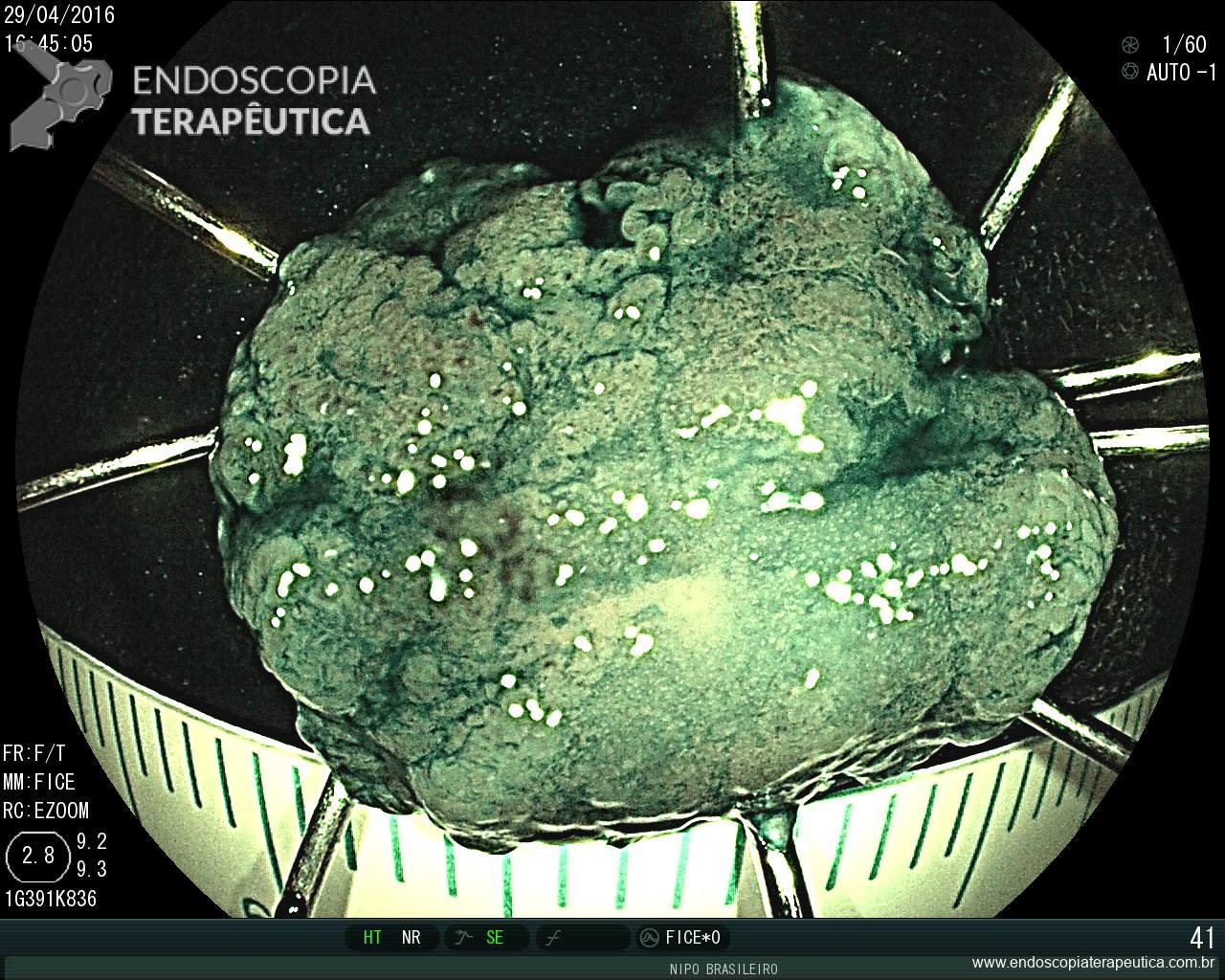
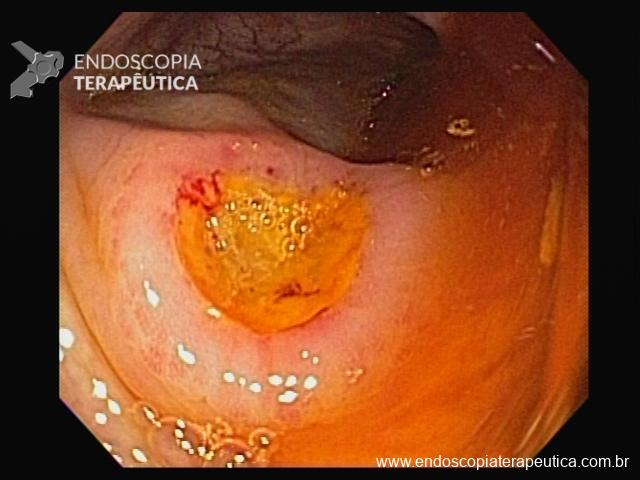
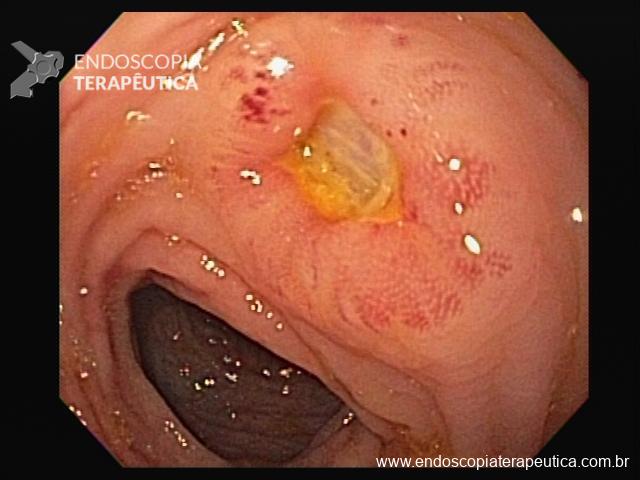
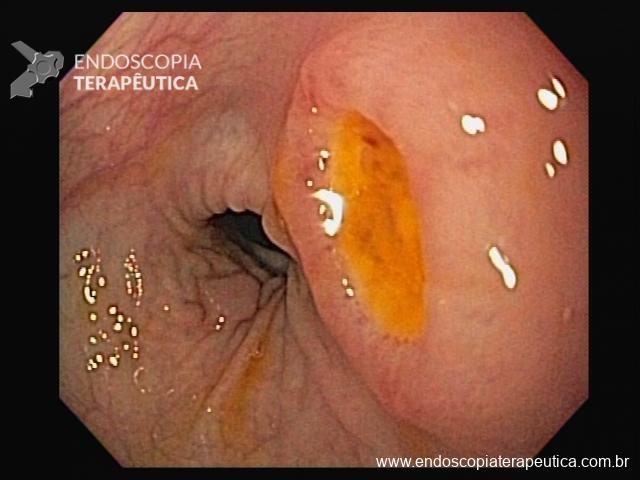
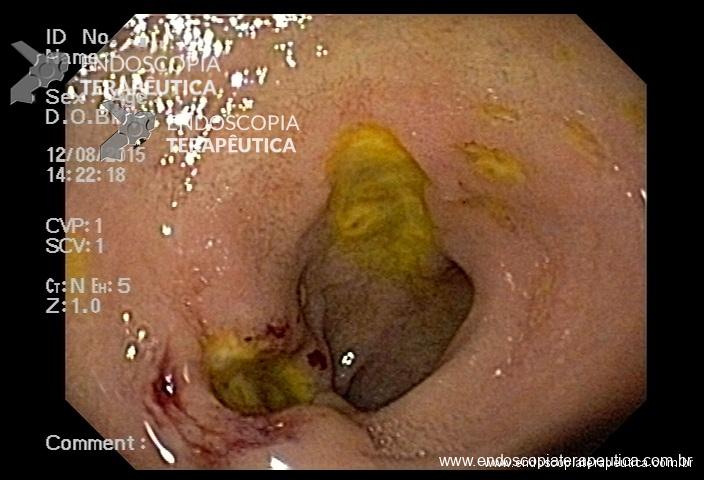
A ecoendoscopia intervencionista está cada vez ganhando mais espaço na literatura, e também em nosso meio, como opção para drenagem das vias biliares após falha da CPRE.
Sendo importante para todos os médicos endoscopistas, mesmo aqueles que não realizam ecoendoscopia, terem conhecimento sobre as técnicas e as indicações da drenagem biliar ecoguiada (EUS-BD).
Este post será dividido em tópicos, e terá enfoque principal na revisão das mais recentes evidências sobre a EUS-BD:
1- EUS-BD vs DBTP
Por um bom tempo a drenagem biliar transhepática percutânea (DBTP) constituiu a principal modalidade de resgate para drenagem biliar após falha da CPRE.
Entretanto, ensaio-clínico randomizado, com amostra de 25 pacientes com obstrução biliar maligna irresecável, comparando a EUS-BD com a DBTP, demonstrou taxas semelhantes de sucesso técnico, clínico e de complicações.(1)
Estudo retrospectivo mais recente demonstrou que, apesar de um sucesso técnico maior com a DBTP, a taxa de sucesso clínico foi semelhante entre os dois procedimentos. Sendo que a DBTP esteve associada com maior taxa de eventos adversos, de reintervenção não-programada e consequentemente com maiores custos.(2) Outros estudos também sugeriram que a combinação da CPRE e do EUS no mesmo procedimento parece ser uma estratégia de menor custo, comparada ao encaminhamento parar a drenagem percutânea.(3,4)
Dessa forma, na falha da CPRE para drenagem da via biliar, além da drenagem transparietal percutânea, a drenagem ecoguiada é boa opção. As evidências atuais apontam para eficácias semelhantes, sendo que a EUS-BD parece ser uma técnica com menores complicações.
2 – EUS-BD: extrahepático vs intrahepático
A drenagem biliar ecoendoscópica em pacientes com anatomia preservada, seja pela técnica de rendezvous ou transluminal, pode ser realizada através do acesso intra ou extra-hepático. Metanálise realizada com oito estudos, que incluíram pacientes com estenose biliar distal, comparou a drenagem biliar ecoguiada realizada pelo acesso intra-hepático com o acesso extra-hepático, e evidenciou eficácia semelhante entre ambos os métodos, porém o acesso extra-hepático apresentou menores taxas de complicações.(5)
As principais complicações relacionadas com o acesso intra-hepático são: pneumoperitônio, fístula biliar, dor pós-procedimento e migração da prótese. Sendo explicados pelo fato de que nessa forma de acesso: a agulha percorre a cavidade peritoneal; o estômago e o fígado se movimentam de forma independente durante a respiração; e o menor calibre dos ductos intra-hepáticos pode não acomodar adequadamente a prótese.(6) Também tem sido relatado na literatura menor tempo de procedimento e de internação com drenagem biliar por via extra-hepática.(7)
Dessa forma conclui-se que para a drenagem ecoguiada das vias biliares, seja pela técnica rendezvous ou transluminal, pode-se utilizar o acesso intra ou extra-hepático. As técnicas parecem apresentar eficácias semelhantes, porém com menores taxas de complicações com o acesso extra-hepático.
3 – EUS-BD: Rendezvous vs transluminal
Existem poucos trabalhos comparando as técnicas de drenagem biliar rendezvous guiada por ecoendoscopia (EUS-RV) com a drenagem biliar transluminal guiada por ecoendocopia (EUS-TL). Estudo retrospectivo, com amostra de 35 pacientes com obstrução biliar distal maligna, comparou essas duas técnicas e demonstrou eficácia e segurança semelhantes.(8)
Para muitos endoscopistas, a EUS-RV tem sido a técnica preferida pois evita a criação de uma fístula bilioentérica permanente, bem como evita também a necessidade de dilatação do trajeto fistuloso que é uma etapa do procedimento que pode provocar sangramento, pneumoperitônio e pneumomediastino.
Já as vantagens da EUS-TL são a possibilidade de ser realizada em pacientes com anatomia alterada ou com obstrução gastroduodenal, evitar o risco de perda do fio-guia na troca para o duodenoscópio, menor tempo de execução do procedimento, e diminuição do risco de pancreatite pós-procedimento.
Atualmente há uma tendência por boa parte dos ecoendoscopistas em ser inicialmente tentada a EUS-RV, e no caso de falha, seja por dificuldade de transpor a estenose ou a papila, ser posteriormente realizada a EUS-TL.
4 – EUS-TL: hepaticogastrostomia vs coledocoduodenostomia
Na opção por realização da EUS-TL, deve-se considerar a realização de hepaticogastrostomia ou coledocoduodenostomia.
Metanálise que incluiu 7 estudos, dos quais 6 retrospectivos, com pacientes com estenose biliar distal, comparou a drenagem biliar ecoguiada pelas técnicas de hepaticogastrosotomia vs coledocoduodenostomia, e evidenciou sucesso técnico semelhantes entre as duas modalidades. Entretanto, a análise comparativa favoreceu a coledocoduosdenostomia por ter apresentado menores taxas de complicações.(5)
5 – EUS-TL: prótese plástica vs metálica
Até o momento, não existem artigos que comparem o uso de próteses plásticas e metálicas na drenagem ecoguiada transluminal. Entretanto é consenso entre os ecoendoscopistas que deve-se favorecer o uso de próteses metálicas totalmente cobertas, para que haja uma minimização do risco de migração e formação de fístula.(6)
Para observação de caso clínico com imagens e vídeo ilustrando a drenagem biliar ecoguiada clicar na referência abaixo:
Ribeiro MSI, Franco MC, Maluf-Filho F. An easier option for endoscopic ultrasound-guided biliary drainage: cannulation using two antiparallel guidewires. Endoscopy 2016.
Referências:
- Artifon EL, Aparicio D, et al. Biliary Drainage in Patients With Unresectable, Malignant Obstruction Where ERCP Fails. J Clin Gastroenterol. 2012;46(9):768–74.
- Khashab MA, Valeshabad AK, et al. A Comparative Evaluation of EUS-Guided Biliary Drainage and Percutaneous Drainage in Patients with Distal Malignant Biliary Obstruction and Failed ERCP. Dig Dis Sci. 2015;60(2):557–65.
- Gornals JB, Moreno R, et al. Single-session endosonography and endoscopic retrograde cholangiopancreatography for biliopancreatic diseases is feasible, effective and cost beneficial. Dig Liver Dis. 2013;45(7):578–83.
- Fabbri C, Luigiano C, et al. Endoscopic ultrasound-guided treatments: Are we getting evidence based – A systematic review. World J Gastroenterol. 2014;20(26):8424–48.
- Khan MA, Akbar A, et al. Endoscopic Ultrasound-Guided Biliary Drainage: A Systematic Review and Meta-Analysis. Dig Dis Sci. 2015;61(3):684–703.
- Khashab MA, Levy MJ, et al. EUS-guided biliary drainage. Gastrointest Endosc. 2015;82(6):993–1001.
- Dhir V, Bhandari S, et al. Comparison of transhepatic and extrahepatic routes for EUS-guided rendezvous procedure for distal CBD obstruction. United Eur Gastroenterol J. 2013;1(2):103–8.
- Khashab MA, Valeshabad AK, et al. EUS-guided biliary drainage by using a standardized approach for malignant biliary obstruction: Rendezvous versus direct transluminal techniques (with videos). Gastrointest Endosc. 2013;78(5):734–41.