QUIZ! – Qual o diagnóstico?
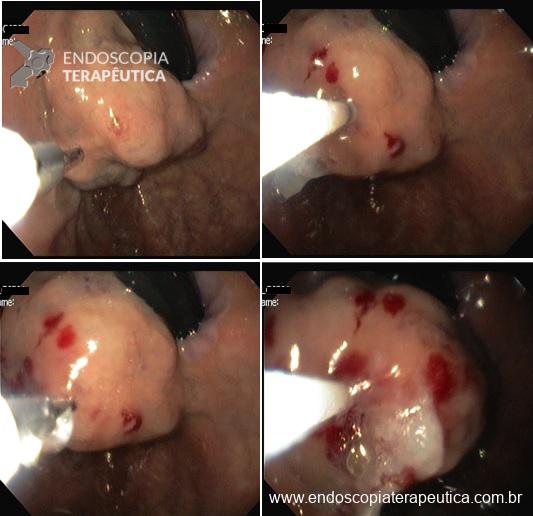
Tratamento endoscópico de variz de fundo gástrico com injeção de cola de cianoacrilato
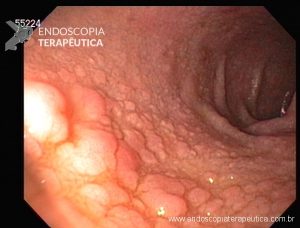
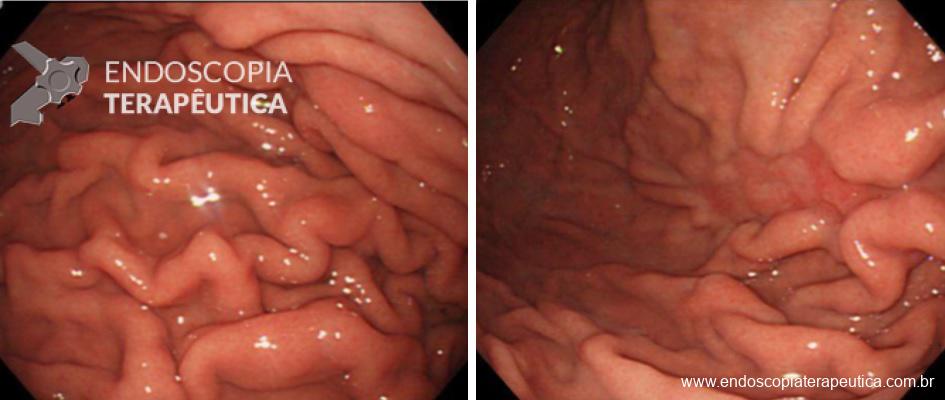
Paciente do sexo feminino, 67 anos, com anemia e história de episódios frequentes de melena. À endoscopia foi diagnosticada grande variz de fundo gástrico. Devido à história de hemorragia prévia foi optado pela obliteração com cola de cianoacrilato.
A obliteração de varizes gástricas com cianoacrilato é um tratamento efetivo e com baixo índice de complicações. Porém, alguns cuidados técnicos devem ser observados:
-
- Utilizar aparelho de visão frontal, lubrificando sua estrutura externa distal com silicone ou lipiodol para prevenir a adesão do cianoacrilato ao aparelho
-
- Inserir também no canal de trabalho do aparelho soluções lubrificantes como silicone para facilitar a inserção do cateter e evitar adesão potencial do cianoacrilato
-
- Evitar realizar sucção de secreções durante o procedimento (evita possível sucção acidental de cianoacrilato extravasado)
-
- Utilizar cateter injetor pré escovado com solução salina (ou com lipiodol).
-
- Preparar o adesivo tissular a ser injetado em solução habitual de 1:1 de cianoacrilato e lipiodol
-
- Após a punção da variz injetar a solução de cianoacrilato e seguir com a injeção de solução salina para total remoção do adesivo tissular de dentro do cateter e inserção no lúmen do vaso
-
- Quando retirar a agulha do interior do vaso (atentar para realizar isso de forma ágil após a injeção para evitar impactação do cateter ao adesivo tissular dispensado no vaso), realizar nova injeção de solução salina para lavagem completa do cateter do lúmen gástrico
-
- Logo que a injeção for completada, retirar o aparelho com a agulha recolhida e o cateter no seu interior. Com o aparelho removido do paciente, expõe-se o cateter e corta-se a sua ponta, evitando o contato do cianoacrilato residual do cateter com o canal de trabalho.
-
- Limpar a ponta do aparelho com silicone e atentar para uma lavagem adequada dos canais de trabalho
Para saber mais sobre o tratamento das varizes de fundo gástrico acesse o link abaixo:
https://endoscopiaterapeutica.net/pt/assuntosgerais/assuntos-gerais-tratamento-endoscopico-de-varizes-de-fundo-gastrico/
Qualidade em Endoscopia – Como diagnosticar o câncer gástrico precoce?
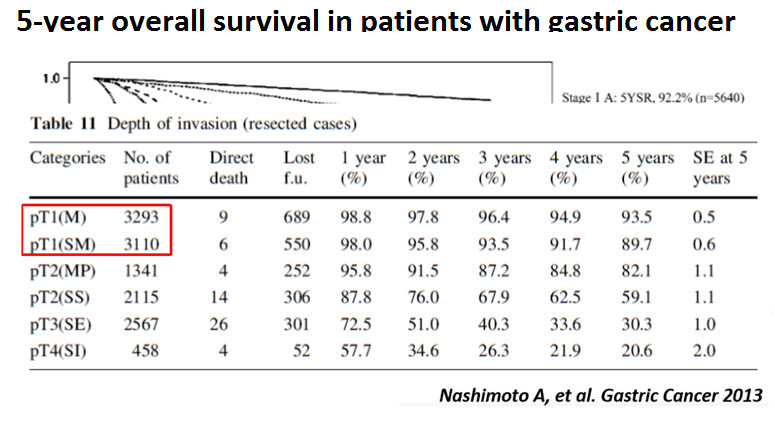
Quanto mais cedo for realizado o diagnóstico do câncer gástrico, melhor o prognóstico e a qualidade de vida dos pacientes. Lesões diagnosticadas e tratadas quando ainda estão restritas à mucosa ou submucosa e sem comprometimento linfonodal (estadio I) apresentam sobrevida média em 5 anos acima de 90%. No Japão, metade dos cânceres gástricos são diagnosticados nesta fase. Esta é uma realidade muito diferente da brasileira. Por aqui, o diagnóstico no estadio I está bem abaixo dos 10% com grande variação entre os trabalhos e a sobrevida média em 5 anos é em torno de 20% (1).
Tabela 1. (Clique para ampliar) Sobrevida média em 5 anos de pacientes com câncer gástrico. Nashimoto A, et al. Gastric Cancer 2013.
A pergunta que fica é: O que nós podemos fazer para melhorar nosso diagnóstico? Neste post tentaremos responder essa pergunta através de dicas para melhorar a técnica endoscópica, caracterizar melhor as alterações endoscópicas sugestivas de neoplasia precoce e discutir sobre como descrever corretamente estas lesões. Este artigo é baseado na conferência da ESGE “Quality in Endoscopy – Upper GI endoscopy and neoplasia”, realizada em Berlin na Alemanha no mês de abril deste ano. Todas as aulas desta conferência estão disponíveis no link http://www.quality-in-endoscopy.org/meeting-presentations-qie9.html.
O exame endoscópico
Para melhorar o diagnóstico precisamos melhorar a nossa técnica de avaliação. Muitas vezes, devido à falta de tempo, baixa remuneração ou grande número de pacientes para fazer exame, deixamos de observar algumas coisas de extrema importância.
- Preparo
A presença de saliva, bolhas e muco durante o exame pode impedir a identificação de lesões discretas. Além disso, os movimentos peristálticos ou a hipercontratilidade do órgão também podem prejudicar a avaliação. Para reduzir estes problemas algumas medidas podem ser utilizadas:
- Administrar alguns minutos antes do exame:
- Pronase 20.000 U ou 2 ml de Acetilcisteína (Fluimucil) para diminuir o muco.
- Simeticona – 2 ml diluídos em 50 ml de água para reduzir as bolhas.
- Logo antes de iniciar o procedimento:
- Administrar Buscopan 10 mg por via endovenosa para reduzir o peristaltismo.
- Após a introdução do aparelho:
- Aspirar todo o líquido e se ainda houverem bolhas ou muco, realizar a lavagem com simeticona diluída em água até a limpeza completa.
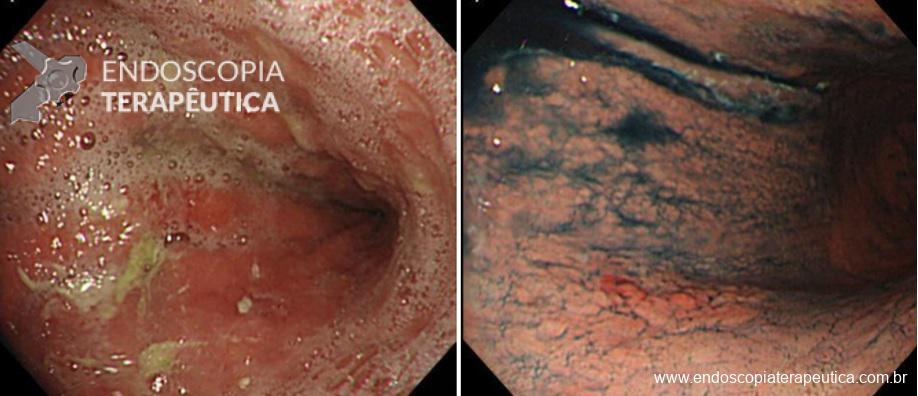
Figura 1. (Clique para ampliar) Estômago com grande quantidade de saliva e bolhas, prejudicando a avaliação. Lesão deprimida identificada após a limpeza, insuflação e cromoscopia com índigo carmin. Imagem da aula “What we can learn with the japanese” de Akido Ono, apresentada na conferência “Quality in Endoscopy – Upper GI endoscopy and neoplasia” da ESGE.
2. Insuflação
A falta de uma insuflação adequada muitas vezes impede a avaliação completa do órgão. O endoscopista deve insuflar completamente o estômago até as pregas se afastarem permitindo a avaliação da mucosa entre elas. Se o paciente tem um esfíncter esofágico inferior muito frouxo, com escape de ar impedido a adequada insuflação, a manobra de Sellick (compressão suave da cartilagem crico-tireóidea colabando o esôfago) pode ser utilizada para obter uma boa insuflação.
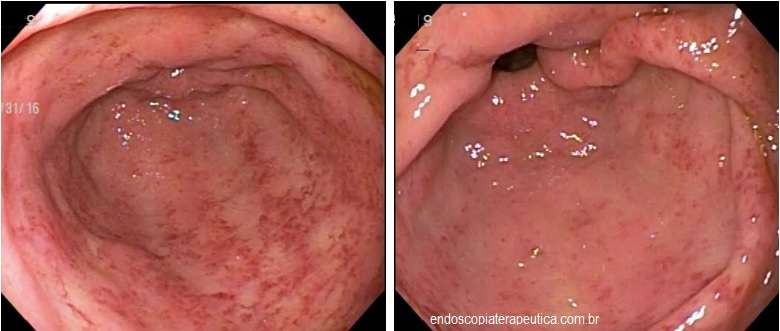
Figura 2. (Clique para ampliar) Estômago mal insulflado. Lesão deprimida com retração de pregas identificada após a adequada insuflação. Imagem da aula “What we can learn with the japanese” de Akido Ono, apresentada na conferência “Quality in Endoscopy – Upper GI endoscopy and neoplasia” da ESGE.
3. Exame cuidadoso
Para diagnosticar alterações discretas é necessário procurar com cuidado. Todas as paredes do órgão devem ser avaliadas e de preferência mais de uma vez, utilizando níveis diferentes de insuflação. Também é necessário dedicar tempo ao exame. Quanto maior o tempo de exame, maior a chance de identificar uma lesão precoce. Utilizando um valor de corte de 7 minutos é observada uma taxa de detecção 2 x maior de lesões de alto risco (atrofia, metaplasia intestinal e displasia gástrica) e 3 x maior no diagnóstico de displasia e câncer gástrico (2).
Reconhecendo as lesões
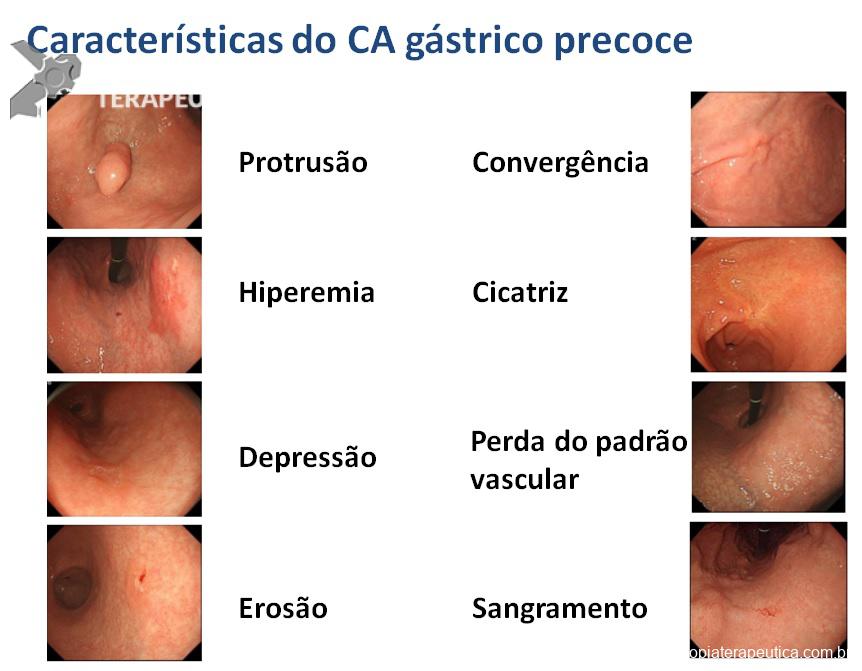
As lesões precoces muitas vezes apresentam alterações muito sutis que podem inclusive ser confundidas com mucosa normal ou trauma causado pelo aparelho. A utilização de um equipamento com alta definição e a utilização de corantes pode ajudar muito no diagnóstico. Sempre que uma área suspeita é identificada, ela deve ser avaliada com cuidado. Todo o muco e saliva devem ser removidos, o estômago deve ser bem distendido e a cromoscopia eletrônica (NBI, Fice, I-Scan) ou com corantes (Índigo Carmin) devem ser utilizadas para caracterizar melhor a lesão.
Figura 3. (Clique para ampliar) Características endoscópicas das lesões precoces. Figura editada utilizando imagens da aula “What we can learn with the japanese” de Akido Ono, apresentada na conferência “Quality in Endoscopy – Upper GI endoscopy and neoplasia” da ESGE.
Descrevendo as lesões
A descrição das lesões é muito importante. O laudo deve descrever todos os detalhes da lesão. Isto é fundamental para a decisão terapêutica e também para reduzir a repetição desnecessária do exame endoscópico.
Deve ser descrita a localização, distância de áreas de referência (cárdia, TEG, piloro, incisura angularis), tamanho e extensão da lesão, número, morfologia e suspeita clínica. Também, se aplicável, deve ser descrita a presença de sinais de hemorragia, cirurgias prévias, presença de estenose, se a lesão é transponível ou não e também as técnicas endoscópicas utilizadas (cromoscopia, magnificação, biópsias, ressecções). A documentação fotográfica ou em vídeo também é importante para a avaliação da lesão pela equipe que vai decidir a conduta terapêutica.
Para a descrição morfológica das lesões é importante utilizarmos classificações validadas. Isso permite uma comunicação eficiente entre o endoscopista e qualquer outro médico que avaliar o laudo. A mais indicada é a classificação Japonesa do câncer gástrico precoce. Utilizando esta classificação é possível estimar o risco de invasão submucosa.
Classificação Japonesa do Câncer Gástrico precoce: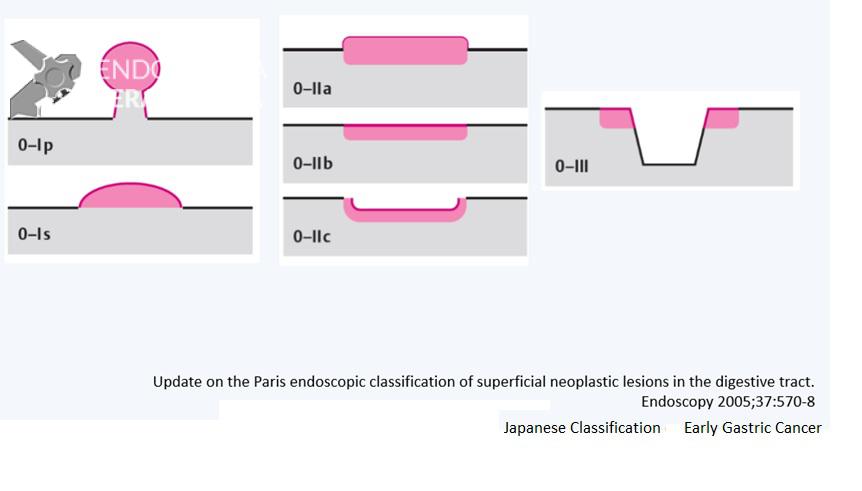
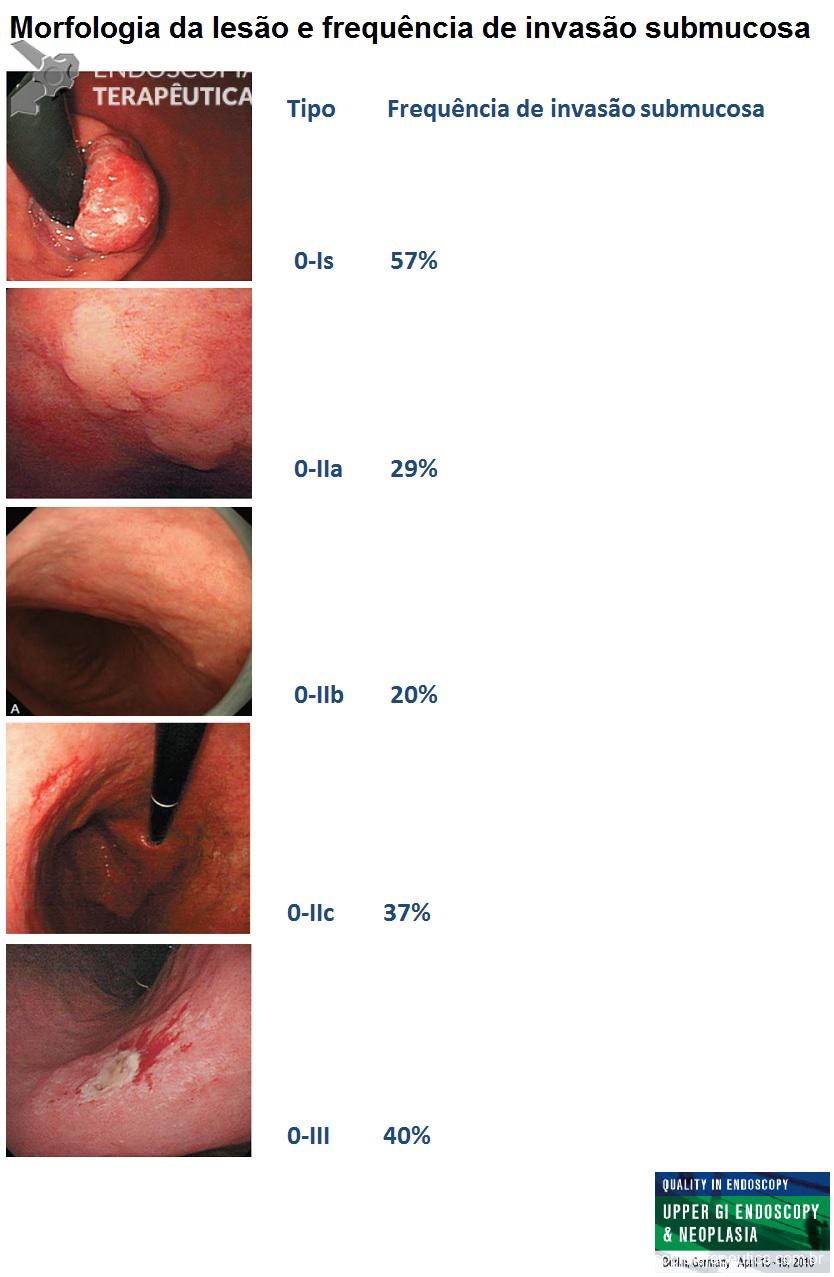
Figura 4. Clique para ampliar.
Figura 5. (Clique para ampliar) Classificação endoscópica e correlação com risco de invasão submucosa. Figura editada utilizando imagens da aula “What we can learn with the japanese” de Akido Ono, apresentada na conferência “Quality in Endoscopy – Upper GI endoscopy and neoplasia” da ESGE.
Conclusão
No Brasil, o câncer gástrico é o quarto mais comum entre os homens e o sexto mais comum entre as mulheres. A mortalidade desta doença no nosso país continua bastante alta. Ainda vai demorar muito para nos aproximarmos das taxas de sobrevida japonesas, pois, não temos um programa de rastreamento (que provavelmente não seria custo-efetivo devido à nossa incidência), não temos a mesma tecnologia de imagem e muitos de nós, também não tem o tempo (ou a remuneração adequada) para um exame tão detalhado. Porém, nós podemos tentar melhorar um pouco esta situação nos pacientes que passam por nós, através da aplicação das medidas descritas anteriormente. Podemos também, selecionar os pacientes que tem um risco aumentado e nestes casos, dedicar um pouco mais de tempo. Pacientes acima de 50 anos que realizam o exame pela primeira vez, pacientes com HP positivo e principalmente os pacientes portadores de atrofia gástrica com metaplasia intestinal, tem um risco aumentado. Realizando um exame dedicado nestes pacientes podemos aumentar significativamente a taxa de identificação de câncer gástrico precoce.
Referências
1.Bruno Zilberstein; Carlos Malheiros; Laercio Gomes Lourenço; Paulo Kassab; Carlos Eduardo Jacob; Antonio Carlos Weston; Cláudio José Caldas Bresciani; Osvaldo Castro; Joaquim Gama-Rodrigues e Grupo do Consenso. Consenso brasileiro sobre câncer gástrico: diretrizes para o câncer gástrico no Brasil. Arq Bras Cir Dig; 26 (1); 2013
2. Teh JL, Tan JR et al. Longer examination time improves detection of gastric cancer during diagnostic upper gastrointestinal endoscopy. Clin Gastroenterol Hepatol. 2015.
3. ESGE “Quality in Endoscopy – Upper GI endoscopy and neoplasia”, conferência realizada em Berlin na Alemanha no mês de abril deste ano. Todas as aulas desta conferência estão disponíveis no link http://www.quality-in-endoscopy.org/meeting-presentations-qie9.html.
Pólipo colônico – Qual a conduta agora?
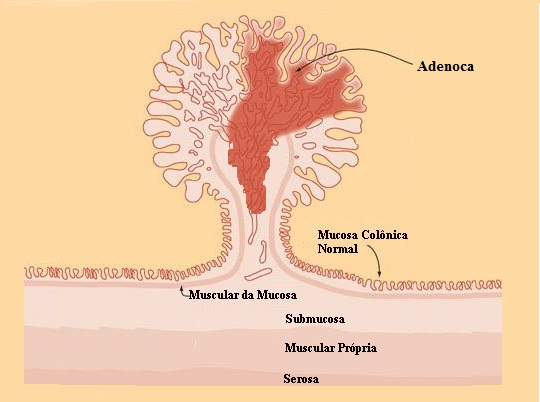
A lesão acima foi ressecada endoscopicamente. O anatomopatológico mostrou tratar-se de pólipo adenomatoso medindo 20 mm, com área de adenocarcinoma invasivo bem diferenciado medindo 5 mm, sem invasão linfática e sem invasão vascular. A lesão apresenta invasão do pedículo com invasão submucosa de1000 micra. A margem do pedículo está livre e dista 5 mm da lesão.
Quiz! Complicação após tratamento de varizes gástricas
Paciente do sexo feminino, 67 anos, com anemia e história de episódios frequentes de melena. À endoscopia foi diagnosticada grande variz de fundo gástrico. A paciente foi tratada com injeção de cianoacrilato e lipiodol sendo realizadas 2 punções em locais diferentes. O procedimento transcorreu sem intercorrências, não houve sangramento e a variz ficou bem endurecida sugerindo sucesso na obliteração. Após o procedimento a paciente evoluiu com dispneia e aumento da frequência respiratória. A ausculta pulmonar estava normal. Qual a principal hipótese que deve ser pesquisada?
Obstrução intestinal por fecaloma no cólon direito – uma doença potencialmente fatal
Paciente do sexo feminino, 76 anos, com história de diabetes, constipação crônica e ressecção segmentar de transverso há 10 anos por adenoma não ressecável por colonoscopia. Foi internada com quadro de distensão e dor abdominal difusa ha 2 dias e sem evacuar ha 5 dias. Nos dias anteriores ao início dos sintomas relatava evacuações a cada 2 dias, sempre em pequena quantidade.
A paciente estava em bom estado geral, abdome distendido com ruídos presentes e desconforto à palpação difusamente, sem sinais de peritonite e sem massas palpáveis. No toque retal não se notavam lesões e não havia fecaloma tocável.
Os exames laboratoriais mostravam eletrólitos, amilase e função renal normais. Hemograma com hemoglobina normal mas com 17000 leucócitos, sem desvio à esquerda.
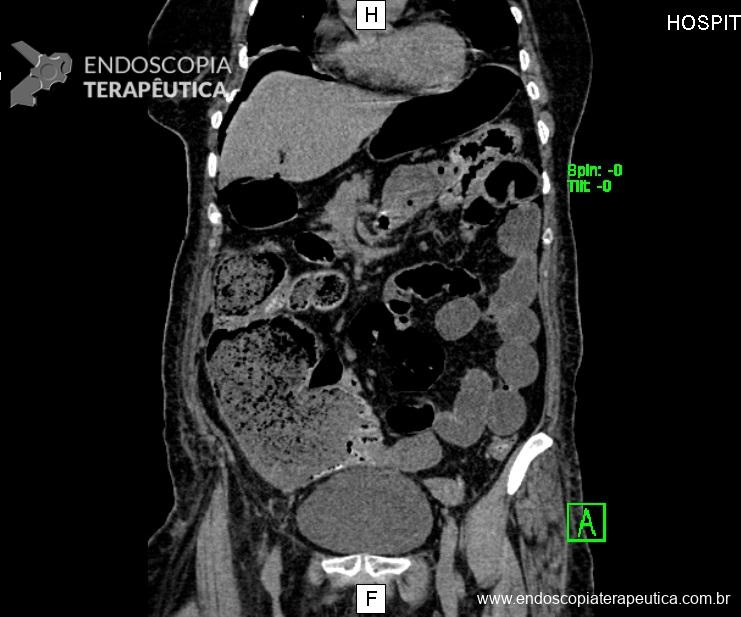
Realizou tomografia de abdome total com os seguintes achados:
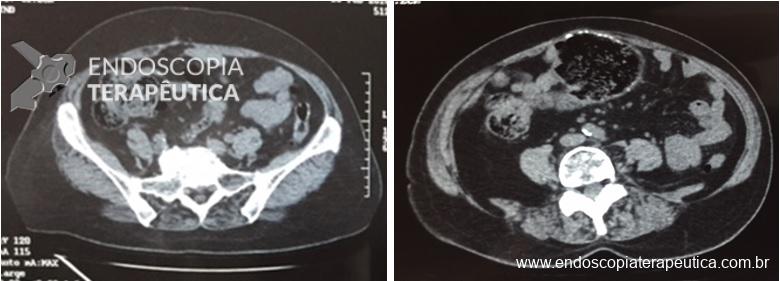
Ausência de líquido livre ou sinais de pneumoperitônio. Estômago e intestino delgado sem distensão. Volumosa coprostase no cólon direito e cólon transverso sem se identificar ponto de obstrução evidente.
Com este achado foi iniciado o uso de laxativos via oral, ingestão aumentada de líquidos e lavagem retal com glicerina 12 %. Mesmo após várias lavagens retais e uso de laxativos orais a paciente evoluiu com piora da dor e distensão abdominal.
Neste momento foi indicada a realização de uma colonoscopia (preparo exclusivamente retrógrado) para descartar a presença de um fator obstrutivo não identificado na tomografia e tentar descomprimir o cólon.
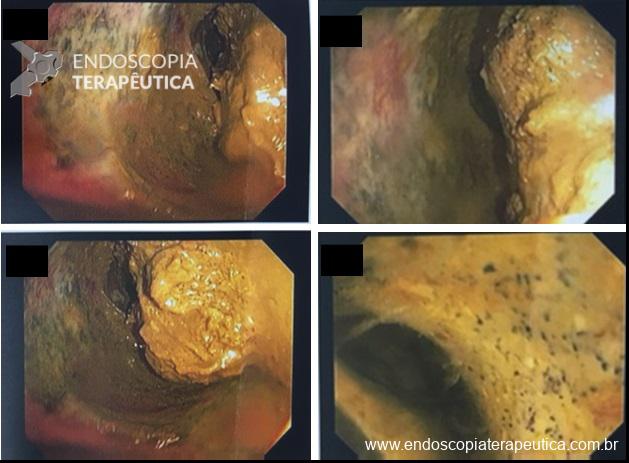
Colonoscopia: Volumoso fecaloma impactado no cólon transverso. Foi realizada infusão lenta de 1000 ml de soro fisiológico morno com amolecimento do fecaloma, permitindo a passagem do aparelho através da área de obstrução e descompressão do cólon direito que também apresentava grande quantidade de resíduos fecais. O local de impactação apresentava sinais de isquemia e necrose da mucosa. O cólon direito apresentava grande quantidade de resíduos fecais aderidos às paredes, impedindo a avaliação da mucosa.
Após a colonoscopia descompressiva a paciente apresentou melhora significativa da dor e distensão abdominal e estava em ótimo estado geral. Foi mantida internada com antibióticos, dieta líquida sem resíduos e laxativos via oral. Apresentou eliminação de gases e evacuações no mesmo dia da colonoscopia.
No dia seguinte a paciente voltou a apresentar distensão abdominal e evoluiu com taquicardia, taquipnéia e alteração do nível de consciência.
Realizou nova tomografia de abdome que demonstrou grande distensão do ceco e presença de pneumoperitônio. Ausência de líquido livre. Neste momento foi indicada abordagem cirúrgica. Devido à distensão abdominal foi optado por laparotomia convencional.
No intra-operatório foi identificada grande área de necrose no ceco, ainda sem perfuração e outro ponto de necrose no cólon transverso. Não havia perfuração evidente e nem contaminação da cavidade. Foi realizada uma colectomia direita ampliada (ceco, ascendente, transverso residual e descendente). Como a paciente estava estável hemodinamicamente, sem anemia, o intestino delgado e o sigmóide não estavam distendidos e não havia contaminação da cavidade foi realizada anastomose primária íleo-sigmóide.
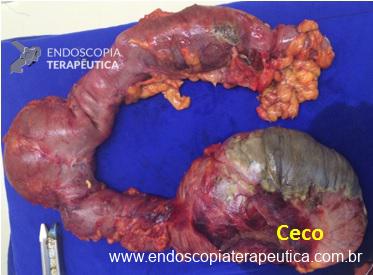
Colectomia direita ampliada. Nota-se grande área de necrose no ceco e outra pequena no transverso. Também é possível identificar a área de anastomose da ressecção prévia.
A paciente apresentou uma boa evolução no pós operatório, recebendo alta da UTI no 5º pós operatório com evacuações presentes e recebendo dieta via SNE.
Revisão
A impactação fecal é uma patologia comum e potencialmente fatal que pode ocorrer em todos os grupos etários. Crianças, pacientes acamados e idosos são as populações que estão sob maior risco. A impactação geralmente ocorre na presença de constipação severa, anormalidades anorretais e nas disfunções neurogênicas e funcionais gastrointestinais1.
O reconhecimento precoce desta doença é importante devido à sua alta morbidade, mortalidade e grande custo ao sistema de saúde. O tratamento minimiza o risco de complicações que incluem obstrução intestinal levando à úlcera estercoral, perfuração, peritonite e sepse1.
Uma revisão incluindo 188 artigos, analisou 280 casos de obstrução por fecaloma. Destes 43,5% pacientes tinham mais do que 65 anos, 49% apresentavam história de constipação severa, 29% eram portadores de doenças neuropsiquiátricas e 15% estavam institucionalizados. Um total de 346 complicações médicas secundárias à impactação fecal foram identificadas incluindo perfuração, obstrução, fístulas para órgãos adjacentes e complicações clínicas como pneumonia aspirativa e sepse2.
Não há diferença na distribuição por sexo mas a idade avançada aumenta a incidência desta patologia. No exame físico a distensão e a dor abdominal são os achados mais frequentes. No exame retal, a presença de fezes tocáveis é encontrada em menos da metade dos casos, pois a impactação pode ocorrer em qualquer local, desde o cólon direito até o reto. Os achados laboratoriais são inespecíficos mas a leucocitose e alterações eletrolíticas são comuns. A radiografia de abdome costuma mostrar dilatações difusas do delgado e do cólon além de grande quantidade de fezes acumuladas. A tomografia de abdome é o melhor exame pois pode identificar o local preciso da impactação, descartar complicações e outras causas de obstrução3.
A sigmoidoscopia e a colonoscopia podem ser utilizadas para descartar a presença de obstrução mecânica de outra etiologia e também para ajudar na fragmentação e irrigação da massa fecal impactada, porém, devem ser realizadas com cuidado devido ao risco de perfuração iatrogênica3.
A perfuração intestinal causada por impactação fecal é rara e quando ocorre apenas 10-20 % dos casos tem o diagnóstico confirmado antes da operação. Neste cenário é importante a realização de ressecção do segmento colônico acometido (já que a área isquêmica costuma ser grande) e a realização de uma ostomia. A sutura da perfuração ou a simples derivação estão associadas à um maior risco de complicações e mortalidade4.
Referências
- Hussain ZH, Whitehead DA, Lacy BE. Curr Gastroenterol Rep. 2014 Sep;16(9):404.
- Serrano Falcón B, Barceló López M, Mateos Muñoz B, Álvarez Sánchez A, Rey E. Fecal impaction: a systematic review of its medical complications. BMC Geriatr. 2016 Jan 11;16(1):4.
- Byun YH, Park YS, Myung SJ, Eom WY, Choi WW, Kim TH, Jo YJ, Kim SH, Song MH. Transient intestinal obstruction due to stool impaction in the elderly. Korean J Gastroenterol. 2005 Sep;46(3):211-7.
- Serpell JW, Nicholls RJ. Stercoral perforation of the colon. Br J Surg. 1990 Dec;77(12):1325-9.
Volumosa lesão subepitelial no fundo gástrico. Qual a conduta?
Paciente do sexo feminino, 67 anos, com história de episódios frequentes de melena e anemia . Foi encaminhada para avaliação de volumosa lesão subepitelial no fundo gástrico.
Qual o melhor forma de ressecção para os pólipos subcentimétricos do cólon e reto?
A polipectomia é o procedimento terapêutico endoscópico mais comum e todos os colonoscopistas devem estar aptos à realizar este procedimento de forma segura e efetiva. A prática evoluiu consideravelmente nos últimos anos e atualmente dispomos de várias técnicas e equipamentos para diferentes cenários clínicos.
O endoscopista deve considerar o tamanho, características morfológicas e localização do pólipo no cólon antes de escolher a técnica apropriada. Para pólipos pequenos existem várias técnicas que podem ser utilizadas, mas são poucos os estudos disponíveis para nos guiarem entre qual a mais indicada para cada caso.
Os pólipos devem ser divididos entre sésseis ou pediculados, e também de acordo com o tamanho da lesão (até 3 mm, 3-7 mm e 7-9 mm). Em relação à localização, a maioria dos estudos considera cólon direito do ceco ao ângulo esplênico, e esquerdo os segmentos distais à esta região.
PÓLIPOS PEDICULADOS
- Melhor tratamento sugerido pela maioria dos estudos e guias é a polipectomia com alça diatérmica, não importando se é no cólon direito ou esquerdo.
- Pólipos com pedículos maiores do que 1 cm sugere-se o uso de clipe ou endoloop para prevenção do sangramento.
PÓLIPOS SÉSSEIS
O tratamento varia de acordo com o tamanho e localização.
Existe um certo consenso no tratamento das seguintes lesões:
- Pólipos sésseis até 3 mm podem ser tratados por pinça de biópsia fria.
- Lesões sésseis com 1 cm ou mais, em qualquer lugar do cólon, devem ser sempre tratadas por mucosectomia.
- Lesões planas ou deprimidas maiores do que 3-4 mm (que não podem ser ressecadas adequadamente por pinça fria/hot/jumbo) são tratadas por mucosectomia.
Lesões de tamanho intermediário
Para as lesões de 3-7 mm e 7-9 mm as condutas variam bastante.
- Lesões de 3-7 mm: Boa parte dos estudos considera segura a ressecção das lesões de 3-7 mm com alça fria. Não se recomenda ressecção com pinça de biópsia devido à alta frequência de ressecção incompleta. Hot biopsy pode ser usada no cólon esquerdo mas é contra indicada no cólon direito devido ao risco de perfuração (cada vez menos usada). Alça diatérmica pode ser usada com relativa segurança no cólon esquerdo mas tem um risco de perfuração maior quando utilizada no cólon direito. A mucosectomia se mostra segura, efetiva, com baixo risco de perfuração e maiores taxas de ressecções completas destas lesões. Estudos demonstram que a aplicação da mucosectomia nas ressecções de lesões maiores do que 5 mm no cólon direito tem aumentado e é sugerida como a melhor opção por alguns autores.
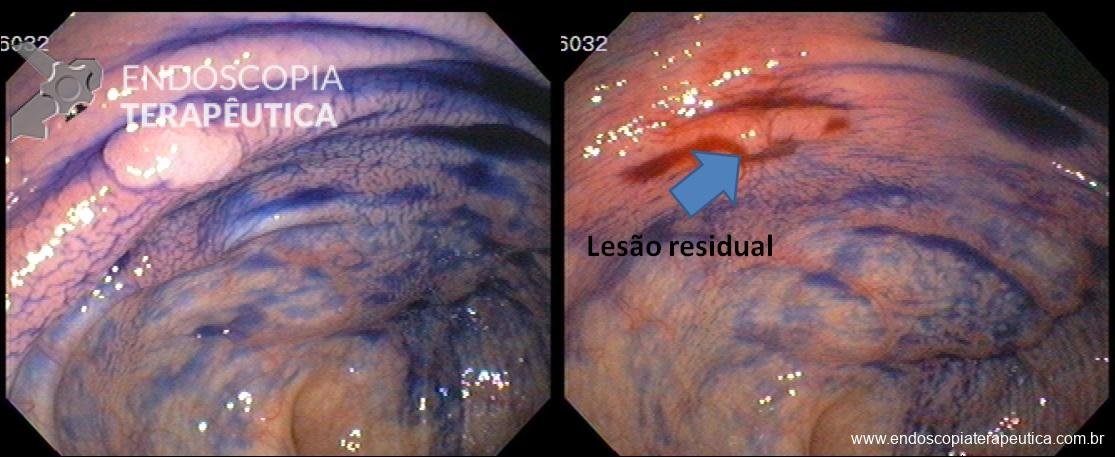
(Clique para aumentar) Lesão plana de 6 mm no ceco. Tentativa de ressecção com pinça de biópsia fria. Após a primeira mordida foi observada lesão residual com necessidade de ressecção adicional. Este tipo de tratamento deve ser evitado pois quanto maior o número de fragmentos em que a lesão for ressecada, maior a incidência de recidiva.
- Lesões de 7-9 mm: Não se deve usar pinça de biópsia fria. Hot biopsy é contra indicada no cólon direito e tem grande taxa de ressecção incompleta em lesões maiores do que 5 mm. A alça fria é uma opção possível, porém, as técnicas mais utilizadas e sugeridas nos artigos para este tipo de lesão são a ressecção com alça diatérmica e a mucosectomia. O uso de terapia térmica (alça) sem injeção submucosa no cólon direito tem uma maior incidência de perfuração e síndrome pós polipectomia, levando à uma tendência em se indicar mucosectomia para estas lesões quando localizadas nesta região. No cólon esquerdo a ressecção com alça diatérmica é mais segura do que no cólon direito mas a mucosectomia também é uma opção que deve ser considerada. Em um estudo multicêntrico prospectivo (6) realizado em 11 instituições japonesas incluindo 624 pacientes, foi avaliado a aplicação da mucosectomia em lesões menores do que 2 cm. O tamanho médio das lesões era de 8,3 mm + 3,2 (5-20 mm). A ressecção em bloco foi obtida em 93,3% dos pacientes com 78,3% de ressecções completas. A taxa de perfuração foi 0 (zero) e a taxa de sangramento 1,1%. Este estudo demonstra que a mucosectomia é uma técnica simples, rápida, segura e com altas taxas de ressecção completa de lesões menores do que 1 cm.
Como medir as lesões?
Outra dificuldade na decisão terapêutica dos pólipos subcentimétricos é como estimar o tamanho da lesão. Infelizmente não exite um método 100% preciso. O tamanho é estimado, na maioria das vezes, comparando-se a lesão com algum dos instrumentos endoscópicos, geralmente uma pinça. Para isso o endoscopista deve conhecer o material que utiliza. A concha da pinça de colonoscopia padrão mede em torno de 5 mm de comprimento e quando aberta tem aproximadamente 8 mm.
(Clique para aumentar). A) Comparação da pinça aberta (visão endoscópica) com área arredondada de 5 mm. B) Medida da pinça aberta (aproximadamente 8 mm).
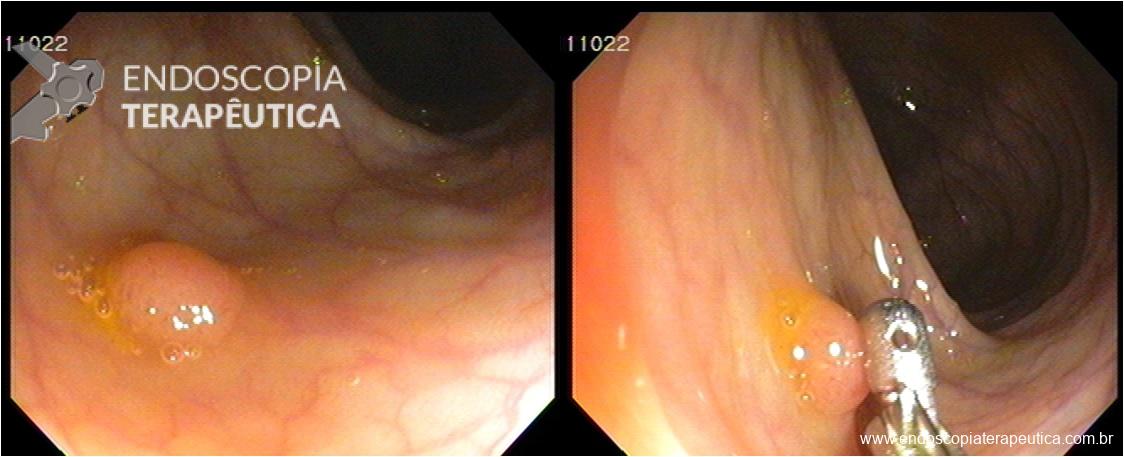
(Clique para aumentar). A) Pólipo pequeno no cólon descendente. B) Comparação do pólipo com uma das conchas da pinça de colonoscopia que mede 5 mm de comprimento.
Referências
- Riley SA. Colonoscopic polypectomy and endoscopic mucosal resection: A pratical Guide. Britihs Society of Gastroenterology. 2008. Disponível no endereço: http://www.bsg.org.uk/pdf_word_docs/polypectomy_08.pdf
- Saunders B. “HOW I DO IT” Removing large or sessile colonic polyps. World Endoscopy Organization. Disponível no endereço: http://www.worldendo.org/assets/downloads/pdf/publications/how_i_doit/2007/omed_hid_removing_large_or_sessile_colonic_polyps.pdf
- Lee TJ, Rutter MD, Blanks RG, Moss SM, Goddard AF, Chilton A, Nickerson C, McNally RJ, Patnick J, Rees CJ.Colonoscopy quality measures: experience from the NHS Bowel Cancer Screening Programme. Gut 2012;61:1050e1057. doi:10.1136/gutjnl-2011-300651
- Ross WA, Thirumurthi S, Lynch PM, Rashid A, Pande M, Shafi MA,
Lee JH, Raju GS. Detection rates of premalignant polyps during screening colonoscopy: time to
revise quality standards? GASTROINTESTINAL ENDOSCOPY Volume 81, No. 3 : 2015 - Lee TJ, Blanks RG, Rees CJ, Wright KC, Nickerson C, Moss SM, Chilton A, Goddard AF, Patnick J, McNally RJ, Rutter MD. Longer mean colonoscopy withdrawal time is associated with increased adenoma detection: evidence from the Bowel Cancer Screening Programme in England. Endoscopy 2013; 45: 20–26
- Yoshida N(1), Naito Y, Inada Y, Kugai M, Yagi N, Inoue K, Okuda T, Hasegawa D, Kanemasa K, Kyoichi K, Matsuyama K, Ando T, Takemura T, Shimizu S, Wakabayashi N, Yanagisawa A, Yoshikawa T. Multicenter study of endoscopic mucosal resection using 0.13% hyaluronic acid solution of colorectal polyps less than 20 mm in size. Int J Colorectal Dis (2013) 28:985–991.
Confira também: Lesões sésseis serrilhadas | vídeo sobre: Ressecção de pólipo pediculado gástrico com auxílio de endoloop
HDA – Qual o diagnóstico e conduta?
Paciente de 68 anos com quadro de melena ha 3 dias. Realizou endoscopia evidenciando coágulo aderido no bulbo duodenal. Após remoção do coágulo foi identificada lesão com sangramento ativo. Qual o diagnóstico e melhor conduta para este caso?
Assuntos relacionados
Caso clínico – Hemorragia digestiva alta de tumor metastático de estômago
Tratamento endoscópico das varizes de fundo gástrico
HDA – Guia resumido de condutas desde a admissão até a alta
Artigo comentado – Tratamento de ectasia vascular antral com ligadura elástica