Tratamento de tumor neuroendócrino gástrico
INTRODUÇÃO
- Os tumores neuroendócrinos são formados por hiperplasia das células enterocromoafins, responsáveis pela produção de serotonina
- As células enterocromafins que situam-se na lâmina própria (entre epitélio e a muscular da mucosa)
- São classificadas como lesões de padrão subepitelial e não submucoso
- Os padrões histológicos são variados e confirmam-se pela imunohistoquímica (positividade para marcadores como cromogranina A)
- Incidência vem aumentando, talvez pelo maior disponibilidade de acesso a endoscopia e aos exames de imunohistoquímica
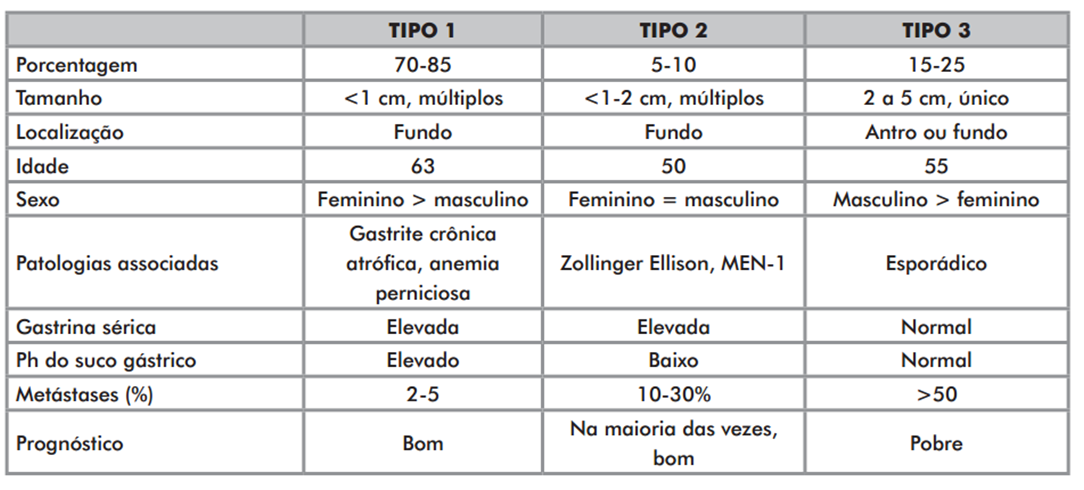
CLASSIFICAÇÃO CLÍNICA
Tipo 1: mais comum (70%)
- ocorre num contexto de gastrite atrófica
- associado a hipergastrinemia
- geralmente múltiplos
Tipo 2: são raros (5%)
- geralmente menores que 1,5 cm, multifocais no corpo
- Associado a síndrome neuroendócrina múltipla (NEM tipo 1) e síndrome de Zollinger Ellison
Tipo 3: segundo mais comum (25%)
- esporádico e isolado
- sem associação com gastrite atrófica e sem hipergastrinemia
- ocorrem em qualquer local do estômago
O principal marcador para o diagnóstico dos tumores do tipo 1 é o aumento da gastrina sérica usualmente maior que 500 em pacientes que não estão usando inibidores de bomba de prótons. (2)
CLASSIFICAÇÃO HISTOLÓGICA
A classificação histológica da OMS (2010) dos TNE gástricos é feita através:
Contagem mitótica em campos de grande aumento (10 cga) e índice de Ki67, sendo assim divididos em:
- Grau I (G1 – bem diferenciado, cerca de 90%): Ki67 ≤ 2% e < 2 mitoses/10 cga
- Grau II (G2 – bem diferenciado): Ki67 de 3 a 20% e 2 a 20 mitoses/10 cga
- Grau III (G3 – pouco diferenciado): Ki67 > 20% e > 20 mitoses/10 cga
O prognóstico deste tumores depende da junção da classificação clínica com a histológica, sendo que cerca de 80% dos tumores do tipo 1 apresentam grau histológico I e cerca de 90% dos tumores do tipo 3 apresentam grau histológico II ou III. (2).
DIAGNÓSTICO
- Biópsia do pólipo para análise histológico e imunohistoquímica
- Biópsia do corpo gástrico para verificar a presença de atrofia
- Dosagem de gastrina sérica
- Pesquisa de autoanticorpos para gastrite autoimune (anti-célula parietal e anti-fator intrínseco)
- Ecoendoscopia nas lesões com suspeita de invasão da muscular própria (>10mm) para avaliar a possibilidade de ressecção endoscópica
Na suspeita de tumor neuroendócrino, antes de ser realizada a ressecção, o ideal é a realização de uma simples biópsia da lesão para diagnóstico especifico do tipo de tumor e seu grau histológico
TRATAMENTO
Tumores de classificação clínica 1:
Tratamento endoscópico se:
– número de lesões menor que 5
– lesões menores que 1 cm
– sem suspeita de invasão da camada muscular própria (ecoendoscopia obrigatória apenas em lesões maiores que 10mm)
Tumores de classificação clínica 3:
- Análise individualizada de cada caso
- Pode-se considerar o tratamento endoscópico em tumores menores que 10mm
- Desde que não possuam fatores de risco para metástase
Fatores de risco para metástase
- Classificação histológica grau III (G3-pouco diferenciado – Ki67 > 20% e IM > 20)
- Invasão da muscular própria
- Invasão angiolinfática
Em estudo publicado na World Journal of Gastroenterology em 2013 (3), foram avaliados 119 casos de tumores neuroendócrinos do tipo 3 que foram tratados e acompanhados por 46 meses. Destes 39 foram para cirurgia, 50 foram ressecados endoscopicamente e 15 foram observados clinicamente.
Dos 39 pacientes operados, 33 seguiram o acompanhamento sendo que 29 não tiveram recidiva, 4 tiveram recidivas sendo dois casos evoluíram para óbito e outros dois foram reoperados.
Dos 15 pacientes que foram observados, 14 seguiram o acompanhamento, destes 11 não tiveram evolução da doença e 3 tiveram evolução sendo que um destes foi a óbito.
Dos 50 pacientes tratados endoscopicamente, 40 tiveram ressecção completa do tumor, destes 36 fizeram o acompanhamento e nenhum teve recidiva da doença. Os 10 pacientes que tiveram a ressecção incompleta da lesão, 7 tiveram comprometimento vertical ou lateral da margem sendo apenas observados posteriormente com endoscopia. Já 3 pacientes tiveram invasão angiolinfática, sendo todos os três encaminhados para complementação cirúrgica. Todos os 10 pacientes que tiveram ressecção incompleta, inclusive o que tiveram que ser submetidos a complementação cirúrgica não tiveram recidiva da doença.
Este estudo mostra a efetividade do tratamento endoscópico mesmo nos tumores do tipo 3, desde que sigam as indicações e contra-indicações do procedimento e principalmente se os tumores forem ressecados completamente.
Por isto as técnicas ideais para a ressecção de tumores neuroendócrinos, são aquelas que tem o potencial de fazer ressecção profundas (mucosa e submucosa) tendo em vista que o tumor cresce na lâmina própria e o comprometimento da submucosa nestes casos é esperado.
Técnicas de polipectomia simples ou mucosectomia tem altos índices de ressecção incompleta, principalmente de comprometimendo vertical da margem pois geralmente não conseguem ressecar completamente a submucosa. (4)
Técnicas de ressecção endoscópica profunda (mucosa + submucosa):
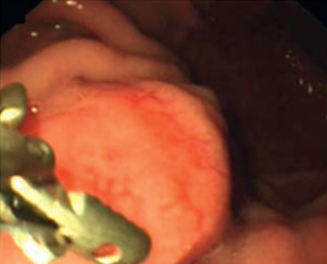
- Ligadura elástica + Polipectomia (assista vídeo da técnica)
- Ressecção com alça monofilamentar (assista vídeo da técnica)
- Dissecção endoscópica da submucosa (ESD)
TRATAMENTO EM CASOS ESPECIAIS
- Tumores neuroendócrinos que apresentam fator de risco para metástase, está indicada a gastrectomia com linfadenectomia.
- Pacientes com TNE tipo 1, que não responderam ou tiveram recorrência após tratamento endoscópico, pode-se tentar terapia para supressão da gastrina sérica com análagos da somastotastina (ex: octeotride) ou antrectomia
- Nos casos de metástases, há opções como técnicas de radiologia intervencionista, radioterapia para disseminação óssea sintomática e quimioterapia em doença metastática irressecável.
CONCLUSÃO
- Os tumores neuroendócrinos gástricos constituem um espectro de neoplasias com características clínico-patológicas, mecanismo patogênico e prognóstico diferentes do adenocarcinoma podendo ser mais indolentes ou se comportar como tal
- O conhecimento deste complexo tema com suas classificações e apresentações é de fundamental importância para a condução adequada de tumores desta linhagem
- Antes de ser realizado o tratamento endoscópico, deve ser feito o correto diagnóstico do tipo de tumor neuroendócrino em questão, com simples biópsia da lesão, exames laboratoriais e de imagem para estadiamento
VEJA AQUI ALGUNS CASOS CLÍNICOS SOBRE TUMOR NEUROENDÓCRINO GÁSTRICO
REFERÊNCIAS
Link dos artigos originais:
5- David A. Crosby , Gastric Neuroendocrine Tumours , Dig Surg 2012;29:331–348
Revisão sistemática e metanálise sobre recidiva local após a ressecção endoscópica de lesões colorretais não pediculadas
Em estudo realizado através de revisão sistemática e metanálise, publicado em março de 2014 na revista Endoscopy , os autores avaliaram a recorrência local após mucosectomia de lesões não pediculados do cólon.
O objetivo foi estudar a frequência e os fatores de risco de recorrência e fornecer uma recomendação de seguimento destes casos.
Dos 45 estudos selecionados conforme os critérios abaixo, 12 foram excluídos, tendo sido selecionados 33 estudos no total.
Foram excluídos pólipos pediculados e sésseis que não foram ressecados com a técnica de injeção da submucosa. Assista um vídeo que demonstra a técnica de mucosectomia empregada no estudo.
Os autores concluiram que índice médio de recorrência local da lesão foi de 3% para lesões ressecadas em monobloco de 20% para lesões ressecadas em “piecemeal”.
Alguns estudos mostraram que o tamanho da lesão, o aspecto plano, e o maior número de fragmentos quando da ressecção em “piecemeal” seriam fatores de risco para esta recidiva local. Porém o único fator estatisticamente significativo foi a ressecção em “piecemeal” independente do número de fragmentos.
No estudos realizados com seguimento pós ressecção, quando da presença de recidiva local, esta foi encontrada em 76% dos casos em 3 meses, 96% dos casos em 6 meses.
Sendo assim os autores recomendam o controle endoscópico 6 meses após ressecção de todas as lesões feitas pela técnica de “piecemeal”.
Clique aqui e confira também as diretrizes do rastreamento e seguimento endoscópico para o câncer de cólon.
Referência: Tim D. G. Belderbos, Max Leenders, Leon M. G. Moons, Peter D. Siersema. Local recurrence after endoscopic mucosal resection of nonpedunculated colorectal lesions: systematic review and meta-analysis. Endoscopy. 2014 May;46(5):388-402. doi: 10.1055/s-0034-1364970. Epub 2014 Mar 26.
Link para o artigo original: https://www.thieme-connect.com/DOI/DOI?10.1055/s-0034-1364970
Tumor Neuroendócrino Gástrico
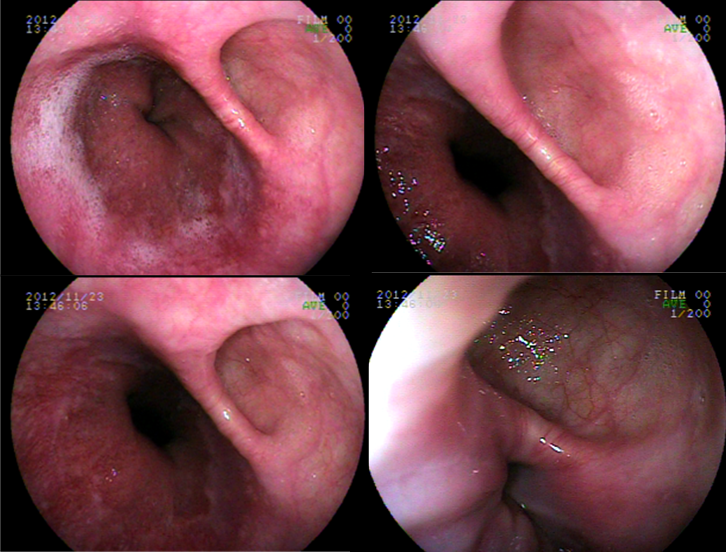
Os tumores neuroendócrinos gástricos são lesões compostas por hiperplasia das células enterocromafin-like. Os padrões histológicos são variados e confirmam-se pela imunohistoquímica, tendo positividade para marcadores como cromogranina A.
Os tumores neuroendócrinos (TNE) gástricos são divididos clinicamente em três tipos:
Tipo 1: mais comum (80%), ocorre num contexto de gastrite atrófica associado a hipergastrinemia, geralmente múltiplos. Apresentam-se como pequenos nódulos no corpo e limitados à submucosa e mucosa. Geralmente benignos, podendo regredir. As metástases linfonodais são raras, podendo ocorrer em lesões maiores de 2 cm.
Tipo 2: são raros (5%), geralmente menores que 1,5 cm, multifocais no corpo e associado a síndrome neuroendócrina múltipla (MEN tipo 1) e síndrome de Zollinger Ellison. Há metástase em 30% dos casos, preferencialmente quando lesões maiores de 2 cm e com invasão da muscular própria.
Tipo 3: segundo mais comum (15%), é esporádico, solitário e sem associação com gastrite atrófica e sem hipergastrinemia. Ocorrem em qualquer local do estômago e, como os demais, as metástases estão relacionadas com o tamanho, presença de invasão angiolinfática e invasão da muscular própria.
A nova classificação histológica dos TNE gástricos, da Organização Mundial de Saúde, é feita através da contagem mitótica em campos de grande aumento (10 HPF) e pelo índice de Ki67, sendo assim divididos em:
Grau I (bem diferenciado, cerca de 90%): Ki67 ≤ 2% e < 2 mitoses/10 campos de maior aumento;
Grau II (bem diferenciado): Ki67 de 3 a 20% e 2 a 20 mitoses/10 cma;
Grau III (pouco diferenciado): Ki67 > 20% e mitose > 20/10 cma.
Quanto a conduta, deve-se considerar a classificação clínica, o grau histológico, o grau de invasão, o número de lesões, o tamanho do tumor e a presença de invasão angiolinfática ou de metástases.
Nos tumores do tipo 1 e 2, nos casos em que há menos de 5 pólipos e o maior deles for inferior a 1 cm é recomendado ressecção endoscópica, se não houver invasão da camada muscular própria (quando diagnosticado por ecoendoscopia antes da ressecção). O acompanhamento é feito com endoscopia digestiva alta anualmente. Quando houver margens comprometidas da ressecção endoscópica, a ressecção cirúrgica local está indicada (gastrectomia subtotal).
Fatores de risco para doença metastática:
– Invasão da muscular própria
– Invasão angiolinfática
– Classificação histológica grau III (pouco diferenciado)
Tumores neuroendócrinos que apresentam qualquer fator de risco para metástase ou classificados clinicamente como tipo 3, está indicada a gastrectomia com linfadenectomia.
Nos casos de metástases, há opções como técnicas de radiologia intervencionista, radioterapia para disseminação óssea sintomática e quimioterapia em doença metastática irressecável.
CASOS CLÍNICOS
Caso 1: feminina, 32 anos, com hipotireoidismo e depressão, refere pirose e epigastralgia diariamente, sem sinais de alarme. Na EDA, evidenciaram-se pólipos em corpo gástrico e gastrite antral erosiva plana moderada, foram feitas polipectomias. À biópsia e imunohistoquímica, constatou-se tumor neuroendócrino (cromogranina positivo) , Grau I (Ki67 < 2%) , apresentando também atrofia, metaplasia intestinal e padrão morfológico sugerindo gastrite autoimune. Exame laboratorial demonstrou hipergastrinemia, anti- célula parietal positivo e deficiência de vitamina B12. A conduta feita foi reposição de vitamina B12 e orientações quanto ao quadro e seguimento endoscópico.
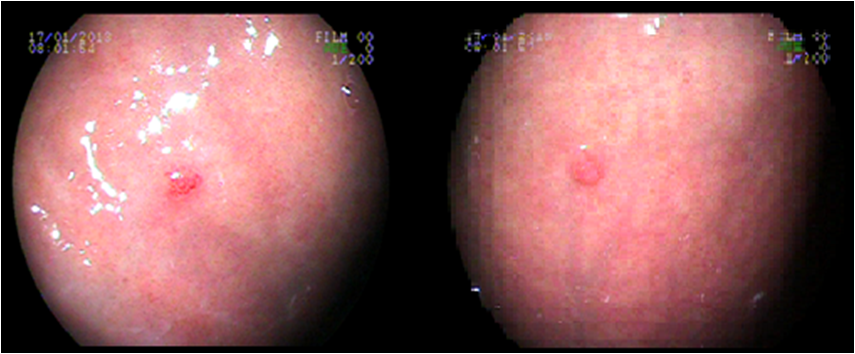
CLASSIFICAÇÃO CLÍNICA: Tipo 1 CLASSIFICAÇÃO HISTOLÓGICA: Grau I
Caso 2: masculino, 33 anos, com queixa de dispepsia intermitente há 10 meses, tem hipotireoidismo. É irmão da paciente do caso 1. EDA evidenciou pangastrite enantematosa leve e pólipos gástricos. À biópsia e imunohistoquímica, constatou-se tumor neuroendócrino (cromogranina positivo), Grau II (Ki67 7 %) , invadindo submucosa e com margem profunda comprometida. Apresentando também atrofia, metaplasia intestinal e padrão morfológico sugerindo gastrite autoimune. Devido as margens de ressecção comprometidas e grau histológico um pouco mais agressivo foi indicado o tratamento cirúrgico do qual o paciente se recusou em fazer e perdeu o acompanhamento.
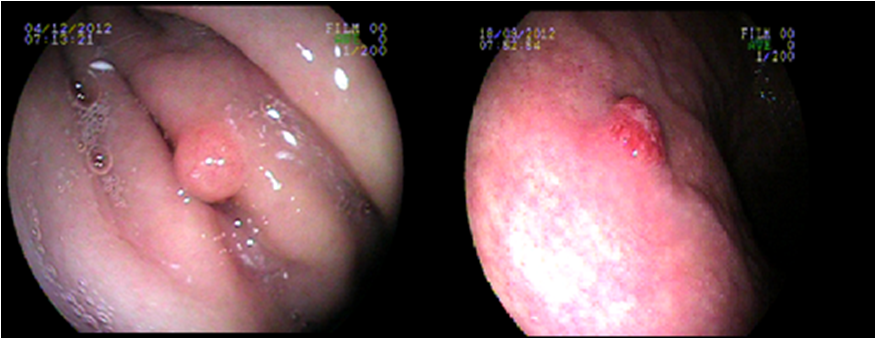
CLASSIFICAÇÃO CLÍNICA: Tipo 1 CLASSIFICAÇÃO HISTOLÓGICA: Grau II
Caso 3: feminina, 37 anos., com queixa de epigastralgia,. Endoscopia evidenciando pólipos em corpo gástrico sendo um com cerda de 10mm, sendo este ressecado por mucosectomia. Diagnóstico histológico e imunohistoquímico compatível com tumor neuroendócrino, invasor da submucosa e margens cirúrgicas comprometidas, associado a gastrite atrófica. Laboratório com hipergastrimenia e investigação de metástase a distância negativa. Paciente submetida a gastrectomia parcial devido margens cirúrgicas comprometidas.
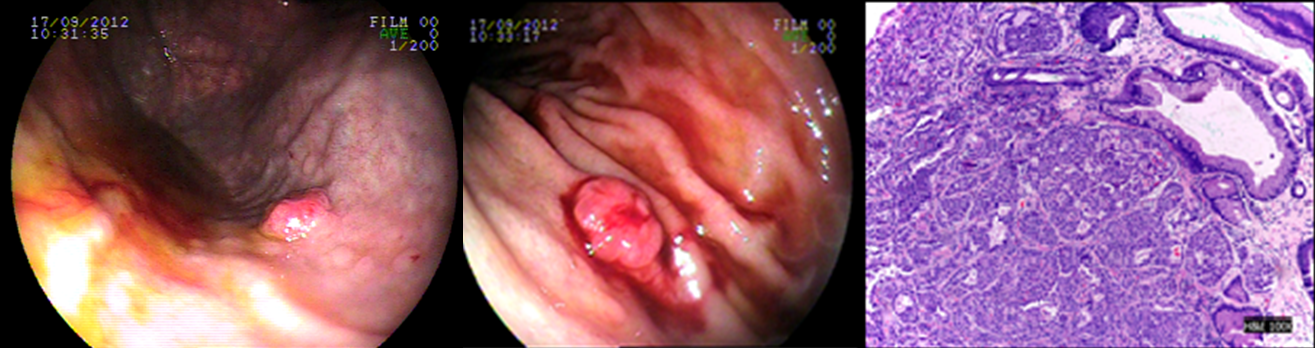
CLASSIFICAÇÃO CLÍNICA: Tipo 1 CLASSIFICAÇÃO HISTOLÓGICA: Grau I
Caso 4: feminina, 60 anos, HAS prévia, tendo como queixa principal pirose. EDA apresentando 2 pólipos gástricos na grande curvatura sendo o maior com cerca de 8mm. À biópsia e imunohistoquímica, constatou-se pólipo hiperplásico e o outro como tumor neuroendócrino (cromogranina positivo), Grau I (Ki67 <2%), sem invasão angiolinfática, com margem profunda comprometida, sem atrofia associada. Solicitado tomografia de abdome e gastrina sérica. Paciente não retornou e o seguimento do caso foi perdido.
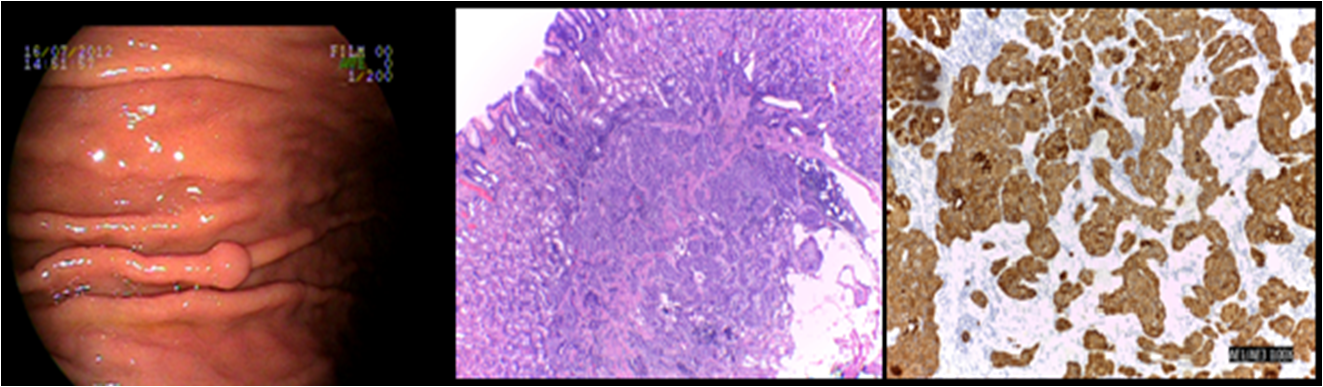
CLASSIFICAÇÃO CLÍNICA: Tipo 3 CLASSIFICAÇÃO HISTOLÓGICA: Grau I
Discussão
Os pacientes dos casos 1 e 2 possuem hipotireoidismo e atrofia gástrica, sendo por um com gastrite autoimune confirmada, mostrando a relação que pode existir entre as doenças autominues
Os pacientes dos casos 1 e 2 são irmãos sugerindo a associados do tumor neuroendócrino com fatores genéticos ou com doenças autoimunes que levam a atrofia da mucosa gástrica
Os pacientes dos caso 2 e 3 apresentaram margem cirúrgica comprometida após a ressecção endoscópica tendo sido indicada complementação cirúrgica das lesões.
O paciente do caso 4 apresentava lesão única não associada a gastrite atrófica o que poderia sugerir a classificação clinica como tipo 3. Fala contra este hipótese o pequeno tamanho da lesão.
Conclusão
Apesar de ser uma neoplasia rara, tem-se demonstrado um aumento progressivo da incidência dos tumores neuroendócrinos gástricos e representam atualmente cerca de 10% de todos os TNE gastrointestinais
Constituem um espectro de neoplasias com características clínico-patológicas, mecanismo patogênico e prognóstico diferentes do adenocarcinoma
O conhecimento deste complexo tema com suas classificações e apresentações é de fundamental importância para a condução adequada de tumores desta linhagem
Bibliografia
Dal Pizzol AC, Linhares E, Gonçalves R, Ramos C. Tumores Neuroendócrinos do Estômago: Série de Casos. Revista Brasileira de Cancerologia 2010; 56(4):453-461, Outubro 2010.
Pathology and Genetics of Tumours of the Digestive System. World Health Organization Classification of Tumours 2010. p. 53-57.
College of American Pathologists .Protocol for the Examination of Specimens From Patients With Neuroendocrine Tumors (Carcinoid Tumors) of the Stomach. Based on AJCC/UICC TNM, 7th Edition.
Ruszniewski P, Delle Fave G, Cadiot G, et al. Frascati Consensus Conference; European neuroendocrine Tumor Society. Well-differentiated gastric tumors/ carcinomas. Neuroendocrinology 2006;84:158–64.
Tumor neuroendócrino retal bem diferenciado: o impacto do tamanho do tumor sobre a história natural e resultados terapêuticos
Em estudo retrospectivo publicado em julho de 2014 na revista Gastrointestinal Endoscopy os autores avaliaram o prognóstico e a sobrevida de tumores neuroendócrinos bem diferenciados de reto em relação ao tamanho da lesão em sua apresentação inicial.
Dos 87 pacientes avaliados, 66 apresentavam tumores menores que 10mm, 6 apresentavam tumores entre 11-19mm e 15 apresentavam tumores maiores que 20mm. Destes 87 pacientes, 75 foram tratados conforme seu estadiamento clínico, com ressecção local endoscópica ou cirúrgica.
Ao diagnóstico inicial, dos 87 pacientes, 17 pacientes já apresentavam metástases, 2 (3%) do grupo com tumor menor que 10mm, 4 (66%) do grupo com tumores entre 11-19mm e 11 (73%) do grupo com tumores maiores que 20mm.
Os 70 pacientes que não apresentavam metástases ao diagnóstico foram tratados conforme seu estadiamento. Destes 70 pacientes, 55 (79%) foram seguidos por um período de até 78 meses, sendo que 6 apresentaram metástases neste período.
O estudo sugere que lesões maiores que 10mm possuem agressividade semelhante das lesões maiores que 20mm e por isto deve ser vistas e tratadas de forma forma mais agressiva.
A crítica ao estudo foi sua realização reprospectiva, a ausência de marcadores imuno-histoquímicos no estadiamento de todos os casos, estimativa subjetiva do tamanho do tumor, uma conduta de tratamento não uniforme variando entre as técnicas endoscópicas e cirúrgicas aplicadas e a não padronização dos exames (Tomografia, Ressonância magnética ou Ecoendoscopia) para o estadiamento e seguimento após intervenção local.
Referência: Gleeson FC, Levy MJ, Dozois EJ, Larson DW, Wong Kee Song LM, Boardman LA. Endoscopically identified well-differentiated rectal carcinoid tumors:impact of tumor size on the natural history and outcomes. Gastrointest Endosc. 2014 Jul;80(1):144-51. doi: 10.1016/j.gie.2013.11.031. Epub 2014 Jan 23.
Link para o artigo original: http://www.giejournal.org/article/S0016-5107(13)02627-8/abstract
Colite por Clostridium difficile simulando doença inflamatória Intestinal
Paciente do sexo feminino, 60 anos, apresentou em setembro de 2013, dores abdominais recorrentes, com diarreia sem produtos patológicos, associado distensão abdominal e flatulência excessiva. Teste respiratório com lactulose positivo para Supercrescimento Bacteriano do Intestino Delgado. Realizado tratamento com ciprofloxacina com melhora dos sintomas.
Em janeiro de 2014 houve retorno dos sintomas anteriores, sendo realizado novo ciclo de ciprofloxacina associado a probiótico com boa resposta. Após a suspensão do antibiótico evolui com piora do quadro de diarreia com presença de muco e queda do estado geral.
Colonoscopia
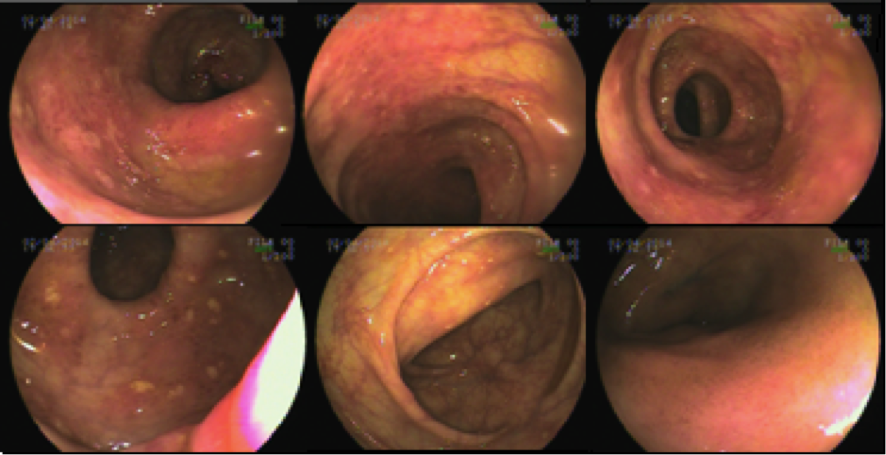
Realizou colonoscopia que demostrou as imagens abaixo:
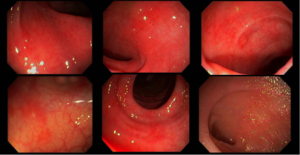
Fez uso de mesalazina por suspeita de Doença Inflamatória Intestinal. Mesmo assim teve piora do quadro, surgindo com pequenos episódios de hematoquezia. Como não houve melhora do quadro com mesalazina foi suspeitado de infecção por clostridium. Realizada nova colonoscopia evidenciando pancolite com atividade intensa no cólon esquerdo, com presença de erosões e úlceras rasas, friabilidade da mucosa e focos de fibrina aderidas a mucosa.
Apesar do especto na colonoscopia não ser tão típico da colite pseudomembranosa, a pesquisa fecal da toxina A e B para clostridium foram positivas. A paciente foi tratada com metronidazol (400mg 8/8hs por 28 dias) com boa resposta clínica. Colonoscopia de controle ao final do tratamento evidenciou resposta completa do quadro.
Discussão:
Clostridium difficile é uma bactéria anaeróbica gram-positiva, formadora de esporos, que se encontra amplamente no meio ambiente responsável por diarreia infecciosa e colite pseudomembranosa com significativa morbimortalidade.
A exposição prévia a antibioticoterapia é considerada um fator maior para o desenvolvimento da doença. A presença de comorbidades, como por exemplo, doenças neoplásicas (principalmente hematológicas), distúrbios gastrointestinais e estados de imunossupressão, são fatores de risco para a infecção adquirida na comunidade (67% dos casos). Importante destacar que nem sempre os fatores considerados como de risco estão associados ao desenvolvimento da doença. Foi comprovado que metade dos casos de infecção adquirida na comunidade não tinha exposição prévia a terapêutica antibiótica no mês anterior e cerca de 1/3 dos casos não tinha exposição hospitalar recente.
A colite por Clostridium difficile deve ser suspeitada em pacientes com quadro diarreia crônica mesmo em pacientes ambulatoriais e que não possuem os fatores de risco clássicos como internação hospitalar ou uso de antibióticos previamente. Em pacientes com diarréia crônica e suspeita de Doença Inflamatória intestinal deve-se investigar colite por Clostridium difficile como diagnóstico diferencial
Em cerca de 10% dos pacientes não é possível fazer a diferenciação entre colite e uma doença inflamatória intestinal, sendo esses classificados como colite indeterminada.
Fatores de risco para diferenciar Colite por C. difficile de Doença Inflamatória Intestinal:
- Mulheres tem o dobro de chance quando comparadas com os homens
- Primavera e verão tem maior incidência de infecção por clostridium
- Internação prévia por um intervalo de 3 a 12 meses (29% dos casos)
- Uso de antimicrobiano durante 3 meses anteriores aos sintomas (68 % dos casos)
Bibliografia
Kristin E. Burke and J. Thomas Lamont. Clostridium difficile infection: a worldide disease. Ut Liver. Jan 2014; 8(1): 1-6.232
Kazanowski, S. Smolarek, F. Kinnarney, and Z. Grzebieniak. Clostridium difficile: epidemiology, diagnostic and therapeutic possibilities – a systematic review. Tech Coloproctol. 2014; 18: 223-232.
Odze RD. Pathology of indeterminate colitis. J Clin Gastroenterol. 2004 May-Jun;38(5 Suppl 1):S36-40.2009
A. Adalja, MD. C. Difficile in the Community Setting. November 23, 2009.
M. Xavier. Clostridium Difficile: Uma infecção emergente na comunidade. Mestrado Integrado em Medicina. Faculdade de Medicina. Universidade de Porto.