A discussão sobre doença do refluxo gastroesofágico (DRGE) é ampla e envolve fatores de prevalência (ambientais, genéticos, culturais), fisiopatológicos (relaxamento do EEI, hipotonia do EEI), sintomatologia (típicos, atípicos), apresentação (erosiva, não erosiva), tipo de refluxato (ácido, não ácido, gasoso), tratamento (clínico,cirúrgico,endoscópico).
O objetivo deste post é dar um enfoque ao diagnóstico da DRGE. Atualmente para o diagnóstico é necessário que além da sintomatologia, deve-se ter alteração ao menos em um método diagnóstico. O conceito anterior que bastava ter sintomatologia mais de 2 vezes por semana por mais de 4-8 semanas não é suficiente, pois gera uma certeza diagnóstica de apenas 40%.
A doença do refluxo gastroesofageano (DRGE) tem uma prevalência de cerca de 12- 20% em nosso meio. Pode ser classificada pelas suas manifestações como:
- Típica: pirose e regurgitação
- Atípica: epigastralgia, distensão abdominal, eructação, empachamento, otalgia, laringite, tosse crônica, asma, erosão dentária
Apesar de comum e com tratamento relativamente fácil na maioria dos casos, o diagnóstico de DRGE não é tão simples. Isto porque não existe método diagnóstico com 100% de acurácia.
MÉTODOS DIAGNÓSTICOS:
-
Teste terapêutico com IBP
Realizado geralmente através do uso de IBP em dose plena para DRGE por 4 semanas (não existe uma boa padronização nos estudos sobre dose e tempo a ser utilizado). Possui uma sensibilidade diagnóstica de cerca de 70% e pode ser realizado em pacientes com sintomas típicos e que não possuem sinais de alarme, porém tem baixa especificidade.
Deve-se lembrar que alguns pacientes com pirose funcional respondem ao uso de IBP através de efeito placebo, o que gera um falso positivo ao teste terapêutico, e também influencia no resultado do teste diagnóstico.
Problemas relacionados ao próprio medicamento também devem ser considerados (paciente com DRGE resistente ao IBP, falha na adesão, medicamento de baixa qualidade).
-
Endoscopia digestiva alta
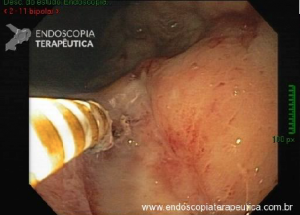
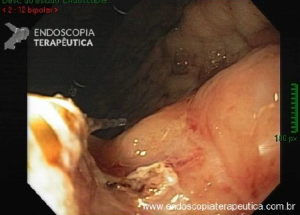
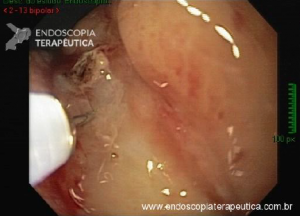
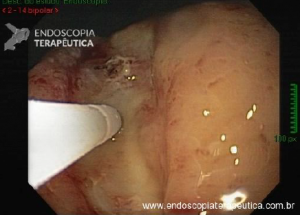
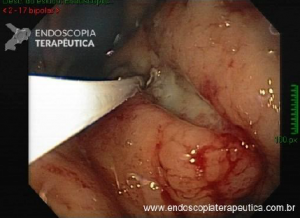
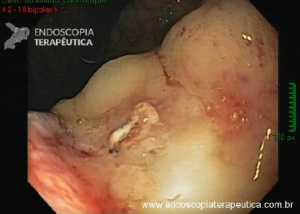
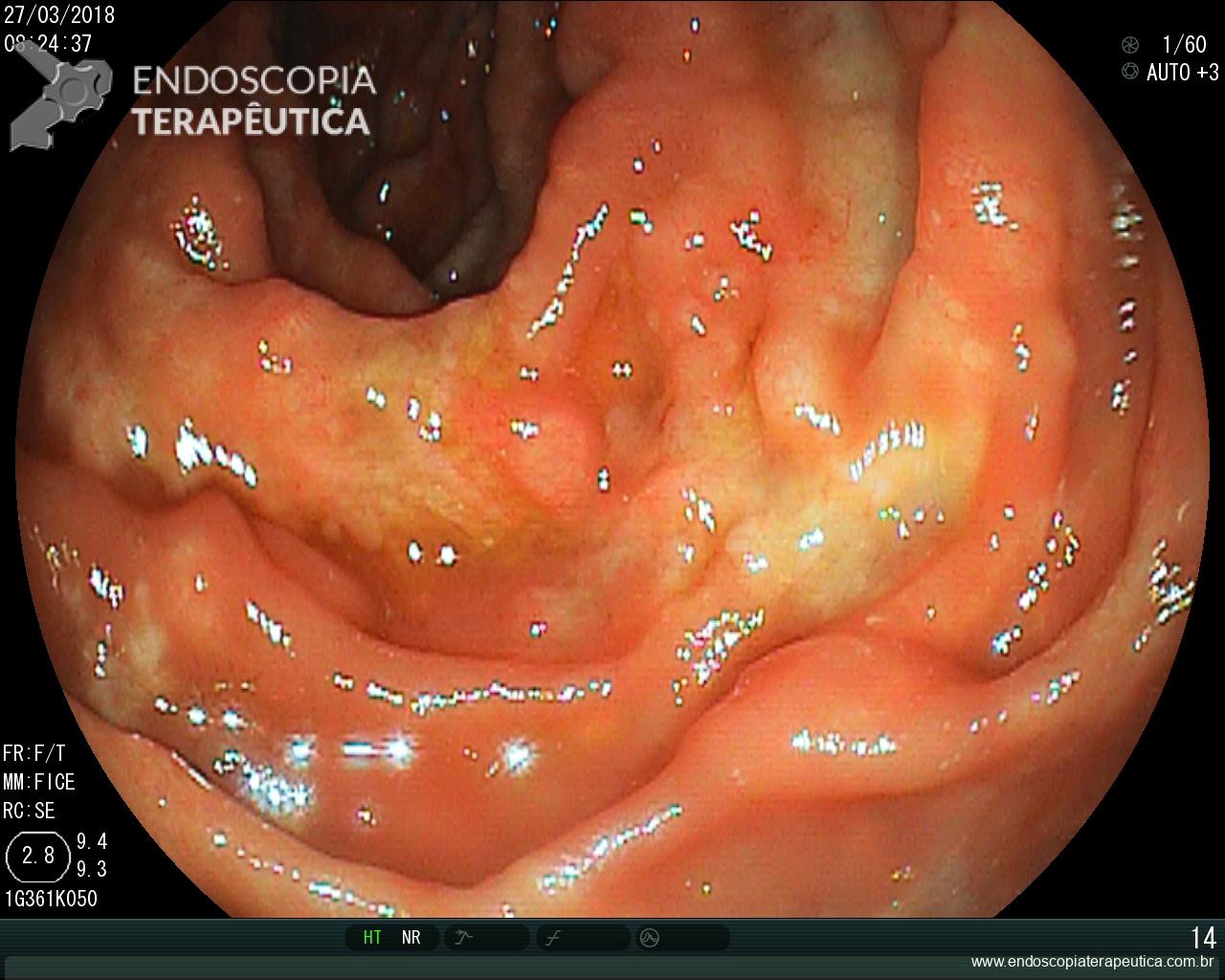
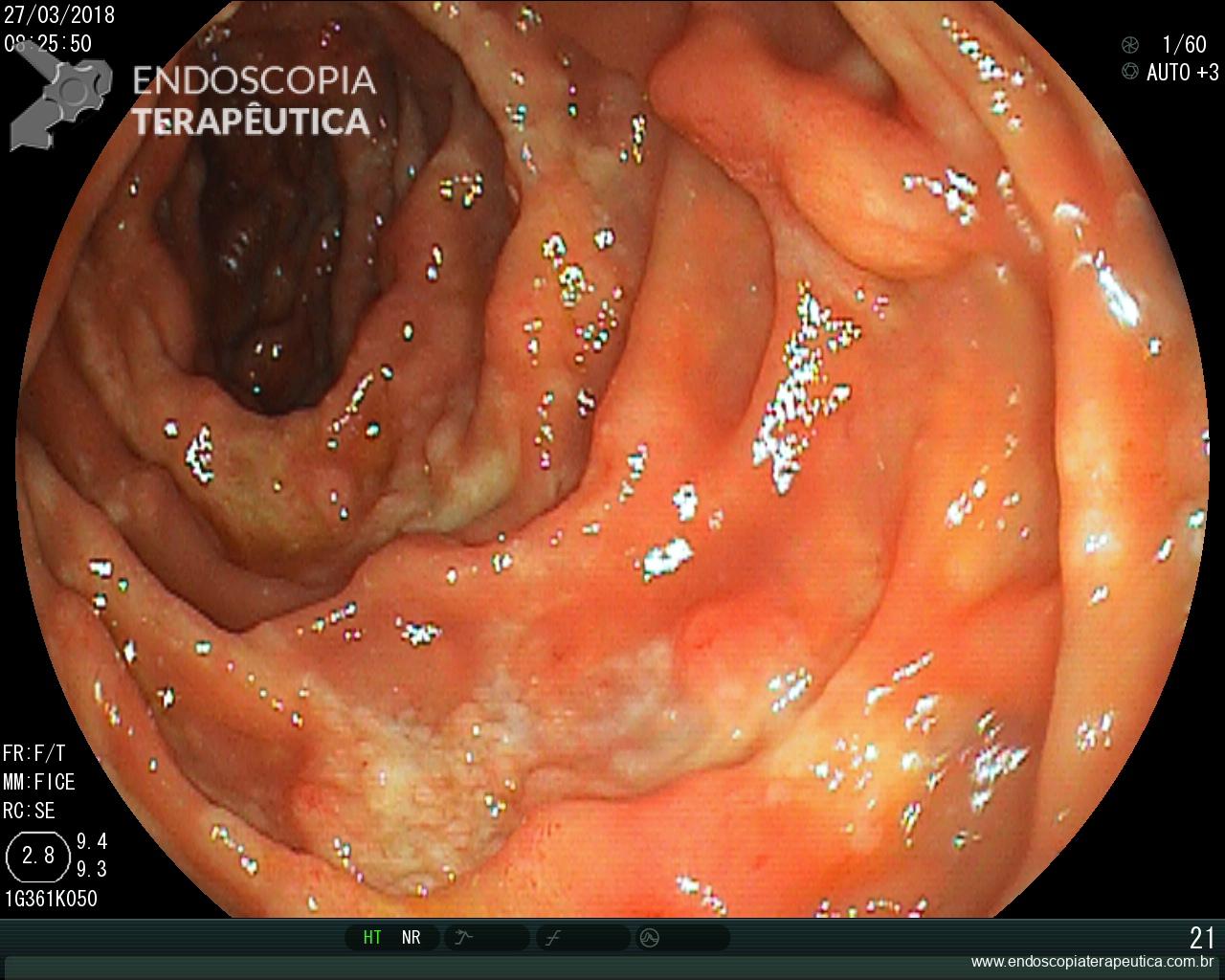
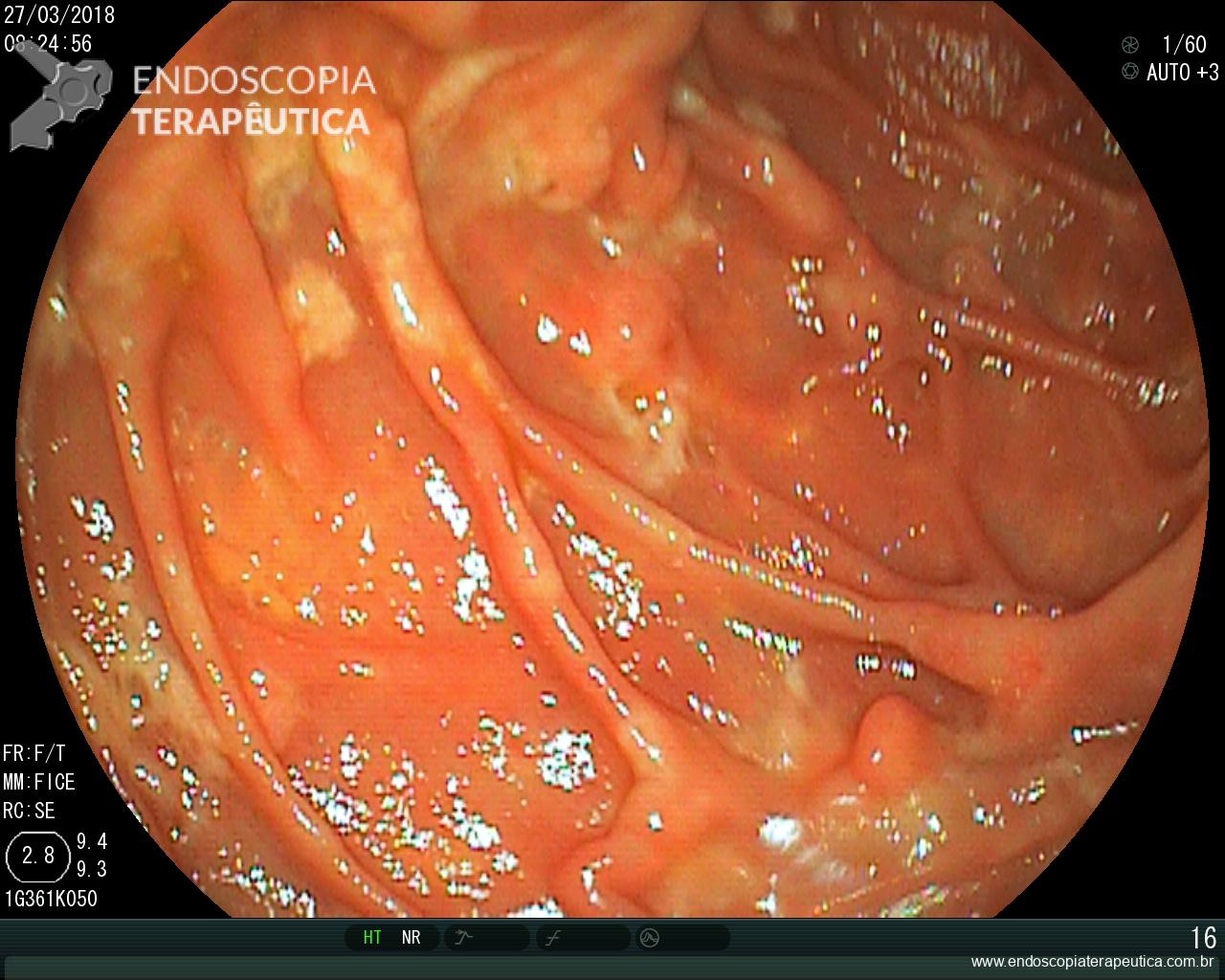
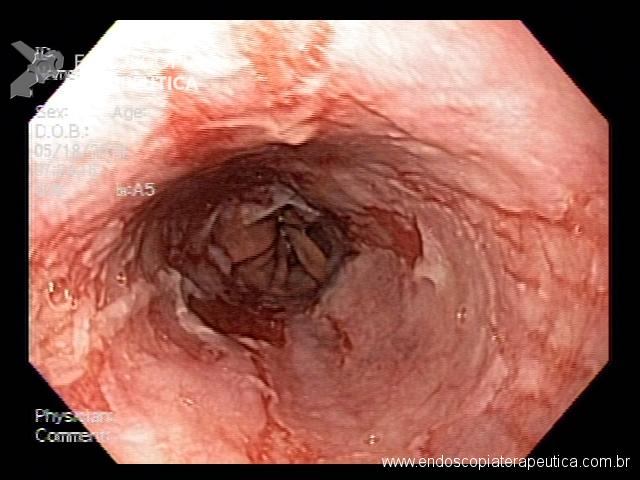
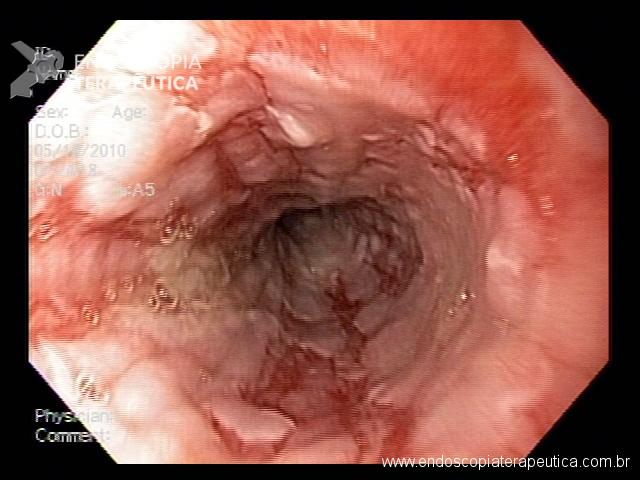
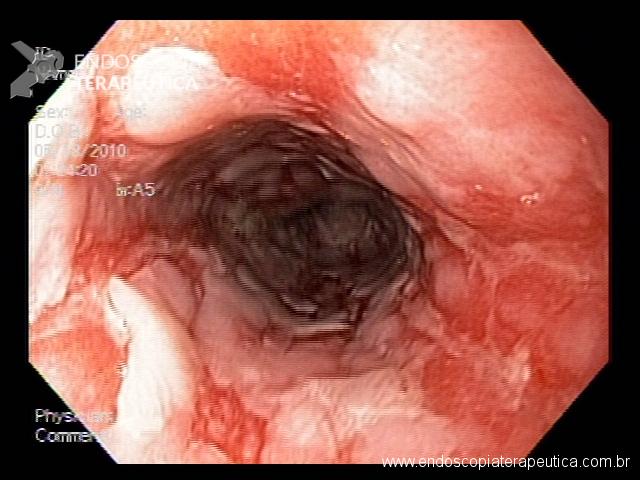
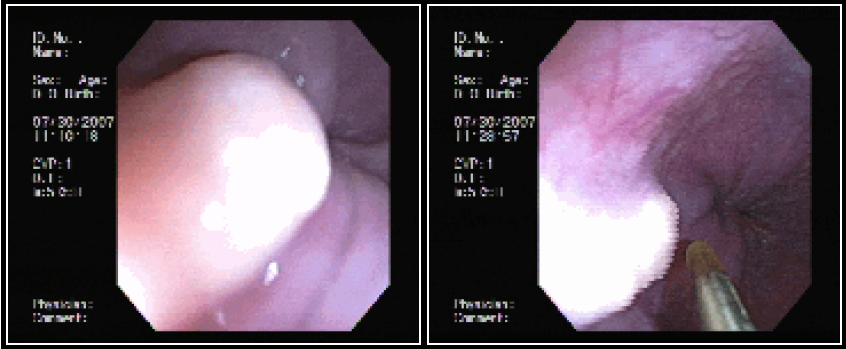
Geralmente é o primeiro método diagnóstico utilizado para diagnosticar DRGE. A endoscopia deve ser realizada preferencialmente antes do inicio do IBP, pois assim a classificação entre DRGE erosiva e não erosiva pode ser realizada de forma mais fidedigna.
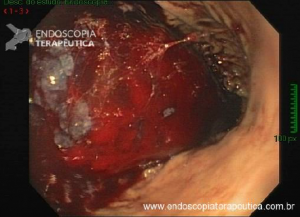
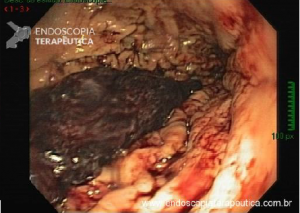
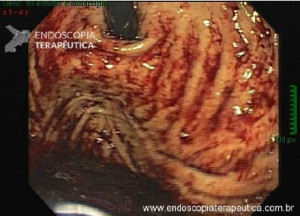
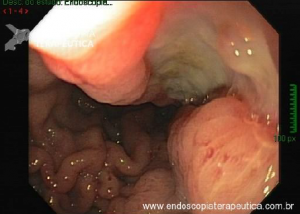
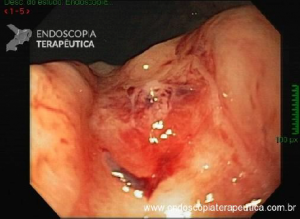
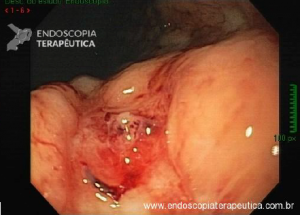
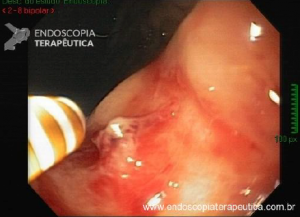
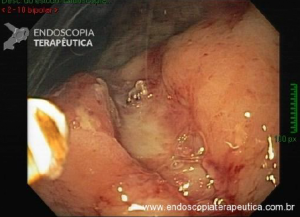
A endoscopia digestiva além de avaliar a presença de esofagite erosiva, achado de alta especificidade para DRGE, pode também observar suas eventuais complicações (ex: úlceras, estenoses, Barrett).
Porém a sensibilidade diagnóstica da EDA é baixa, cerca de 40-50% nos pacientes com sintomas típicos e apenas 20-30% nos pacientes com sintomas atípicos.
Observa-se assim que a maioria dos pacientes com DRGE não apresentam alterações na endoscopia digestiva alta
https://endoscopiaterapeutica.net/pt/esofagite-erosiva-por-doenca-do-refluxo/
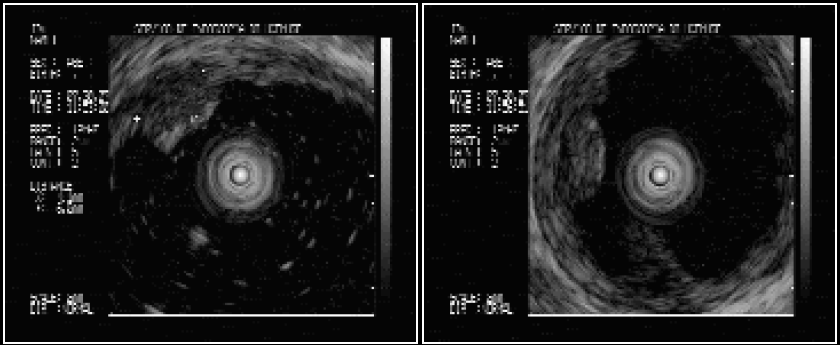
A manometria na DRGE é fundamental para definir o posicionamento do cateter do exame de pHmetria, que deve ficar 5cm acima do esfíncter esofágico inferior. Medidas fixas ou cálculos baseados na altura do paciente não são fidedignos para a realização da pHmetria.
Também tem como objetivo fazer o diagnóstico diferencial com outras patologias como acalásia e distúrbios motores do esôfago que podem gerar sintomas semelhantes de DRGE. A manometria de alta resolução possui vantagens diagnósticas e de conforto ao paciente em relação a manometria convencional porém tem um custo muito superior em nosso meio.
Manometria esofágica de alta resolução: principais vantagens em relação à convencional e uma breve interpretação da classificação de Chicago
-
pHmetria convencional de 24hs
Indicado para diagnosticar pacientes que apresentam sintomatologia de DRGE que não possuem alterações na endoscopia. É um método examinador dependente e só tem validade se a colocação da sonda tiver sido orientada pelo exame de manometria esofágica.
Através deste método pode-se estudar melhor o paciente, avaliando a posição onde ocorrem os refluxos (supino x ortostático), o alcance do refluxato ácido (proximal x distal) e a relação dos refluxos com a sintomatologia do paciente (índices como IS e PAS).
A phmetria convencional de 24hs possui uma sensibilidade diagnóstica de cerca de 90% nos pacientes com sintomas típico de DRGE.
Pacientes com sintomas típicos e sem erosão na endoscopia (que são os que mais realizarão a phmetria sem uso de IBP) apresentam na phmetria convencional sensibilidade e especificidade de cerca de 90% para o diagnóstico de DRGE por refluxos ácidos.
Para pacientes com sintomas atípicos, a sensibilidade é de cerca de 30-40% e a especificidade de cerca de 20-30% mesmos com uso de sonda de dois canais (sendo o proximal localizado na faringe). Importante salientar que a maioria (70%) dos sintomas atípicos ocorrem independentemente dos refluxos.
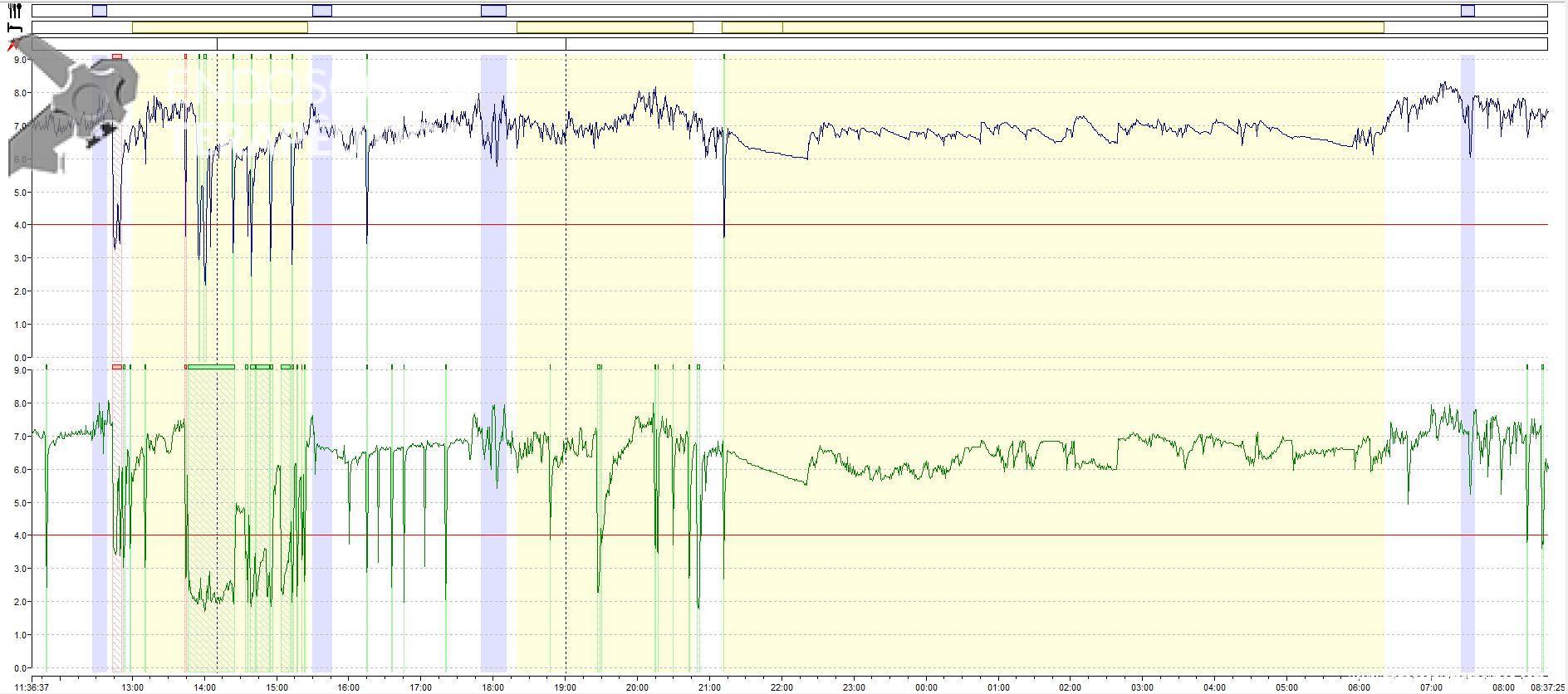
Traçado azul: sensor proximal, localizado junto ao esfíncter esofágico superior. Traçado verde: sensor distal, localizado 5cm acima do esfíncter esofágico inferior. Área em branco: posição ortostática. Área em amarelo: posição supino. Área em azul: período de alimentação. Linha tracejada: horário que ocorreu algum sintoma.
A pHmetria convencional tem pouco valor diagnóstico na vigência de IBP, pois nesta situação os refluxos que ocorrem são não acido e não podem ser mensurados, fazendo com que o exame seja normal em mais de 90% dos casos.
Quando a pHmetria convencional realizada na vigência de IBP tem um resultado positivo para refluxo isto mostra uma supressão ácida ineficaz onde deve-se considerar aderência ao tratamento, a dose utilizada e até mesmo a qualidade do medicamento usado.
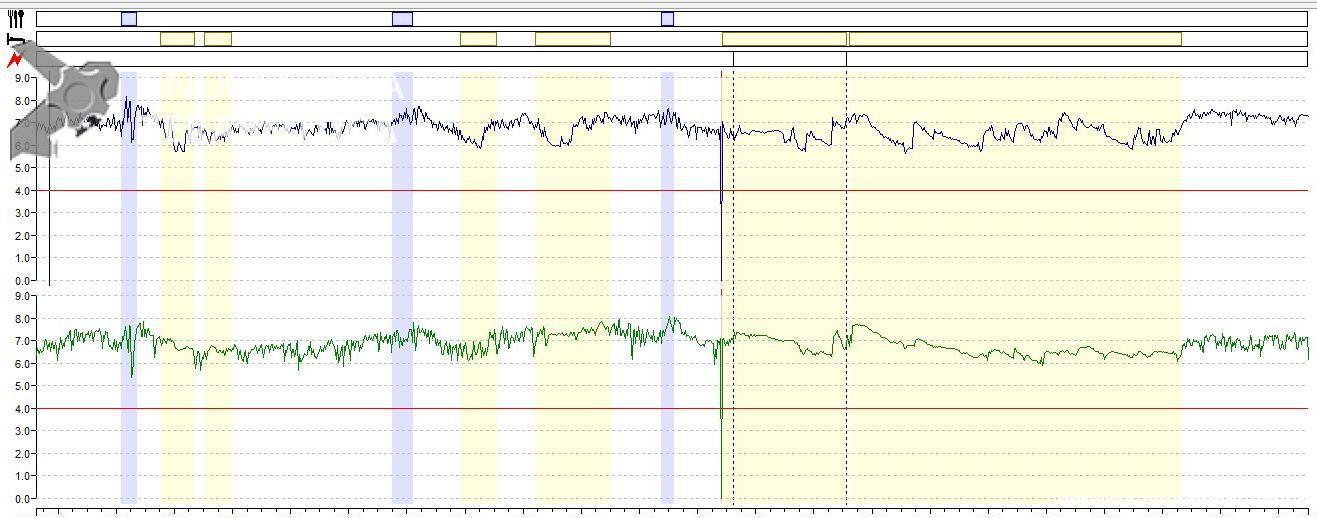
Ausência de refluxo gastroesofágico ácido proximal e distal
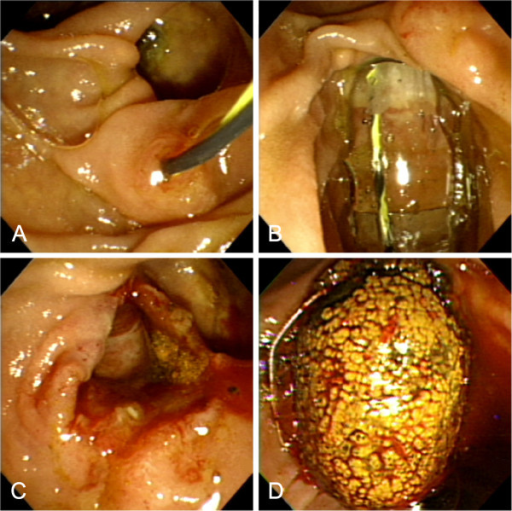
Colocada via endoscopia a 6 cm acima da transição esofagogástrica. Pelo maior conforto permite a avaliação por 48hs. Por ser mais discreta possibilita que o paciente mantenha a sua rotina normal de trabalho e atividades sem se preocupar com a sonda nasal do exame tradicional. Possui uma acurácia diagnóstica semelhante a pHmetria convencional com sensibilidade maior de 90% nos pacientes com DRGE erosiva e de 60% nos pacientes com DRGE não erosiva. Apesar de algumas vantagens possui alto custo que praticamente inviabiliza seu uso em nosso meio.
Tem a vantagem de avaliar a presença de refluxo ácido e não ácido (liquido ou gasoso), por isto atualmente é considerada como Gold Standard para o diagnóstico de DRGE.
Indicado para pacientes com sintomas de DRGE mas que não apresentam alterações na EDA e na pHmetria convencional, onde possui uma sensibilidade e especificidade de cerca de mais de 90% em pacientes com sintomas típicos, onde há predominância de refluxos ácidos. A presença patológica de refluxos, principalmente se houver associação dos sintomas, é um preditor positivo de resposta ao uso de IBP.
Outra indicação é avaliação de refluxo em pacientes em tratamento com IBP mas que não respondem adequadamente aos mesmos. A impedâncio realizada na vigência de IBP mostra a presença de refluxo não ácido em cerca de 40% e de refluxo ácido (escape ácido) em 10% dos pacientes. Nestes casos a positividade no exame é um fator preditivo de boa resposta ao tratamento cirúrgico.
Cerca de 30% dos pacientes com DRGE continuam com sintomas típicos mesmo fazendo uso de IBP adequadamente
Em pacientes com sintomas atípicos a impedanciophmetria tem uma sensibilidade diagnóstica de cerca de 70%, sendo um bom método diagnóstico para esta investigação ao contrário da pHmetria convencional. Esta sensibilidade é maior pois os sintomas atípicos estão mais relacionados com refluxos não ácidos que não podem ser visualizados na pHmetria convencional.
Em pacientes com refluxo faringolaringeo a impedancioPHmetria tem valor preditivo de resposta ao IBP. Os pacientes que apresentam alteração no exame respondem bem ao tratamento com IBP.
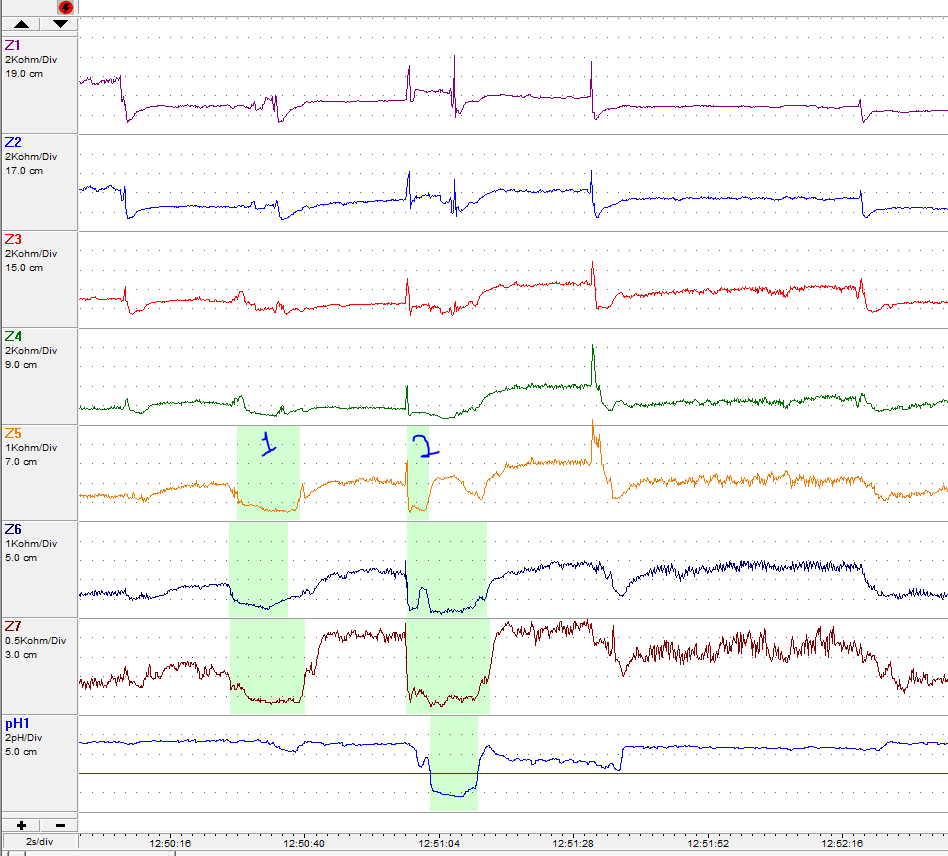
1- Refluxo não ácido. 2- Refluxo ácido. Observar a queda do pH no sensor da pHmetria (pH1).
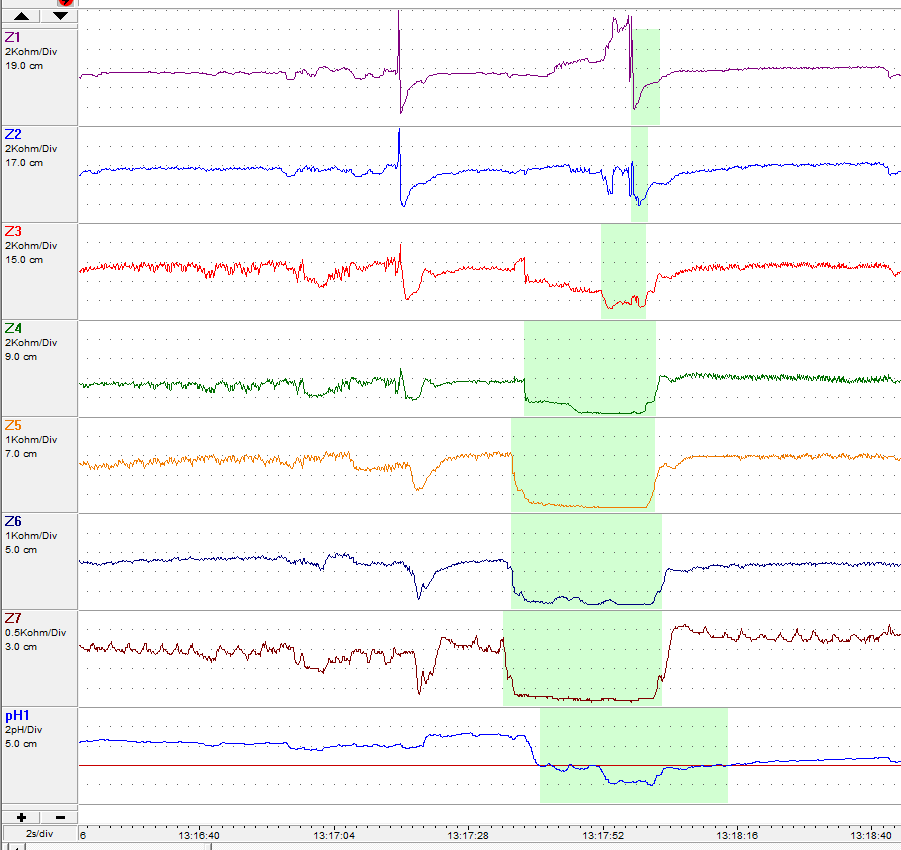
Refluxo ácido. Ascensão retrógrada com queda do pH.
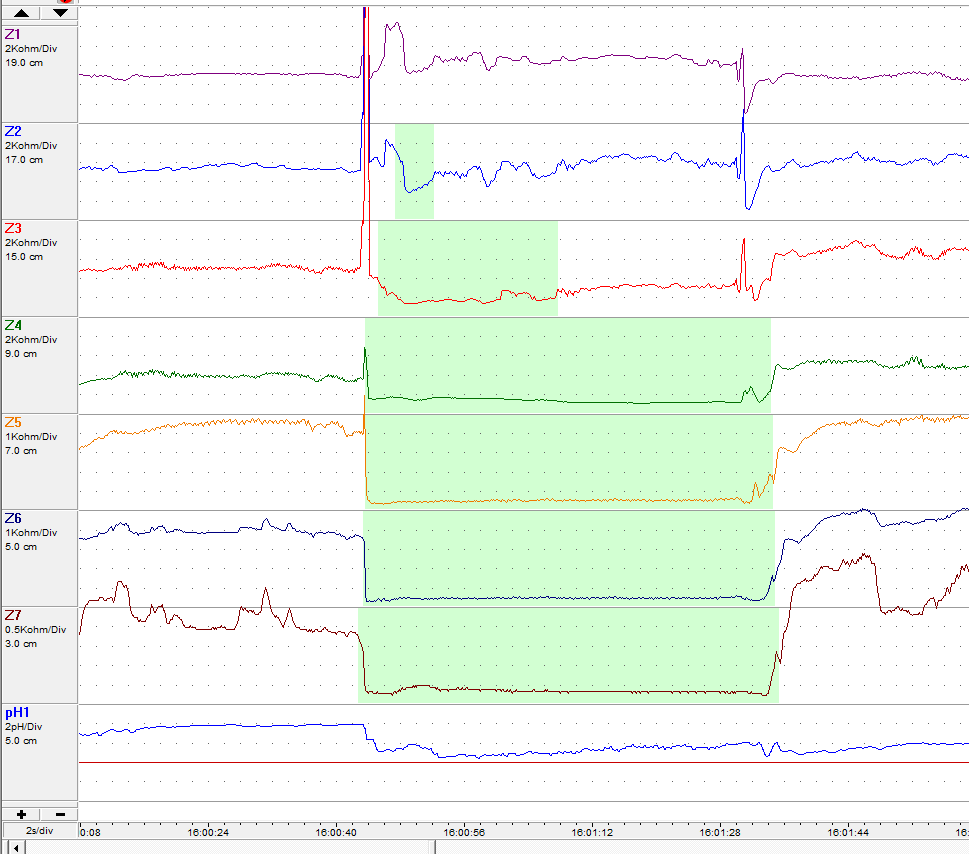
Refluxo levemente ácido. Observe a queda do pH porém não abaixo de 4.
Segue abaixo um fluxograma simples para investigação e tratamento de DRGE:
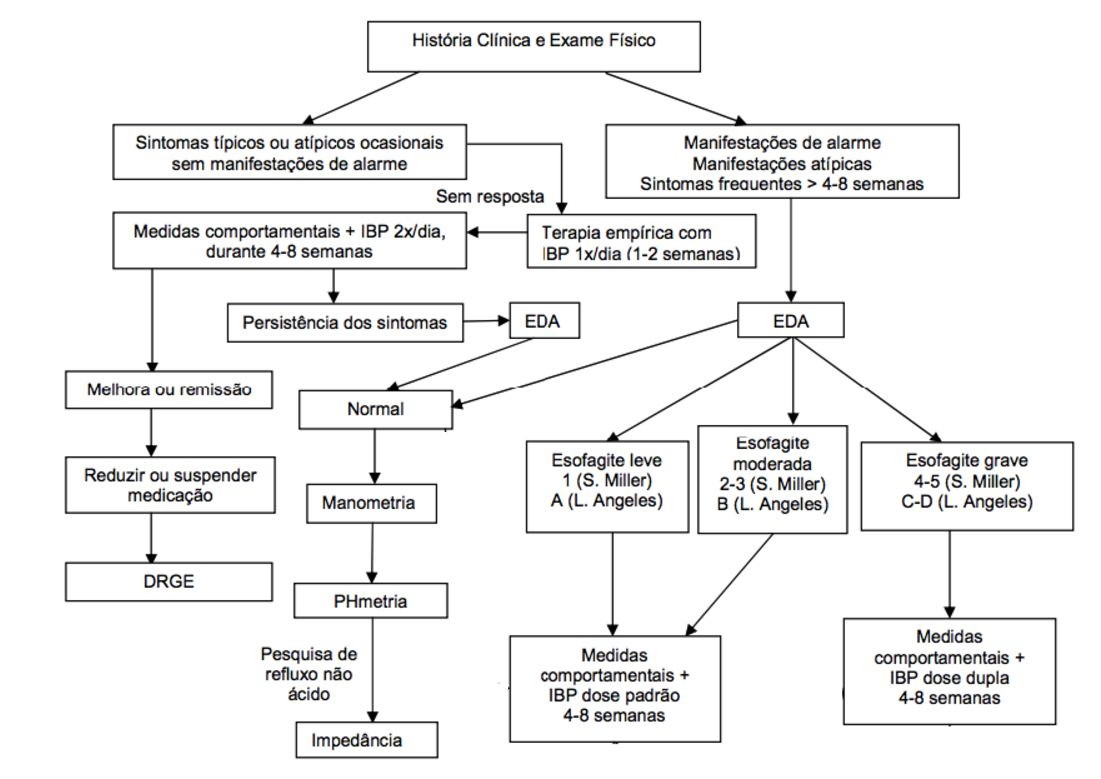
Se toda a investigação diagnóstica for negativa exclui-se o diagnóstico de DRGE e o tratamento com IBP deve ser suspenso. A investigação deve ser continuada para os diagnósticos diferencias como esofagite eosinofílica, acalásia, gastroparesia, síndrome de ruminação. Se esta investigação também for negativa deve-se atribuir os sintomas a um quadro funcional onde podem ser utilizados antidepressivos tricíclicos ou ISRS.
Referências:
- Ates F, Francis DO, Vaezi MF. Refractory gastroesophageal reflux disease: advances and treatment. Expert Rev Gastroenterol Hepatol. 2014;8(6):657–67.
- Scarpellini E, Ang D, Pauwels A, De Santis A, Vanuytsel T, Tack J. Management of refractory typical GERD symptoms. Nat Rev Gastroenterol Hepatol [Internet]. 2016;13(5):281–94. Available from: http://www.nature.com/doifinder/10.1038/nrgastro.2016.50
- Nennstiel S, Andrea M, Abdelhafez M, Haller B, Schmid RM, Bajbouj M, et al. pH/multichannel impedance monitoring in patients with laryngo-pharyngeal reflux symptoms ? Prediction of therapy response in long-term follow-up. Arab J Gastroenterol [Internet]. Pan-Arab Association of Gastroenterology; 2016;17(3):8–11. Available from: http://dx.doi.org/10.1016/j.ajg.2016.08.007
- Endoscopia D De, Brasileira M. Sociedade Brasileira de Endoscopia Digestiva Sociedade Brasileira de Endoscopia Digestiva. 2011;(11):1–6.
- Villa N, Vela MF. Impedance-pH Testing. Gastroenterol Clin North Am [Internet]. Elsevier Inc; 2013;42(1):17–26. Available from: http://dx.doi.org/10.1016/j.gtc.2012.11.003
- Frazzoni M, de Bortoli N, Frazzoni L, Tolone S, Savarino V, Savarino E. Impedance-pH Monitoring for Diagnosis of Reflux Disease: New Perspectives. Dig Dis Sci. Springer US; 2017;1–9.
- de Bortoli N, Ottonello A, Zerbib F, Sifrim D, Gyawali CP, Savarino E. Between GERD and NERD: the relevance of weakly acidic reflux. Ann N Y Acad Sci. 2016;1380(1):218–29.
- Vela MF. Diagnostic Work-Up of GERD. Gastrointest Endosc Clin N Am [Internet]. Elsevier Inc; 2014;24(4):655–66. Available from: http://dx.doi.org/10.1016/j.giec.2014.07.002