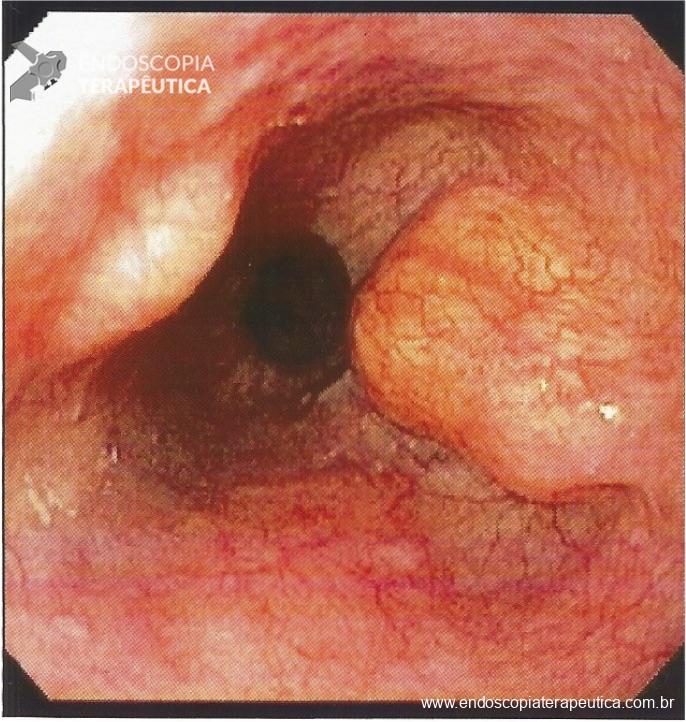
Classificação das neoplasias colorretais precoces segundo Workshop de Paris
Em 2002, um grupo internacional de endoscopistas, cirurgiões e patologistas se reuniram em Paris para discutir a utilidade e a relevância clínica da classificação endoscópica Japonesa de neoplasias superficiais do trato GI.
Desde então, a classificação de Paris tem sido adotada mundialmente como a classificação padrão-ouro para a descrição macroscópica das lesões do TGI.
Neste post, vamos resumir brevemente como aplicar a classificação de Paris para as lesões colorretais precoces.
Modelos do crescimento do tumor durante o desenvolvimento da neoplasia colorretal:
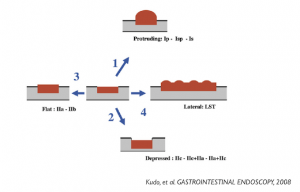
A progressão ocorre em 4 modelos distintos:
- como uma lesão de projeção polipoide, sentido ascendente
- como uma lesão não polipoide, crescendo para para baixo na profundidade da parede
- como uma lesão não polipoide que permanece plana ou plano-elevada
- como uma LST (lateral spreading tumor)
No esôfago, estômago e no cólon, o termo superficial foi adotado para descrever as lesões cuja aparência endoscópica sugiram uma lesão neoplásica não invasiva (displasia/adenoma) ou uma neoplasia invasiva confinada a mucosa/submucosa (T1).
Importante não confundir os termos neoplasia invasiva, com neoplasia avançada:
- As neoplasias avançadas são aquelas que invadem a camada muscular própria (T2).
- As lesões invasivas são aquelas que as células mitóticas extrapolam a região do epitélio glandular e começam a invadir a lâmina própria (T1a), muscular da mucosa e a submucosa (T1b).
Isso quer dizer que uma lesão pode ser invasiva e mesmo assim ser precoce (T1).
O termo “tipo 0” foi adotado para diferenciar as lesões superficiais das lesões avançadas descritas por Bormann (tipo 1-4).
CLASSIFICAÇÃO DE PARIS
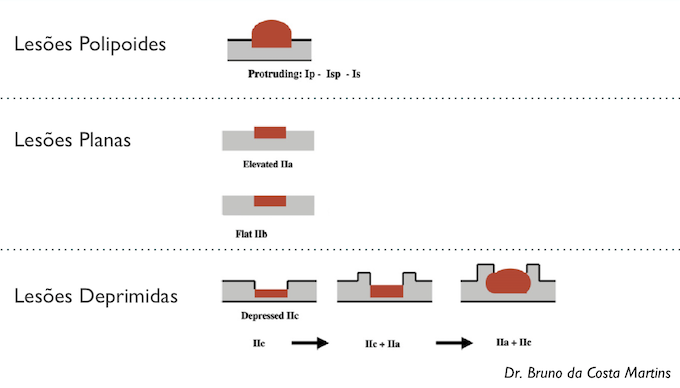
O tipo 0 da classificação de Paris pode ser subdividido em POLIPOIDES vs NÃO POLIPOIDES (vide figura)
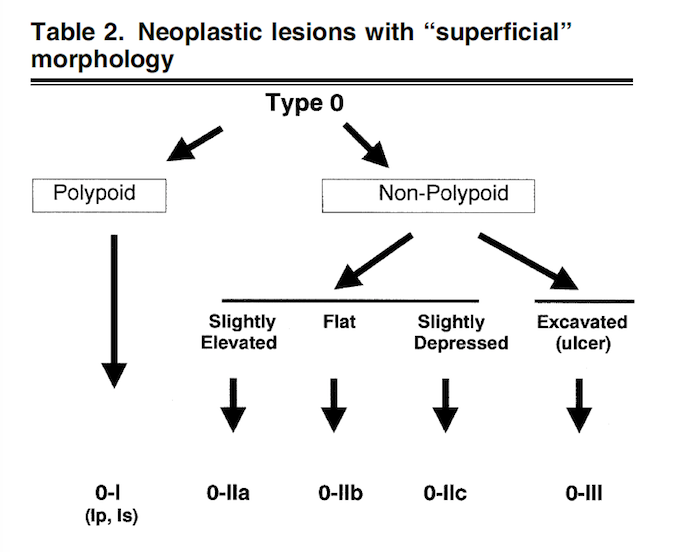
Especialmente no cólon, a subdivisão das lesões não polipoides entre lesões planas (0-IIa e 0-IIb) vs lesões deprimidas (0-IIc) tem um significado clínico extremamente importante, com implicação na conduta, visto que as lesões deprimidas carregam um risco muito maior de invasão da submucosa do que as lesões planas (vide abaixo).
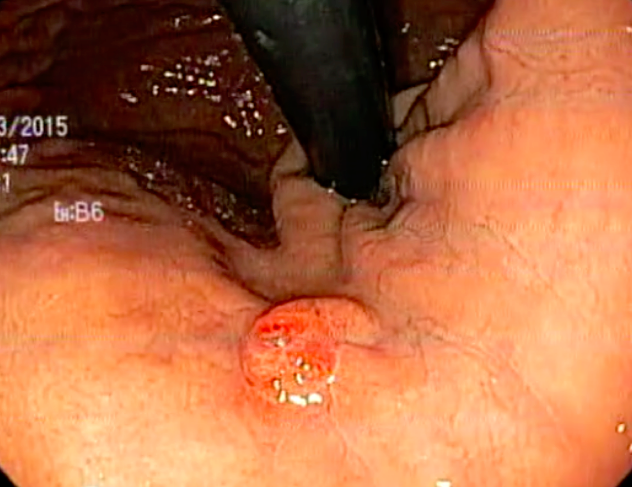
TIPO Is
Nas lesões tipo I, a altura da lesão é maior do que a altura da pinça de biópsia fechada (2.5mm). As lesões podem ser sésseis Is (como na figura apresentada) ou pediculadas (Ip). O consenso de Paris não proíbe, mas desencoraja o termo subpediculado (Isp), visto que essas lesões são normalmente tratadas como lesões sésseis. m, mucosa; mm, muscularis mucosae; sm, submucosa
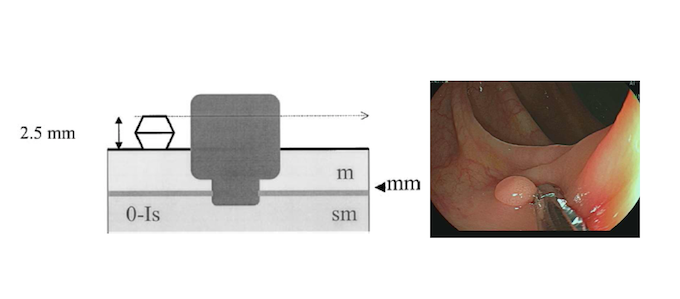
TIPO II
Nas lesões tipo II, a altura da lesão é menor do que a altura da pinça de biópsia fechada (2.5mm). Podem ser subdivididas em elevadas (IIa), completamente planas (IIb) e deprimidas (IIc). As lesões IIa e IIb são relativamente estáveis, com evolução lenta mas podem progredir para lesões polipoides ou para LST. As lesões deprimidas tem comportamento distinto (veja a seguir). m, mucosa; mm, muscularis mucosae; sm, submucosa
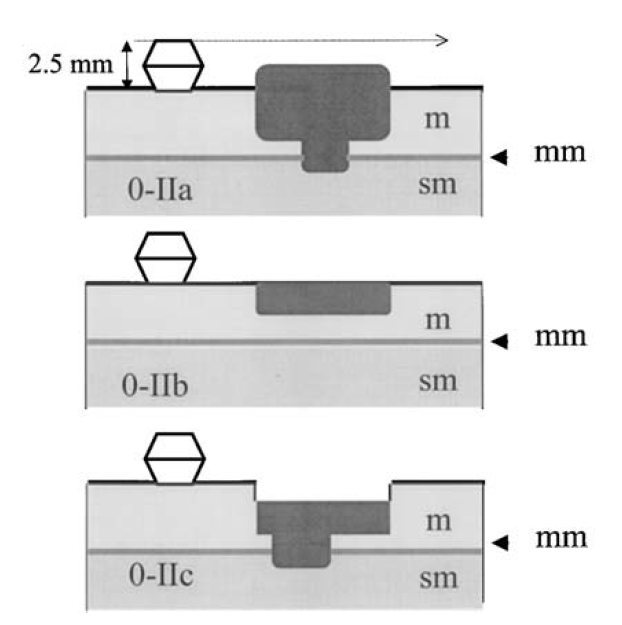
TIPO III
As lesões escavadas (ulceradas) são praticamente inexistentes no cólon.
LESÕES DEPRIMIDAS E TIPOS MISTOS
“No cólon, lesões tipo IIc, mesmo que de pequeno diâmetro, estão geralmente em um estágio mais avançado de neoplasia, com invasões mais profundas do que todos os outros tipos”
Esta frase está entre aspas pois foi traduzida exatamente como no texto do consenso de Paris, e é autoexplicativa.
Conforme o crescimento em profundidades das lesões deprimidas, sua superfície começa a se elevar, bem como suas bordas, evoluindo para os tipos mistos (IIc + IIa e então IIa + IIc). Segue mais um trecho do consenso de Paris:
“As a rule, type IIa + IIc lesions have a poorer prognosis, with a risk of large invasion in the submucosa than all other types of lesions”
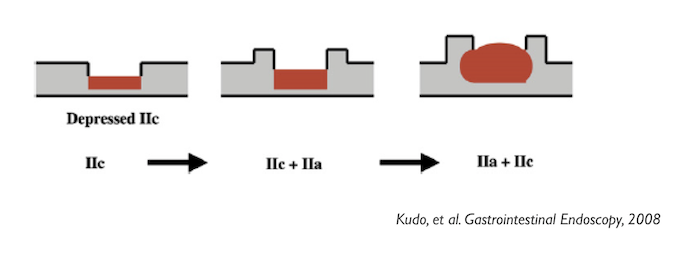
Esse conceito é muito importante compreender, pois é muito comum o emprego da classificação IIa + IIc em lesões relativamente mais “inocentes” do tipo IIa.
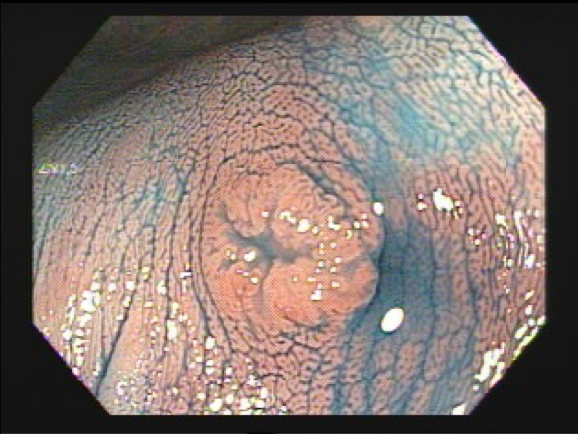
Muitos argumentam: “mas existe uma pequena depressão no centro da lesão”. Existe mesmo. Mas infelizmente a classificação não é perfeita. Alguns endoscopistas orientais utilizam o termo IIa + dep (abrev de deprimido). Nesse caso, a lesão deveria ser classificada como IIa. Daí a importância do olho treinado do endoscopista. Veja abaixo o exemplo de uma lesão tipo IIa+IIc:
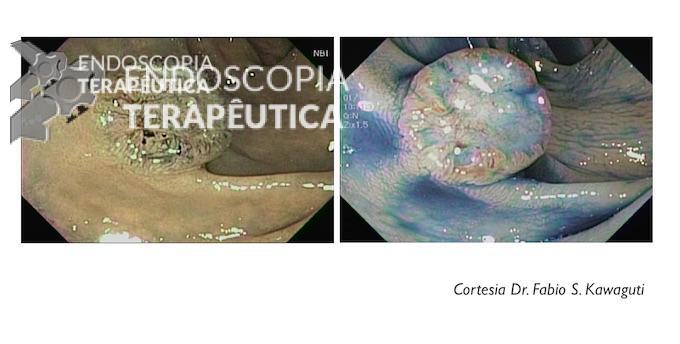
Em resumo, a mensagem mais importante desta classificação é saber diferenciar entre lesões polipoides x lesões não polipoides x lesões deprimidas, pois isso tem grande implicação clínica como descrito no tópico a seguir.
Importância da Classificação
Apesar de muitos endoscopistas criticarem as classificações Japonesa e de Paris, alegando que não passa de um exercício de botânica, existe uma correlação importante entre a forma da lesão e o risco de abrigar lesões mais avançadas, com invasão de submucosa.
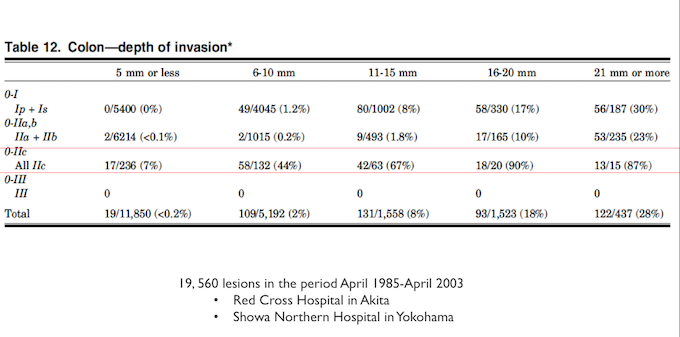
A tabela abaixo resume a experiência de dois serviços de referência no Japão, demonstrando um risco muito elevado de invasão da submucosa em lesões tipo IIc tão pequena quanto 6-10 mm (44%!!!)
Referências:
- O consenso de Paris pode ser acessado pelo site da WEO: http://www.worldendo.org/wp-content/uploads/2016/03/ParisClassification2000.pdf
- Nonpolypoid neoplastic lesions of the colorectal mucosa. Kudo SE, et al. Gastrointest Endosc. 2008 Oct;68(4 Suppl):S3-47.
Como citar esse artigo
Martins BC. Classificação das neoplasias colorretais precoces segundo Workshop de Paris. Em Endoscopia Terapêutica, 2017, vol I. Disponível em: https://endoscopiaterapeutica.net/pt/classificacao-das-neoplasias-colorretais-precoces-segundo-workshop-de-paris