Síndrome da Polipose Juvenil
Definição:
A síndrome da Polipose Juvenil (SPJ) é caracterizada por predisposição a pólipos hamartomatosos no trato gastrointestinal.
Primeiramente, vamos lembrar o que são pólipos hamartomatosos:
-
Os pólipos hamartomatosos são compostos por elementos celulares normais, mas com arquitetura distorcida.
-
As síndromes de polipose hamartomatosa incluem Síndrome da Polipose Juvenil, Síndrome de Peutz-Jeghers e Síndrome do Tumor Hamartomatoso PTEN.
-
As síndromes de polipose hamartomatosas são incomuns, e juntas são responsáveis por menos que 1% dos casos de câncer colorretal nos EUA.
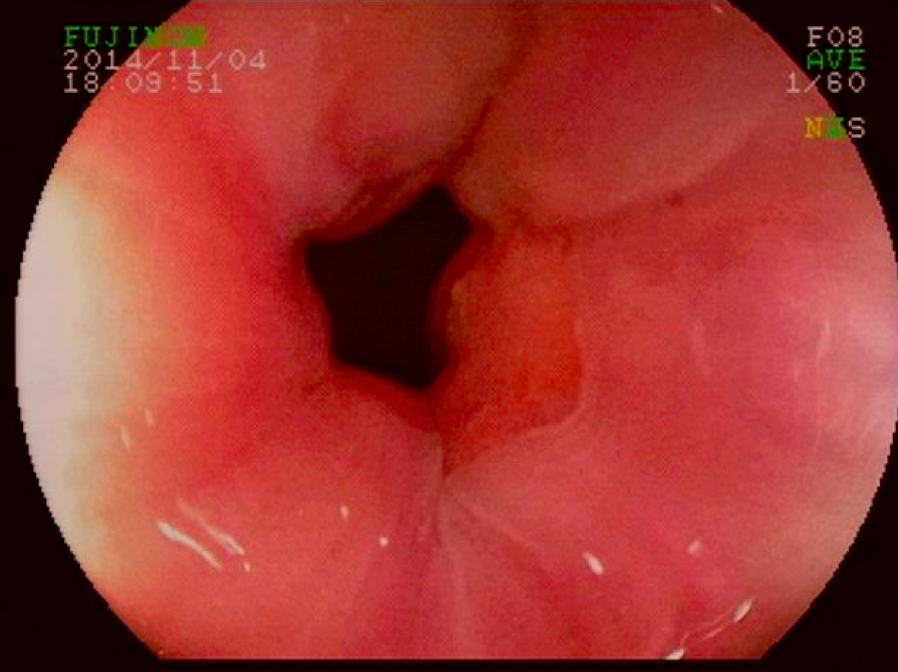
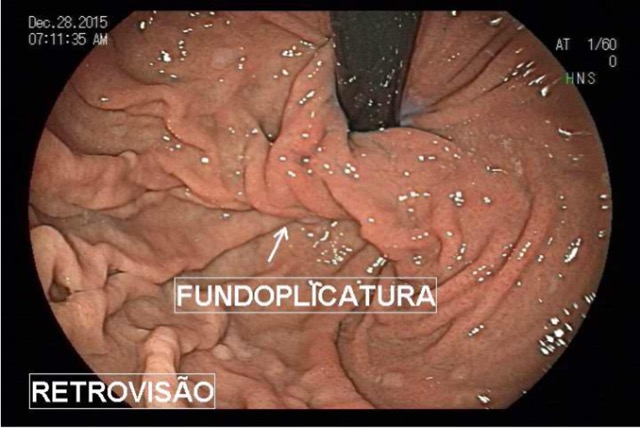
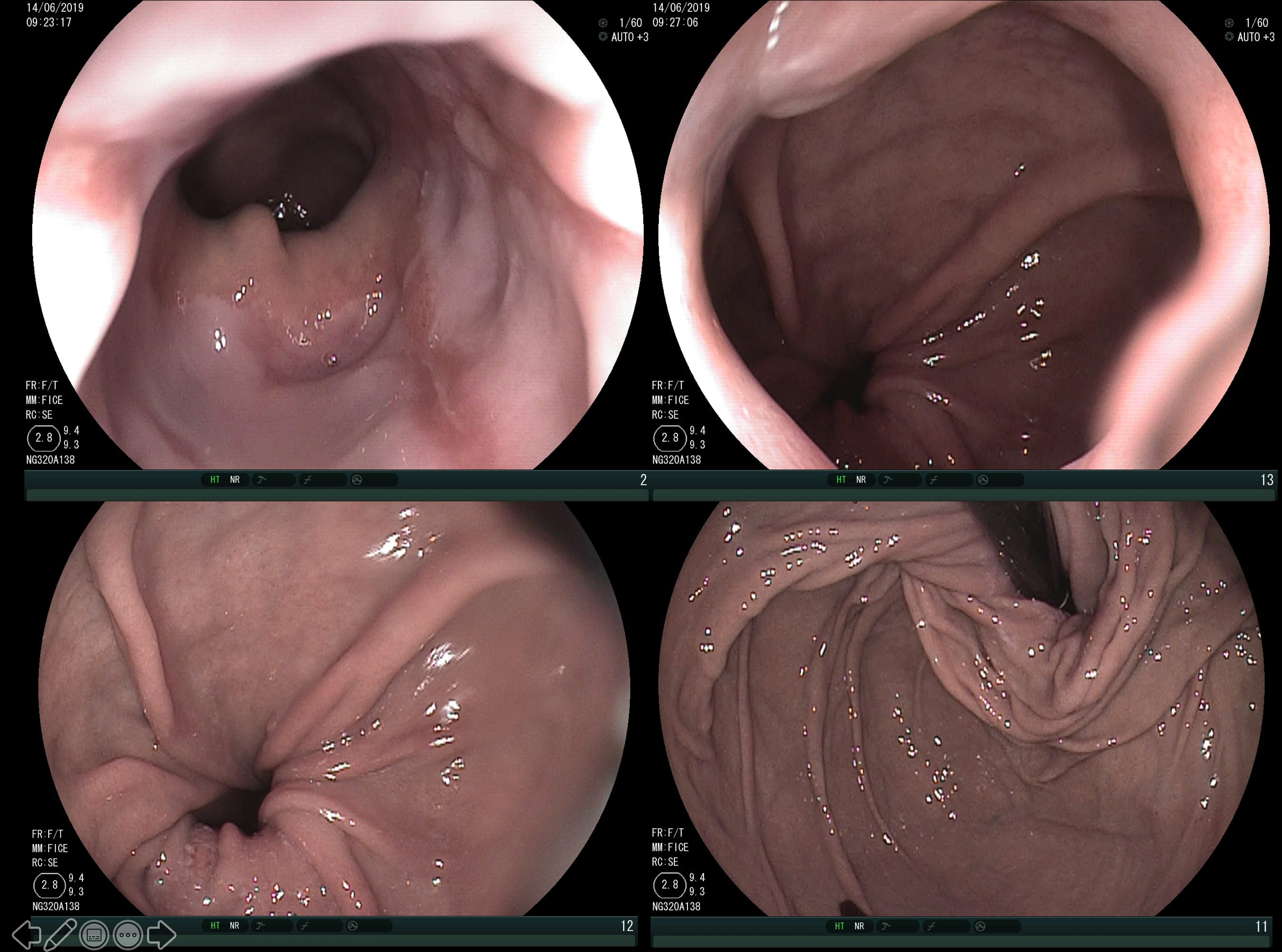
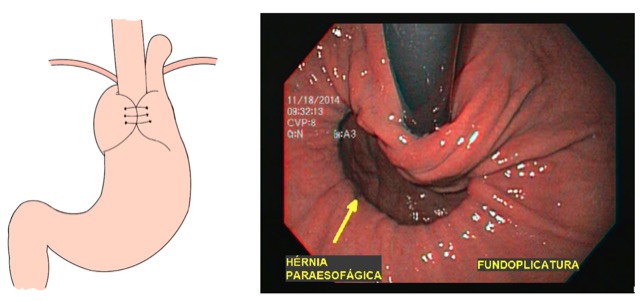
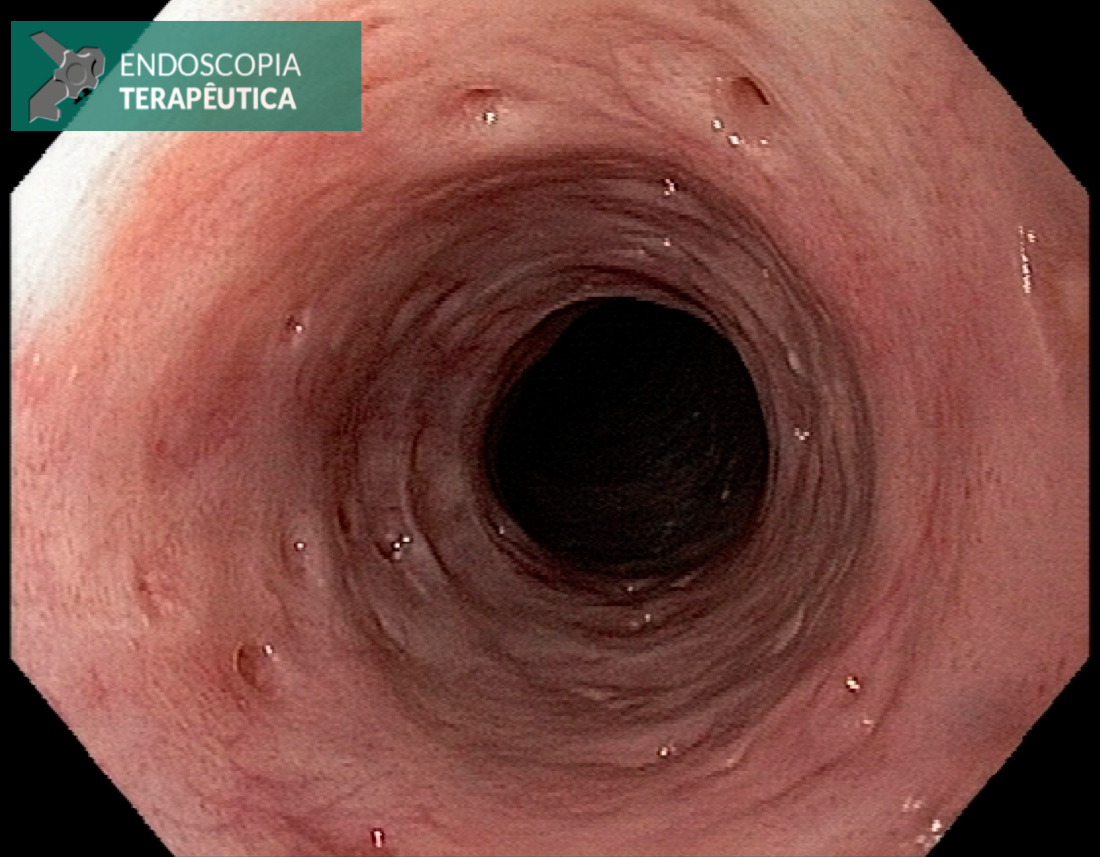
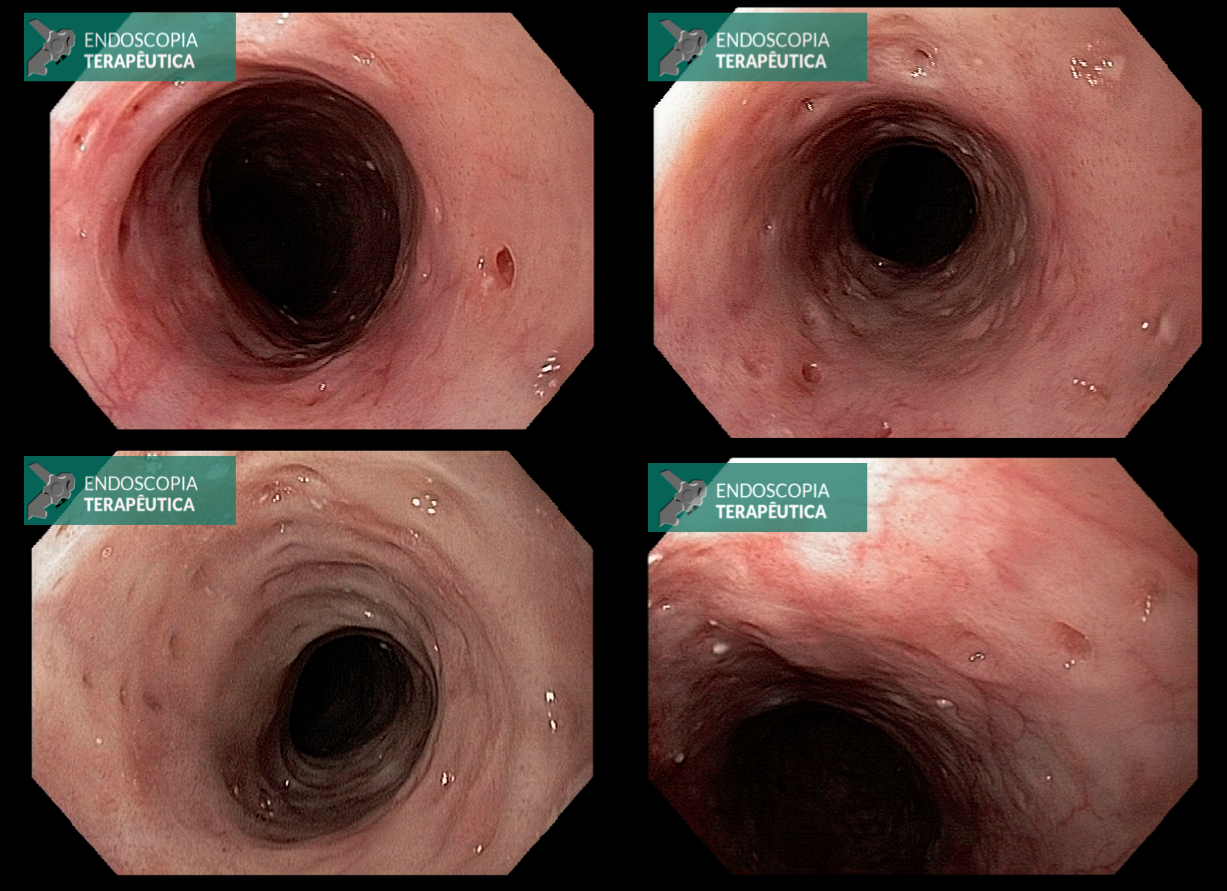
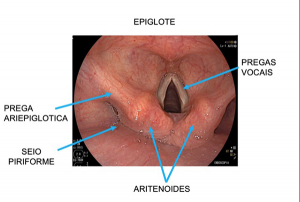
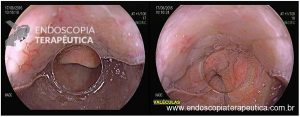
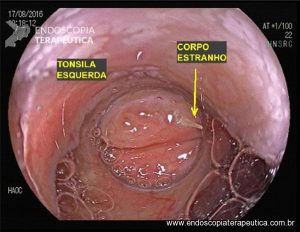
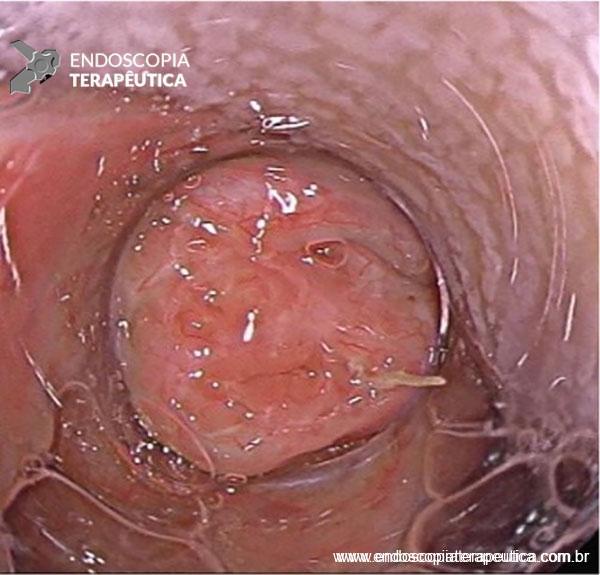
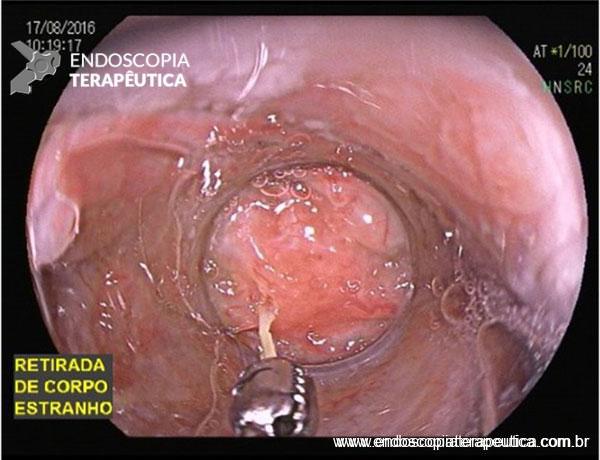
A SPJ É uma condição autossômica dominante, associada a mutação do gene SMAD4 ou BMPR1A. 75% dos pacientes têm história familiar positiva, mas 25% são mutação de novo. É uma condição rara, com incidência na população geral de 1:100.000 – 1:160.000 (Figuras 1 a 4)
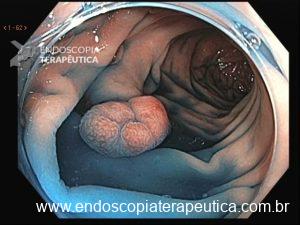
Figura 1
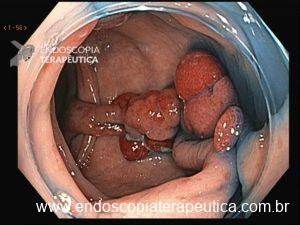
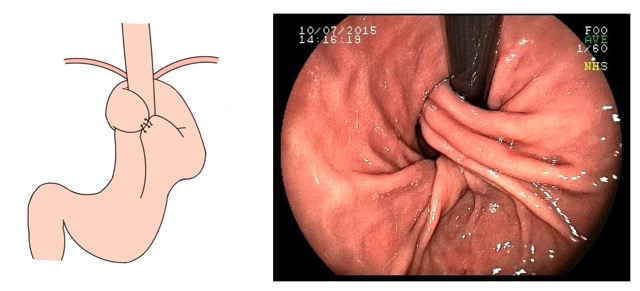
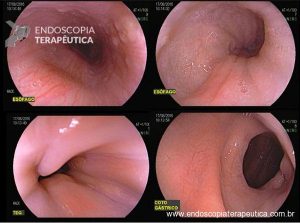
Figura 2
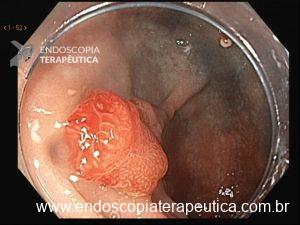
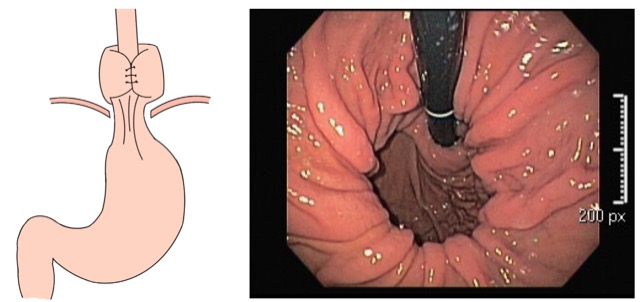
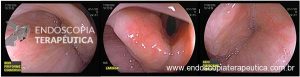
Figura 3
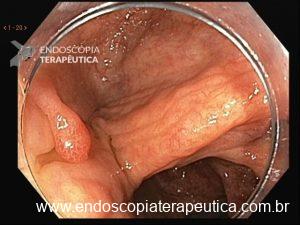
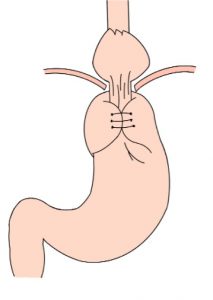
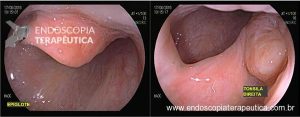
Figura 4
.
Apresentação clínica
O número de pólipos varia, podendo indivíduos da mesma família ter 4 – 5 pólipos por todo o tempo de vida, enquanto outros podem apresentar centenas.
Os pólipos estão presentes em sua maioria no cólon (98%) sendo mais comum no cólon direito (70%), mas também podem estar presentes no estômago (14%), duodeno (7%), jejuno e íleo (7%). O tamanho varia de pólipos sésseis pequenos até pólipos pediculados maiores que 3 cm, geralmente têm a superfície lisa, enantematosa, podendo haver um exsutado esbranquiçado em sua superfície (Figuras 5 a 7).
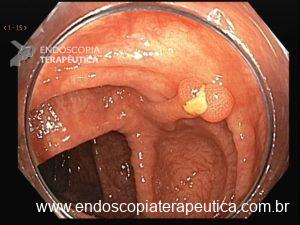
Figura 5
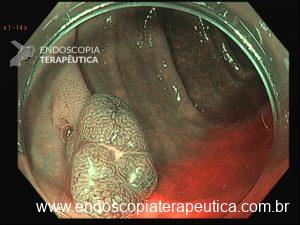
Figura 6
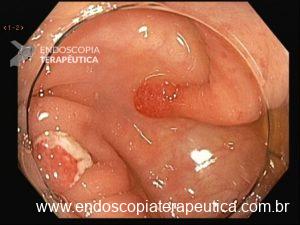
Figura 7
Os sintomas começam geralmente nas primeiras duas décadas de vida, e os mais comuns são sangramento e anemia (90%), mas os pacientes também podem apresentar dor abdominal, diarreia, intussuscepção e obstrução intestinal.
A SPJ também pode estar associado a condições extracolônicas, como telangiectasia hemorrágica hereditária, macrocefalia, hidrocéfalo, coarctação de aorta e tetralogia de Fallot.
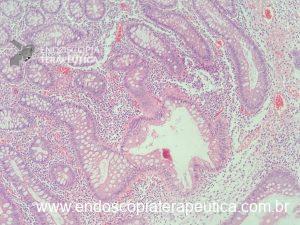
Histologia
A histologia mostra glândulas dilatadas e ecctasiadas, com espaços císticos preenchidos por mucina, lâmina própria abundante e infiltrado inflamatório crônico. Diferentemente de Peutz-Jeghers, não há proliferação da camada muscular lisa. Cerca de 50% dos pólipos tem áreas de adenoma.
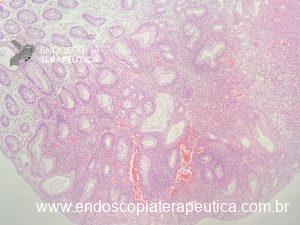
Notam-se glândulas dilatadas e ectasiadas, algumas preenchidas com mucina, além de congestão vascular
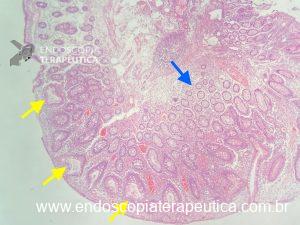
Notam-se glândulas dilatadas e preenchidas por mucina (setas amarelas); glândulas normais representadas pela seta azul
Risco de Câncer
- Estes pacientes têm risco aumentado de câncer gástrico, colorretal, duodenal e pâncreas.
- O risco de câncer colorretal varia de 17-22% aos 35 anos, chegando a 68% aos 60 anos.
- A incidência de câncer no trato gastrointestinal superior pode chegar a 30%.
Diagnóstico
O diagnóstico da SPJ exige o preenchimento de 1 dos seguintes critérios:
- Cinco ou mais pólipos juvenis do cólon e reto,
- Pólipos juvenis em outros segmentos do trato gastrointestinal
- Qualquer número de pólipos juvenis se história familiar positiva.
Importante: A presença de pólipos juvenis esporádicos no cólon não é tão incomum, estando presente em até 2% das crianças abaixo de 10 anos, sem caracterizar SPJ ou representar risco aumentado de câncer.
Rastreamento e vigilância
Para o rastreamento / vigilância, o guideline da ACG de 2015 recomenda para os pacientes em risco:
- Colonoscopia inicialmente aos 12 anos ou quando iniciarem os sintomas, devendo ressecar os pólipos maiores que 5 mm e repetir anualmente até erradicação dos pólipos, depois pode-se espaçar para 3/3 anos.
- Endoscopia inicialmente aos 12 anos, repetir a cada 1-3 anos, devendo ressecar todos os pólipos maiores que 5 mm.
- Estudo do delgado: Se houver pólipos no duodeno, anemia ou enteropatia perdedora de proteínas, recomenda-se cápsula endoscópica, enteroscopia ou enterotomografia
Tratamento:
Pacientes com número limitado de pólipos podem ser manejados com polipectomia e vigilância endoscópica (Figuras 8 a 10).
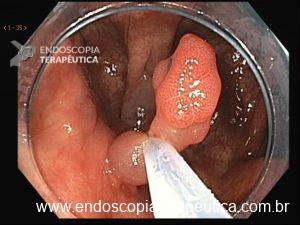
Figura 8
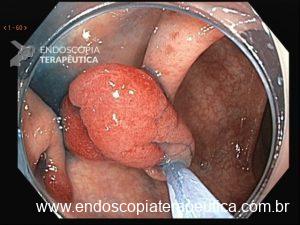
Figura 9
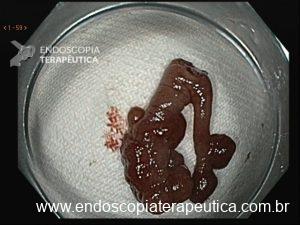
Figura 10
Colectomia com anastomose ileorretal é indicado em caso de câncer, displasia de alto grau ou se não for possível controlar a polipose adequadamente. O reto no entanto deve permanecer em vigilância endoscópica.
Proctocolectomia pode ser necessária dependendo do número de pólipos no reto. Metade dos pacientes submetidos a colectomia, vão precisar de proctectomia posteriormente.
Gastrectomia total ou parcial pode ser necessária para pacientes com displasia avançada, câncer gástrico ou polipose que não pode ser adequadamente controlada por endoscopia.
Como citar esse artigo:
Figueiredo LZ, Martins BC. Síndrome da Polipose Juvenil. Endoscopia Terapêutica. 2022; vol 1. Disponível em: endoscopiaterapeutica.net/pt/assuntosgerais/sindrome-da-polipose-juvenil
Referências:
Zbuk KM, Eng C. Hamartomatous polyposis syndromes. Nat Clin Pract Gastroenterol Hepatol. 2007 Sep;4(9):492-502. doi: 10.1038/ncpgasthep0902. PMID: 17768394.
Larsen Haidle J, MacFarland SP, Howe JR. Juvenile Polyposis Syndrome. 2003 May 13 [updated 2022 Feb 3]. In: Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Gripp KW, Mirzaa GM, Amemiya A, editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993–2022. PMID: 20301642.
Calva, Daniel, and James R Howe. “Hamartomatous polyposis syndromes.” The Surgical clinics of North America vol. 88,4 (2008): 779-817, vii. doi:10.1016/j.suc.2008.05.002
Syngal S, Brand RE, Church JM, Giardiello FM, Hampel HL, Burt RW; American College of Gastroenterology. ACG clinical guideline: Genetic testing and management of hereditary gastrointestinal cancer syndromes. Am J Gastroenterol. 2015 Feb;110(2):223-62; quiz 263. doi: 10.1038/ajg.2014.435. Epub 2015 Feb 3. PMID: 25645574; PMCID: PMC4695986.