Acesso Transgástrico Endoscópico GATE (EDGE) em Bypass Gástrico: o passo a passo
Segundo o Ministério da Saúde, a obesidade atinge 6,7 milhões de pessoas no Brasil. Devido ao crescimento das taxas de obesidade adjunto a eficácia da cirurgia bariátrica, um levantamento da Sociedade Brasileira de Cirurgia Bariátrica e Metabólica (SBCBM) contabilizou 315.720 mil cirurgias bariátricas no período de 2017 a 2022. Com a crescente prevalência de pacientes com anatomia alterada principalmente pelo bypass gástrico com reconstrução em Y de Roux (BGYR), a necessidade de acesso no estômago excluso para tratamento de coledocolitíase, síndromes colestáticas obstrutivas benignas e malignas nessa população são fatores que motivaram o desenvolvimento de técnicas para acesso transgástrico e viabilizar a abordagem endoscópica.
Atualmente, as abordagens mais tradicionais são:
- acesso por enteroscopia
- acesso transgástrico intraoperatório: necessita equipe cirúrgica (assista ao vídeo – clique aqui)
- gastric access temporary for endoscopy – GATE: realizado por ecoendoscopia. Essa técnica também pode ter a nomenclatura de Endoscopic ultrasound-Directed transGastric Endoscopic retrograde cholangiopancreatography – EDGE.
saiba mais sobre esse assunto nesse outro artigo – clique aqui
Dentre as três possibilidades, o GATE mostra-se mais promissor segundo uma metanálise head-to-head de Deliwala et al., cujo trabalho demonstrou
- alta taxa de sucesso técnico quando comparado aos outros métodos: GATE 100% vs. enteroscopia 66% e GATE 97% vs. intraoperatorio 98%)
- efeito adverso menor (GATE 9,6% vs. enteroscopia 16% e GATE 13% vs. intraop 17,6%),
- tempo de procedimento menor (GATE 61,26 min vs. entero 169,38 min e GATE 75,64 min vs. intraop 187,73 min)
- tempo de internação menor (GATE 1,8 dias vs. entero 6,9 dias e GATE 2,2 dias vs. intraop 5,4 dias).
As principais complicações do GATE são: falha de fechamento da fístula confeccionada (chegando a 17%) e migração do Stent (7% dos casos). Ambas as complicações são passíveis de correção por endoscopia e a abordagem cirúrgica é rara.
A seguir, descreveremos o passo a passo para o GATE.
A técnica
Consiste na confecção de acesso transgástrico através de uma gastrogastroanastomose ou por jejunogastroanastomose através da alça jejunal proximal do Y de Roux até o estômago excluso, por meio de ecoendoscopia setorial e uso de prótese metálica de aposição de lumens – LAMS (Figura 1);

Passo 1: Avaliação ecoendoscópica
- Em transição esofagogástrica, localizar a borda inferior do fígado e girar sentido horário pela visão ecoendoscópica até localizar a “bolacha do mar”, sand dollar sign, que seria o estômago excluso em sua porção antral (Figura 2);
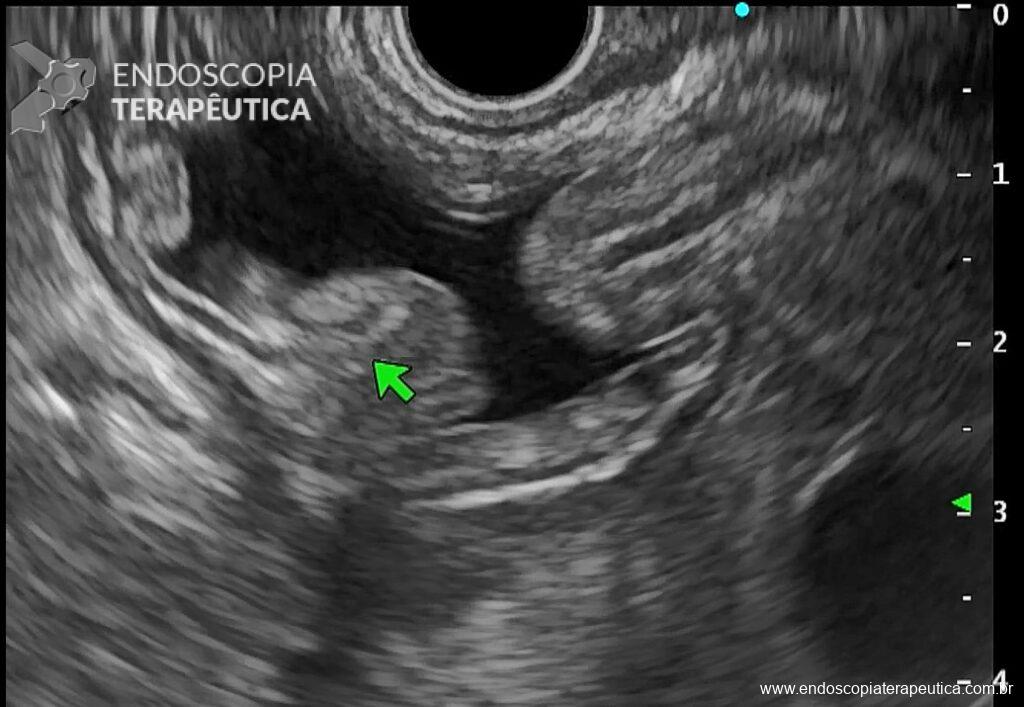
- Puncionar a porção distal do estômago com agulha FNA de 19G até encostar na parede contralateral e retrair a agulha discretamente para centralizar no lúmen (Figura 3);
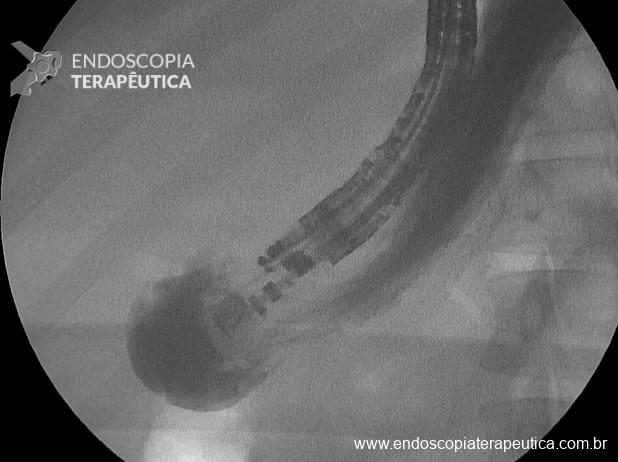
- Administrar contraste iodado pela agulha (optar por seringas pequenas e contraste iodado (diluído em 50% com soro fisiológico), confirmando e dilatando o estômago excluso por ecoendoscopia e fluoroscopia (Figura 4);
- Conectar a agulha com uma bomba de água adaptada com luer lock e preencher com soro fisiológico até distender o estômago de forma segura (distender com ao menos o diâmetro de uma coluna vertebral (estimado em 2,5 cm);
- Dica: utilizar o doppler para evitar vasos no trajeto de punção e sangramento desnecessário é essencial.
Passo 2: Disparo do LAMS
- Retrair a agulha e reposicionar o ecoendoscópico até visualizar a parte proximal do corpo gástrico excluso, logo abaixo da transição esogagogástrica, confirmando com ecoendoscopia, visão endoscópica e fluoroscopia;
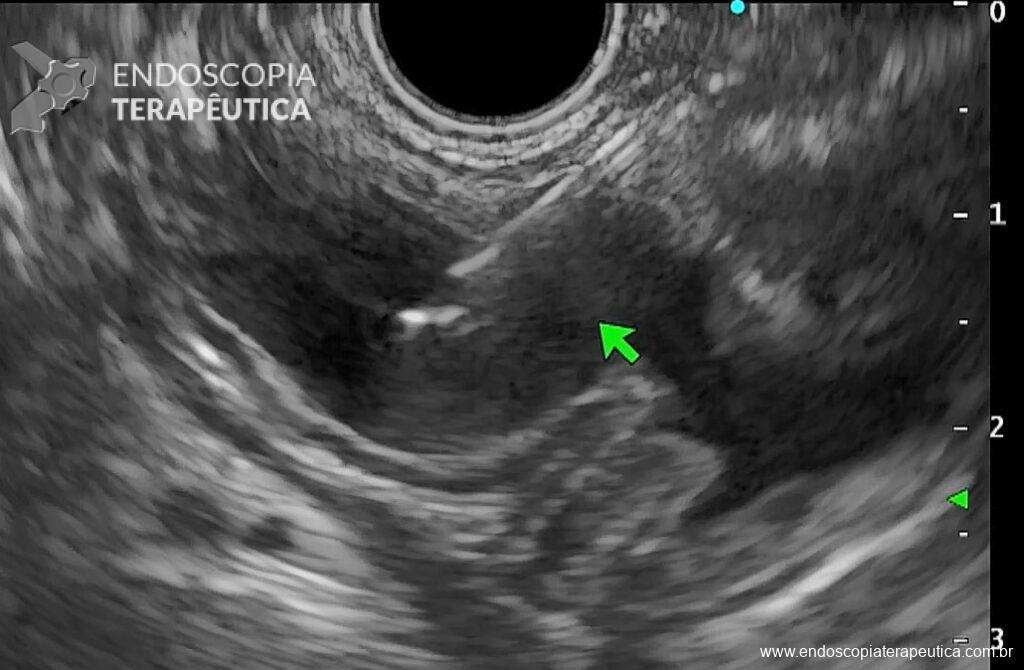
- Repuncionar com FNA 19G, em corpo proximal e distender o estômago excluso novamente com soro fisiológico em bomba até ter uma janela de punção com lúmen de ao menos 3 cm e visualizar o contraste em fundo (Figura 5);
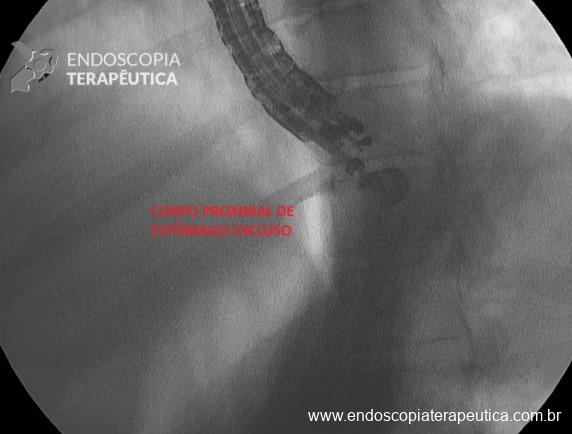
- Caso o LAMS não seja diatérmico, será necessário uso de cistótomo para dilatação do trajeto guiada por fio-guia antes;
- Disparo do LAMS (preferencialmente de 20 mm de diâmetro) em corpo proximal do estômago excluso o mais distal à transição esofagogástrica e proximal à anastomose gastrojejunal (Figura 6);
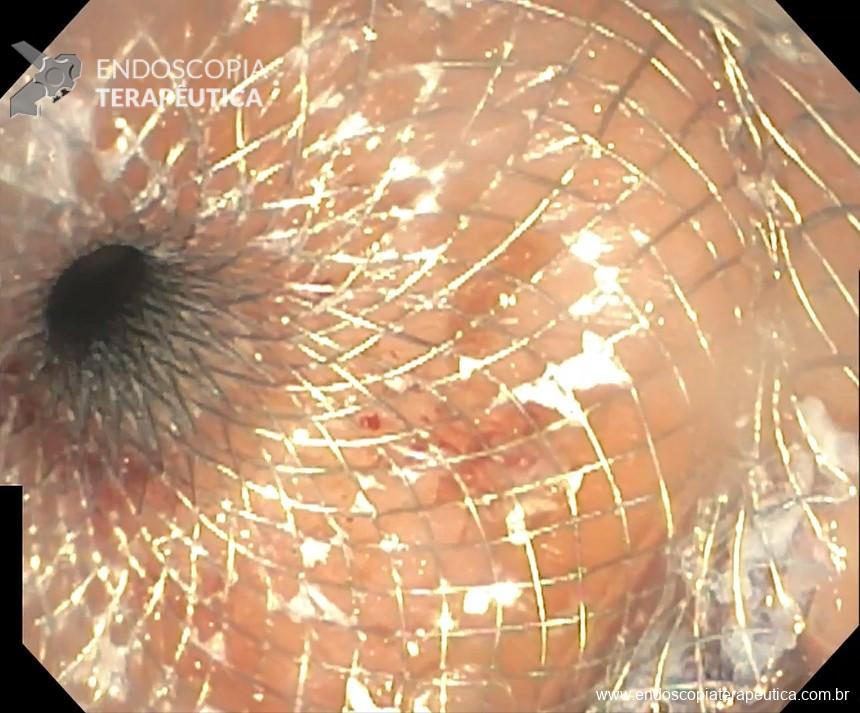
- Dicas: não distar mais de 1 cm da parede do estômago remanescente com o excluso; molhar todo o catéter do LAMS antes de introduzir no aparelho; evitar puncionar em cima da linha de grampo afim de evitar permanência de fístula e área de fibrose.
Passo 3: Dilatação do LAMS e procedimento
Nesta etapa há duas possibilidades:
- Em duas etapas: aguardar maturar a fístula em 1 a 2 semanas e seguir com procedimento após esse período com a prótese metálica já expandida ou dilatação do LAMS logo após disparo;
- Etapa única: realizar dilatação logo após passagem da LAMS. Há opção de fixação da prótese com over-ther-scope-clip (Padlock e Ovesco) ou endossutura (Apollo) para minimizar a migração;
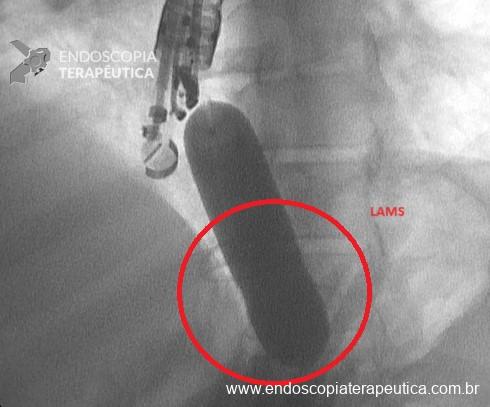
Dilatação da LAMS com balão hidrostático até 20 mm de diâmetro, com confirmação da dilatação por visão endoscópica e fluoroscópica (Figura 7 e 8);
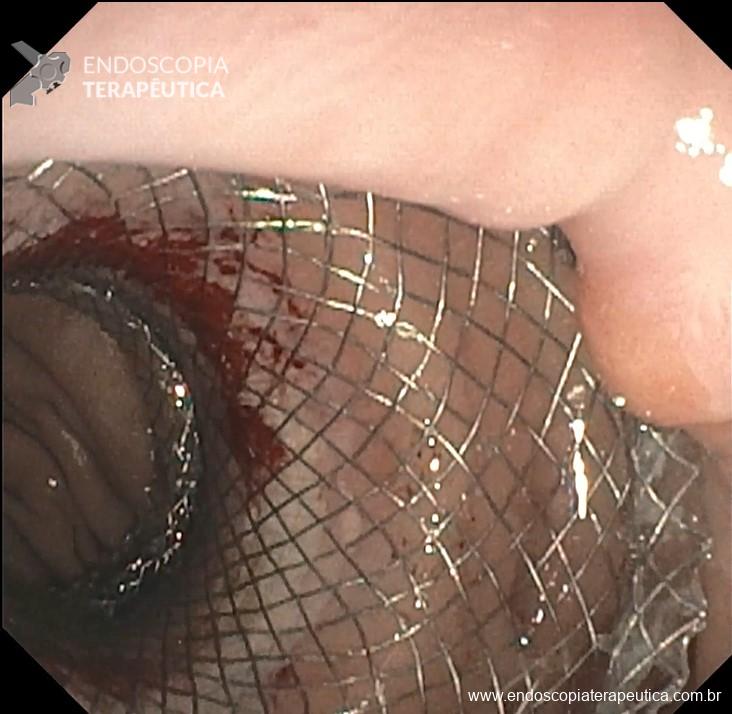
- Prosseguir com o tratamento endoscópico proposto: CPRE principalmente
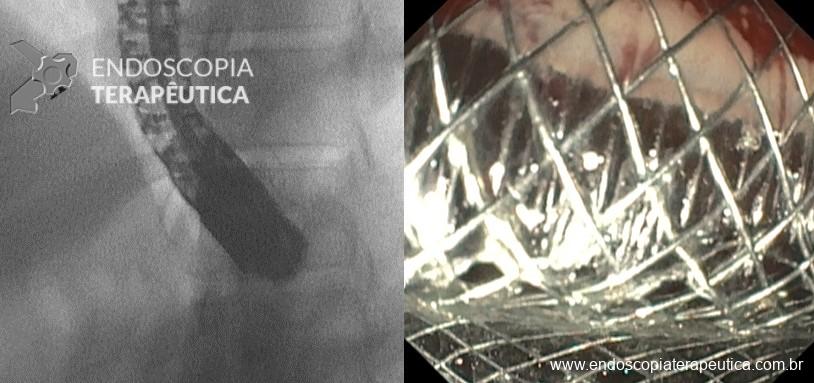
- Dicas: em uso de duodenoscópios ou ecoendoscópios, entrar com aparelho em paralelo com a prótese; a prótese é móvel, então a fluoroscopia ajuda no posicionamento e minimiza a fricção com a prótese, evitando migração (Figura 9).
Passo 4: Fechamento da fístula
- Devido ao risco de complicações pós-procedimentos endoscópicos, como sangramento e perfuração pós-CPRE, mantém-se a LAMS por 1 a 2 semanas, possibilitando a reabordagem endoscópica. Alguns autores, preconizam a retirada imediata seguida por colocação de prótese plástica;
- Após esse período, revisa-se por endoscopia digestiva alta (EDA), seguida de retirada do LAMS com pinça de corpo estranho ou com alça endoscópica, tracionando-se preferencialmente pela falange proximal da prótese;
- Alguns autores preconizam troca por prótese plástica duplo pigtail de tamanho curto e outros por apenas retirar e deixar a fístula ocluir por cicatrização em segunda intenção;
- O controle de fechamento da fístula com o estômago excluso pode ser feita com EDA, radiografia contrastada (EED) ou tomografia computadorizada com contraste não-baritado por via oral após 6 a 8 semanas da retirada da LAMS.
Em suma, o GATE mostra-se como um procedimento seguro e eficaz com taxa de sucesso técnico e clínico comparável a abordagem transgástrica intraoperatória, sem necessidade de combinar duas especialidades médicas, com menor taxa de efeitos adversos, menor tempo de procedimento e internação. A realização do procedimento após GATE em tempo único, com dilatação sem fixação do LAMS está cada vez mais se mostrando seguro e eficaz com o avanço das técnicas endoscópicas.
Referências
- Sociedade Brasileira de Cirurgia Bariátrica e Metabólica (SBCBM). SBCBM, 2023. Disponível em: https://www.sbcbm.org.br/obesidade-atinge-mais-de-67-milhoes-de-pessoas-no-brasil-em-2022/. Acesso em: 16, novembro, 2023.
- Deliwala SS, Mohan BP, Yarra P, Khan SR, Chandan S, Ramai D, et al. Efficacy & safety of EUS-directed transgastric endoscopic retrograde cholangiopancreatography (EDGE) in Roux-en-Y gastric bypass anatomy: a systematic review & meta-analysis. Surg Endosc. 2023 Jun;37(6):4144–58.
- Wang TJ, Thompson CC, Ryou M. Gastric access temporary for endoscopy (GATE): a proposed algorithm for EUS-directed transgastric ERCP in gastric bypass patients. Surg Endosc. 2019 Jun;33(6):2024–33.
Como citar este artigo
Kum AST, Nunes CM, Rocha SPR. Acesso Transgástrico Endoscópico GATE (EDGE) em Bypass Gástrico: o passo a passo. Endoscopia Terapeutica 2023, Vol II. Disponível em: https://endoscopiaterapeutica.net/pt/uncategorized/acesso-transgastrico-endoscopico-gate-edge-em-bypass-gastrico-com-y-de-roux-o-passo-a-passo/