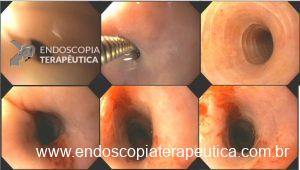
Ecoendoscopia para câncer gástrico: Quando, como e o porquê. Uma análise crítica da utilidade do método.
Atualmente, o câncer gástrico (CG) é o quinto câncer mais diagnosticado e a terceira causa de morte oncológica no mundo. O estadiamento preciso é imperativo para a escolha do tratamento mais apropriado. A ecoendoscopia (EUS) é o melhor método não cirúrgico disponível para a avaliação da profundidade da invasão do câncer gástrico.
Quando solicitar a ecoendoscopia (indicações)?
-
Avaliação pré-tratamento endoscópico (ESD)
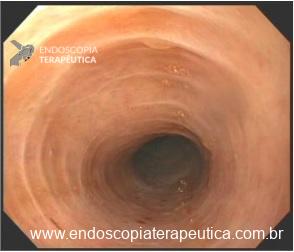
No estômago, a avaliação endoscópica pré-operatória nem sempre consegue predizer com acurácia a profundidade de invasão (diferente do cólon e esôfago, onde temos classificações que guiam a conduta).
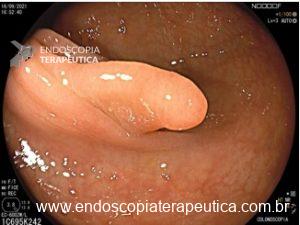
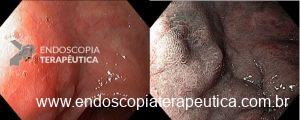
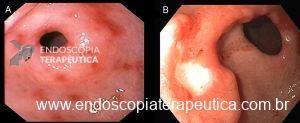
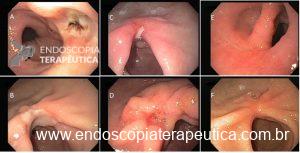
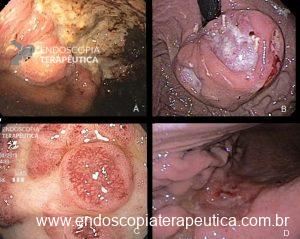
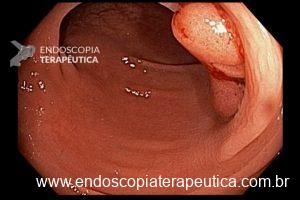
Alguns achados endoscópicos sugerem invasão maciça da submucosa: hipertrofia ou convergência de pregas, ulcerações extensas, superfície muito irregular, sinal da não extensão.
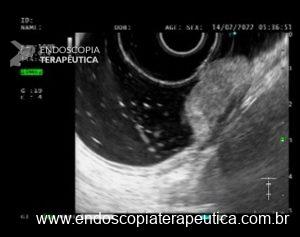
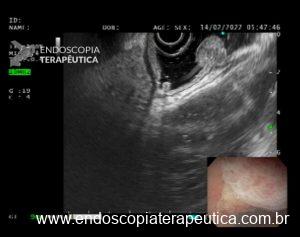
Na ausência destes sinais ou na dúvida, a ecoendoscopia pode ser útil. Lembrando que em revisão sistemática, Mocellin & Pasquali encontraram uma sensibilidade de 85% e uma especificidade de 90% para diferenciar T1 (precoce) de T2 (quando a muscular própria está comprometida), sendo a sensibilidade de 87% e uma especificidade bem menor de 75% para a diferenciação de tumores intramucosos (T1a) daqueles com invasão da submucosa (T1b).
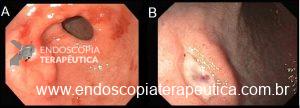
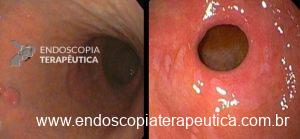
Um ponto que vale a pena ressaltar é que a maioria das lesões que teve o estadiamento incorreto de invasão da SM pela EUS era overstaging, isto é, eram na verdade lesões intramucosas (T1a).
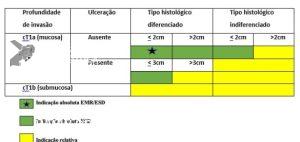
Peça histológica da ESD comprovou que a lesão era mesmo restrita a mucosa. Além disto, tradicionalmente, o tratamento endoscópico era restrito as lesões intramucosas, sendo algumas lesões com comprometimento superficial da submucosa (SM1 < 500 micra) consideradas como critério expandido. Entretanto, no último Guideline Japonês, algumas lesões SM1 foram consideradas como indicações relativas (Vide figura 3).
Outro dado importante, publicado recentemente na conceituada revista Nature, é que ESD antes da cirurgia para CG com invasão da SM ≥ 500 micra não prejudicou a sobrevida após cirurgia adicional. “Trocando em miúdos”, se a lesão na endoscopia – parecer superficial; na histologia – bem diferenciado e na ecoendoscopia – não invadir a muscular própria e não tiver linfonodoadenomegalia. Então, propor para o paciente a ressecção endoscópica com a intenção curativa e preservação do órgão, mas deixando claro que de acordo com o estadiamento histológico (invasão maciça da SM e infiltração angiolinfática) poderá ser necessária cirurgia complementar; e que neste caso, a ESD não prejudica em nada os resultados cirúrgicos.
-
Decisão de quimio perioperatória
Desde o estudo MAGIC, a quimioterapia perioperatória (antes e depois da cirurgia) mostrou-se benéfica no aumento da sobrevida para tumores (T ≥ 2, qualquer N e M0) Entretanto, alguns cirurgiões e alguns protocolos institucionais, preferem a cirurgia upfront nos casos T2 N0 M0. Se esta for a estratégia proposta, a EUS pode ser útil. A acurácia da EUS para Estadiamento N varia de 65 a 90%. E a sensibilidade e especificidade entre diferenciar T1-2 de T3-4 é de 86 e 91%, respectivamente.
-
Diagnóstico de metástases não detectadas pela tomografia
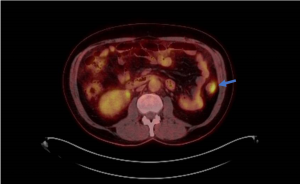
EUS tem um papel limitado no diagnóstico de metástases à distância. Entretanto, com uma tomografia negativa, a EUS pode identificar pequenas metástases no lobo esquerdo hepático e ascites neoplásicas de baixo volume mudando a conduta destes casos para tratamento paliativo.
.
|
NÃO SÃO INDICAÇÕES DE ECOENDOSCOPIA – Quando o resultado não vai mudar a conduta – Se lesões metastáticas já foram identificadas a tomografia – Reestadiamento pós quimio ou radioterapia. |
COMO realizar a EUS para o estadiamento do CG.
-
Aparelhos
A maioria dos estudos utilizou aparelhos radiais. Mini-probes com frequência de até 20 MHz podem ser úteis especialmente para o Estadiamento T mas são pouco disponíveis e tem limitação para lesões maiores de 3 cm e para o estadiamento linfonodal. Aparelhos lineares são mais disponíveis e podem ser especialmente úteis para lesão distais, da incisura e da pequena curvatura. Por vezes, a combinação de aparelho pode permitir um estadiamento mais preciso.
-
Aspecto gerais
Decúbito lateral esquerdo e sedação consciente.
-
Princípios específicos e dicas
Imagens devem ser obtidas perpendiculares e mantendo uma distância de 0,5 -1,0 cm da parede ao probe.
Aspire o ar de todo o estômago, infusão de 200-400 ml de água (cuidado para não broncoaspirar). Comece da parte mais distal e vá puxando o aparelho.
Não existe definição restrita de valores da parede gástrica, mas considere um valor de 2-4 mm e uma relação de 1:1:1 da mucosa, submucosa e muscular própria.
|
LIMITAÇÕES
|
O porquê de realizar a EUS para estadiamento do CG?
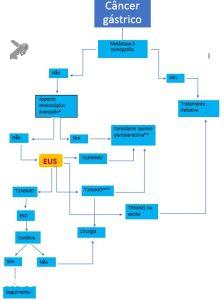
Apesar do último Guideline europeu não recomendar o uso rotineiro da EUS antes da ESD; para indicações precisas, com uma técnica correta, com aparelhos adequados e conhecendo as limitações do método; a EUS é uma ferramenta útil para definir a conduta de muitos casos de CG. Este é um tema controverso, com dados por vezes conflitantes. Mais estudos, com metodologia mais homogênea e com um tratamento endoscópico mais difundido e incluindo os casos com invasão superficial da SM, são desejados para definir com exatidão o papel da EUS na conduta do CG. Algoritmo racional baseado do tratamento do CG com ênfase no papel da EUS está na figura 3.
E você o que acha? Concorda que a ecoendoscopia pode ser útil no estadiamento do câncer gástrico ou acha que não serve para nada? Ou que até atrapalha? Deixe sua opinião nos comentários abaixo
Referências
- Kuroki K, Oka S, Tanaka S, Yorita N, Hata K, Kotachi T, et al. Clinical significance of endoscopic ultrasonography in diagnosing invasion depth of early gastric cancer prior to endoscopic submucosal dissection. Gastric Cancer [Internet]. 2021;24(1):145–55. Available from: https://doi.org/10.1007/s10120-020-01100-5
- Ono H, Yao K, Fujishiro M, Oda I, Uedo N, Nimura S, et al. Guidelines for endoscopic submucosal dissection and endoscopic mucosal resection for early gastric cancer (second edition). Dig Endosc. 2021;33(1):4–20.
- Mocellin S, Pasquali S. Diagnostic accuracy of endoscopic ultrasonography (EUS) for the preoperative locoregional staging of primary gastric cancer. Cochrane Database Syst Rev. 2015;2015(2).
- Ioannis S. Papanikolaoua, Maria Triantafylloua, Konstantinos Triantafylloua, Thomas Röschb. EUS in the management of gastric cancer. Ann Gastroenterol. 2011;24(1):9–15.
- Kuroki K, Oka S, Tanaka S, Yorita N, Hata K, Kotachi T, et al. Preceding endoscopic submucosal dissection in submucosal invasive gastric cancer patients does not impact clinical outcomes. Sci Rep [Internet]. 2021;11(1):1–9. Available from: https://doi.org/10.1038/s41598-020-79696-y
- Pei Q, Wang L, Pan J, Ling T, Lv Y, Zou X. Endoscopic ultrasonography for staging depth of invasion in early gastric cancer: A meta-analysis. J Gastroenterol Hepatol. 2015;30(11):1566–73.
- Pimentel-Nunes P, Libânio D, Bastiaansen BAJ, Bhandari P, Bisschops R, Bourke MJ, et al. Endoscopic submucosal dissection for superficial gastrointestinal lesions: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2022. Endoscopy. 2022;591–622.
- Moura RN. Você sabe quais os critérios de indicação e cura do ESD gástrico (eCura)? Endoscopia Terapêutica; 2022. Disponível em: endoscopiaterapeutica.net/pt/assuntosgerais/criterios-esd-gastrico-ecura
- National Comprehensive Cancer Network – Clinical Practice Guidelines in Oncology – Version 2.2022 Gastric Cancer January 2022