Microlitiasis biliar y dispepsia
Introducción
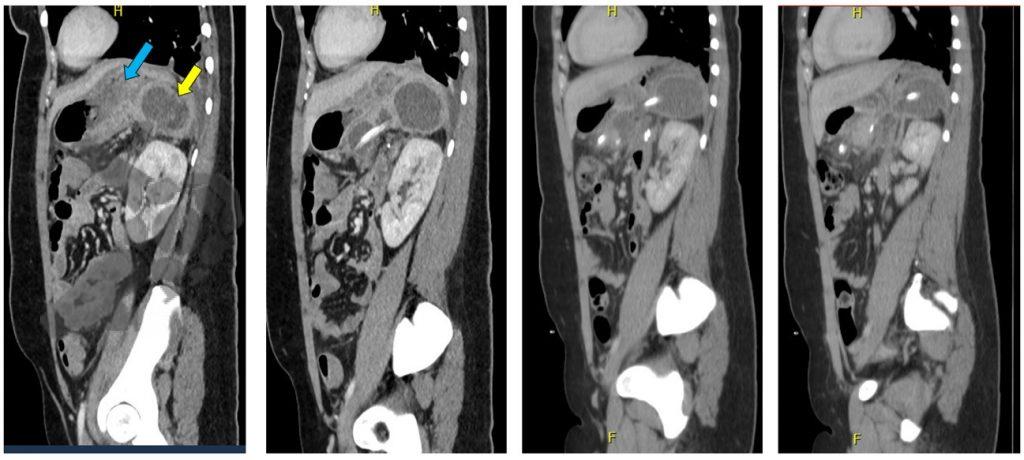
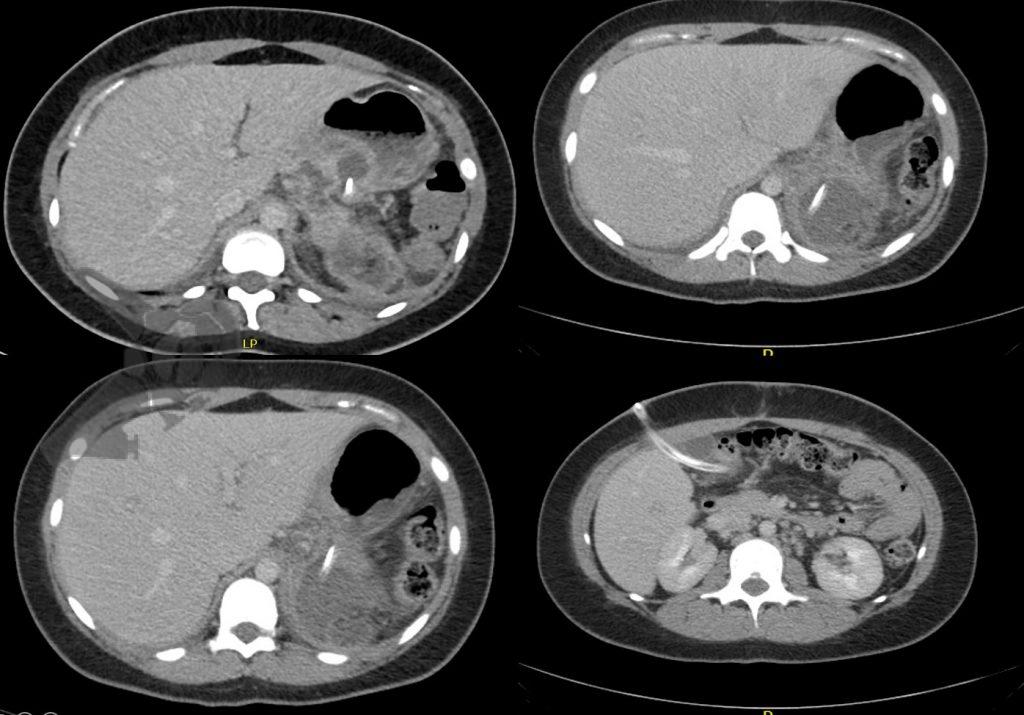
La microlitiasis biliar es una entidad identificada y descrita hace relativamente poco tiempo, aún siendo tema de mucha controversia en la literatura, desde su definición y diagnóstico hasta su relevancia clínica y manejo. Con el aumento de la disponibilidad del examen de ecoendoscopia y la consiguiente ampliación de las indicaciones y solicitudes de este examen, se ha convertido en una condición cada vez más identificada en una población muy heterogénea de pacientes, que varía desde pacientes con obstrucción de las vías biliares, pasando por pacientes con dolor abdominal o dispepsia, hasta pacientes asintomáticos en exámenes “de rutina” o indicados por otros motivos. Tal situación nos hace cuestionar, investigar y revisitar el concepto y el manejo de esta condición que se vuelve cada vez más presente en nuestro día a día.
Ya se ha discutido anteriormente la cuestión de la microlitiasis biliar y del barro biliar en este portal, donde se señalaron las diferencias ecográficas de las dos entidades consideradas en nuestro medio y posibles conductas, así como la relevancia de la microlitiasis biliar en el contexto de la investigación etiológica de la pancreatitis aguda.
En este artículo, evaluaremos las definiciones más aceptadas en la literatura así como las controversias aún no resueltas y discutiremos la relación entre la microlitiasis biliar y síntomas dispépticos.
Definición
Las definiciones para microlitiasis biliar y barro biliar varían inmensamente en la literatura, y van desde descripciones distintas para las dos entidades, pasando por autores que las tratan como sinónimos, hasta publicaciones que ignoran una u otra entidad.
Para intentar resolver ese problema fácilmente identificable en la literatura, ?orniak y col. (1) publicaron un consenso sobre el tema en 2023. El estudio contó con tres principales etapas de elaboración: inicialmente se realizó una revisión sistemática de la literatura que identificó 69 artículos originales y 26 artículos de revisión que definían “microlitiasis biliar” y “barro biliar”; en un segundo momento, 30 “expertos” en ecoendoscopia fueron consultados a través de un cuestionario sobre el tema; por fin, las definiciones más aceptadas fueron organizadas y revalidadas por los autores, pasando por una última etapa de votación.
Para demostrar la heterogeneidad en la literatura, cito algunos de los descriptores más encontrados en esta revisión:
– Microlitiasis biliar: “señal/foco/forma hiperecoica con o sin sombra acústica posterior”, “señal/foco/forma hiperecoica necesariamente con sombra acústica posterior”, “señal/foco/forma hiperecoica necesariamente sin sombra acústica posterior”, “imagen ecogénica móvil sin sombra acústica posterior”.
En relación al tamaño, los estudios variaron desde <1mm hasta <10mm, pero la gran mayoría definió entre <3mm o <5mm.
– Barro biliar: “sustancia fluida”, “nivel fluido”, “múltiples cálculos sin sombra acústica posterior”, “contenido en capas en la porción pendiente de la vesícula”, “contenido de baja amplitud ecográfica”, “imágenes hiperecoicas móviles sin sombra acústica posterior”, “agregado hiperecoico sin sombra acústica posterior”, “material un poco hiperecoico móvil”, “material ecogénico homogéneo”, “material ecogénico heterogéneo”.
Se observa tanto una superposición como un intercambio o mezcla de definiciones entre las dos entidades en la literatura especializada.
Con la difícil misión de determinar un consenso, los autores llegaron en las siguientes definiciones (original en inglés y respectiva traducción por el autor de este artículo):
-Microcálculo biliar: “calculi in the biliary tract and gallbladder of ?5 mm in diameter with acoustic shadowing” / “cálculo en las vías biliares o vesícula biliar con sombra acústica posterior con diámetro menor o igual a 5mm”
– Barro biliar: “Discrete, hyperechoic material inside the gallbladder or the bile duct, without acoustic shadowing, which sediments in the most dependent part of the gallbladder.” / “Material discretamente hiperecoico, sin sombra acústica posterior, con sedimentación en la parte más pendiente de la vesícula biliar”
– Cálculo biliar: “calculi in the biliary tract and gallbladder of >5 mm in diameter with acoustic shadowing” / “cálculo en las vías biliares o vesícula biliar con sombra acústica posterior con diámetro mayor que 5mm”
En otro trabajo, Quispel y col. (2) estudiaron el grado de concordancia entre ecoendoscopistas en relación a microlitiasis biliar y barro biliar. Ellos evaluaron la concordancia entre 41 ecoendoscopistas “expertos” utilizando 30 vídeos. Las definiciones aceptadas en este trabajo fueron (original en inglés y traducción del autor de este artículo):
– Barro biliar (“sludge”): “Layered, cloud shaped, mobile echoic bile duct content, without acoustic shadowing” / “contenido ecogénico móvil en capas sin sombra acústica posterior”
– Microlitiasis biliar (“microlithiasis”): “Hyperechoic circumscript bile duct content, < 3mm with or without acoustic shadowing” / “imagen hiperecoica con o sin sombra acústica posterior menor que 3mm”
– Cálculo biliar (“stones”): “Hyperechoic circumscript bile duct content, ? 3mm with or without acoustic shadowing” / “imagen hiperecoica con o sin sombra acústica posterior mayor o igual a 3mm”
En este estudio, hubo una concordancia interobservador considerada moderada para uno o más cálculos biliares – kappa de Fleiss (IC95%) 0,46 (0,13-0,78) -, débil para microlitiasis – kappa de Fleiss (IC95%) 0,25 (0,07-0,43) – y muy débil para barro biliar – kappa de Fleiss (IC95%) 0,16 (0,07-0,25).
En nuestro medio, tendemos a definir de forma diferente tanto del consenso publicado como del estudio de Quispel y col., como demostrado en el artículo publicado previamente (“Microcálculos y barro biliar – ¿Cuáles son sus valores para la práctica clínica?“) y en el último manual de ecoendoscopia de la Sociedad Brasileña de Endoscopia Digestiva (SOBED) (3).
– Microcálculos/microlitiasis: imagen móvil, hiperecoica, sin sombra acústica posterior y ?3mm

– Barro biliar: contenido ecogénico móvil, sin sombra acústica posterior, con formación de nivel.

– Cálculo: imagen hiperecoica con sombra acústica posterior, independientemente del tamaño (pueden ser llamados de cálculos pequeños si menores que 5mm).

En el entendimiento del autor de este artículo, las definiciones que utilizamos en nuestro medio presentan mayor correlación con los hallazgos ecográficos y con los diferentes perfiles de pacientes. Sin embargo, con la publicación del consenso, si la comunidad de ecoendoscopistas comienza a utilizar la clasificación propuesta, la tendencia será unificar los hallazgos que hoy consideramos en nuestro medio “microlitiasis biliar” y “barro biliar” denominándolos ambos como “barro biliar”, mientras que el término “microlitiasis biliar” será utilizado para cálculos pequeños ?5mm.
De cualquier manera, el mismo consenso hizo un levantamiento retrospectivo que mostró que no hay diferencia en relación a la gravedad de la pancreatitis aguda biliar, independientemente de cuál entidad biliar (cálculo, microcálculo o barro) esté relacionada al evento, y algunos autores consideran que el barro biliar y la microlitiasis biliar comparten la misma significancia clínica (4).
Por último, creemos que aún habrá discusiones en la literatura para establecimiento de las definiciones para que haya una mejor comunicación tanto entre los ecoendoscopistas, como entre médicos asistentes/solicitantes, y también en la propia literatura, a fin de homogeneizar la nomenclatura para estudios futuros. De esta forma, hasta una pacificación sobre el tema en la literatura, se sugiere a los ecoendoscopistas describir los hallazgos con precisión en el cuerpo del informe y realizar adecuada documentación de imágenes, para que el médico asistente/solicitante tenga herramientas para interpretar correctamente los hallazgos y tomar las mejores conductas cabibles en cada caso, independientemente de la definición utilizada en la conclusión del informe.
Microlitiasis biliar y síntomas dispépticos
Como se comentó en la introducción de este artículo, con el aumento de la disponibilidad de la ecoendoscopia, los pedidos de examen para pacientes con síntomas dispépticos variados se han convertido en parte importante de la agenda de ecoendoscopia en los grandes centros, con identificación de “microcálculos/barro biliar” en un amplio perfil de pacientes y llevando muchas veces a la indicación de colecistectomía. Tal escenario nos hace cuestionar el papel de la ecoendoscopia para este perfil de pacientes, la indicación de la colecistectomía y la relación con los síntomas presentados.
Montenegro y col. (4) estudiaron retrospectivamente pacientes con síntomas dispépticos variados, remitidos para realización de ecoendoscopia tras resultados negativos para litiasis biliar por ultrasonido abdominal, que fueron diagnosticados con microlitiasis y/o barro biliar en la ecoendoscopia y sometidos a colecistectomía. Excluyeron pacientes asintomáticos y pacientes que tuvieron cualquier complicación relacionada con la litiasis biliar (pancreatitis, colangitis, colestasis o colecistitis).
En este artículo, los autores utilizaron la siguiente definición (original en inglés y traducción del autor de este artículo):
– Minilitiasis y/o barro biliar (minilitiasis y/o barro biliar): “la presencia de focos isoecoicos y/o hiperecoicos sin sombra acústica posterior, menores que 5mm, que pueden ser visualizados con o sin compresión del epigastrio o hipocóndrio derecho”
A partir de una base de datos de 1121 pacientes que realizaron ecoendoscopia entre los años de 2014 y 2018, se incluyeron 50 pacientes compatibles con los criterios de inclusión.
Entre los síntomas relatados, 58% (29/50) presentaban cólica biliar típica y 42% (21/50) presentaban síntomas atípicos, siendo estos: dolor en el cuadrante superior derecho (24%), epigastralgia + dolor en el cuadrante superior derecho (2%), epigastralgia + náuseas/vómitos (6%), epigastralgia aislada (2%), dolor abdominal difuso con o sin distensión (8%).
Setenta por ciento de los pacientes (35/50) tuvieron remisión de los síntomas tras la colecistectomía. En el grupo de los pacientes con cólica biliar típica, la remisión fue del 86,2% mientras que en el grupo de pacientes con síntomas atípicos fue del 47,6%. En el grupo de pacientes con síntomas atípicos, hubo una diferencia importante en la respuesta al tratamiento de acuerdo con el síntoma presentado, notándose remisión en la mayor parte de los pacientes con dolor en el cuadrante superior derecho y en ninguno de los 4 pacientes con dolor abdominal difuso. La tabla a continuación resume los síntomas pre y post-colecistectomía (tabla 2 del artículo original).

Se identificó solo una (2%) complicación con necesidad de reabordaje post colecistectomía debido a hemoperitoneo y 18% (9/50) de pacientes que evolucionaron con diarrea post colecistectomía.
Los autores concluyen que pacientes con cuadro de cólica biliar típica con presencia de microcálculos/barro biliar a la ecoendoscopia deben ser sometidos a colecistectomía, mientras que pacientes con síntomas atípicos deben ser ampliamente investigados para descartar otras etiologías antes de ser sometidos a colecistectomía, siendo esta evaluación la clave para una adecuada correlación entre los síntomas y los hallazgos ecográficos y consecuente resolución de los síntomas tras colecistectomía.
Jang y col. (5) estudiaron el uso de medicaciones litolíticas (Ácidos Quenodesoxicólico y Ursodesoxicólico) para tratamiento de pacientes con diagnóstico de dispepsia funcional refractaria (DFR). La DFR se define como síntomas dispépticos sin causa definida, persistentes tras tratamiento con sintomáticos, siendo difícil la diferenciación entre dispepsia funcional y dispepsia biliar en muchos casos.
En este estudio prospectivo no aleatorizado simple ciego, se incluyeron 37 pacientes con diagnóstico de DFR y con exámenes de Endoscopia Digestiva Alta (EDA), ultrasonido de abdomen y examen de contractilidad de la vesícula biliar normales. Importante notar que no se realizó ecoendoscopia en los pacientes de este estudio. Se utilizó una escala de síntomas llamada “Escala de síntomas globales de 7 puntos” (“7-point global symptom scale”), que relaciona los síntomas dispépticos con la severidad e impacto en la vida del paciente, en la cual 1 punto el paciente refiere no tener problemas con los síntomas dispépticos y 7 el paciente presenta un problema muy severo que interfiere y limita las actividades diarias. Los síntomas relatados fueron dolor epigástrico, quemazón epigástrica, saciedad precoz y empacho postprandial.
Tras 12 semanas de tratamiento, la media de la escala de síntomas cayó de 5,6 a 2,6, siendo que 94,6% (35/37) refirieron algún grado de mejora de los síntomas y solo 5,4% (2/37) no presentaron ninguna mejora.
Los autores concluyen que la mayoría de los pacientes con diagnóstico de DPR podrían presentar dispepsia biliar y beneficiarse del tratamiento propuesto con litolíticos. También señalan que la microlitiasis biliar no se evaluó adecuadamente en el estudio y podría estar presente en algunos o todos los pacientes que respondieron al tratamiento.
Al evaluar los estudios presentados en conjunto, podemos inferir que la microlitiasis/barro biliar debe considerarse en el diagnóstico diferencial de pacientes con dispepsia, pero el éxito del tratamiento, ya sea con colecistectomía o con litolíticos, depende del tipo de síntoma presentado y de la exclusión de otras etiologías.
Es importante considerar que estos estudios tienen baja calidad metodológica para evaluar la eficacia del tratamiento, pero apuntan a una posibilidad que debería considerarse y estudiarse más a fondo, preferiblemente con ensayos clínicos aleatorizados.
Conclusión
La microlitiasis biliar sigue siendo un tema muy controvertido, con divergencias que van desde la definición hasta el tratamiento, especialmente cuando se relaciona con síntomas dispépticos.
En cuanto a la definición de microlitiasis y barro biliar, existe un debate que será necesario abordar para llegar a conclusiones más consensuadas y compatibles con los hallazgos cotidianos. Considerando la literatura disponible, que aún es muy controvertida a pesar de los esfuerzos por establecer un consenso, corresponde al especialista en ecoendoscopia describir y documentar con precisión los hallazgos para que el médico en cuestión pueda identificar correctamente la entidad descrita, independientemente de la definición utilizada.
En relación a microlitiase/barro biliar y los síntomas dispépticos, algunos estudios de baja calidad metodológica sugieren la posibilidad de correlacionar entre esas entidades y síntomas dispépticos, con posible mejora de los síntomas en parte de los pacientes después de la colecistectomía o el tratamiento con litolíticos. Sin embargo, es fundamental resaltar que cada paciente deber ser evaluado con parsimonia, considerando los síntomas presentados y realizando una amplia investigación de otras etiologías mas probables, especialmente cuando síntomas considerados atípicos para enfermedad biliar son los mas importantes.
Referências
- Żorniak, M., Sirtl, S., Beyer, G., Mahajan, U. M., Bretthauer, K., Schirra, J., Schulz, C., Kohlmann, T., Lerch, M. M., Mayerle, J., & LMU Microlithiasis Expert Survey Team (2023). Consensus definition of sludge and microlithiasis as a possible cause of pancreatitis. Gut, 72(10), 1919–1926. https://doi.org/10.1136/gutjnl-2022-327955
- Quispel, R., Schutz, H. M., Hallensleben, N. D., Bhalla, A., Timmer, R., van Hooft, J. E., Venneman, N. G., Erler, N. S., Veldt, B. J., van Driel, L. M. J. W., & Bruno, M. J. (2021). Do endosonographers agree on the presence of bile duct sludge and the subsequent need for intervention?. Endoscopy international open, 9(6), E911–E917. https://doi.org/10.1055/a-1452-8919
- De Araújo W.C., Nahoum R.G., Como eu faço: pesquisa de pancreatite idiopática. In: Salomão B.C., Moura E.G.H.M. Ecoendoscopia como eu faço? / núcleo de ecoendoscopia SOBED – São Paulo : Editora dos Editores, 2023. Cap. 5 p.87-96
- Montenegro, A., Andújar, X., Fernández-Bañares, F., Esteve, M., & Loras, C. (2022). Usefulness of endoscopic ultrasound in patients with minilithiasis and/or biliary sludge as a cause of symptoms of probable biliary origin after cholecystectomy. Gastroenterologia y hepatologia, 45(2), 91–98. https://doi.org/10.1016/j.gastrohep.2021.03.010
- Jang, S. I., Lee, T. H., Jeong, S., Kwon, C. I., Koh, D. H., Kim, Y. J., Lee, H. S., Do, M. Y., Cho, J. H., & Lee, D. K. (2022). Efficacy of Chenodeoxycholic Acid and Ursodeoxycholic Acid Treatments for Refractory Functional Dyspepsia. Journal of clinical medicine, 11(11), 3190. https://doi.org/10.3390/jcm11113190
Como citar este artigo
Proença IM, Penaloza CSQ. Microlitíase biliar y dispepsia. Endoscopia Terapeutica 2024 vol II. Disponível em: https://endoscopiaterapeutica.net/es/temas-generales/microlitiasis-biliar-y-dispepsia/